气相二氧化硅/季铵Gemini表面活性剂稳定的泡沫体系
2016-09-09孙小祥赵剑曦
孙小祥 陈 宇 赵剑曦
(福州大学化学化工学院胶体界面化学研究所,福州350108)
气相二氧化硅/季铵Gemini表面活性剂稳定的泡沫体系
孙小祥陈宇赵剑曦*
(福州大学化学化工学院胶体界面化学研究所,福州350108)
以zeta电位法研究了季铵Gemini表面活性剂亚甲基-α,ω-双(十二烷基二甲基溴化铵)(12-s-12,s=2, 6)在水溶液中修饰气相二氧化硅(F-SiO2)粒子。这些粒子随表面活性剂浓度C增加经历了表面从原先的亲水到疏水再重新亲水的改变,其中疏水粒子可以自发吸附在气泡液膜中,从而很好地稳定泡沫。重新亲水的粒子脱附出液膜,仅留下表面活性剂稳定气泡。强的液膜弹性对应于稳定的泡沫。联接链长度影响了Gemini 在F-SiO2粒子表面的吸附,因而也影响了液膜的弹性和对泡沫的稳定。超短s=2联接链的12-2-12由于反离子解离不完全而带有较少的正电荷,在粒子表面的初始吸附弱于12-6-12,但因此减少了吸附分子头基间的静电排斥,可以形成更致密的吸附层。由于12-2-12本身比12-6-12具有更强的界面吸附能力,F-SiO2粒子和12-2-12的协同作用可以更好地稳定泡沫体系。
气相二氧化硅粒子;Gemini表面活性剂;表面改性;泡沫稳定性
www.whxb.pku.edu.cn
1 引言
泡沫是具有重要应用的分散体系1-6,它的形成和稳定需要表面活性剂帮助。相比于乳液,长期暴露于空气中的气泡更难被稳定2。两亲性的固体微粒也能自发富集在气/液界面形成粒子层,这层粒子由于彼此间的摩擦不易被解体7,因此能够很好地稳定气泡。常用于此的纳米或微米级的固体微粒有二氧化硅8,9、胶乳10,11、金属微粒12,13等。
气相二氧化硅(F-SiO2)是常用的精细化学品,通过在氢氧焰中燃烧挥发性的硅烷(例如四氯化硅)得到初始粒子,经降温凝结成多粒子聚集体,再进一步簇集成最终的商品化产品14,这些粒子已经被用于稳定乳液15,16。表面化学改性可以得到两亲性的固体粒子,但更为便捷和价廉的方法是在水溶液中原位吸附表面活性剂来实现粒子表面的两亲性改造17,18。本文选择季铵Gemini表面活性剂亚甲基-α,ω-双(十二烷基二甲基溴化铵)(简记为12-s-12,s=2,6)来修饰F-SiO2。这个系列Gemini表面活性剂的自组织性质已被广泛研究19,它们具有比相应单体表面活性剂(十二烷基三甲基溴化铵,C12TABr)更强的界面吸附能力,因此被期望能很好地改性F-SiO2。联接链是Gemini分子的重要结构基团,其长度强烈影响了它们的自组织19,本文重点考察两个典型长度联接链对改性微粒进而稳定泡沫的影响。
2 实验部分
2.1试剂
气相二氧化硅(Degussa Aerosil 200,德国产),99.8%纯度,BET法测得比表面积为(200±25)m2· g-1。商品的透射电镜(TEM)照片见图1。12-s-12由本实验室合成,其纯度经核磁共振氢谱(1H NMR)和元素分析检测20,分子结构如示意图1所示。

图1 气相二氧化硅透射电镜图Fig.1 Transmission electron microscope(TEM)image of the fumed silica

示意图1 Gemini表面活性剂12-s-12化学结构式Scheme 1 Chemical structure of the Gemini surfactant 12-s-12
2.2泡沫生成与性质测试
泡沫形成及性质测试用自制的装置21。在底部带有玻璃砂芯的起泡管(管内径25 mm,高度140 mm)中加入5 mL试液,待温度恒定后,气体以固定流速68 mL·min-1经毛细管通入起泡管底部,测定生成20 mL泡沫的进气时间(t·min-1)。将生成泡沫体积与进气体积之比Rv定义为溶液起泡性参数:

式中S为气体流速(mL·min-1),可由流量计读出。
在停止进气后,测定20 mL泡沫衰减至一半所需的时间t1/2,作为泡沫的稳定性参数。实验温度通过恒温水浴保持在(25.0±0.1)°C。
2.3Zeta电位测定
用zeta电位仪(ZetaPlus,美国Brookhaven仪器公司)测定。测试样品在25°C下恒温振荡72 h以达到吸咐平衡。移取1.5 mL溶液置于比色皿中,插上电极,放入样品池中。静置30 min后,利用光散射原理测定带电微粒在外电场下的迁移,进而计算zeta电位(ζ)。每个样品测定10次取平均值为最终的zeta电位值。
2.4界面膜粘弹性质测定
用光学视频接触角测量仪(OCA-20,德国Dataphysics)及振荡滴附件ODG-20测定。从注射管中挤出一滴合适大小的溶液,固定在装有与待测液相似溶液的恒温玻璃池中。待液滴平衡后,通过由马达控制的活塞运动对平衡液滴进行正弦扰动,液滴表面积和半径随之按正弦变化。在事先测定的线性粘弹区范围内,固定相对面积变化dA/A为6%,扰动频率为0.01-1 Hz(按对数平均分布为13个频率)。电荷耦合(CCD)摄像机以50张/秒的速率拍录振荡过程,由软件计算振荡过程中各个周期的面积变化(dA)以及对应的表面张力变化(dr),得ε*=dr/AdA,再由下式求得扩张弹性ε和扩张粘性η:


式中θ为扩张模量的角,ω为界面面积正弦变化的频率。以上实验测试在25°C进行。
3 结果与讨论
3.1F-SiO2粒子表面原位疏水化
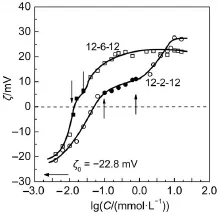
图2 气相二氧化硅颗粒(0.05%(w))的zeta电位(ζ)随表面活性剂浓度变化Fig.2 Zeta potential(ζ)of fumed silica particles (0.05%(w))as a function of concentration of 12-2-12(○)or 12-6-12(□)
F-SiO2粒子表面原位疏水化依靠F-SiO2粒子在水溶液中原位吸附表面活性剂来完成。图2为FSiO2/Gemini溶液的ζ随表面活性剂浓度(C)变化的半对数曲线,可见随着C增大,ζ的值从初始的负值(-22.8 mV)快速上升,越过零ζ值后呈正值地趋向平台。这个变化趋势在微粒/阳离子表面活性剂体系被普遍观察到,反映了表面活性剂在微粒表面的吸附22,23:初始吸附通过静电吸引进行,表面活性剂以其阳离子头基附着在负电性的微粒表面,烷烃尾链朝向溶液,这减小了粒子的负电性(表现为ζ的上升),同时增加了粒子的疏水性。在零ζ值之后,烷烃尾链间的疏水相互作用主导了进一步的吸附,新吸分子通过其尾链与已吸附分子尾链间的相互作用实现了在粒子表面的定向富集,这增加了粒子的正电性,也使粒子重新获得亲水性。以Gemini为例的吸附机理示意于图3中。从溶液表观看(图3),在零ζ值附近样品出现了明显的沉淀(图2两个箭头中间的区域),对应了吸附机理指明的疏水性粒子表面,在吸附更多表面活性剂使粒子重新呈现明显亲水性后,样品又再次澄清。
两个Gemini表面活性剂达到零ζ值对应的浓度Cz=0分别为0.049 mmol·L-1(s=2)和0.014 mmol·L-1(s=6),前者高于后者,这与Gemini的联接链长度有关。已知这个Gemini系列的联接链伸直长度(ds)可由下式计算:ds=0.127(s+1)24,ds分别为0.381 nm(s=2)和0.889 nm(s=6)。在它们的单体表面活性剂C12TABr胶束中,两个季铵头基的静电平衡距离约为0.9 nm24,相当于s=6时的联接链伸直长度,可见12-2-12的两个离子头基被强制性地拉近了距离。先前研究表明25,在这样超短的头基距离(s=2)下反离子的解离受到限制,12-2-12的正电性要小于+2,这使得中和微粒表面电荷要求的浓度要高于12-6-12。由于电性排斥减小,12-2-12分子可以排列得更紧密,更多的吸附使得它最终具有比12-6-12略微更高的正ζ值平台。二者吸附的比较示意图见图4。

图3 气相二氧化硅(0.05%(w))与12-2-12(a)或12-6-12(b)共存下的溶液表观照片Fig.3 Appearance of the dispersion of fumed silica particles(0.05%(w))in the presence of 12-2-12(a)and 12-6-12(b)with different concentrations

图4 Gemini表面活性剂双层吸附的示意图Fig.4 Schematic of the adsorbed bilayers of Gemini surfactants
3.2泡沫生成与稳定
泡沫的生成能力可以用Rv表征,其定义见式(1)。图5为Rv-lgC曲线,随着C增大,Rv增加至平台。平台值Rvmax分别为2.88(F-SiO2/12-2-12)和2.68(F-SiO2/12-6-12),表明这两个体系具有相近的泡沫生成能力,前者稍微更强些。

图5 F-SiO2(0.05%(w))/表面活性剂混合体系起泡性能(Rv)与表面活性剂浓度的半对数曲线Fig.5 Semilogarithmic plots of foamability(Rv)of F-SiO2(0.05%(w))/surfactant mixed systems against surfactant concentration
当泡沫塌陷至原先高度一半时的时间(t1/2)常用来表征泡沫的稳定性26。图6(a)为t1/2随12-2-12浓度变化的半对数曲线,可见当C增大,t1/2快速增大到极大值,然后下降至极小值后再一次增大到平台。图中同时给出单纯12-2-12(无F-SiO2)的t1/2曲线,它的t1/2随C单调上升至平台,这个平台值与F-SiO2/12-2-12的一致。结合微粒表面疏水化机理(3.1节),可解读F-SiO2/12-2-12曲线为:第一阶段的上升是由F-SiO2微粒吸附主导,随后的下降是微粒表面重新亲水后脱附所致,之后t1/2的再上升是过剩12-2-12的吸附。需要提到,即使是微粒吸附主导的阶段,并存的自由12-2-12吸附也同时进行,但参考单纯12-2-12的t1/2曲线可见,此时12-2-12对稳定泡沫的贡献很小。在微粒脱附后,表面活性剂浓度已达到其独自发挥效果的阶段,t1/2因此又重新上升。由这些讨论可见,固体粒子与12-2-12是在竞争和协同中发挥了稳定泡沫的作用。
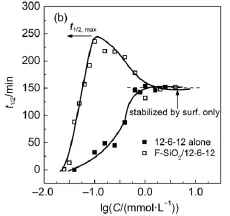
图6 泡沫稳定性(t1/2)与表面活性剂浓度(C)的半对数曲线Fig.6 Semilogarithmic plots of foam stability(t1/2)against surfactant concentration(C)
F-SiO2/12-6-12的t1/2曲线也呈现了上升再下降的过程。如3.1节讨论,12-6-12在F-SiO2粒子表面的覆盖不像12-2-12那样紧密,这样改性粒子的疏水性稍逊,这既影响它的t1/2极大值远不如F-SiO2/12-2-12体系,也应该是t1/2曲线的下降延续了一段较宽浓度范围的原因(图6(b))。在这个阶段,自由12-6-12的吸附已开始实质性地发挥稳定泡沫的作用,其结果掩盖了t1/2下降的极小值,直接使其趋向单纯12-6-12效应的平台。
对F-SiO2微粒主导吸附膜的阶段,极大值t1/2,max分别为820 min(F-SiO2/12-2-12)和245 min(F-SiO2/ 12-6-12)。前者是后者的3倍多,显示了明显更强的对泡沫的稳定能力。如上面讨论,比起12-6-12,12-2-12修饰的F-SiO2粒子具有更致密的烷烃链覆盖表面,它可以构成更理想的微粒主导的液膜,进而更好地稳定泡沫。上述比较都说明了联接链长度的影响,尽管两者长度只相差4个碳原子,但t1/2,max差了3倍多,体现了Gemini表面活性剂的魅力。

图7 F-SiO2/12-2-12(a)和单纯12-2-12(b)的界面扩张弹性(ε)随频率(v)变化的实验曲线Fig.7 Experimental plots of interfacial elasticity(ε)for F-SiO2/12-2-12(a)and single 12-2-12(b)aqueous solutions as a function of frequency(v)
3.3吸附膜的扩张粘弹性
图7为F-SiO2/12-2-12和单纯12-2-12在不同浓度时的扩张弹性ε随扰动频率v曲线,可见这些吸附膜的ε均依赖于v,不同扰动频率时ε的数值不同。扩张粘性η数值也同样依赖于扰动频率(曲线见图S1(见Supporting Information)),这与文献21,27报道一致。不同的扰动频率v意味着不同的响应时间,在低频扰动时,各种微观过程有足够的时间响应,包括粒子/表面活性剂在气/液界面的吸附和解吸,界面上吸附单元的重排等;当扰动频率高时,响应时间急剧减少甚至几乎消失,此时的吸附膜就像不溶膜28,29。

图8 F-SiO2/12-2-12(a)和单纯12-2-12(b)的界面扩张弹性ε与表面活性剂浓度的半对数图Fig.8 Semilogarithmic plots of dilational interfacial elasticity(ε)for F-SiO2/12-2-12(a)and 12-2-12(b)as a function of surfactant concentration
ε的变化也呈现出对表面活性剂的浓度依赖,图8直接给出ε与C关联图像。与单纯12-2-12相比(图8(b)),F-SiO2/12-2-12混合膜的ε出现了两个峰(图8(a))。F-SiO2/12-6-12的情况类似,也出现了两个ε峰(图S2)。对单纯表面活性剂吸附膜,ε-lgC的峰值现象已被归结为两个方面效应的结果27:一是浓度增加导致界面吸附量(Γ)增大,由此增加了膜的弹性;另一是加速了表面活性剂分子在界面和溶液体相之间的交换,这能快速抹平界面张力梯度dγ,降低ε。两个效应的综合结果表现为低浓度时由弹性增加主导,在高浓度时弹性减小,因此出现了极大值。当作为气泡稳定剂时,两亲性的固体微粒在很多方面与表面活性剂类似7。但是情况常常更加复杂30-32,例如当前观察到的两个ε-lgC极大值。
结合上两节讨论,F-SiO2/Gemini的两个ε-lgC峰应该分别对应F-SiO2粒子和Gemini混合吸附以及F-SiO2粒子脱附后的单纯12-2-12吸附,这是粒子吸附表面活性剂产生的表面疏水和再次亲水的结果。比较而言,F-SiO2/12-2-12混合膜的ε高于单纯的12-2-12,表明粒子稳定泡沫的效果更好。

图9 F-SiO2/12-2-12(a)和F-SiO2/12-6-12(b)体系的界面扩张弹性ε和泡沫稳定性t1/2的比较Fig.9 Comparison between interfacial elasticity(ε)and foam stability presented as t1/2for F-SiO2/12-2-12(a)and F-SiO2/12-6-12(b)
图9关联了粒子吸附阶段的膜弹性ε与泡沫稳定性t1/2,可见两者趋势很好地一致:膜弹性越强,气泡越稳定。在单纯表面活性剂稳定的泡沫体系中,这个结论已经被获得21,27,33-36。当前的结果表明,这个关联性不仅存在于纯表面活性剂稳定的泡沫体系,也适用固体微粒作为气泡稳定剂的场合。
4 结论
Gemini表面活性剂12-2-12和12-6-12都能有效地修饰F-SiO2。联接链长度强烈影响了Gemini表面活性剂对F-SiO2粒子的修饰,超短的s=2联接链造就的12-2-12由于反离子解离不完全,在粒子表面的初始吸附弱于12-6-12,但因此减少了吸附分子头基间的静电排斥,可以形成更致密的吸附层。改性F-SiO2粒子和表面活性剂分子在泡沫液膜的竞争和协同吸附可以很好地稳定泡沫,稳定效果优于单纯表面活性剂。相比较而言,F-SiO2/12-2-12稳定泡沫的效果更好,泡沫最大半衰期时间t1/2,max是F-SiO2/12-6-12的3倍多。与单纯表面活性剂稳定泡沫的体系类似,F-SiO2/Gemini构成的泡沫液膜其弹性越强,气泡也就越稳定。
References
(1)Wilson,A.J.Foams:Physics,Chemistry and Structure; Springer:Berlin,1989;p 233.
(2)Dicknson,E.Curr.Opin.Colloid Interface Sci.2010,15,40. doi:10.1016/j.cocis.2009.11.001
(3)Popp,N.;Kutuzov,S.;Boeker,A.Adv.Polym.Sci.2010,228, 39.doi:10.1007/12_2010_52
(4)Yang,X.C.;Mo,Z.H.Prog.Chem.2010,22,1735.
(5)Zhao,Y.;Jones,S.A.;Brown,M.B.J.Pharm.Pharmacol. 2010,62,678.doi:10.1211/jpp.62.06.0003
(6)Tang,C.;Xiao,E.;Sinko,P.J.;Szekely,Z.;Prud′homme,R.K. Colloids Surf.B 2015,133,81.doi:10.1016/j. colsurfb.2015.05.038
(7)Binks,B.P.Curr.Opin.Colloid Interface Sci.2002,7,21. doi:10.1016/S1359-0294(02)00008-0
(8)Horozov,T.S.;Aveyard,R.;Clint,J.H.;Binks,B.P.Langmuir 2003,19,2822.doi:10.1021/la020858x
(9)Horozov,T.S.;Aveyard,R.;Binks,B.P.;Clint,J.H.Langmuir 2005,21,7405.doi:10.1021/la050923d
(10)Aveyard,R.;Clint,J.H.;Nees,D.;Paunov,V.N.Langmuir 2000,16,1969.doi:10.1021/la990887g
(11)Aveyard,R.;Clint,J.H.;Nees,D.;Quirke,N.Langmuir 2000, 16,8820.doi:10.1021/la000060i
(12)Schwartz,H.;Harel,Y.;Efrima,S.Langmuir 2001,17,3884. doi:10.1021/la0100690
(13)Huang,S.;Minami,K.;Sakaue,H.;Shingubara,S.;Takahagi,T. Langmuir 2004,20,2274.doi:10.1021/la0302293
(14)Barthel,H.;Rösch,L.;Weis,J.Fumed Silica-Production, Properties,andApplications.In Organosilicon Chemistry Set: From Molecules to Materials;Auner,N.,Weis,J.Eds.;Wiley-VCH Verlag GmbH:Weinheim,1996;pp 761-778. doi:10.1002/9783527620777.ch91a
(15)Horozov,T.S.;Binks,B.P.;Aveyard,R.;Clint,J.H.Colloids Surf.A 2006,282-283,377.doi:10.1016/j.colsurfa.2005.11.085
(16)Katepalli,H.;Bose,A.Langmuir 2014,30,12736.doi:10.1021/ la502291q
(17)Tiberg,F.;Brinck,J.;Grant,L.Curr.Opin.Colloid Interface Sci.1999,4,411.doi:10.1016/S1359-0294(00)00016-9
(18)Somasundaran,P.;Huang,L.Adv.Colloid Interface Sci.2000, 88,179.doi:10.1016/S0001-8686(00)00044-0
(19)Zana,R.;Xia,J.D.Gemini Surfactants;Marcel Dekker Inc.: New York,2004.
(20)You,Y.;Zhao,J.X.;Jiang,R.;Cao,J.J.Colloid Polym.Sci. 2009,287,839.doi:10.1007/s00396-009-2038-8
(21)Wu,X.N.;Zhao,J.X.;Li,E.J.;Zou,W.S.Colloid Polym.Sci. 2011,289,1025.doi:10.1007/s00396-011-2425-9
(22)Binks,B.P.;Rodrigues,J.A.Colloids Surf.A 2009,345,195. doi:10.1016/j.colsurfa.2009.05.001
(23)Cui,Z.G.;Yang,L.L.;Cui,Y.Z.;Binks,B.P.Langmuir 2010, 26,4717.doi:10.1021/la903589e
(24)Danino,D.;Talmon,Y.;Zana,R.Langmuir 1995,11,1448. doi:10.1021/la00005a008
(25)Zheng,O.;Zhao,J.X.;You,Y.Chem.J.Chin.Univ.2002,23, 1352.[郑欧,赵剑曦,游毅.高等学校化学学报,2002,23, 1352.]
(26)Tehrani-Bagha,A.R.;Holmberg,K.Langmuir 2010,26,9276. doi:10.1021/la1001336
(27)Stubenrauch,C.;Miller,R.J.Phys.Chem.B 2004,108,6412. doi:10.1021/jp049694e
(28)Lucassen,J.;van den Tempel,M.Chem.Eng.Sci.1972,27, 1283.doi:10.1016/0009-2509(72)80104-0
(29)Monroy,F.;Rivillon,S.;Ortega,F.;Rubio,R.G.J.Chem.Phys. 2001,115,530.
(30)Liggieri,L.;Santini,E.;Guzman,E.;Maestro,A.;Ravera,F. Soft Matter 2011,7,7699.doi:10.1039/C1SM05257H
(31)Guzmán,E.;Liggieri,L.;Santini,E.;Ferrari,M.;Ravera,F.Soft Matter 2012,8,3938.doi:10.1039/C2SM07097A
(32)Guzmán,E.;Santini,E.;Ferrari,M.;Liggieri,L.;Ravera,F.J. Phys.Chem.C 2015,119,21024.doi:10.1021/acs.jpcc.5b07258
(33)Espert,A.;Klitzing,R.V.;Poulin,P.;Colin,A.;Zana,R.; Langevin,D.Langmuir 1998,14,4251.doi:10.1021/la9800957
(34)Bergeron,V.Langmuir 1997,13,3474.doi:10.1021/la970004q
(35)Santini,E.;Ravera,F.;Ferrari,M.;Stubenrauch,C.;Makievski, A.;Krägel,J.Colloids Surf.A 2007,298,12.doi:10.1016/j. colsurfa.2006.12.004
(36)Georgieva,D.;Cagna,A.;Langevin,D.Soft Matter 2009,5, 2063.doi:10.1039/B822568K
Foams Stabilized by Fumed Silica Particles with a Quaternary Ammonium Gemini Surfactant
SUN Xiao-XiangCHEN YuZHAO Jian-Xi*
(Institute of Colloid and Interface Chemistry,College of Chemistry and Chemical Engineering, Fuzhou University,Fuzhou 350108,P.R.China)
Fumed silica(F-SiO2)particles were hydrophobized in situ in aqueous solutions of alkanediyl-α,ωbis(dodecyldimethylammonium bromide)(12-s-12,s=2,6)gemini surfactants.This process was assessed using zeta potential measurements.The particles were found to transit from their original hydrophilic nature to hydrophobic and then back to hydrophilic with increases in the surfactant concentration(C).The hydrophobic particles could spontaneously adsorb at the air/water interface,resulting in significant stabilization of aqueous foams.The re-hydrophilic particles desorbed from the interface,leaving only surfactant molecules to stabilize the foam.The strong interfacial elasticity of the surface films was reflected in the highly stable foams.The length of the surfactant spacer also affected the adsorption of the gemini surfactant on the F-SiO2particles,and therefore had an effect on the elasticity of the adsorbed film and the stability of the foam.The 12-2-12 surfactant, having a relatively short spacer,carried less positive charges because of the incomplete dissociation of its counter ions,resulting in less initial adsorption on the F-SiO2particles compared with the 12-6-12,but eventually formed a denser monomeric layer because of decreased repulsion between the adsorbed molecules.The 12-2-12 exhibited stronger adsorption at the air/water interface;therefore,the synergistic action of the F-SiO2particles together with the 12-2-12 produced better foam stabilization compared with the 12-6-12.
Fumed silica particle;Gemini surfactant;Surface modification;Foam stability
March 8,2016;Revised:April 28,2016;Published on Web:May 4,2016.
O647
10.3866/PKU.WHXB201605042
*Corresponding author.Email:jxzhao.colloid@fzu.edu.cn;Tel:+86-591-22866338.
The project was supported by the National Natural Science Foundation of China(21273040,21473032).
国家自然科学基金(21273040,21473032)资助项目
©Editorial office ofActa Physico-Chimica Sinica
[Article]
