亚硫酸钠还原法制备氧化亚铜工艺优化研究*
2016-09-01王胜广王守绪
王胜广,何 为,王 翀,王守绪,谭 泽
(1 电子科技大学微电子与固体电子学院,四川 成都 610054;2 广东光华科技股份有限公司,广东 汕头 515061)
亚硫酸钠还原法制备氧化亚铜工艺优化研究*
王胜广1,2,何为1,2,王翀1,2,王守绪1,谭泽2
(1 电子科技大学微电子与固体电子学院,四川成都610054;2 广东光华科技股份有限公司,广东汕头515061)
采用优化试验方法,通过对亚硫酸钠还原法制备超细Cu2O粉末的工艺路线优化,获得了不添加表面活性剂情况下高纯Cu2O制备工艺参数。利用X射线粉末衍射仪(XRD)、扫描电镜等对最优工艺参数条件下制备的样品进行了表征。结果表明,未添加表面活性剂的最优试验条件下制备Cu2O的粒径为2 μm左右、含量为99.3%,样品中Cu2O、杂质等含量均优于HG2961-2010标准中优等品的要求。
氧化亚铜;亚硫酸钠还原法;优化试验方法
氧化亚铜以其具有特殊的光学、光电和催化性能,在涂料、玻璃、陶瓷、农业以及有机工业催化剂等领域应用广泛,现已成为材料科学研究的热点[1-2]。目前,制备氧化亚铜的方法主要有有固相法、液相法和电解法[3]。固相法制备氧化亚铜具有能耗大,三废污染严重,而且不容易制备颗粒小、纯度高的氧化亚铜的缺点[4-5]。Cu2O 的电解法制备通常是以金属Cu 作阳极在含铜离子的溶液中电解, 在阴极上得到纯度较高的氧化亚铜粉体,但是电解法电耗高、生产效率低而且为了有效地抑制电解过程中CuO和阴极区海绵状铜粉的生成, 电解时需加入NaNO2和Na2Cr2O7等添加剂, 这不符合绿色化学的要求[6-7]。液相法制备Cu2O 粉末是近年来发展最快的方法,该方法制备的氧化亚铜粒径小,纯度高,分散性好[8]。
由于工业氧化亚铜HG2961-2010标准的实施,对于氧化亚铜产品的要求也随之提高。张萍等[4]用亚硫酸钠还原法制备氧化亚铜工艺所制备的氧化亚铜产品已经不能满足新标准,故迫切需要新的优化工艺来提高产品质量。张萍等通过添加明胶、十六烷基三甲基溴化铵等添加剂来改善氧化亚铜颗粒大小均匀性,最终制得产品粒径在10 μm左右,有机添加剂的使用既增加了成本,也增大了后处理的难度。而且,新标准中增加了对硫酸盐含量控制(≤0.5),根据张萍等[9]的实验条件进行实验发现,硫酸盐含量在1%以上,不符合标准。在氧化亚铜制备过程中硫酸盐的含量过高是影响氧化亚铜产品质量的最关键因素。所以本实验通过优化反应过程,将硫酸铜溶液与亚硫酸钠溶液在60 ℃条件下反应0.5 h后再加入碳酸钠调节反应pH,既可以降低产品中硫酸盐含量也可以提高氧化亚铜含量。通过正交试验优化反应物浓度、反应液pH、温度、反应时间等因素,在不需要添加表面活性剂的情况下,使制备的氧化亚铜产品纯度在99%以上,硫酸盐含量在0.5%以下。
1 实 验
1.1实验仪器和试剂
HH-8型数显恒温水浴锅;DZF型真空干燥箱;WBF型玻璃反应釜;X-650型场发射电子显微镜(FESEM),日本日立公司;X-射线衍射仪(Cu靶,管流30 mA,管压40 kV),日本岛津XRD-6000。
五水硫酸铜(AR)、无水亚硫酸钠(AR)、碳酸钠(AR)、无水乙醇(AR)、二次蒸馏水。
1.2实验过程
将适量亚硫酸钠溶液、硫酸铜溶液分别预热至60 ℃,然后混合,同时强力搅拌,反应0.5 h后,滴加碳酸钠溶液,控制反应液pH,反应完全后经二次蒸馏水水洗数次,离心分离后将样品置于80 ℃真空干燥箱中干燥,即得鲜红色氧化亚铜粉末。
1.3样品表征
根据HG2961-2010标准中的测试方法,测试样品的各项指标;采用X射线衍射仪表征产物的物相组成;采用扫描电镜表征产物的形貌。
2 结果与讨论
2.1硫酸盐含量优化实验
通过一系列探索性实验后,发现影响产品氧化亚铜中硫酸盐含量最大的因素是反应液pH,反应过程要控制pH。在硫酸铜浓度300 g/L(还原剂Na2SO3的用量为理论量的1.2倍)、温度363 K、反应时间2 h等条件下,研究反应液pH对硫酸盐含量的影响。实验结果如图1所示。

图1 反应pH对含量的影响
由图1可以看出随着反应pH的增大,硫酸盐含量逐渐减少。当pH<5时,硫酸盐含量很大,而且通过增加洗涤次数的方式也不会降低硫酸盐的含量;当pH>5时,硫酸盐含量基本趋于稳定而且含量低于0.5%,满足工业标准HG2961-2010最高标准。
2.2正交分析
为探讨影响产物中Cu2O含量的因素,对反应物浓度、反应液pH、温度、反应时间等四项基本因素进行正交分析(其中还原剂Na2SO3的用量为理论量的1.2倍),正交试验结果及分析见表1。

表1 正交实验结果与极差分析
续表1

43582.56005.588.753631400586.463631.53005.587.373632600481.583632.5500484.2936815005.595.1103681.5600596.41136823004.594.4123682.5400492.11337316004.596.5143731.5500498.71537324005.597.3163732.5300599.3K184.7288.5789.3387.15K284.8591.0589.489.22K394.591.3292.5393.55K497.9591.0790.7792.1R13.232.753.26.4
由表1可以看出,影响Cu2O含量的四个因素中反应温度的极差(13.23)最大,说明反应温度的变化对Cu2O的含量影响最大,是主要因素,其次是反应液pH、反应物浓度、反应时间。分析表明制备高纯度Cu2O的最佳条件为反应温度100 ℃、pH=5、反应物浓度500 g/L、反应时间2 h。在此条件下制备获得到样品的X射线衍射谱图如图3所示。

图2 Cu2O含量与反应条件关系图
2.2.1反应温度对Cu2O含量的影响
反应温度对提高Cu2O的含量有很大的影响,随着反应温度的升高Cu2O含量逐渐增加,如图2a所示,升高反应温度不仅可以提高反应速率,而且可以提高Cu2O的含量。这是因为在反应过程中会产生SO2气体,从而使溶液pH降低,不利于Cu2O的生成,升高反应温度,有利于SO2气体从溶液中挥发。所以在水溶液中,温度宜控制在100 ℃左右,以保持其沸腾状态。
2.2.2反应时间对Cu2O含量的影响
反应时间与Cu2O含量的关系如图2b所示。Cu2O含量随着时间的增加先增加后减少,反应时间是2 h时,Cu2O含量最高。这说明在随着反应时间的增加时,还原的Cu(OH)分解为Cu2O越充分,2 h后,基本完全分解为Cu2O,之后,继续增加时间,反而会使Cu2O被氧化为CuO。
2.2.3反应物浓度对Cu2O含量的影响
反应物硫酸铜浓度与Cu2O含量的关系如图2c所示。Cu2O含量随着反应物硫酸铜浓度的增加先增加后减少,硫酸铜浓度为500 g·L-1时,Cu2O含量最高,所以硫酸铜浓度宜控制在500 g·L-1。
2.2.4溶液pH对Cu2O含量的影响
溶液pH对Cu2O含量的关系如图2d所示。Cu2O含量随着pH的增加先增加后减少。溶液pH=5时,Cu2O含量最高。pH小于5时,还原的Cu(OH)不易分解为Cu2O。pH大于5时,容易生成CuO。
2.3XRD分析
图3为最优反应控制参数条件下制备Cu2O粉体的XRD图。
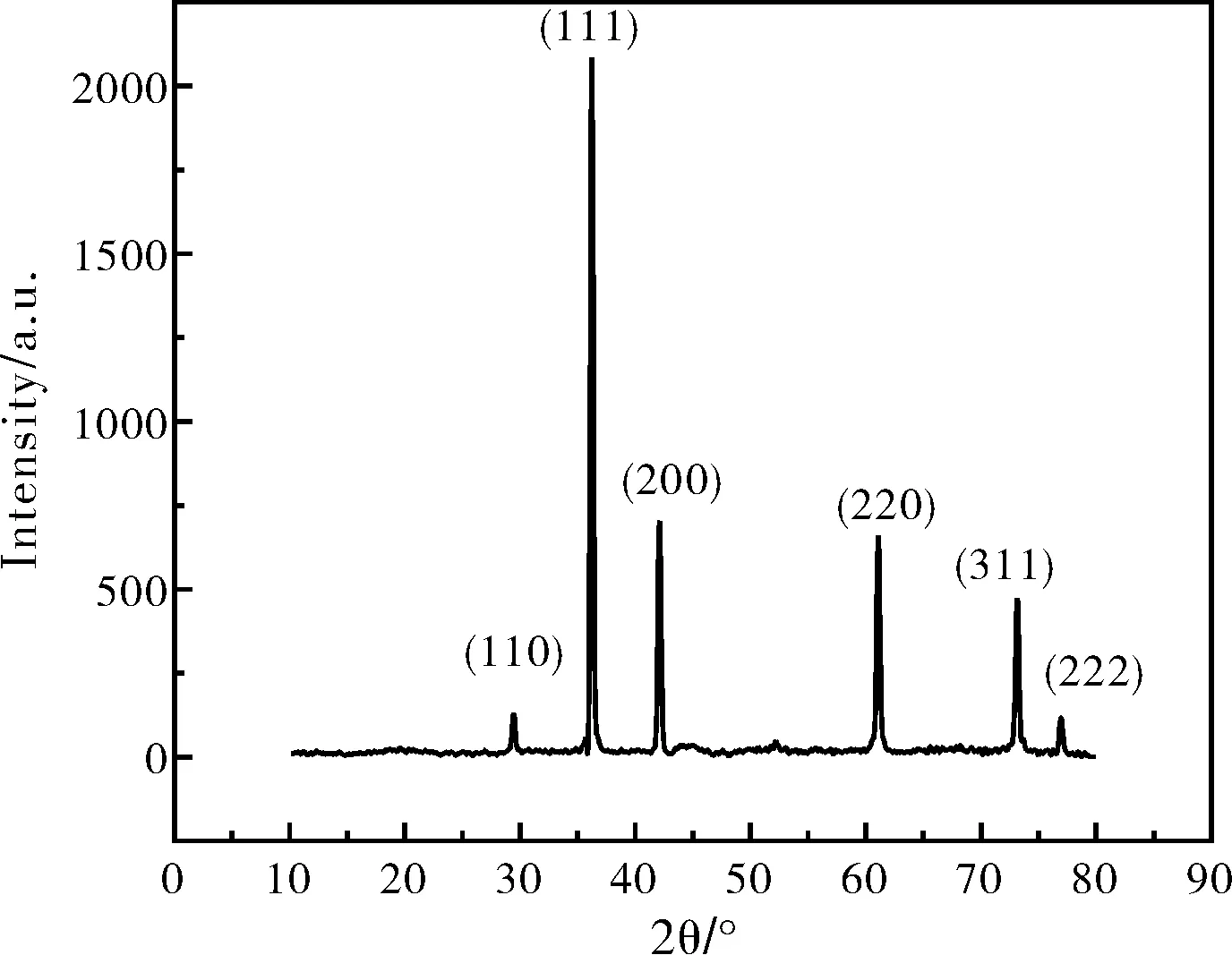
图3 制备Cu2O样品的XRD图
从图3可以看出,与标准卡片(78-2076)吻合,呈立方相Cu2O的结构,属于立方晶系。衍射峰从左到右分别对应于立方相Cu2O的(110)、(111)、(200)、(220)、(311)及(222)晶面。由图中的谱线可以看出,除Cu2O的衍射峰外,没有发现CuO和Cu的衍射峰。
2.4SEM分析
图4为最优反应组合条件下制备样品的SEM照片。从图4可以看出,实验所制得Cu2O主要以八面体形颗粒为主,粒径较为均一,产品分散性好,粒径在2 μm左右。

图4 制备Cu2O样品的SEM图
3 结 论
通过优化亚硫酸钠还原硫酸铜制备Cu2O,得到最优反应条件组合:反应温度100 ℃、pH=5、反应物浓度500 g/L、反应时间2 h。根据HG2961-2010标准中的测试方法,测试样品的各项指标,总还原率、硫酸盐含量、稳定性实验后还原率减少量等各项指标均能满足该标准中优等品的要求。在此工艺条件下不需要添加任何表面活性剂,Cu2O纯度可达99%以上,粒径1~3 μm,晶型完整。
[1]胡敏,周康根,陈瑞英.超细氧化亚铜粉体的制备与应用[J].中国粉体技术,2006(5):44-48.
[2]舒余德.电解法制备氧化亚铜的研究[J].沈阳化工,1991(3):11-13.
[3]柳建,舒余,陈白珍.电解法制取氧化亚铜的研究[J].湖南冶金,1996(6): 12-14.
[4]张萍,刘恒,李大成.亚硫酸钠还原法制备超细氧化亚铜粉末[J].四川有色金属,1998(2): 16-18.
[5]朱俊武,陈海群,谢波,等.纳米Cu2O的制备及其对高氯酸铵热分解的催化性能[J].催化学报,2004,25(8): 637-640.
[6]翟纪伟,高荣杰,姜魁光,等.均相还原法制备氧化亚铜微晶及粒径控制[J].材料导报,2009,23(9):107-112.
[7]毕文团.氧化亚铜制备方法的研究进展[J].广州化工,2009,37(8):56-58.
[8]靳正国,郭瑞松,师春生,等.材料科学基础[M].天津:天津大学出版社, 2005: 321
[9]中华人民共和国工业和信息化部,HG2961-2010工业氧化亚铜[S].北京:化学工业出版社,2011.
Optimization of Processes for Preparation of Cuprous Oxide by Sodium Sulfite Reduction*
WANGSheng-guang1,2,HEWei1,2,WANGCong1,2,WANGShou-xu1,TANZe2
(1 School of Microelectronics and Solid-state Electronics, University of Electronics and Technology of China, Sichuan Chengdu 610054;2 Guangdong Guanghua Sci-Tech Co., Ltd., Guangdong Shantou 515000, China)
By optimizing of processes for preparation of cuprous oxide by sodium sulfite reduction, the technological parameters of the high pure Cu2O were got without adding surfactant preparation. The powders were characterized by X-rays diffraction(XRD) and scanning electron microscopy(SEM). The test results showed that under the best conditions, Cu2O content in sample was 99.3%, the content of impurities met HG2961-2010 standard.
cuprous oxide; sodium sulfite; optimization of test methods
广东省引进创新科研团队计划项目(No. 201301C0105324342)。
王胜广(1990-),男,在读硕士研究生,主要从事电子化学品领域研究。
何为。
TQ632.4
A
1001-9677(2016)02-0044-03
