免疫佐剂治疗儿童呼吸道感染临床疗效的Meta分析*
2016-08-29郑丽丽姚莉范芳芳胡兰李治纲
郑丽丽,姚莉,范芳芳,胡兰,李治纲
(1.新疆医科大学附属中医医院 药学部,新疆 乌鲁木齐 830054;2.喀什地区第二人民医院 药学部,新疆 乌鲁木齐 830000)
免疫佐剂治疗儿童呼吸道感染临床疗效的Meta分析*
郑丽丽1,姚莉1,范芳芳1,胡兰1,李治纲2
(1.新疆医科大学附属中医医院 药学部,新疆 乌鲁木齐 830054;2.喀什地区第二人民医院 药学部,新疆 乌鲁木齐 830000)
目的采用Meta分析方法评价免疫佐剂治疗儿童反复呼吸道感染的临床疗效和安全性。方法计算机检索EMBASE(1974年9月-2013年9月)、PUBMED(1966~2013年)、The Cochrane Register of Controlled Trials(2013年第1期)和VIP(1989年9月~2013年9月),万方数据库(1994年1月-2013年9月),CNKI(1979年1月-2013年9月),手工检索最近1年国内已发表的相关论文及会议资料。按照纳入与排除标准选择文献、提取资料和评价纳入研究的方法学质量后,采用Cochrane协作网提供的RevMan 5.3软件进行Meta分析。结果共纳入13个研究,1 088例患儿。Meta分析结果显示,免疫佐剂+常规治疗组能提高患儿的T淋巴细胞亚群CD3(WMD=7.97;95%CI:5.6,10.34;P=0.000)、CD4(WMD=5.44;95%CI:1.27,9.6;P=0.010)水平,提高免疫球蛋白IgA(WMD=0.43;95%CI:0.08,0.77;P=0.010),IgG(WMD=1.07;95%CI:0.25,1.89,P= 0.000)水平;延缓RRI发作天数(WMD=-5.14;95%CI=6.72,3.56;P=0.040);对CD8(WMD=0.7;95%CI:0.19,1.59;P=0.130)及CD4/CD8(WMD=0.25;95%CI:0.04,0.45;P=0.130)及免疫球蛋白IgM(WMD=0.04;95%CI:-0.05,0.12;P=0.370)和不良反应发生率(WMD=1.5;95%CI:0.52,4.28;P=0.450)试验组与对照组之间差异无统计学意义。结论基于现有临床证据,免疫佐剂联合常规治疗可有效治疗儿童反复呼吸道感染,安全性好。但由于纳入研究数量少,研究质量不统一,本结论尚需要更多大样本、高质量的RCT予以证实。
免疫佐剂;儿童反复呼吸道感染;系统评价;meta分析
反复呼吸道感染(recurrent respiratory infection,RRI)是儿童的常见病,患儿病情常反复发作、迁延不愈,严重影响儿童的生长发育。有关RRI的病因与发病机制尚不完全清楚,发病原因是多方面的,现代医学认为,RRI主要与儿童免疫功能低下、T细胞功能紊乱、及营养、感染、遗传等因素有关,其发病率约为10%[1]。近年来研究认为,其发病机制与儿童的细胞免疫功能低下有关,主要与T淋巴细胞亚群的失调密切相关[2]。国内常用的免疫佐剂有脾氨肽口服冻干粉、匹多莫德和细菌溶解产物(泛福舒)。目前国内免疫佐剂治疗RRI的经验性报道不少,但质量参差不齐,对RRI各种具体症状的改善程度亦缺少系统性分析。本研究采用Meta分析方法总结分析免疫佐剂治疗儿童反复呼吸道感染的临床试验,以期为临床实践提供证据。
1 资料与方法
1.1纳入与排除标准
1.1.1研究类型所有单用或联用免疫佐剂(脾氨肽、匹多莫德或细菌溶解产物)与常规药物(抗感染药物:阿奇霉素/克拉霉素,对症治疗)比较治疗RRI患者疗效的随机对照试验,文种限定于英文和中文。
1.1.2研究对象参照《诸福棠实用儿科学》第7版所制订的肺炎支原体感染诊断标准[3],患儿出现反复咳嗽、发热、鼻黏膜出血及肺部呼吸音异常等症状。每年出现上呼吸道感染5次,下呼吸道感染4次且其年龄小于2岁;每年患上呼吸道感染4次或是下呼吸道感染3次且其年龄小于6岁大于3岁者;每年上呼吸道感染3次,下呼吸道感染2次且年龄小于15岁大于7岁的患者。
1.1.3干预措施试验组:单用免疫佐剂(脾氨肽、匹多莫德或细菌溶解产物)或免疫佐剂(脾氨肽、匹多莫德或细菌溶解产物)+常规药物,对照组:常规药物(抗感染药物:阿奇霉素/克拉霉素,对症治疗)。
1.1.4测量指标主要结局:症状、体征、实验室检查及病原学检查。次要结局:不良反应发生率。
1.1.5排除标准排除原始研究数据不能运用的研究。
1.2文献检索
计算机检索1966年1月-2013年9月国内外生物医学期刊发表的关于免疫佐剂(脾氨肽、匹多莫德或细菌溶解产物)单用或联用常规药物与常规药物治疗比较,治疗RRI的相关文献检索PubMed(1966年-2013年9月)、EMbase(1974年-2013年9月)和CoChrane图书馆(2013年第1期)及发现国内研究者在非中文期刊上发表的非重复报告。同时,追溯检索所得论文的参考文献寻找相关的研究。
1.3文献质量评价
文献质量评价采用Cochrane Handbook 5.2[4]的标准,推荐的质量评价标准:①随机方法是否正确;②是否实施分配方案隐藏;③是否采用盲法;④是否存在缺失数据所致偏倚;⑤是否存在选择性报道所致偏倚;⑥是否存在其他类型的偏倚。每条质量标准按达到情况划分为“是”、“否”、“不清楚”。
1.4统计学方法
采用Review Manager 5.3统计软件进行数据分析。计数资料采用比值比为效应量,计量资料用均数差为效应量,均给出其95%CI[5-7]。各研究间异质性用χ2检验[8]。当各研究间有统计学异质性(P>0.05,I2<25%)时,采用固定效应模型;反之采用随机效应模型。当研究间出现异质性,应尽量找出异质性的来源。对于二分类变量,采用相对危险度及95%可信区间(Confidenceinterval,CI)表示疗效分析统计量;对于连续性资料,采用加权均数差及95%CI为疗效分析统计量。潜在的发表偏倚采用“倒漏斗”图示分析,并对纳入文献试验偏倚进行讨论。
2 结果
2.1纳入研究的一般情况及质量评价
初检共获得75篇中文文献,3篇英文文献,通过阅读文题及摘要,排除明显不相关的文献以及综述、会议报道及重复发表的文献后,共纳入18篇文献。进一步阅读全文复筛,排除空白研究、临床观察、以及干预方式不符合纳入标准、数据不完整的文献后,最终纳入13篇文献,共1 088例患儿。其中,对照组544例,试验组553例。文献检索流程见图1。
2.2纳入研究的基本特征
纳入研究试验特征与风险偏倚评价,结果见附表和图 2。13篇均为随机对照试验(randomized controlled trial,RCT),10篇中文,3篇英文。其中,3篇描述不良反应的发生情况[10,15,17],5篇研究[9-13]以脾氨肽为研究对象,2篇[14-15]研究以匹多莫德为研究对象,6篇[12,14-18]研究以细菌溶解产物为研究对象。经Cochrane协作网所推荐的文献质量评价工具所示,纳入所有文献均具有可纳入Meta分析的质量。见图2。
2.3Meta分析结果
2.3.1免疫佐剂对T淋巴细胞亚群CD3的影响共纳入6个研究[9-10,13-15,17],治疗期最长6个月(P= 0.000,I2=93%),故采用随机效应模型进行Meta分析。图3表明联用免疫佐剂提高患者的CD3水平优于对照组。试验组CD3明显高于对照组(WMD= 7.97;95%CI:5.6,10.34;P=0.000),差异有统计学意义。表明脾氨肽+常规治疗可以显著提高患儿的CD3。
2.3.2免疫佐剂对T淋巴细胞亚群CD4的影响共纳入5个研究[9-10,13-15],(P=0.000,I2=95%)故采用随机效应模型进行Meta分析。试验组CD4明显高于对照组(WMD=5.44;95%CI:1.27,9.6;P=0.010),差异有统计学意义。表明脾氨肽+常规治疗可以显著提高患儿的CD4。见图4。
2.3.3免疫佐剂对T淋巴细胞亚群CD8的影响共纳入5个研究[9-10,13-15],(P=0.000;I2=94%),故采用随机效应模型进行Meta分析。试验组CD8未明显高于对照组(WMD=0.70;95%CI:0.19,1.59;P=0.130),差异无统计学意义。见图5。

图1 文献检索流程图
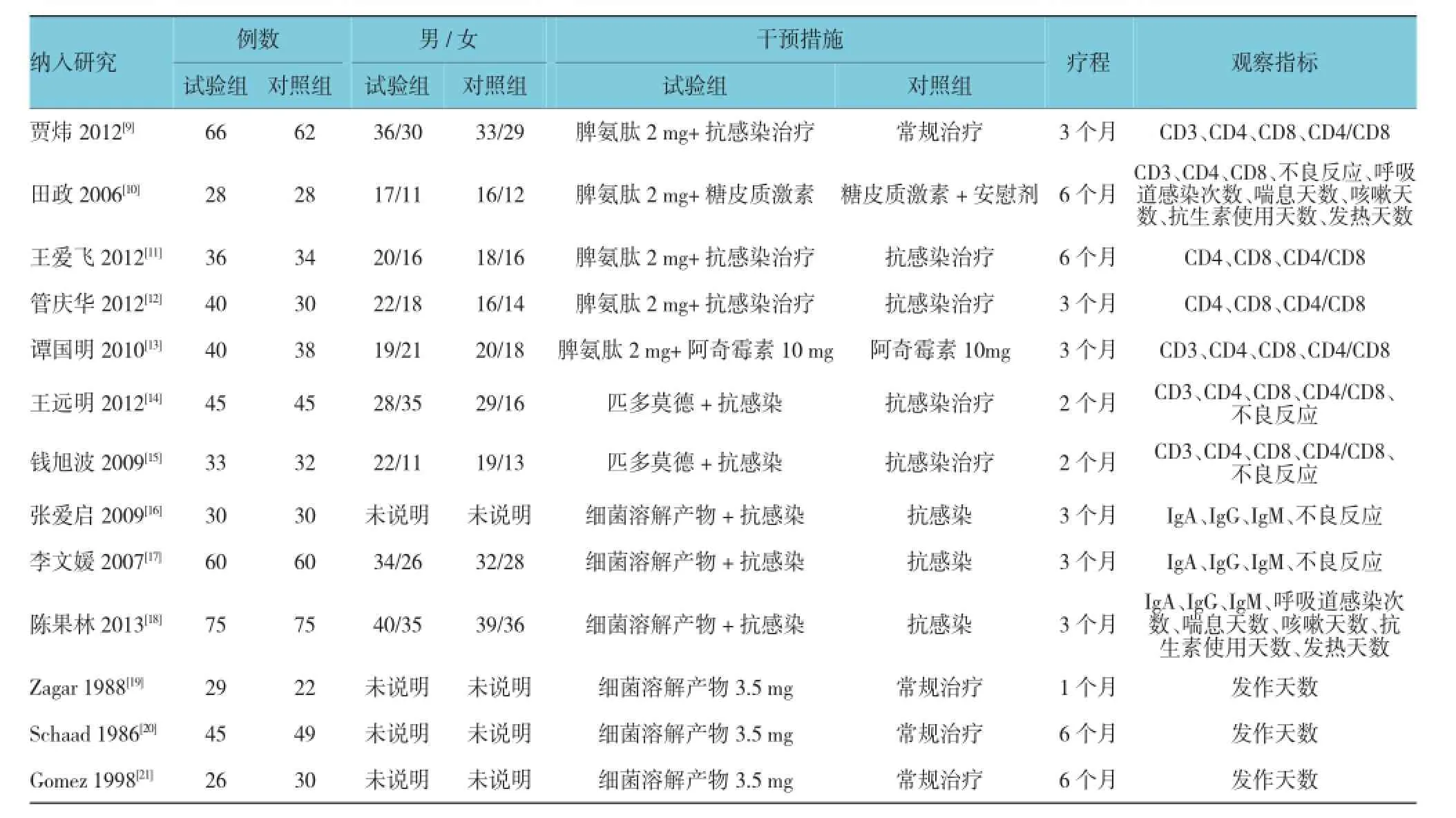
附表 纳入Meta分析研究的主要特征
2.3.4免疫佐剂对T淋巴细胞亚群CD4/CD8的影响共纳入5个研究[9-10,13-15],(P=0.000,I2=94%),故采用随机效应模型进行Meta分析。试验组CD4/CD8未明显高于对照组(WMD=0.25;95%CI:0.04,0.45;P=0.130),差异无统计学意义。见图6。
2.3.5免疫佐剂对免疫球蛋白IgA的影响共纳入3个研究[16-18],(P=0.000,I2=96%),故采用随机效应模型进行Meta分析。试验组IgA明显高于对照组(WMD=0.43;95%CI:0.08,0.77;P=0.010),差异有统计学意义。见图7。
2.3.6免疫佐剂对免疫球蛋白IgG的影响共纳入3个研究[16-18],(P=0.000;I2=88%),故采用随机效应模型进行Meta分析。试验组IgG明显高于对照组(WMD=1.07;95%CI:0.25,1.89;P=0.010),差异有统计学意义。见图8。
2.3.7免疫佐剂对免疫球蛋白IgM的影响共纳入3个研究[16-18],各纳入研究间无统计学异质性(P= 0.150,I2=47%),采用固定效应模型进行Meta分析,结果显示两组差异无统计学意义(WMD=0.04,95%CI:-0.05,0.12;P=0.370),故尚不能认为联用免疫佐剂组和对照组比较对提高IgM有差异。见图9。

图2 纳入研究风险偏倚评价结果
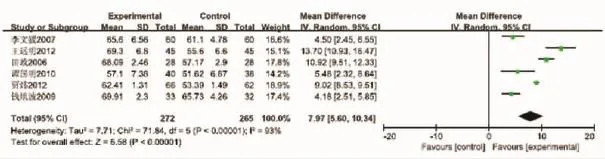
图3 免疫佐剂与常规治疗对CD3影响的Meta分析

图4 免疫佐剂与常规治疗对CD4影响的Meta分析

图5 免疫佐剂与常规治疗对CD8影响的Meta分析

图6 免疫佐剂与常规治疗对CD4/CD8影响的Meta分析

图7 免疫佐剂与常规治疗对IgA影响的Meta分析

图8 免疫佐剂与常规治疗对IgG影响的Meta分析

图9 免疫佐剂与常规治疗对IgM影响的Meta分析

图10 免疫佐剂泛福舒与常规治疗对RRI发作天数影响的Meta分析

图11 不良反应的发生情况
2.3.8免疫佐剂细菌溶解产物对RRI发作天数的影响共纳入3个研究[19-21],根据异质性提示(P=0.030;I2=70%),故采用随机效应模型进行Meta分析。试验组较对照组能延缓RRI发作的天数(WMD=-4.01;95%CI:-7.93,-0.10;P=0.040),差异有统计学意义。见图10。
2.4不良反应发生情况分析
3个研究[10,15,17]报道了不良反应发生率。各研究间异质性差异无统计学意义(P=0.550;I2=0%),采用固定效应模型进行Meta分析,结果显示两组差异无统计学意义(WMD=1.50;95%CI:0.52,4.28)即联用免疫佐剂组和对照组比较不良反应发生率无差异。见图11。
2.5发表性偏倚
以免疫佐剂治疗对CD3、CD4、CD8、CD4/CD8、IgA、IgG、IgM、RRI发作天数的影响进行倒漏斗图分析,免疫佐剂对CD3、CD4、CD8、CD4/CD8、IgA、IgG、IgM、RRI发作天数影响的发表性偏倚结果见图12A、12B、12C、12D、12E、12F、12G、12H。结果显示,图12A和图12B中的散点集中分布在无效线两侧,漏斗图基本对称,提示根据CD3、CD4纳入文献存在发表偏倚的可能性小。图12C中的散点主要集中在无效线的左侧,提示根据CD8纳入的文献存在一定程度的发表偏倚。图12D中的散点主要集中在无效线的两侧较均匀分布,提示纳入的文献存在发表偏倚的可能性小。图12E、图12F、图12G中的散点在无效线两侧不均匀分布,提示纳入的文献存在一定程度的发表偏倚。分析原因可能为本研究在评价过程中发现多数文献并未对儿童反复呼吸道感染的患儿病因、年龄及病程进行具体描述,仅仅在文中提及治疗组和观察组在病因、年龄和病程上没有统计学意义。其次对于部分失访的患儿及部分阴性结果未报道等可能是导致发表偏倚的可能原因。另外图12E、图12F、图12G、图12H分别纳入的文献只有3篇,样本量偏小,其可能是导致发表偏倚的另一个原因。见图12。

图12 发表性偏倚漏斗图
3 讨论
儿童反复呼吸道感染临床发病率高,该病发病机制较为复杂,目前广泛认为与患儿免疫系统有密切关联性。脾氨肽冻干粉主要成分为肽及核苷酸类复合物,含有多种氨基酸和免疫调节因子,具有促进干扰素及淋巴因子释放的机能。匹多莫德口服液是人工合成的唯一口服具有生物活性和免疫活性的生物反应调节剂,其本身不具有抗感染活性,通过刺激和调节免疫反应的不同阶段起免疫增强效应。细菌溶解产物是免疫调节剂之一,是由8种细菌冻干溶解物组成,具有激发呼吸系统特异性和非特异性免疫的特点,可加快淋巴细胞的循环,提高唾液中lgA分泌水平。lgA是机体黏膜局部抗感染的重要的免疫因子。
本研究结果显示,在常规治疗的基础上联合免疫佐剂治疗反复呼吸道感染是安全的,有利于改善总体症状。免疫佐剂+常规治疗总体疗效高于常规药物治疗,免疫佐剂能够增强患儿抗病能力,而RRI的病因与小儿机体免疫功能未完善及免疫功能异常有关,儿童处于生理性免疫功能低下状态,易受细菌和病毒感染的侵袭,极易发生呼吸道感染,而免疫佐剂可以刺激非特异性免疫及特异性免疫,显著减少呼吸道感染的发作次数,减少RRI的复发,减少患儿反复或长时间使用抗生素,避免耐药细菌产生,免疫佐剂相对常规治疗没有增加不良反应发生率,故具有良好的安全性。
本研究局限性:①纳入研究均未描述具体的随机方法和隐蔽分组,研究结果测量均未实施盲法。因此,存在高度选择性偏倚、实施偏倚和测量性偏倚的可能。②由于检索条件限制,检索可能不全而漏掉一部分文献。③纳入资料均为已发表文献,评估中可能漏掉阴性结果的研究,存在发表偏倚。④本系统评价所比较的指标存在一定的异质性,因此需要谨慎看待结论。
由于纳入分析的大多研究样本量小,方法学质量均偏低,仍需要更大规模的前瞻性随机对照双盲试验进一步证实免疫佐剂治疗的有效性及安全性。并且,在中国人群中针对免疫佐剂的探索也仍需持续,包括对免疫佐剂作用机制的基础研究以及在RRI中发挥的作用有待进一步研究。
[1]GENEL F,ATLIHAN F,GULEZ N,et al.Proper indeficiency in a boy with fulm inant men in go septic shock[J].Act Paediatr,2006,95(11):1498-1500.
[2]韩瑞珠,郝艳艳,侯安存.反复呼吸道感染儿童细胞免疫及体液免疫状况[J].实用儿科临床杂志,2008,23(10):736-737.
[3]胡亚美,江载芳.诸福棠实用儿科学[M].北京:第7版.人民卫生出版社,2002:559-621.
[4]PT-HIGGINS J,GREEN S.Cochrane Handbook for Systematic Reviews of Interventions[M].The Cochrance Collaboration,2011(3).
[5]陈耀龙,蔡羽嘉,王梦书,等.循证医学术语介绍Ⅱ[J].中国循证医学杂志,2009,9(2):143-146.
[6]吴泰相,商洪才,卞兆祥.随机对照实况试验的概念,设计和实施[J].中国循证医学杂志,2009,9(12):1277-1280.
[7]陈耀龙,李晓,梅又文,等.循证医学术语介绍[J].中国循证医学杂志,2009,9(7):734-739.
[8]王丹,翟俊霞,牟振云,等.Meta分析中的异质性及其处理方法[J].中国循证医学杂志,2009,9(10):1115-1118.
[9]贾炜.脾氨肽佐治68例小儿反复呼吸道感染临床观察[J].中国社区医师(医学专业),2012(21):130.
[10]田政,钱旭波.脾氨肽对儿童哮喘合并反复呼吸道感染的疗效观察[J].临床儿科杂志,2006(7):600-602.
[11]王爱飞,叶建敏,胡文辉,等.脾氨肽治疗和预防儿童反复呼吸道感染发作的疗效及对T淋巴细胞亚群的影响[J].中国药物与临床,2012(11):1457-1458.
[12]管庆华.脾氨肽口服冻干粉治疗反复呼吸道感染的疗效及对患儿免疫功能的影响观察[J].中国基层医药,2012(19):919-920.
[13]谭国明.脾氨肽口服冻干粉治疗小儿反复呼吸道感染的疗程与疗效相关性研究[J].黑龙江医学,2011(2):125-127.
[14]王远明,杜惠容.匹多莫德治疗小儿反复下呼吸道感染疗效观察及免疫功能变化[J].重庆医学,2012(35):3758-3759.
[15]钱旭波,蔡晓红,高原.匹多莫德对儿童哮喘合并反复呼吸道感染的疗效观察[J].临床儿科杂志,2009(4):375-378.
[16]张爱启,张磊,付姝丽.泛福舒对反复呼吸道感染儿童免疫功能的影响[J].现代生物医学进展,2009(19):3690-3691.
[17]李文媛,王团美.泛福舒佐治小儿支原体肺炎的临床观察[J].湖南师范大学学报(医学版),2007(4):70-71.
[18]陈果林,蓝雪容,叶华生.泛福舒治疗小儿反复呼吸道感染疗效观察[J].中国实用医药,2013(1):163-164.
[19]ZAGAR S,LOFLER-BADZEK D.Broncho-Vaxom inchildren with rhinosinusitis:a double-blind clinical trial[J].ORL J Otorhinolaryngol Relat Spec,1988,50(6):397-404.
[20]SCHAAD U B,FARINE J C.Prospective placebocontrolled double-blind study using a bacterial lysate in infections of the respiratory tract and ENT region in children[J].Helv Paediatr Acta,1986,41(1/2):7-17.
[21]GOMEZ BARRETO D,DE LA TORRE C,ALVAREZ A,et al. Safety and efficacy of OM-85-BV plus amoxicillin/clavulanate in the treatment of subacute sinusitis and the prevention of recurrent infections in children[J].Allergol Immunopathol(Madr),1998,26(1):17-22.
(张西倩编辑)
Systematic review of immune adjuvant for recurrent respiratory infection of children*
Li-li Zheng1,Li Yao1,Fang-fang Fan1,Lan Hu1,Zhi-gang Li2
(1.Department of Pharmacy,Traditional Chinese Medical Hospital Affiliated to Xinjiang Medical University,Urumqi,Xinjiang 830054,China;2.Department of Pharmacy,the Second People's Hospital of Kashgar,Urumqi,Xinjiang 830000,China)
Objective To evaluate the clinical curative effect of immune adjuvant treatment in treating children recurrent respiratory tract infections by meta analysis method.Methods EMBASE(1974.9-2013.9),PUBMED(1966~2013),the Cochrane Register of Controlled Trials(2013.1)and VIP(1989.9-2013.9),WanFang Data(1994.1-2013.9),CNKI(1979.1-2013.9)were retrived by using computer.And domestic published information on papers and conference in recent 1 year was manually retrived.Literature were selected according the inclusion and exclusion criteria.Information and evaluation into the study of methodological quality was extracted using the Cochrane Revman5.3 software for Meta analysis.Results Participants included 13 researches,1088 cases of pediatric patients. Meta analysis showed that immune adjuvant combined with conventional treatment group can improve the patient's immune adjuvant T-lymphocyte subsets CD3 (WMD=7.97,95%CI=5.6,10.34,P=0.000),CD4 (WMD=5.44,95%CI=1.27,9.6,P=0.010)and improve the immunoglobulin IgA(WMD=0.43,95%CI=0.08,0.77,P=0.010),IgG(WMD=1.07,95%CI=0.25,1.89,P=0.010),and can delay the onset of several days of RRI(WMD=-5.14,95%CI:6.72,3.56,P=0.040).The CD8(WMD=0.7,95%CI:0.19,1.59,P=0.130)and CD4/CD8(WMD= 0.25,95%CI:0.04,0.45,P=0.130),IgM(WMD=0.04,95%CI:-0.05,0.12,P=0.370)and the incidence of adverse reactions(WMD=1.5,95%CI:0.52,4.28,P=0.450)had no statistically significant difference between experimental group and control group.Conclusions The results of Meta-analysis indicate that immune adjuvant combined with conventional treatment can reduce the frequency of recurrent respiratory infection with safety. Howerver,due to the number and quality of included studies,more large-scale and high-quality RCTs are needed.
immune adjuvant;recurrent respiratory infection of children;systematic review;meta analysis
R725.6
B
10.3969/j.issn.1005-8982.2016.16.017
1005-8982(2016)16-0081-07
2015-11-18
自治区自然基金(No:2014211C102)
李治纲,E-mail:1441758443@qq.com;Tel:13899156109
