N、Bi共掺杂的TiO2可见光光催化剂的制备及其光催化性能
2016-07-25丁臻尧季丽婷
王 鹏,王 秋,丁臻尧,季丽婷,黄 琼,2,3*
(1.南京信息工程大学环境科学与工程学院,江苏 南京 210044;2.南京信息工程大学江苏省大气环境与装备技术协同创新中心,江苏 南京 210044;3.江苏省大气环境监测与污染控制高技术研究实验室,江苏 南京 210044)
N、Bi共掺杂的TiO2可见光光催化剂的制备及其光催化性能
王鹏1,王秋1,丁臻尧1,季丽婷1,黄琼1,2,3*
(1.南京信息工程大学环境科学与工程学院,江苏 南京 210044;2.南京信息工程大学江苏省大气环境与装备技术协同创新中心,江苏 南京 210044;3.江苏省大气环境监测与污染控制高技术研究实验室,江苏 南京 210044)
摘要:采用溶胶-凝胶法制备系列BixTi1-xO2光催化剂以及N和Bi共掺杂TiO2光催化剂,采用XRD、UV-Vis、N2-物理吸附和TEM等对催化剂进行微观结构表征,以普通节能灯为光源,考察催化剂光催化氧化室内甲醛的性能。结果表明,在Bi掺杂的TiO2光催化剂体系中,Bi0.15Ti0.85O2光催化剂催化降解甲醛效果最佳,400℃焙烧2.5 h,节能灯光照48 h,可将(1.05±0.05) mg·m-3甲醛降解至0.08 mg·m-3,甲醛转化率92.8%,达到室内空气质量标准。当N与Bi共掺杂时,节能灯光照24 h,Bi0.15Ti0.85O2-N(0.2)光催化剂表现出最佳的光催化氧化降解甲醛性能,即可将甲醛由(1.05±0.05) mg·m-3降解至0.082 mg·m-3,甲醛转化率达92.0%,较Bi0.15Ti0.85O2催化剂光催化效率提高50%。
关键词:催化剂工程;N和Bi共掺杂TiO2;光催化;甲醛
CLC number:TQ426.6;TQ034Document code: AArticle ID: 1008-1143(2016)05-0039-07
随着国民经济的快速发展,人民的生活水平不断提高,室内装修日益普及,室内密闭程度不断加深,由此造成的室内环境污染日趋严重[1-2]。全球30%以上的新建及重修建筑物内发现了对人体健康不利的有害物质,其中甲醛是主要污染物之一[3-4]。TiO2光催化降解室内甲醛作为一种高效环保技术[5],其实用化研究开发受到关注。TiO2是一种性能优良、用途广泛的半导体材料,特别是作为光催化剂在大气、水体等环境有机和无机污染物降解方面应用前景广阔,但TiO2带隙较宽,仅能吸收利用太阳光中波长小于380 nm的紫外线,加上光生电子和空穴易于复合,光量子效率低,阻碍了TiO2光催化材料的实际应用[6]。采用多种手段对TiO2进行改性处理,主要有贵金属修饰[7]、半导体复合[8]、聚合物修饰[9]和过渡金属离子掺杂[10-12]等,其中,金属和非金属离子掺杂是改变光催化剂光谱响应范围的有效方法之一[13]。
本文采用溶胶-凝胶法制备金属Bi掺杂和N、Bi共掺杂的TiO2光催化剂,并利用XRD、UV-Vis、N2-物理吸附和TEM等对催化剂进行结构表征,以甲醛的催化降解作为探针反应物,考察Bi与Ti以及N与Ti物质的量比、焙烧温度、催化剂用量和甲醛浓度等因素对催化剂光催化氧化降解甲醛性能的影响。
1实验部分
1.1催化剂制备
以钛酸四丁酯和硝酸铋为原料,采用溶胶-凝胶法制备催化剂。称取一定量钛酸四丁酯和无水乙醇均匀混合形成溶液A,再将一定量的无水乙醇、冰醋酸和水均匀混合形成溶液B,并加入适量硝酸铋,持续搅拌直至溶液澄清,再将溶液B缓慢滴加至持续搅拌的溶液A中,继续搅拌30 min,自然陈化48 h成凝胶状态,烘箱80℃干燥2 h,研磨成细粉,400℃焙烧2.5 h,即制得金属Bi掺杂TiO2光催化剂BixTi1-xO2。
N、Bi共掺杂TiO2光催化剂的制备是在溶液B中再添加适量碳酸铵,其他步骤不变,即制得BixTi1-xO2-N(y)光催化剂,Bi与Ti和N与Ti物质的量比主要通过控制硝酸铋和碳酸铵的用量实现。
1.2催化剂光催化氧化甲醛降解性能评价
在0.2 m3密闭玻璃反应装置中,通过降解初始浓度为(1.05±0.05) mg·m-3的甲醛测定催化剂的光催化活性。
首先将甲醛溶液滴至培养皿上,置入玻璃反应器,待其充分挥发,使反应器内甲醛气体浓度为(1.05±0.05) mg·m-3,再将0.4 g粉末态催化剂均匀摊放至另一培养皿(φ80 mm)上,置入玻璃反应器,培养皿正上方悬挂40 W普通节能灯泡,点亮灯泡后每隔12 h采用甲醛分析仪(PPM-400ST)采样分析反应器中残留的甲醛浓度。
1.3催化剂表征
采用德国布鲁克公司AXSD8衍射仪对催化剂进行XRD检测,Cu靶,扫描速率4°·min-1,2θ=10°~80°。
催化剂比表面积、孔径及其分布采用N2吸附的Autosorb-iQ-AG-MP表面积分析仪检测。
表面形貌采用日本日立公司SU1510扫描电镜检测分析。
催化剂的紫外可见漫反射分析采用美国安捷伦科技公司Cary 100紫外可见吸收光谱仪检测。
2结果与讨论
2.1UV-Vis DRS
图1为400℃焙烧2.5 h制备的不同Bi掺杂量的BixTi1-xO2催化剂的UV-Vis DRS谱图。

图1 不同Bi掺杂量的BixTi1-xO2催化剂的UV-Vis DRS谱图Figure 1 Diffuse reflectance UV-Vis absorption spectra of BixTi1-xO2 photocatalysts
由图1可以看出,随着金属Bi的掺杂,TiO2即发生不同程度的红移,显示出一定的可见光吸收,且随着金属Bi掺杂量增加,其可见吸收光谱逐渐降低,Bi0.05Ti0.95O2表现出最佳的可见光吸收,可能是由于在催化剂焙烧过程中,Bi3+通过扩散和迁移进入TiO2晶格,部分取代Ti4+,使催化剂的能带结构发生变化,使材料产生光生电荷所需的能量较TiO2小,即能吸收波长较长的可见光,使光谱红移,拓宽光谱响应范围。适量的金属Bi掺杂时,易于在催化剂表面富集[14]形成Bi2O3,由于Bi2O3的禁带宽度仅为2.8 eV,有利于光生电子和空穴的分离,而过量Bi2O3成为光生电子和空穴的复合中心,使可见光吸收及可见光催化性能降低。
不同N掺杂量的Bi0.15Ti0.85O2-N(y)催化剂的UV-Vis DRS谱图如图2所示。由图2可以看出,N、Bi共掺杂的TiO2催化剂具有较金属Bi单独掺杂的Bi0.15Ti0.85O2更强的可见光吸收性能,可见光吸光度随着N掺杂量的增加先增后降,且均高于Bi0.15Ti0.85O2催化剂,并出现明显红移现象,其中,Bi0.15Ti0.85O2-N(0.4)显示出最佳的可见光吸光度。

图2 不同N掺杂量的Bi0.15Ti0.85O2-N(y)催化剂的UV-Vis DRS谱图Figure 2 Diffuse reflectance UV-Vis absorption spectra of Bi0.15Ti0.85O2-N(y) photocatalysts
2.2比表面积及孔径分析
表1为Bi掺杂量对BixTi1-xO2催化剂的比表面积、孔容及孔径的影响。由表1可以看出,随着金属Bi掺杂量增加,催化剂比表面积增大,而催化剂孔容及孔径略有变化,可能是由于Bi的掺杂形成大量晶格缺陷,且表面富集大量Bi2O3,比表面积增大有助于TiO2光催化剂降解甲醛性能的提高[15]。

表1 不同Bi掺杂量对BixTi1-xO2催化剂比表面积、孔容及孔径的影响
2.3XRD
不同温度焙烧的Bi0.15Ti0.85O2催化剂的XRD图如图3所示。由图3可见,焙烧温度低于450℃时,无明显晶体衍射峰,TiO2显示为无定型态;焙烧温度(500~600)℃时,在2θ为25.3°、48.1°及54.5°处均有较强的衍射峰,与锐钛矿相TiO2不同晶面的衍射峰位置完全一致,表明温度高于500℃时,TiO2基本转变为锐钛矿相,且随着温度升高,锐钛矿相TiO2衍射峰越来越尖锐,表明催化剂的结晶度越来越好[16]。焙烧温度600℃时,在2θ为29.9°、34.5°和49.9°处出现Bi2O3衍射峰,表明高温促使Bi2O3晶粒长大且独立存在于TiO2表面。由于Bi2O3物种的存在占据TiO2晶粒表面,减少了锐钛矿相TiO2颗粒间在焙烧过程中直接接触几率,从而有效阻止TiO2晶粒的进一步长大和团聚,进而阻碍锐钛矿相TiO2向金红石相的转变[17]。
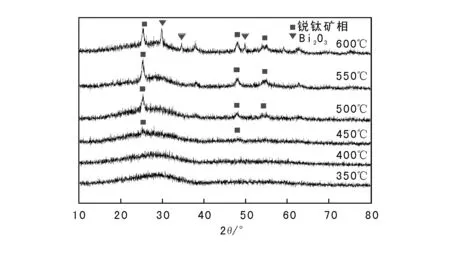
图3 不同焙烧温度制备的Bi0.15Ti0.85O2催化剂的XRD图Figure 3 XRD patterns of Bi0.15Ti0.85O2 photocatalysts prepared at differet calcination temperatures
2.4TEM
Bi0.15Ti0.85O2和Bi0.15Ti0.85O2-N(0.2)催化剂的TEM照片见图4。

图4 Bi0.15Ti0.85O2和Bi0.15Ti0.85O2-N(0.2)光催化剂的TEM照片Figure 4 TEM images of Bi0.15Ti0.85O2 and Bi0.15Ti0.85O2-N(0.2) photocatalysts
由图4可以看出,Bi0.15Ti0.85O2催化剂为块状结构,以无定型态存在,但部分区域发现有TiO2和Bi2O3晶体,晶格条纹分别为0.35 nm和0.23 nm,与实际情况一致;Bi0.15Ti0.85O2-N(0.2)催化剂以颗粒状形式存在,结构蓬松,粒径约为(10~20) nm,可能是由于碳酸铵经热处理后产生大量气泡,致使催化剂结构蓬松,有利于催化剂对甲醛和光的吸收,有助于光催化氧化性能的提高。
2.5Bi0.15Ti0.85O2催化剂光催化氧化降解甲醛
图5为不同Bi掺杂量的BixTi1-xO2催化剂光催化氧化降解甲醛的性能。

图5 不同Bi掺杂量BixTi1-xO2催化剂光催化降解甲醛性能Figure 5 Photocatalytic activities of BixTi1-xO2photocatalysts for degradation of formaldehyde
由图5可以看出,掺杂金属Bi的TiO2催化剂较纯TiO2具有显著的光催化氧化降解甲醛性能,且随着Bi掺杂量的增加先提高后降低,其中,催化剂Bi0.15Ti0.85O2性能最佳,节能灯光照48 h,可将(1.05±0.05) mg·m-3甲醛催化降解至0.08 mg·m-3,达到室内空气质量标准,与UV-Vis DRS分析结果不一致,这主要是由于Bi0.15Ti0.85O2光催化剂具有较Bi0.05Ti0.95O2更大的比表面积,吸附甲醛性能更佳,Bi0.20Ti0.80O2催化剂虽具有更大的比表面积,但由于Bi掺杂量过大,导致Bi易富集于催化剂表面形成Bi2O3,成为光生电子和空穴的复合中心,致使可见光吸收及可见光催化性能降低,确定Bi0.15Ti0.85O2为催化剂的最佳配比。
不同焙烧温度对Bi0.15Ti0.85O2催化剂光催化降解甲醛性能的影响如图6所示。由图6可以看出,Bi0.15Ti0.85O2催化剂光催化氧化甲醛活性随着焙烧温度升高先增后降,其中,400℃焙烧2.5 h制得的Bi0.15Ti0.85O2光催化剂表现出最佳的光催化性能,光照48 h,降解率达88.7%,TEM和XRD分析表明,此时催化剂仍以无定型态为主,部分区域已形成TiO2和Bi2O3晶体。600℃焙烧2.5 h制得的Bi0.15Ti0.85O2显示出较为完整的TiO2和Bi2O3晶体,但光催化性能较差,光照48 h,催化降解率仅为59.5%,选择400℃为催化剂最佳焙烧温度。

图6 不同焙烧温度对Bi0.15Ti0.85O2催化剂光催化降解甲醛性能的影响Figure 6 Photocatalytic activities of Bi0.15Ti0.85O2 photocatalysts obtained at different calcination temperatures for degradation of formaldehyde
Bi0.15Ti0.85O2催化剂、TiO2和市售P25光催化降解甲醛性能见图7(A)。由图7(A)可见,光催化氧化降解甲醛的活性依次为市售P25>Bi0.15Ti0.85O2
>TiO2,市售P25仅需17 h即可将甲醛由(1.05±0.05) mg·m-3降至0.092 mg·m-3,转化率达91.5%。图7(B)和图7(C)为催化剂在暗光条件下的吸附性能以及过滤掉节能灯中紫外光的催化性能。由图7(B)可见,3种催化剂在暗光条件下均表现出一定的吸附甲醛性能,其中,市售P25在24 h时的吸附率达39.0%,而Bi0.15Ti0.85O2和TiO2分别为26.3%和20.8%。经24 h暗光吸附后,打开节能灯进行光照,其甲醛浓度均迅速降低,而在含有P25粉末催化剂的反应器中,甲醛浓度先降低后逐渐增加,这主要是后期甲醛脱附造成甲醛浓度持续升高,而含有Bi0.15Ti0.85O2催化剂的反应器中甲醛浓度始终维持在国标浓度以下,无明显上升趋势,表明P25在节能灯作用下仍以吸附-脱附为主,而Bi0.15Ti0.85O2主要以光催化氧化降解为主。由图7(C)可见,在可见光作用下,两种催化剂催化氧化性能均下降,主要是由于过滤掉紫外光所致,但Bi0.15Ti0.85O2催化剂催化活性在可见光条件下明显优于市售P25。
Bi0.15Ti0.85O2催化剂稳定性能测试结果如图8所示。

图8 Bi0.15Ti0.85O2催化剂稳定性能Figure 8 Stability of Bi0.15Ti0.85O2 photocatalyst
由图8可见,Bi0.15Ti0.85O2催化剂经5次平行测试后,均表现出良好的催化降解甲醛性能,经48 h节能灯光照,即可将甲醛催化降解至0.08 mg·m-3,甲醛转化率为92.8%,催化剂稳定性良好。
2.6Bi0.15Ti0.85O2-N(y)催化氧化降解甲醛
不同N掺杂量的Bi0.15Ti0.85O2-N(y)催化剂光催化降解甲醛性能如图9所示。由图9可以看出,Bi0.15Ti0.85O2-N(0.2)催化剂表现出最佳的光催化氧化降解甲醛性能,节能灯光照24 h,即可将甲醛由(1.05±0.05) mg·m-3降至0.082 mg·m-3,甲醛转化率92.0%,较Bi0.15Ti0.85O2催化剂催化效率提高50%。

图9 Bi0.15Ti0.85O2-N(y)催化剂光催化降解甲醛性能Figure 9 Photocatalytic activityes of Bi0.15Ti0.85O2-N(y) photocatalysts for degradation of formaldehyde
3结论
(1) 采用溶胶-凝胶法制备具有可见光响应的BixTi1-xO2催化剂。研究结果表明,掺杂适量Bi的TiO2具有显著的可见光响应,催化剂Bi0.15Ti0.85O2光催化降解甲醛效果最佳,经48 h节能灯照射后即可将浓度为(1.05±0.05) mg·m-3的室内甲醛降至0.08 mg·m-3以下,达到室内空气质量标准。
(2) 市售P25较Bi0.15Ti0.85O2催化剂具有更快的吸附甲醛效率,其主要在于高效的吸附性能以及节能灯灯光中微弱的紫外光作用。而Bi0.15Ti0.85O2催化剂降解甲醛浓度始终维持在0.08 mg·m-3以下,无升高趋势,且在过滤掉紫外光后催化降解甲醛性能优于市售P25。
(3) 在N与Bi共掺杂的TiO2催化剂体系中,Bi0.15Ti0.85O2-N(0.2)催化剂表现出最佳的光催化氧化降解甲醛性能,节能灯光照24 h,即可将甲醛由(1.05±0.05) mg·m-3降至0.082 mg·m-3,甲醛转化率92.0%,较Bi0.15Ti0.85O2催化剂催化效率提高50%。
参考文献:
[1]于立群,徐应军.装饰材料引起的室内空气污染及对人体危害[J].中国煤炭工业医学杂志,2003,6(11):1124-1125.
[2]Mitchell C S,Junfeng J Z,Torben S,et al.Current state of the science:health effects and indoor environmental quality[J].Environmental Health Perspectives,2007,115(6):958-964.
[3]罗晓红,顾艳.室内甲醛污染对人类健康影响的研究进展[J].职业与健康,2011,27(21):2501-2503.
Luo Xiaohong,Gu Yan.Study progress on effects of indoor formaldehyde pollution on human health[J].Occupation and health,2011,27(21):2501-2503
[4]Endo Y,Miyazaki T,Hikita Y,et al.Sampling methods and residential factors affecting formaldehyde concentration in indoor air[J].Journal of Experimental Medicine,2001,195(4):227-236.
[5]Noguchi T,Fujishima A,Sawunyama P,et al.Photocatalytic degradation of gaseous formaldehyde using TiO2film[J].Environmental Science & Technology,1998,32(23):3831-3833.
[6]丛野.基于非金属掺杂的改性纳米二氧化钛光催化剂的制备与性能研究[D].上海:华东理工大学,2006.
Cong Ye.Preparation and study on the properties of nano-TiO2photocatalyst based on nonmetal doping[D].East China University of Science and Technology,2006.
[7]Sung-Suh H M,Choi J R,Hah H J,et al.Comparison of Ag deposition effects on the photocatalytic activity of nanoparticulate TiO2under visible and UV light irradiation[J].Journal of Photochemistry & Photobiology A:Chemistry,2004,163(3):37-44.
[8]Bessekhouad Y,Robert D,Weber J V.Bi2S3/TiO2and CdS/TiO2heterojunctions as an available configuration for photocatalytic degradation of organic pollutant[J].Journal of Photochemistry & Photobiology A:Chemistry,2004,163(3):569-580.
[9]Su B,Liu X,Peng X,et al.Preparation and characterization of the TiO2/polymer complex nanomaterial[J].Materials Science & Engineering A,2003,349(1):59-62.
[10]Choi W,Termin A,Hoffmann M R.The role of metal ion dopants in quantum-sized TiO2:correlation between photoreactivity and charge carrier recombination dynamics[J].The Journal of Physical Chemistry,1994,98(51):13669-13679.
[11]Graetzel M,Howe R F.Electron paramagnetic resonance studies of doped titanium dioxide colloids[J].The Journal of Physical Chemistry,1990,94(6):2566-2572.
[12]Paola A D,Marcì G,Palmisano L,et al.Preparation of polycrystalline TiO2photocatalysts impregnated with various transition metal ions:characterization and photocatalytic activity for the degradation of 4-nitrophenol[J].The Journal of Physical Chemistry B,2001,106(3):637-645.
[13]Cheng Ping,Gu Mingyuan,Jin Yanping.Recent progress in titania photocatalyst operating under visible light[J].Progress in Chemistry,2005,17(1):8-14.
[14]严前古,高利珍,储伟,等.甲烷部分氧化制合成气Pt-Ni/Al2O3催化剂的研究[J].化学学报,1998,56(10):1021-1026.
Yan Qiangu,Gao Lizhen,Chu Wei,et al.Partial oxidation of methane to syngas over Pt-Ni/Al2O3catalyst[J].Acta Chimica Sinica,1998,56(10):1021-1026.
[15]崔海萍,闫军,张永涛,等.Na2SnO3掺杂TiO2的结构及对TNT的降解研究[C]//第十五届全国高技术陶瓷学术年会.北京:中国硅酸盐学会,2008.
[16]冯彩霞,王岩,金振声,等.N掺杂纳米TiO2可见光催化氧化丙烯的动力学行为[J].物理化学学报,2008,(4):633-638.
Feng Caixia,Wang Yan,Jin Zhensheng,et al.Kinetic behavior of visible light photocatalytic oxidation of propylene for N-doped nano-TiO2[J].Acta Physico-Chimica,2008,(4):633-638.
[17]Huang Jianhui,Cheuk Wahkit,Wu Yifan,et al.Fabrication of Bi-doped TiO2spheres with ultrasonic spray pyrolysis and investigation of their visible-light photocatalytic properties[J].Journal of Nanotechnology,2012,5(1/2):1-7.
Preparation and photocatalytic properties of N,Bi co-doped TiO2visible-light photocatalysts
Wang Peng1, Wang Qiu1, Ding Zhenyao1, Ji Liting1, Huang Qiong1,2,3*
(1.School of Environmental Science & Engineering, Nanjing University of Information Science & Technology, Nanjing 210044, Jiangsu, China; 2.Jiangsu Collaborative Innovation Center of Atmospheric Environment and Equipment Technologies, Nanjing University of Information Science & Technology, Nanjing 210044, Jiangsu, China; 3.Jiangsu Key Laboratory of Atmospheric Environmental Monitoring & Pollution Control, Nanjing 210044, Jiangsu, China)
Abstract:BixTi1-xO2 photocatalysts and N,Bi co-doped TiO2 photocatalysts were prepared by sol-gel method.The catalysts were characterized by X-ray diffraction,UV-Visible diffuse reflectance spectroscopy,N2-physical adsorption and transmission electron microscope techniques.The photocatalytic activities of the photocatalysts for degradation of indoor formaldehyde under energy-saving lamp irradiation were investigated.The results showed that in Bi doped TiO2 photocatalyst system,Bi0.15Ti0.85O2 photocatalyst calcined at 400℃ for 2.5 h exhibited the best activity for photocatalytic oxidation of formaldehyde.Under energy-saving lamp illumination for 48 h,the concentration of formaldehyde was reduced from (1.05±0.05) mg·m-3to 0.08 mg·m-3,which reached the indoor air quality standards,and formaldehyde conversion of 92.8% was attained.In N,Bi co-doped TiO2 photocatalyst system,Bi0.15Ti0.85O2-N(0.2) photocatalyst possessed the optimal photocatalytic activity.The concentration of indoor formaldehyde was decreased from (1.05±0.05) mg·m-3to 0.082 mg·m-3under energy-saving lamp illumination for 24 h.Formaldehyde conversion over Bi0.15Ti0.85O2-N(0.2) photocatalyst reached 92.0%,and its catalytic efficiency was enhanced 50% compared with Bi0.15Ti0.85O2 photocatalyst.
Key words:catalyst engineering; N-Bi co-doped titanium dioxide; photocatalysis; formaldehyde
收稿日期:2016-03-17;修回日期:2016-04-06
基金项目:国家自然科学基金项目(21272118,21577065,21501097);江苏省自然科学基金项目(BK20150890);江苏省高校优势学科建设工程资助项目
作者简介:王鹏,1994年生,男,江苏省高邮市人,本科在读,研究方向为光催化和催化燃烧VOCs。
doi:10.3969/j.issn.1008-1143.2016.05.008 10.3969/j.issn.1008-1143.2016.05.008
中图分类号:TQ426.6;TQ034
文献标识码:A
文章编号:1008-1143(2016)05-0039-07
催化剂制备与研究
通讯联系人:黄琼,讲师,研究方向为光催化和催化燃烧VOCs。
