高效液相色谱法测定血浆中霉酚酸及其代谢物分化葡萄糖醛麦草酰胺的浓度
2016-07-24杨春兰王琴苏涌夏泉廖贵益许杜娟
杨春兰,王琴,苏涌,夏泉,廖贵益,许杜娟Δ
(1.安徽医科大学 药学院,安徽 合肥 230022;2.安徽医科大学第一附属医院 药剂科,国家中医药管理局中药化学三级实验室,安徽 合肥 230022;3.安徽医科大学第一附属医院 泌尿外科,安徽 合肥 230022)
高效液相色谱法测定血浆中霉酚酸及其代谢物分化葡萄糖醛麦草酰胺的浓度
杨春兰1,2,王琴1,苏涌2,夏泉2,廖贵益3,许杜娟1Δ
(1.安徽医科大学 药学院,安徽 合肥 230022;2.安徽医科大学第一附属医院 药剂科,国家中医药管理局中药化学三级实验室,安徽 合肥 230022;3.安徽医科大学第一附属医院 泌尿外科,安徽 合肥 230022)
目的 建立一种HPLC方法能够同时快速测定血浆中霉酚酸(mycophenolic acid,MPA)及其代谢物分化葡萄糖醛麦草酰胺(mycophenolic acid glucuronide,MPAG)浓度。方法 血浆样品加入卡马西平内标,经硫酸锌甲醇沉淀蛋白前处理,以色谱柱ZORBAX XDB C18(4.6 mm×250 mm,5 μm),流动相甲醇-乙腈-磷酸二氢钾缓冲液梯度洗脱,流速1.0 mL/min,柱温30 ℃,检测波长254 nm,进行HPLC检测。测定32例肾移植受者术后7~14 d期间MPA、MPAG谷浓度。结果 MPA、MPAG分别在0.2~50 μg/mL,2.5~500 μg/mL范围内线性关系良好(r>0.999),绝对回收率均>80%,方法回收率在90%~110%之间,日内及日间RSD均小于10%。32例肾移植受者早期服用霉酚酸酯剂量为1~1.5 g/d,血浆中MPA范围为0.32~6.19 μg/mL,MPAG范围为9.52~149.25 μg/mL。结论 测定人血浆中MPA、MPAG的HPLC法具有准确、方便、快速等优点,可以用于肾移植受者血药浓度监测。
霉酚酸;分化葡萄糖醛麦草酰胺;肾移植受者;高效液相色谱法;血药浓度
霉酚酸酯(mycophenolate mofetil ,MMF)作为免疫抑制剂霉酚酸(mycophenolic acid,MPA)的前体药物,已广泛应用于临床实体器官移植后的抗排斥反应中。MPA重要的代谢产物分化葡萄糖醛麦草酰胺(mycophenolic acid glucuronide,MPAG ),可被分泌入胆汁并进入小肠,在肠道中经微生物的作用再次分解为MPA。约87%MPA以MPAG 的形式通过肾小管排泄[1]。目前临床上应用常规剂量(1~2 g/d)用于肾移植后的抗排斥反应,但由于MPA的血药浓度普遍存在个体差异,所以常规剂量可能会产生免疫抑制疗效的差异,甚至导致不良反应的发生。因此,临床可通过监测MPA 的血药浓度,调整MMF给药剂量,减少不良反应的发生,达到最佳疗效。
1 材料与方法
1.1 材料
1.1.1 仪器:Waters alliance高效液相色谱仪(美国Waters公司) ,配备Waters e2695 separation Module,Waters E10SMH614G柱温箱、Waters2489UV/Visible检测器;-80 ℃超低温冰箱DW-HL328(中科美菱低温科技有限责任公司);TGL-185小型低温离心机(长沙平凡仪器仪表有限公司);pH计(梅特勒-托利多);AB135-5电子天平(上海梅特勒多-托利多) ;XW-80A漩涡振荡器(上海医科大学仪器厂)。
1.1.2 试剂:MPA对照品(南京泽朗医药科技有限公司,纯度≥98.0%);MPAG 对照品(TORONTO RESEARCH CHEMICAL INC,纯度≥98.0%);卡马西平对照品(中国药品生物制品检定所,批号:0142-9503);磷酸、磷酸二氢钾、硫酸锌(分析纯);甲醇、乙腈(色谱级,Tedia公司);健康人空白血浆,重蒸馏水。
1.2 方法
1.2.1 色谱条件:色谱柱ZORBAX XDB C18(4.6 mm×250 mm,5 μm);流动相为:乙腈-甲醇-磷酸氢二钾缓冲溶液(pH3.0),线性梯度洗脱24:20:56起始(0 min)→34:20:40(6.5 min);流速:1.0 mL/min,检测波长:254 nm;进样量:20 μL;柱温:30 ℃。
1.2.2 试剂的配制:精密称取MPA对照品1 mg,用甲醇稀释成浓度为0.2~50 μg/mL的系列标准工作液。精密称取 MPAG对照品5 mg,用甲醇稀释成浓度为25~5000 μg/mL的系列标准工作液。两者均放置于4 ℃冰箱避光保存。
1.2.3 血样预处理:取患者血浆100 μL ,加入卡马西平(10 mg/L)内标10 μL,涡旋30 s ,加入10%磷酸5 μL,混匀;加入100 μL蛋白沉淀剂(32 mg/L ZnSO4甲醇溶液),涡旋混合2 min,14000 r/min离心5 min,取上清液加入5 μLNaOH(1 mol/L)溶液,混合30 s,14000 r/min离心5 min,取上清液20 μL进样。
1.2.4 系统适应性及方法专属性:血浆样品按“1.2.3”项下的前处理方法,在“1.2.1”项色谱条件下检测。
1.2.5 标准曲线:取空白血浆,加入MPA、MPAG 标准工作液适量,配置成MPA血浆浓度为0.2、1.0、10.0、20.0、40.0、50.0 μg/mL,MPAG血浆浓度为2.5、12.5、25.0、250.0、400.0、500.0 μg/mL,按“1.2.3”项下方法前处理后进样测定,以MPA、MPAG检测峰面积与内标峰面积比值(y1,y2)分别对MPA、MPAG(x1,x2)进行线性回归。
1.2.6 精密度与回收率实验:精密称取对照品适量,用甲醇作为溶剂配制高、中、低3种浓度的MPA及MPAG 的溶液,使MPA、MPAG溶液浓度分别为5、20、40 μg/mL 和12.5、100、400 μg/mL,同时取空白血浆配制相同浓度的质控血浆,质控血浆按照“1.2.3”项下进行前处理,以同浓度质控血浆的峰面积与溶液相应峰面积的比值表示绝对回收率,实验操作平行3次。实验于同一天内平行操作测定3次,计算得日内RSD,连续3天每天操作测定1次,计算得日间RSD。
1.2.7 重复性实验:取空白血浆,加入适量MPA、MPAG标准工作液,分别配制成浓度为10、25 μg/mL的质控样品,按“1.2.3”项下前处理进样,计算浓度,连续测定 5次。
1.2.8 临床应用:收集在安徽医科大学第一附属医院2015年8月~2016年2月份期间进行同种异体肾移植的患者32例,其中男27例、女5例,年龄(34.28±8.18)岁,体重指数为(21.76±2.89)kg/m2。患者均采用MMF联合他克莫司、糖皮质激素的免疫方案以抗免疫排斥反应。患者于手术前晚开始服用MMF,MMF日剂量为1~1.5 g,于术后第7~14天期间患者早晨服药前使用EDTA抗凝管采集外周静脉血2 mL,采血后于2 h内用低速离心机3000 r/min离心10 min,取上清血浆,按照“1.2.3”项下处理样品进行HPLC测定,测得结果采用Graphpad prism软件绘制散点图。
2 结果
2.1 系统适应性及方法专属性 MPA,MPAG及内标与血浆中内源性物质分离充分,峰型良好,保留时间分别为(4.0±0.2)、(11.2±0.1)、(7.8±0.1)min,色谱图见图1。
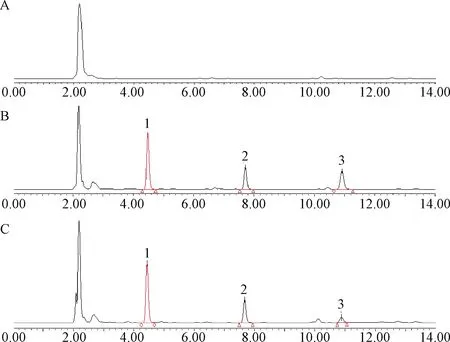
图1 MPA和MPAG色谱图 A.空白血浆;B.空白血浆+MPAG+MPA;C.血浆样品1:MPAG;2:内标;3:MPAFig.1 The chromatogram of MPA and MPAG A.blank plasma; B.blank plasma+MPAG+MPA; C.plasma sample1:MPAG;2:internal standard substance;3:MPA
2.2 标准曲线 MPA标准曲线为y1=0.09855x1+0.03511(r=0.9998),MPAG标准曲线为y2=0.09707x2-0.03043(r=0.9997)。结果表明,MPA、MPAG血浆浓度在0.2~50 μg/mL、2.5~500 μg/mL时线性良好。见图2。
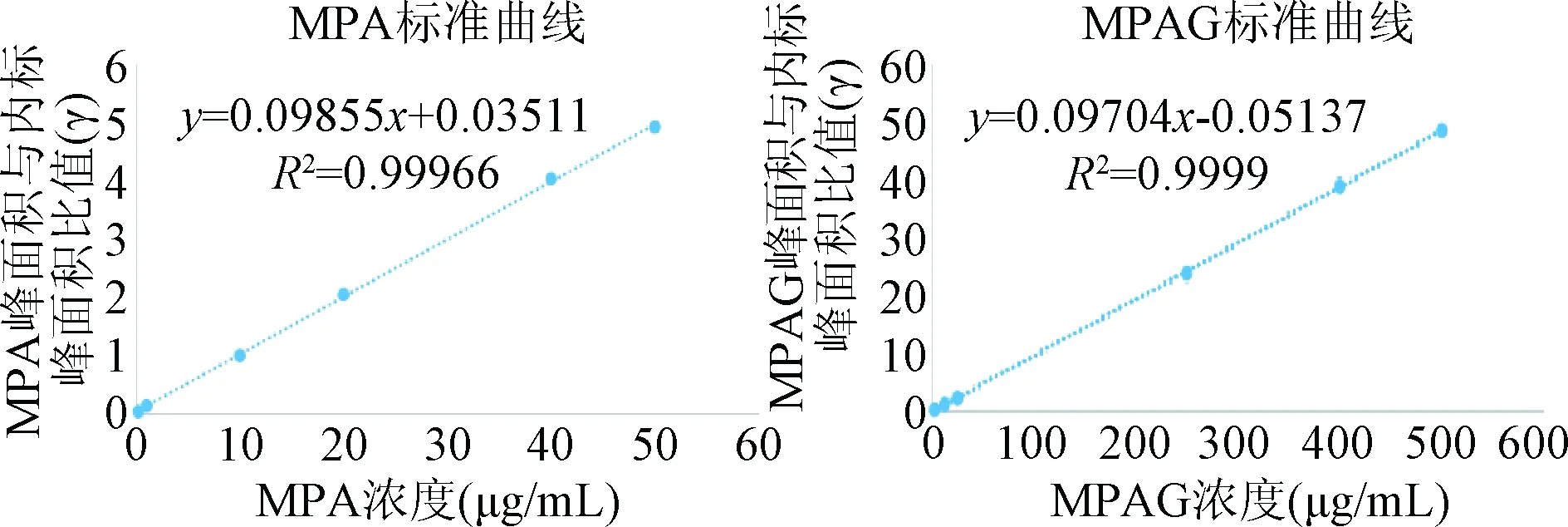
图2 血浆中MPA、MPAG标准曲线Fig.2 The standard curve of MPA and MPAG in plasma
2.3 精密度与回收率实验:MPA、MPAG及内标的绝对回收率在80%以上。用标准曲线测得MPA及MPAG的浓度与配制浓度的比值表示方法回收率。MPA、MPAG的方法回收率均在90%~110%之间,日内及日间RSD均<10%。见表1。
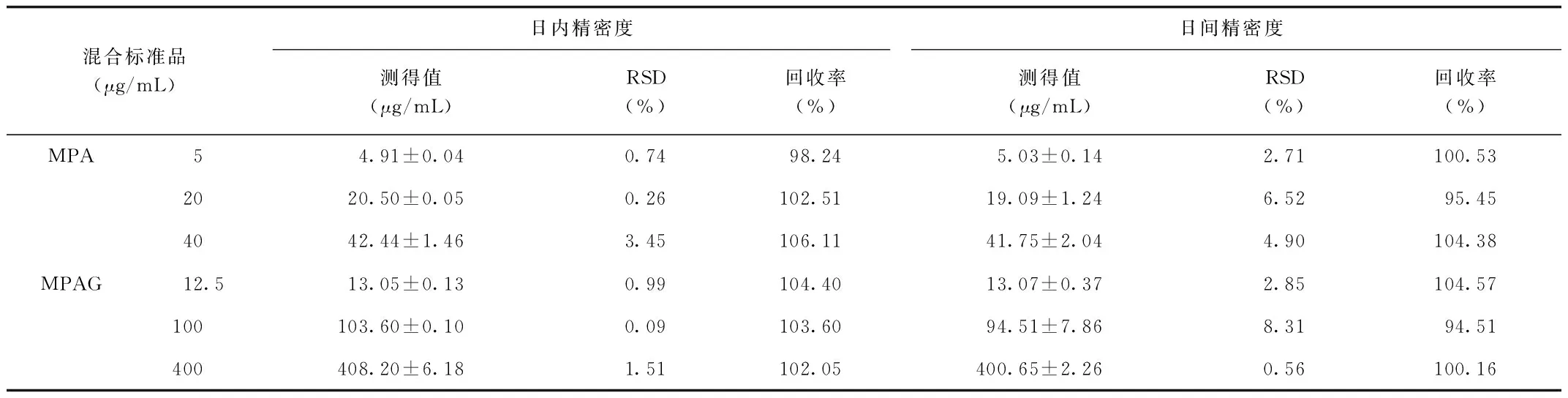
表1 血浆中MPA、MPAG含量测定的回收率和精密度Tab.1 The recovery and precision of plasma MPA and MPAG determination
2.4 重复性实验:MPA平均浓度为10.19 μg/mL,RSD为2.26%,MPAG平均浓度为25.28 μg/mL,RSD为1.88%,表明本方法重复性良好。
2.5 临床应用 32例同种异体肾移植患者血浆样品检测结果,见图3。32例肾移植受者早期服用霉酚酸酯剂量为1~1.5 g/d,7~14 d MPA谷浓度范围为0.32~6.19 μg/mL,MPAG谷浓度范围为9.52~149.25 μg/mL,个体差异较大。MPA谷浓度95%置信区间为1.12~1.99 μg/mL。
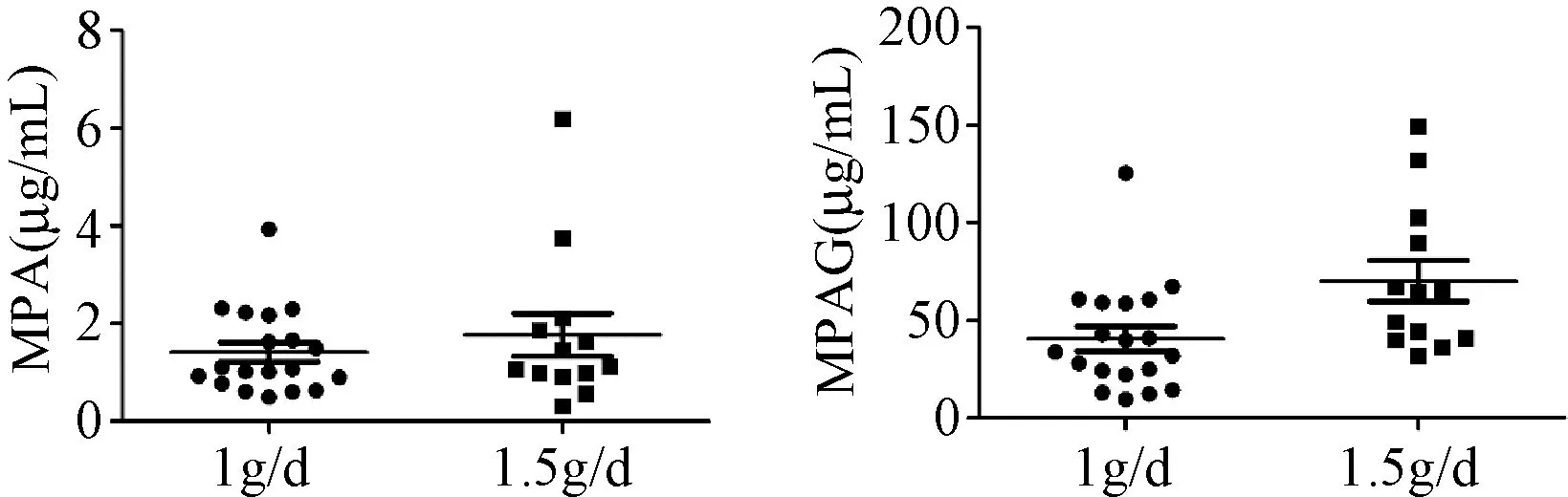
图3 肾移植受者血浆MPA、MPAG浓度分布Fig.3 The concentration distribution of plasma MPA and MPAG of renal transplant recipients
3 讨论
MMF是前体药物,其在体内活性成分为MPA。MPA的作用靶点是次黄嘌呤脱氢酶(inosine 5’-monophosphate dehydrogenase,IMPDH),抑制T、B淋巴细胞内鸟嘌呤的合成,从而达到抑制淋巴细胞增殖的作用[2]。在器官移植患者中的研究表明,由于患者移植后的阶段、肾功能的恢复情况,药物代谢酶的遗传因素,合并用药等多种复杂因素影响,MPA药动学在患者个体间存在极大变异性,进而引起免疫抑制程度的变化,因此需要进行治疗药物浓度监测,实施个体化给药[3]。MPAG是MPA主要的代谢物,虽然MPAG在药理学上是非活性的,但接近82%的MPAG与白蛋白结合[4],而MPA 97%与血浆白蛋白结合,因此MPA、MPAG之间存在竞争蛋白结合,血浆中MPAG的波动,可影响游离MPA浓度,进而影响MPA的免疫抑制效应。 MPAG大部分经过肝肠循环再次水解为 MPA,平均约占MPA时间-浓度曲线下面积(AUC6-12 h)的37%(10%~60%)左右,患者间肝肠循环的差异是引起 MPA血药浓度差异性的重要因素[5]。 而且,MPAG经肾小球滤过及肾小管分泌排泄,肾功能不全的患者使其排泄减少,导致血中 MPAG浓度的升高[6],体内蓄积的MPAG经过肝肠循环,进一步引起 MPA的浓度增加。监测MPA的同时检测MPAG水平可能会给预测MPA暴露量提供一定的依据。
研究中曾尝试用甲醇、乙腈沉淀蛋白,发现沉淀不完全或存在杂质干扰的情况,也曾尝试用有机溶剂反复萃取再用氮气吹干,存在不能将MPA、MPAG萃取完全,回收率低的问题。
最终发现采用硫酸锌蛋白沉淀剂去除血浆蛋白后直接进样,样品预处理方法简便、快速,可避免长时间、复杂样品过程中的药物降解。 MPA和MPAG极性相差较大, 给较短时间内对两者完成测定带来困难。文献报道中有的采用两套色谱系统[7]测定的办法, 也有采用离子对色谱法[8],这些方法存在分析效率低、对仪器设备要求高或日常耗费高等缺点。本实验考察了不同色谱柱对MPAG和MPA 分离特性的影响,最终发现ZORBAX XDB C18色谱柱满足对MPA及MPAG的分离度,同时采用梯度洗脱的方法,使得MPA、MPAG能够在15 min内分离完全,满足短时间内同时测定两者浓度的要求。
本研究测定了32例肾移植患者术后给予1~1.5 g/dMMF后7~14 d MPA、MPAG的血浆谷浓度,MPA浓度范围为0.32~6.19 μg/mL,MPAG浓度范围为9.52~149.25 μg/mL,个体差异较大,与文献报道[9-10]相似。在本研究中MPA谷浓度95%置信区间为1.12~1.99 μg/mL,与文献报道[11]的MPA谷浓度的安全范围1.40~2.80 μg/mL相类似。MPA、MPAG药物浓度波动在本研究所建立的检测范围内,方法满足临床检测需要,检测结果与文献报道相近,该方法可以用于临床肾移植患者的霉酚酸浓度监测。
[1] Lamba V, Sangkuhl K, Sanghavi K,et al. PharmGKB summary: mycophenolic acid pathway[J].Pharmacogenet Genomics,2014,24(1):73-79.
[2] Kawanishi M, Yano I, Yoshimura K,et al. Sensitive and validated LC-MS/MS methods to evaluate mycophenolic acid pharmacokinetics and pharmacodynamics in hematopoietic stem cell transplant patients[J].Biomed Chromatogr,2015,29(9):1309-1316.
[3] Sam WJ, Akhlaghi F, Rosenbaum SE. Population pharmacokinetics of mycophenolic acid and its 2 glucuronidated metabolites in kidney transplant recipients[J].J Clin Pharmacol,2009,49(2):185-195.
[4] 赵本慧,陈丁丁,朱余兵.霉酚酸酯及其代谢产物的研究进展[J].中国医院药学杂志,2014,34(22):1957-1961.
[5] de Jonge H,Naesens M, Kuypers DR.New Insights Into the Pharmacokinetics and Pharmacodynamics of the Calcineurin Inhibitors and Mycophenolic Acid: Possible Consequences for Therapeutic Drug Monitoring in Solid Organ Transplantation[J].Ther Drug Monit,2009,31(4):416-435.
[6] Merkel U, Lindner S, Vollandt R,et al. Trough levels of mycophenolic acid and its glucuronidated metabolite in renal transplant recipients[J].Int J Clin Pharmacol Ther,2005,43(8):379-388.
[7] Atcheson B, Taylor PJ, Mudge DW,et al.Quantification of free mycophenolic acid and its glucuronide metabolite in human plasma by liquid-chromatography using mass spectrometrie and ultraviolet absorbance detection[J].J Chromatogr B Analyt Technol Biomed Life Sci,2004,799(1):157-163.
[8] 仲艳,高宁舟,焦正,等.HPLC法同时测定人尿液中霉酚酸及其代谢物葡糖昔酸结合物的浓度[J].中国临床药学杂志,2006,15(3):164-167.
[9] Figurski MJ, Pawiński T, Goldberg LR,et al.Pharmacokinetic monitoring of mycophenolic acid inheart transplant patients: Correlation the side-effects and rejections with pharmacokinetic parameters[J].Ann Transplant,2012,17(1):68-78.
[10] Mino Y, Naito T, Otsuka A, et al. Inosine monophosphate dehydrogenase activity depends on plasma concentrations of mycophenolic acid and its glucuronides in kidney transplant recipients[J].Clin Chim Acta,2009,409(1-2):56-61.
[11] 于立新,周敏捷,罗敏.肾移植受者应用霉酚酸酯的合理治疗窗[J].南方医科大学学报,2014, 34(12): 1842-1845.
(编校:王俨俨)
作 者 简 介
许杜娟,主任药师、副教授,1985年蚌埠医学院医疗系毕业,1991年安徽医科大学临床药理学硕士毕业,2003年安徽医科大学临床药理学博士毕业。1985年7月~1988年在宿县地区卫校工作,1991年7月~2004年10月在合肥市第二人民医院工作,2004年10月至今在安徽医科大学第一附属医院工作。现任安徽医科大学药学院副院长,第一附属医院药学教研室主任,药剂科副主任。安徽省第十、十一届政协委员。
许杜娟教授主要从事肿瘤耐药机制研究和逆转肿瘤耐药药物研发,以及基因多态性与药物疗效相关性研究。主持省自然科学基金面上项目2项、省级科技攻关项目1项,安徽省高等学校自然科学基金3项、安徽省教学研究重点项目2项。担任中国医药教育协会合理用药专委会副主任委员,中国药理学会临床药理学专委会常委,中国药学会医院药学专委会委员;安徽省药学会副理事长,安徽省药学会药事管理专委会主任委员,安徽康复医学会药物与保健康复专委会主任委员。《安徽医药》常务编委,《安徽医科大学学报》《中国生化药物杂志》《中国药房》《中国药业》编委。全国高等教育医学数字化规划教材国家医学电子书包《临床药理学》、卫计委临床药学“十二五”规划教材《药学服务与沟通技巧》编委;中国医药科技出版社“十三五”规划教材《药学服务实务》主编;人民卫生出版社“十三五”规划教材《药学服务概论》副主编;主编《医疗机构药事管理实用手册》,参编《现代医院诊疗技术》等多部学术著作;发表学术论文90余篇(SCI收录论文10余篇)。获发明专利3项,获安徽省教学成果奖二等奖1项。
Determination of plasma concentration of mycophenolic acid and mycophenolic acid glucuronide by HPLC
YANG Chun-lan1,2, WANG Qin1, SU Yong2, XIA Quan2, LIAO Gui-yi3, XU Du-juan1Δ
(1.College of Pharmacy, Anhui Medical University, Hefei 230022, China; 2.Department of Pharmacy, The First Affiliated Hospital of Anhui Medical University, Third-grade Pharmaceutical Chemistry Laboratory of State Administration of Traditional Chinese Medicine,Hefei 230022, China; 3.Department of Urology, The First Affiliated Hospital of Anhui Medical University, Hefei 230022, China)
ObjectiveTo develop an HPLC method for the determination of mycophenolic acid(MPA), mycophenolic acid glucuronide(MPAG) in plasma.MethodsThe samples were precipitated with zinc sulphate-methanol solution before injection. Carbamazepine was selected as internal standard,ZORBAX XDB C18(4.6 mm×250 mm,5 μm)column was used and the flow rate was 1 mL/min. The mobile phase consisted of methanol-acetonitrile-potassium dihydrogen phosphate buffer solution(gradient elution) .The column temperature was 30 ℃ and the detective wave length was 254 nm. And then the MPA,MPAG concentration of 32 patients in 7-14 days after renal transplantion were determined.ResultsThe assay was linear within 0.2-50 μg/mL for MPA, 2.5-500 μg/mL for MPAG(r>0.999).Absolute recovery rates of MPA,MPAG were more than 80%, the recoveries were between 90%-110%.The intra-day and inter-day RSDs were both lower than 10%.Totally 32 cases of renal transplantion patiens were with mycophenolate mofetil at the dose of 1-1.5 g/d,and MPA in plasma was within the range of 0.32-6.19 μg/mL,MPAG in plasma was within the range of 9.52-149.25 μg/mL.ConclusionThe method is accurate,convenient and rapid,which could be used in the quantitative determination of plasma concentration of MPA,MPAG in renal transplantion patients.
mycophelic acid; mycophenolic acid glucuronide; renal transplant recipients; HPLC; plasma concentration
10.3969/j.issn.1005-1678.2016.11.004
杨春兰,女,硕士,研究方向:临床药学,E-mail:yangchunlan0928@126.com;许杜娟,通信作者,女,博士,主任药师,副教授,研究方向:临床药学、肿瘤药理学,E-mail:xudujuan6365@163.com。
R917
A
