嗜水气单胞菌菌蜕系统的构建及其免疫效果研究
2016-06-15李绍戊刘红柏尹家胜卢彤岩
李绍戊,王 荻,刘红柏,尹家胜,卢彤岩
(中国水产科学研究院 黑龙江水产研究所,黑龙江 哈尔滨 150070)
嗜水气单胞菌菌蜕系统的构建及其免疫效果研究
李绍戊,王荻,刘红柏,尹家胜,卢彤岩
(中国水产科学研究院 黑龙江水产研究所,黑龙江 哈尔滨 150070)
[摘要]【目的】 探讨鱼源嗜水气单胞菌菌蜕系统的可行性和应用性。【方法】 以PhiX174基因组DNA为模板,对LysisE基因进行PCR扩增,并将纯化的PCR产物与原核表达载体pBV220双酶切后连接,构建溶菌质粒pBV220-LysisE。将pBV220-LysisE转入嗜水气单胞菌LN0925株中,构建LN0925(pBV220-LysisE)菌蜕疫苗(AHGs),进而通过溶菌动力学过程检测、电镜下细菌形态观察和动物免疫保护试验等评价所制备的菌蜕疫苗。【结果】 PCR扩增成功获得长度为276 bp的噬菌体LysisE基因;成功构建pBV220-LysisE重组质粒及AHGs。在42 ℃诱导60 min后,LN0925(pBV220-LysisE)菌株开始出现溶菌现象,至3 h后溶菌基本结束;溶菌至210 min时,其裂解效率达到99.99%。菌液浓度对菌蜕裂解效率的影响试验表明,不同浓度质粒pBV220-LysisE均可以高效诱导嗜水气单胞菌LN0925株裂解。电镜观察发现,AHGs形成明显的溶菌孔道,整体细胞形态完好,且内容物流失。动物免疫保护试验结果表明,AHGs疫苗能明显提高鲤鱼的血清抗体水平,在免疫后5-6周血清抗体凝集效价达到1∶256,从第7周开始呈下降趋势;AHGs和甲醛灭活疫苗(FKC)的相对保护率分别为77.78%和55.56%。【结论】 AHGs能够有效激活鱼体的免疫系统并产生免疫保护,且较FKC具有更好的免疫保护效果。
[关键词]嗜水气单胞菌;菌蜕;pBV220-LysisE;免疫保护
嗜水气单胞菌(Aeromonashydrophila)隶属于气单胞菌科(Aermonadaceae)气单胞菌属(Aeromonas),是人、畜及水生动物共患的条件致病菌[1]。在水产养殖动物中,鲤、鲫、鲢、鳙、鳊、草鱼、罗非鱼、鲶鱼、黄鳝、鳜鱼等均可感染嗜水气单胞菌,并因此导致细菌性败血症的发生,发病率和死亡率很高。目前,嗜水气单胞菌已成为我国淡水鱼类养殖业病害的主要病原菌,受到广大专家和学者的高度重视。
国内对淡水鱼细菌性败血症的防治主要采取抗生素和化学药物配合使用的方法,但长期使用会导致药物残留及细菌多重耐药等严峻问题。与抗生素和化学药物相比,疫苗因其安全性好、制备容易等特点成为防控嗜水气单胞菌感染的有效手段之一。目前,已报道的渔用疫苗种类主要包括灭活苗[2]、弱毒苗[3-4]、基因工程亚单位苗[5]等,但都存在一定的缺点。近年来,菌蜕系统(Bacterial ghosts,BGs)作为一种新型的基因工程疫苗体系,因成本低、可大量制备、无需添加佐剂、可同时引起鱼类体液和细胞免疫应答及可作为药物递送载体等优点受到科研人员的青睐[6-7]。同时,BGs还可作为外来细菌或病毒抗原的载体系统,因而可以利用其构建安全有效的多价疫苗。
作为一种新型疫苗,BGs在水产应用方面的研究仍处于实验室阶段,尚未投入生产。科研人员分别制备了嗜水气单胞菌[8]、迟缓爱德华菌(Edwardsiellatarda)[9-10]、鳗弧菌(Vibrioanguillarum)[11]、海豚链球菌(Streptococcusiniae)[12]和柱状黄杆菌(Flavobacteriumcolumnare)[13]等常见致病菌的菌蜕疫苗,并对其免疫保护效果进行了比较,为BGs在水产养殖细菌性疾病免疫防控中的应用提供了可行性评价和实验数据。本试验针对淡水鱼细菌性败血症的病原嗜水气单胞菌制备菌蜕疫苗(AHGs),并通过动物免疫试验评价AHGs的应答水平及免疫保护效果,以期为进一步研发有效的菌蜕疫苗提供理论依据。
1材料与方法
1.1材料
嗜水气单胞菌LN0925和大肠杆菌(E.coli)DH5α,本实验室保存,其中嗜水气单胞菌LN0925株系从患细菌性败血症的鲤鱼体内分离得到。噬菌体PhiX174购自Novagen公司;温控诱导表达载体pBV220由哈尔滨兽医研究所刘思国教授惠赠,其物理图谱见图1[14]。
PCR所用试剂、限制性内切酶EcoRⅠ和PstⅠ、质粒提取试剂盒和胶回收试剂盒均购自Fermentas公司;弗氏佐剂购自Sigma公司;其他常规试剂均为国产分析纯试剂。
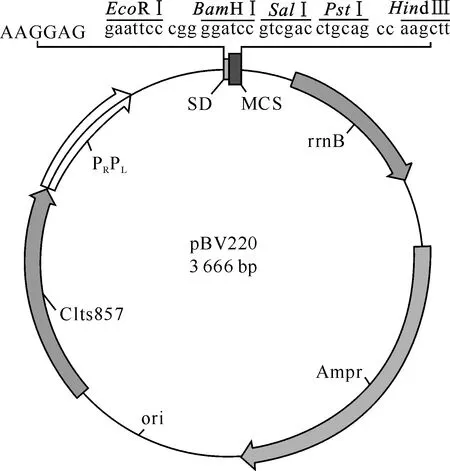
图 1 温控诱导表达载体pBV220的物理图谱
1.2LysisE基因片段的PCR扩增
根据GenBank数据库中噬菌体PhiX174的裂解基因LysisE序列(GenBank登录号:J02482.1)设计1对引物LysisE-F/LysisE-R,在上下游引物序列中分别插入EcoRⅠ和PstⅠ酶切位点,LysisE-F 5′-AGGGAATTCATGGTACGCTGGACTTTGTGG-3′(下划线部分为EcoRⅠ酶切位点),LysisE-R 5′-AGGCTGCAGTCACTCCTTCCG-3′(下划线部分为PstⅠ酶切位点)。引物由生工生物工程上海股份有限公司合成。提取噬菌体PhiX174的基因组DNA,以之为模板对LysisE基因进行PCR扩增。PCR反应体系为:模板0.5μL,10μmol/LLysisE-F/LysisE-R引物各2μL,10×PCR反应缓冲液5μL,10mmol/LdNTP1μL,2U/μLTaqDNA聚合酶0.5μL,加ddH2O补足至50μL。反应条件为:95 ℃预变性5min;94 ℃ 30s,60 ℃ 30s,72 ℃ 30s,30个循环;72 ℃延伸10min。取PCR产物进行1.2%琼脂糖凝胶电泳检测,并用胶回收试剂盒回收目的片段。
1.3pBV220-LysisE重组质粒的构建
将回收纯化的PCR产物和温控诱导表达载体pBV220分别进行EcoRⅠ和PstⅠ双酶切处理后,凝胶回收LysisE目的片段和pBV220载体,并利用T4DNA连接酶将两者相连接。连接体系为LysisE目的片段6μL,pBV220载体2μL,T4ligasebuffer1μL和T4DNAligase1μL,于16 ℃循环水浴锅中连接过夜后,将连接产物转化大肠杆菌DH5α,扩大培养后提取质粒进行PCR、EcoRⅠ/PstⅠ双酶切和测序鉴定,将鉴定正确的重组质粒命名为pBV220-LysisE。
1.4嗜水气单胞菌菌蜕疫苗的制备及其溶菌动力检测
采用CaCl2法[15]制备嗜水气单胞菌LN0925株感受态细胞。从大肠杆菌DH5α(pBV220-LysisE)中提取质粒,将其转入嗜水气单胞菌LN0925中,于含100 mg/L氨苄青霉素(Amp)的LB平板上筛选阳性克隆。挑取单克隆于含有Amp的LB液体培养基中,30 ℃ 180 r/min振荡过夜,提取质粒进行PCR和EcoRⅠ/PstⅠ双酶切鉴定。向鉴定正确的菌液中加入体积分数16%的甘油,保存于-80 ℃冰箱中,备用。
从-80 ℃冰箱取出冻存的LN0925(pBV220-LysisE),划线接种于含100 mg/L Amp的平板上,30 ℃倒置培养过夜;挑取单菌落接种于3 mL含100 mg/L Amp的 LB液体培养基中,30 ℃ 180 r/min振荡培养过夜;次日,按体积比1∶100比例转接至100 mL Amp抗性的LB液体培养基中,30 ℃ 180 r/min振荡至OD600为0.4~0.5时,将温度调至42 ℃诱导LysisE基因表达;每隔15 min取样检测其OD600,直到诱导后培养物的OD600值趋于平稳为止。计算裂解效率:裂解效率=(1-诱导后活菌数/诱导前活菌数)×100%,其中诱导前后的活菌数通过稀释涂板法进行统计。
1.5AHGs菌液浓度对裂解效率的影响
参照1.4节的方法对LN0925(pBV220-LysisE)进行培养,使其初始OD600值分别为0.4,0.6,0.8和1.0后置于42 ℃摇床诱导LysisE基因表达3 h,期间每隔30 min取菌液测OD600值,计算裂解效率。
1.6AHGs的扫描电镜和透射电镜观察
将制备的嗜水气单胞菌菌蜕(A.hydrophilaghosts,AHGs)悬液于离心机中3 000g离心10 min,加入体积分数2.5%的戊二醛4 ℃固定1.5 h,然后用1×PBS缓冲液洗涤3次,经乙醇逐级脱水和叔丁醇置换等步骤处理后,将细胞进行冷冻干燥,用含银离子的包埋剂处理后进行扫描电镜(Hitachi S-3400N)观察。
将制备的AHGs悬液于离心机中3 000g离心10 min,加入体积分数2.5%的戊二醛4 ℃固定2~3 h,用1×PBS缓冲液洗涤3次;再用质量分数2%的锇酸固定1.5 h,PBS洗脱3次,经乙醇逐级脱水后将样品用树脂包埋;包埋样品经切片和染色后进行透射电镜(Hitachi-7650)观察。
1.7AHGs的免疫效果检测
取健康鲤鱼60尾(平均体质量约为100 g/尾,购自黑龙江水产研究所呼兰水产试验站),于室内水族箱中暂养1周,试验期间水温为(26±1) ℃,放养密度为30尾/m3。试验鱼经外观、镜检、剖检及病原分离确定无病后用于后续试验。
按1.4方法制备AHGs,用1×PBS缓冲液洗涤3次,备用。LN0925株灭活疫苗(Formalin-killedA.hydrophila,FKC)按照常规方法制备,甲醛灭活后添加弗氏佐剂。将试验鱼随机分为3组,每组20尾,按照每50 g 0.2 mL的剂量分别腹腔注射AHGs、FKC和PBS。于免疫后第2、3、4、5、6、7周从试验鱼尾静脉取血,分离血清,用微量凝集反应测定血清抗体效价。在微量血凝板上,将被测血清用无菌PBS做连续等比稀释,每孔含稀释血清50 μL,然后向每孔加入50 μL免疫反应抗原,将血凝板轻轻振荡,于37 ℃放置过夜。若血凝板底部出现菌体沉积且边缘模糊,则判定为阳性反应;若底部出现轮廓清晰的圆形沉积物,则判定为阴性反应。呈明显阳性反应的最高稀释度即为血清的抗体效价。
在免疫7周后进行攻毒试验,检测疫苗的保护效果。将密度为2×108CFU/mL的LN0925株腹腔注射试验鱼,连续观察5 d并记录死亡数。根据公式计算疫苗的相对保护率(Relative percent survival,RPS),RPS=(1-免疫组死亡数/对照组死亡数)×100%。
2结果与分析
2.1重组质粒pBV220-LysisE的构建
以噬菌体PhiX174基因组DNA为模板,利用PCR方法对裂解基因LysisE进行扩增。凝胶电泳结果表明,PCR产物在276 bp左右有明显的条带(图2)。将回收纯化的PCR产物和温控诱导表达载体pBV220连接,构建重组质粒pBV220-LysisE,经PCR鉴定获得了276 bp的片段;EcoRⅠ/PstⅠ双酶切鉴定获得了与目的基因片段长度相符的片段(图3);测序分析表明,成功构建了pBV220-LysisE重组质粒(图4)。
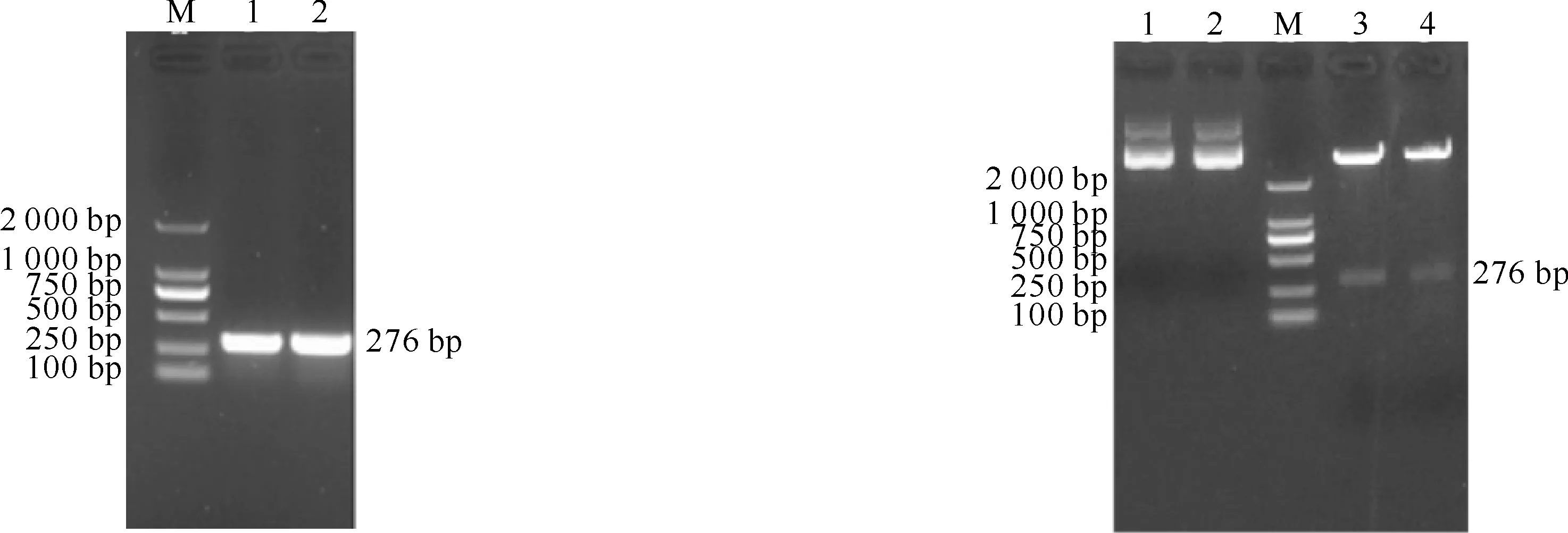
图 2噬菌体PhiX174裂解基因LysisE的PCR扩增
M.DL2000 DNA Marker;1,2.LysisE基因PCR产物
Fig.2PCR amplification ofLysisEgene of PhiX174
M.DL2000 DNA Marker;1,2.PCR products ofLysisEgene
图 3pBV220-LysisE重组质粒的双酶切鉴定
M.DL2000 DNA Marker;1,2.pBV220-LysisE重组质粒;3,4.EcoRⅠ和PstⅠ双酶切的pBV220-LysisE重组质粒
Fig.3Restriction enzyme digestion of recombinant plasmid pBV220-LysisE
M.DL2000 DNA Marker;1,2.Undigested pBV220-LysisE;3,4.pBV220-LysisE digested byEcoRⅠ andPstⅠ

图 4pBV220-LysisE重组质粒测序及序列比对结果下划线标出上下游EcoRⅠ/PstⅠ酶切位点
Fig.4Sequenc analysis of recombinant plasmid pBV220-LysisE The underlines show the restriction enzyme cutting sites ofEcoRⅠ andPstⅠ
2.2嗜水气单胞菌LN0925菌蜕疫苗的制备及其溶菌动力学检测
将pBV220-LysisE重组质粒转入嗜水气单胞菌LN0925株中,经PCR及双酶切鉴定后成功获得LN0925(pBV220-LysisE)。LN0925(pBV220-LysisE)菌株于30 ℃培养至OD600为0.4~0.5时,将温度调至42 ℃诱导LysisE表达,结果显示在42 ℃诱导60 min后开始出现溶菌现象,至180 min后溶菌基本结束,溶菌至210 min时,LN0925(pBV220-LysisE)的裂解效率达到99.99%(图5)。
菌液浓度对菌蜕裂解效率的影响试验结果表明,质粒pBV220-LysisE可以高效诱导嗜水气单胞菌LN0925株的裂解,在培养物的初始OD600值分别为0.4,0.6,0.8和1.0时,溶菌过程均在3 h左右结束(图6),且裂解效率均达到99.99%。

图 5AHGs的溶菌动力学曲线
Fig.5The lysis curve of AH Ghosts
图 6不同初始培养浓度对AHGs裂解效率的影响
Fig.6Effects of different initial concentrations of AHGs on lysis efficiency
2.3嗜水气单胞菌LN0925菌蜕疫苗的扫描电镜和透射电镜观察
扫描电镜观察结果(图7-A、B)显示,菌蜕细胞的形态和表面结构无明显变化,在细胞两极或中央形成溶菌孔道;透射电镜观察结果(图7-C、D、E)也显示,AHGs形成明显的溶菌孔道,整体细胞形态完好,且内容物流失;另外,也有部分未裂解完全的细菌。

图 7嗜水气单胞菌LN0925株菌蜕的扫描电镜(SEM)和透射电镜(TEM)观察
A.正常菌株SEM照片(×10 000);B.菌蜕SEM照片(×10 000);C~E.菌蜕TEM照片,其放大倍数分别为50 000,40 000,40 000倍;白色箭头所示为溶菌孔道
Fig.7Observation of LN0925 (pBV220-LysisE) morphology using scanning electron microscope (SEM) and transmission electron microscope (TEM)
A.Morphology of control strain using SEM (×10 000);B.Morphology of AHGs using SEM (×10 000);C-E:Morphology of AHGs using TEM,with the magnification of 50 000,40 000 and 40 000,respectively;white arrows indicate the lysis tunnels
2.4嗜水气单胞菌LN0925菌蜕疫苗的免疫效果
AHGs对鲤鱼血清抗体水平的影响结果如图8所示。由图8可知,所制备的AHGs疫苗能明显提高鲤鱼的血清抗体水平,在免疫第5-6周后血清抗体凝集效价达到1∶256,从第7周开始呈下降趋势(图8)。
AHGs免疫对嗜水气单胞菌攻毒免疫保护率的影响结果见表1。表1表明,PBS对照组死亡率达90%,而菌蜕免疫组和甲醛灭活疫苗免疫组的相对保护率分别为77.78%和55.56%,说明所制备的菌蜕疫苗能够有效保护鲤鱼抵抗嗜水气单胞菌的感染。
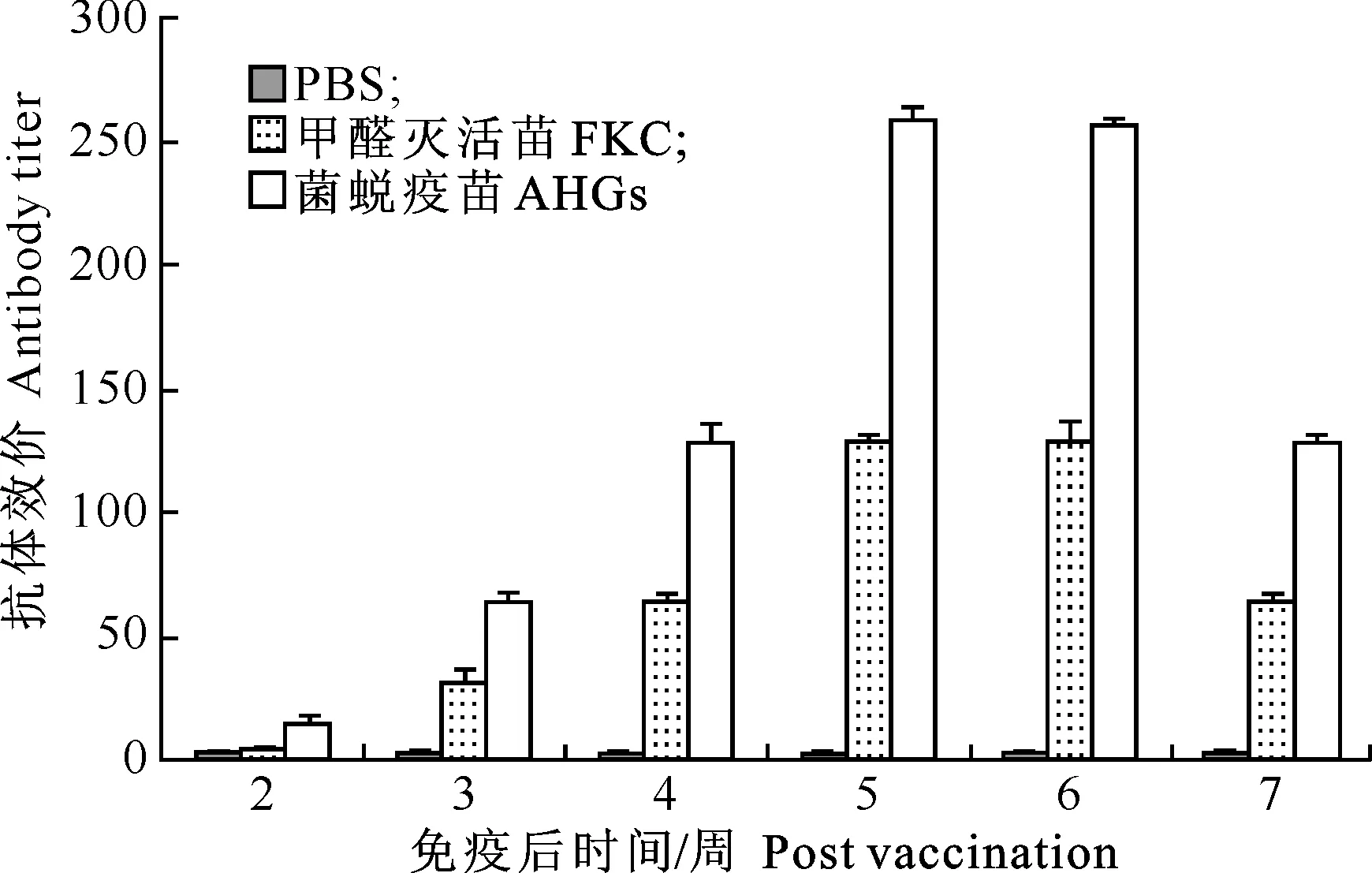
图 8 AHGs对鲤血清中抗体水平的影响

表 1 AHGs免疫对嗜水气单胞菌攻毒保护率的影响
3讨论
菌蜕系统作为一种新型疫苗体系,是通过对噬菌体PhiX174裂解基因LysisE的精确表达调控建立的,其兼顾了抗原免疫原性、佐剂效应和靶向性载体的作用。已有研究表明,病原菌的外膜蛋白、菌毛、脂多糖等成分是重要的免疫保护性抗原[16-17],而菌蜕系统最低限度地改变了细菌的外膜结构,在保留了较完整的细胞膜结构和相关抗原蛋白的基础上,使细菌遗传物质、毒素等流失,消除了耐药基因或毒力岛基因的水平转移引起的潜在危害,从而有效地刺激机体产生免疫应答。
近年来,鱼类细菌性病害大规模爆发,除常规疫苗外,新型渔用菌蜕疫苗逐渐成为研究的热点。本研究以温控诱导表达载体pBV220为骨架,将噬菌体PhiX174的裂解基因LysisE插入其中,并利用PL/PR启动子和编码对该启动子具有抑制作用而又对温度敏感的cI蛋白基因调控其表达,成功构建了pBV220-LysisE重组质粒。溶菌动力学试验表明,嗜水气单胞菌LN0925(含pBV220-LysisE)在42 ℃诱导60 min后开始出现溶菌现象,至3 h后溶菌基本结束,其裂解效率达到99.99%,该结果与储卫华等[8]的研究结果稍有差别,溶菌出现时间提前了30 min左右。其他菌株如迟缓爱德华菌[18]在温控诱导120 min后出现溶菌现象,表明溶菌时间可能受到菌株、载体等因素的影响。另外,不同初始培养物浓度下,细菌菌蜕均具有较高的裂解效率,表明可以通过发酵过程大量制备该疫苗。扫描电镜和透射电镜观察结果显示,所制备的AHGs形成了明显的溶菌孔道,整体细胞形态完好,且内容物流失。
动物免疫试验结果表明,菌蜕组AHGs免疫的鲤鱼血清抗体效价明显高于甲醛灭活组FKC和对照组PBS,且攻毒后AHGs对鱼体的相对保护率达77.78%,而甲醛灭活疫苗FKC和对照组的试验鱼死亡率分别为40%和90%,提示所制备的AHGs能够有效保护鲤鱼抵抗嗜水气单胞菌的感染。目前,渔用菌蜕疫苗的研究仍处于实验室阶段,针对鱼类几种病原菌如链球菌[12]、迟缓爱德华菌[9-10]、鳗弧菌[11]、柱状黄杆菌[13]等的菌蜕疫苗的保护效果分析显示,不同免疫方式如口服、浸泡或腹腔注射均可有效诱导机体产生免疫应答,这些研究结果提示BGs是一种具有良好应用前景的渔用疫苗类型[19]。
[参考文献]
[1]陆承平.致病性嗜水气单胞菌及其所致鱼病综述 [J].水产学报,1992,16(3):282-288.
Lu C P.PathogenicAeromonashydrophilaand the fish diseases caused by it [J].Journal of Fisheries of China,1992,16(3):282-288.(in Chinese)
[2]Kozinska A,Guz L.The effect of variousAeromonasbestiarumvaccines on non-specific immune parameters and protection of carp (CyprinuscarpioL.) [J].Fish and Shellfish Immunology,2004,16(3):437-445.
[3]Shoemaker C A,Klesius P H,Drennan J D,et al.Efficacy of a modified liveFlavobacteriumcolumnarevaccine in fish [J].Fish and Shellfish Immunology,2011,30(1):304-308.
[4]Swain P,Behera T,Mohapatra D,et al.Derivation of rough attenuated variants from smooth virulentAeromonashydrophilaand their immunogenicity in fish [J].Vaccine,2010,28(29):4626-4631.
[5]Poobalane S,Thompson K D,Ardó L,et al.Production and efficacy of anAeromonashydrophilarecombinant S-layer protein vaccine for fish [J].Vaccine,2010,28(20):3540-3547.
[6]Jalava K,Hensel A,Szostak M,et al.Bacterial ghosts as vaccine candidates for veterinary applications [J].Journal of Controlled Release,2002,85(1/3):17-25.
[7]Szostak M P,Hensel A,Eko F O,et al.Bacterial ghosts:non-living candidate vaccines [J].Journal of Biotechnology,1996,44(1/2/3):161-170.
[8]储卫华,庄禧懿,陆承平.嗜水气单胞菌菌蜕的制备及其对银鲫的口服免疫 [J].微生物学报,2008,48(2):202-206.
Chu W H,Zhuang X Y,Lu C P.Generation ofAeromonashydrophilaghosts and their evaluation as oral vaccine candidates inCarassiusauratusgibelio[J].Acta Microbiologica Sinica,2008,48(2):202-206.(in Chinese)
[9]Kwon S R,Nam Y K,Kim S K,et al.Protection of tilapia (Ore-ochromismosambicus) from edwardsiellosis by vaccination withEdwardsiellatardaghosts [J].Fishand Shellfish Immunology,2006,20:621-626.
[10]Kwon S R,Lee E H,Nam T K,et al.Efficacy of oral immunization withEdwardsiellatardaghosts against edwardsiellosis in olive flounder (Paralichthysolivaceus) [J].Aquaculture,2007,269:84-88.
[11]Kwon S R,Kang Y J,Lee D J,et al.Generation of vibrio anguillarum Ghost by coexpression of PhiX 174LysisEgene and staphylococcal nuclease A gene [J].Molecular Biotechnology,2009,42:154-159.
[12]Ra C H,Kim Y J,Park S J,et al.Evaluation of optimal culture conditions for recombinant ghost bacteria vaccine production with the antigen ofStreptococcusiniaeGAPDH [J].Journal of Microbiology and Biotechnology,2009,19:982-986.
[13]Zhu W,Yang G,Zhang Y,et al.Generation of biotechnology-derivedFlavobacteriumcolumnareghosts by PhiX174 gene E-mediated inactivation and the potential as vaccine candidates against infection in grass carp [J/OL].Journal of Biomedicine and Biotechnology,2012[2014-09-10].http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3376489/.DOI:10.1155/2012/760730.
[14]Yu S Y,Peng W,Si W,et al.Enhancement of bacteriolysis of shuffled phage PhiX174 gene E [J].Virology Journal,2011,8:206.
[15]萨姆布鲁克J,拉塞尔D W.分子克隆实验指南 [M].3版.北京:科学出版社,2003:96-99.
Sambrook J,Russell D W.Molecular cloning laboratory manuals [M].3rd Edition.Beijing:Science Press,2003:96-99.(in Chinese)
[16]张崇文,于涟,毛芝娟,等.哈维氏弧菌外膜蛋白OmpK基因的克隆及原核表达 [J].水产学报,2006,30(1):9-14.
Zhang C W,Yu L,Mao Z J,et al.Cloning and expression of OmpK gene fromVibrioharveyiinPseudosciaenacrocea[J].Journal of Fisheries of China,2006,30(1):9-14.(in Chinese)
[17]Mayr U B,Walcher P,Azimpour C, et al. Bacterial ghosts as antigen delivery vehicles [J].Advanced Drug Delivery Reviews,2005,57:1381-1391.
[18]李宁求,余露军,付小哲,等.鳗源迟缓爱德华氏菌菌蜕的构建及制备条件优化 [J].水产学报,2012,36(11):1754-1762.
Li N Q,Yu L J,Fu X Z,et al.Construction ofEdwardsiellatardaghosts from eel and their optimization of preparation conditions [J].Journal of Fisheries of China,2012,36(11):1754-1762.(in Chinese)
[19]李绍戊,卢彤岩.菌蜕系统作为新型渔用疫苗体系的研究进展 [J].生物技术通报,2012(11):43-48.
Li S W,Lu T Y.Advances in the research of the novel fish vaccine system:Bacterial Ghosts [J].Biotechnology Bulletin,2012(11):43-48.(in Chinese)
Establishment ofAeromonashydrophilaghosts system and its immune effect
LI Shao-wu,WANG Di,LIU Hong-bai,YIN Jia-sheng,LU Tong-yan
(HeilongjiangRiverFisheriesResearchInstitute,ChineseAcademyofFisherySciences,Harbin,Heilongjiang150070,China)
Abstract:【Objective】 This study aimed to study thefeasibility and application of BGs in Aeromonas hydrophila isolated from fish.【Method】 ThelysisE gene in the bacteriophage PhiX174 was cloned by PCR amplification and the PCR products were then digestedby double enzyme and ligated to the prokaryotic expression vector pBV220.The lysis plasmid pBV220-LysisE was constructed and then transformed to Aeromonas hydrophila LN0925 strain to prepare A.hydrophila ghosts (AHGs).The lysis curves,morphology observation and animal immunoprotection test of AHGs were performed to evaluate the effects of AHGs prepared.【Result】 The LysisE gene with size of 276 bp was cloned into pBV220 vector and the recombinant plasmid pBV220-LysisE was constructed and successfully transformed to LN0925 strain to prepare AHGs.LN0925 (pBV220-LysisE) lysed at 60 min after induced at 42 ℃ and the lysis process continued for 3 h.The lysis efficiency of AHGs induction was 99.99%.Effects of initial culture concentrations on lysis efficiency indicated that pBV220-LysisE could highly induce lysis of LN0925 strain.The morphology of lysed bacteria was observed by scanning electron microscope and transmission electron microscope,and it was found that AHGs formed obvious lysis tunnels with entire cell structure.Animal protective immunity test was carried out to evaluate the immune effect of AHGs on common carp (Cyprinus carpio).The results suggested that AHGs could obviously improve the level of antibody in serum and the agglutination titer reached 1∶256 after 5-6 weeks by immunization with vaccines.Challenge test showed that the relative percent survival (RPS) of AHGs and Formalin-killed vaccine (FKC) were 77.78% and 55.56%,respectively.【Conclusion】 As a novel type of vaccine system,AHGs could active the immune system of fish and provide a better protective effects against A.hydrophila infection in common carp when compared to FKC.
Key words:Aeromonas hydrophila;bacterial ghosts;pBV220-LysisE;protective immunity
DOI:网络出版时间:2016-03-1408:4510.13207/j.cnki.jnwafu.2016.04.003
[收稿日期]2014-08-21
[基金项目]“十二五”国家科技支撑计划项目(2012BAD25B10);中国水产科学研究院基本科研业务费项目(2014A06XK05);黑龙江省自然科学基金面上项目(C201140)
[作者简介]李绍戊(1982-),男,山东莱阳人,副研究员,博士,主要从事鱼类病原生物学研究。E-mail:swli_1982@163.com[通信作者]卢彤岩(1967-),女,吉林长春人,研究员,博士,主要从事鱼类病害研究。E-mail:lutongyan@hotmail.com
[中图分类号]S942.5
[文献标志码]A
[文章编号]1671-9387(2016)04-0017-07
网络出版地址:http://www.cnki.net/kcms/detail/61.1390.S.20160314.0845.006.html
