太湖沉积物铁形态分布特征及磷铁相关性分析
2016-05-27杨文斌丁士明安徽师范大学环境科学与工程学院安徽芜湖41003中国科学院南京地理与湖泊研究所湖泊与环境国家重点实验室江苏南京10008
杨文斌,唐 皓,韩 超,丁士明(1.安徽师范大学环境科学与工程学院,安徽 芜湖 41003;.中国科学院南京地理与湖泊研究所,湖泊与环境国家重点实验室,江苏 南京 10008)
太湖沉积物铁形态分布特征及磷铁相关性分析
杨文斌1*,唐 皓1,2,韩 超2,丁士明2(1.安徽师范大学环境科学与工程学院,安徽 芜湖 241003;2.中国科学院南京地理与湖泊研究所,湖泊与环境国家重点实验室,江苏 南京 210008)
摘要:通过对太湖藻型湖区、草藻过渡型湖区、草型湖区柱状沉积物进行铁的形态分级分析沉积物中不同提取态磷铁含量,获得不同形态铁的空间分布特征.结果表明:沉积物总铁含量藻型湖区31.57mg/g(SD=8.51)>过渡型湖区30.34mg/g(SD=11.97)>草型湖区25.25mg/g(SD=4.59),不同湖区沉积物中铁形态的含量依次为可还原(晶型)铁氧化物Feox2>碳酸盐铁Fecarb>易还原(无定形)铁氧化物Feox1>低活性硅酸铁Feprs>磁铁矿Femag>可吸附性Fe(Ⅱ),Fecarb、Feox1、Feox2,3种铁形态属于高活性铁Fe(III),含量为7.79,6.16,8.18mg/g,分别占总铁含量的28.56%,21.54%,29.53%,表明高活性铁(III)是沉积物中最主要的铁形态;沉积物中各提取态磷含量大小比较为NH2OH⋅HCl-P>MgCl2-P>NaAc-P>Na2S2O4-P>浓HCl-P>(NH4)2C2O4-P,含量较高的MgCl2-P(0.067mg/g)、NaAc-P(0.061mg/g)、NH2OH⋅HCl-P(0.068mg/g),分别占总提取磷的35.28%、31.97%和22.55%,是沉积物铁分级提取态磷中最主要的形态.磷-铁相关性分析表明,二者之间呈显著的正相关(P<0.05),进一步从铁形态分级角度证实铁是沉积物內源磷释放的关键因子.
关键词:铁形态分级;藻型湖区;草藻过渡型湖区;草型湖区;相关性分析;太湖
∗ 责任作者, 教授, ywb1968@mail.ahnu.edu.cn
磷已被证实是我国大多数湖泊富营养化的主要限制性因子,对水体营养状态和生态系统结构发挥着十分关键的调控作用[1-3].尽管近些年对外源污染治理力度的加大,但湖泊污染现状依然严峻,究其原因与内源污染的强度增加有关,其中,内源磷污染备受关注.已有研究发现,很多浅水富营养化湖泊都会发生高强度的内源磷污染,造成水体富营养化治理效果出现滞后的现象[4-5].国内外围绕沉积物磷内源污染发生过程及界面交换机制开展了大量研究,经典的内源磷释放机制是1941年Mortimer[7]提出的铁-磷耦合机制.该机制认为,沉积物磷的释放能力受铁控制,即好氧条件下,FeO(OH)对无机磷有着较强的吸附能力;在厌氧条件下,FeO(OH)被还原溶解,同时释放所吸附的磷[8].Jensen等[9]在对丹麦100多个湖泊沉积物中Fe和P的调查发现,沉积物中的总铁含量与总磷含量呈显著正相关.铁的还原与有机质氧化降解的耦合作用,是沉积物早期成岩过程中最为重要的生物地球化学反应之一[10].由此可见,沉积物铁是控制内源磷释放的关键因子之一,在调节湖泊生态环境质量及生物生产力方面扮演重要作用.
铁在沉积物中是以不同形态存在的,不同的赋存形态与环境的相互作用会直接影响到其在环境中的生物可利用性、释放、迁移等特性.我国最早对铁的研究是19世纪30年代对水稻土中铁的氧化还原机制及其对层状粘土矿物的掩盖作用[11];邹元春等[12]研究了三江平原典型多级沟渠系统0~60cm沉积物全铁含量的空间分布特征,结果表明各类型、各等级的沉积物铁含量具有极显著差异,整个多级沟渠系统沉积物各层的铁含量没有显著性差异.杨宏伟等[13]应用颗粒物中铁的连续浸提技术研究了黄河干流表层沉积物中铁形态的分布特征及相关性;王超等[14]考察了典型城市浅水湖泊沉积物不同的磷和铁形态分布特征并初步分析二者相关关系,证实沉积物总磷的变化受活泼性铁形态影响最大.尽管如此,目前对太湖沉积物铁或磷形态的单独研究较多,且多集中在表层沉积物形态分布变化,而对太湖沉积物不同湖区不同铁形态的总量测定和空间分布的系统研究,特别是从沉积物铁的形态分级提取角度讨论沉积物中磷铁同步变化规律的研究尚少.本研究选择太湖3种不同类型的湖区,采用铁分级方法获得不同形态的铁和磷浓度在3种类型湖区的空间(水平和垂直)分布特征,并分析不同形态铁与相应结合态磷的相关性,旨在为沉积物中不同铁形态的总量测定和空间分布及为磷铁经典耦合机制提供依据.
1 材料和方法
1.1 研究区域概况
本文以太湖的藻型湖区竺山湾附近(31.338°N,120.180°E,标记为1#)、草藻过渡湖区湖心附近(31.387°N,120.296°E,2#)和草型湖区胥口湾附近(31.289°N,120.321°E,3#)为研究对象,在每个湖区分别选取1个采样点.其中,竺山湾位于太湖北部湖区属于富营养化程度较高的藻型湖泊,该湖湾以浮游植物占优势,水体透明度较低,TN、TP和CODMn平均值分别为:6.08, 0.231, 7.40mg/L高于东部湖区及湖心.东部胥口湾属于相对健康的草型湖泊,水生植物丰富,水质较好,水体透明度为0.57m属3个湖区最高值,另外CODMn、TN和TP的浓度分别为4.99,1.57, 0.054mg/L,该湖区表层沉积物为砂质,颜色呈乌黑色.湖心区水质相对较好,水体透明度为0.24m,CODMn为4.99mg/L,TN平均值为2.93mg/L,TP平均值为0.109mg/L,为草藻过渡型湖区[15].
1.2 样品采集与处理
于2014年10月采用沉积物柱状样品采样器(φ9cm,中国科学院南京地理与湖泊研究所)采集沉积物柱芯,并立即带回实验室,取其上层5cm以0.5cm的厚度进行切片,6~12cm的沉积物以1cm的厚度进行切片,共计17个切片样品,装入自封袋放入冷冻干燥机(ALPHA 1-2LD plus ,德国Christ)干燥,干燥后的土样充分研磨混匀,然后过100目筛,贮存在自封袋中备用,同时同步监测水体水质(HORIBA,U-53)并采集上覆水和表层沉积物,带回实验室进行相关理化分析.

图1 太湖采样点示意Fig.1 Sampling sites in Lake Taihu
1.3 沉积物中铁的分级提取
对太湖沉积物中铁形态采用6级分组法连续提取,具体方法见表1,该法是在铁的化学序列提取法[16]上进行改进.具体改进为:(1)添加了一步可吸附性铁(Adsorbed Fe(II))的提取之后,再对沉积物中剩下的活性铁进行提取;(2)黄铁矿铁(Fepy)主要是由易还原(无定形)铁氧化物(Feox1)和可还原(晶型)铁氧化物(Feox2)转化得到,经过第3、4步的提取后黄铁矿铁已经低于检测限,所以省去这一步的提取;(3)非活性铁或者无活性铁(FeU)则直接用总铁含量减去第2到6步提取的铁含量既得,无需单独提取.样品做3个平行试验,结果用平均值表示.
本文并未对沉积物中磷进行单独的分级提取,而是从铁分级方法提取不同磷形态,按照表1提取方法提取后获得磷含量总和称为提取态总磷TP提取,各结合态磷用浸提剂-P表示.王振华等[17]在研究东部平原湖区对沉积物进行磷连续提取方法测定时,也同时对浸提液中的铁进行了测定.为考察该分级方法的可靠性,将铁分级的方法与杨宏伟[18]总结的沉积物中磷的连续浸提法进行了对比,可以得出在对可吸附性铁Fe(II)、Fecarb、Feox2、Feprs进行提取的同时,其浸提剂和浸提方法也可以提取出部分的可交换态Pex、钙结合态磷中的Paut、闭蓄态磷Pobs以及有机磷Porg.

表1 沉积物中铁的分级和提取方法Table 1 Classification of Fe forms in sediments and extraction methods
1.4 沉积物全量元素及TOC的测定
依据《土壤农业化学分析方法》[19]进行了沉积物土壤元素全量分析,并进行适当修正.具体步骤如下:在滤纸上称取0.200~0.209g偏硼酸锂,称取0.05000~0.05019g样品倒入偏硼酸锂上,小心重复折叠滤纸以将两者混匀.将滤纸折叠成一小球,放入坩埚中,将坩埚放进预先已升温至1000℃的马弗炉中,加热15~20min.取出坩埚,稍冷却后将熔珠倒入预先装有25mL8%(V/V)硝酸的比色管中,将比色管放入超声波清洗器中,超声溶解熔珠.待完全溶解后以去离子水定容,加盖摇匀,经进口PES水系针头滤器(0.45μm)过滤,倒入离心管存储待测.
沉积物TOC含量采用《土壤农化分析(第三版)》[20]中重铬酸钾外加热法进行测定,称取0.1000g~0.5000g(精确至0.0001g),通过0.149mm筛孔的风干土样置于硬质试管中,加入0.1g硫酸银.加入5.00mL 0.8000mol/L重铬酸钾标准溶液,再用注射器注入5mL硫酸,小心旋转摇匀.将盛有土样的硬质试管插入加热至185~190℃的油浴锅内的铁丝笼架中加热,控制油浴锅内温度在170~180℃,并使溶液保持沸腾5min.取出铁丝笼架,待硬质试管稍冷后将混合物洗入250mL锥形瓶中,加入3~4滴邻菲啰啉指示剂,用0.2mol/L硫酸亚铁铵标准溶液滴定至溶液由橙黄色经蓝绿色到棕红色为终点.再根据公式计算有机质含量.
采用Optima 2100DV电感耦合等离子体光谱仪(ICP-AES,美国PerkinElmer公司)对铁分级待测液和全量元素待测液进行测定,得到的3个点位0~12cm深度沉积物中的6种提取态磷、铁的含量和总磷、总铁含量.
1.5 数据处理
本文数据分析使用SPSS19.0,图形绘制使用Origin9.0进行处理.
2 结果与讨论
2.1 理化性质
表2常规水质指标数据中,采样的温度都在16.30~17.35℃,可忽略温度对水质的影响.DO和ORP是衡量水体氧化还原状况的指标,天然水体的饱和溶解氧在4~14mg/L范围内,各采样点的DO均饱和,处于好氧状态,其中1号点位于污染较重的竺山湾,DO明显小于其他点位;一般天然水体的pH值位于6.5~8.5之间,太湖水体的pH位于8.6~9.3之间,偏碱性,这是由于太湖富营养化污染造成,藻类聚集光合作用导致水体的pH值升高[15];总溶解态固体(TDS)、电导率是间接表示水中溶解性盐类的含量,溶解的盐类均以离子状态存在,具有一定的导电能力,因此若水体电导率高,说明水中含有溶解性固体多,可间接说明污染物含量高;浊度(NTU)是水中由于含有悬浮及胶体状态的杂质而产生的浑浊,浊度跟水深、水流和风速等都有关,在不同的点位差异很大.

表2 研究点位常规水质参数、营养盐指标及沉积物部分理化指标值Table 2 Physic-chemical properties of waters and sediments from the investigated locations
从表2可以看出,在污染较重的1#点,水体中氮磷含量明显高于其他区域;而3#点氮磷含量较低,污染较轻,叶绿素含量的分布也呈现同样的趋势.沉积物中总磷的变化趋势和总铁一样,竺山湾最高1.00(0.51~1.65)mg/g,湖心其次0.74(0.34~ 1.25)mg/g,草型湖区含量最低0.45(0.22~ 0.93)mg/g,竺山湾属于西北部藻型湖区,处于富营养化状态,水体污染程度明显高于东部及南部且变化梯度大,这反应了太湖水体的总体污染状况[21].
2.2 不同湖区铁的含量和形态分布特征
2.2.1 不同湖区全量总铁及铁形态分级总铁含量分布特征 将湖泊表层沉积物剖面分级提取所得到的每步铁含量相加,得到太湖表层沉积物铁分级TFe含量(TFe分级),浓度范围为13~47mg/g之间,均值为27.88mg/g.这与Liu等[22]在2012年测得的太湖沉积物金属Fe含量平均值为35.3mg/g基本一致,其中1#柱状沉积物TFe分级含量16~41mg/g,均值为30.29mg/g(SD=8.56);2#柱状沉积物TFe分级浓度范围在13~47mg/g,均值29.06mg/g(SD=11.97);3#柱状沉积物TFe分级含量14~31mg/g,均值24.29mg/g(SD=4.58).通过土壤元素全量分析测得的3个采样点的全量总Fe(TFe)为31.57mg/g(SD=8.51),30.34mg/g(SD= 11.97),25.25mg/g(SD=4.59),TFe分级占全量TFe的比例为95.95%,95.78%,96.21%,太湖3种类型湖区的沉积物总铁含量在藻型湖区富营养化程度最高,过渡型湖区其次,草型湖区具有较强的自净能力,因而3种湖区沉积物表层磷铁的累积能力也依次减弱.

图2 研究点位沉积物剖面中各形态铁浓度及全量总铁浓度Fig.2 Vertical profiles of different iron speices and total iron in the sediments from the investigated locations
2.2.2 不同湖区沉积物中各形态铁含量垂直分布特征 由图2可知,藻型湖区、过渡型湖区可吸附性Fe(II)几乎均低于检测限(<0.011mg/L),这是因为太湖水体偏碱性(pH位于8.6~9.3),水体中大部分铁离子由于形成氢氧化物而沉积在沉积物表面上,自由的可吸附性Fe(II)含量极低.1#剖面TFe分级含量整体趋势是随着深度先略微降低后缓慢升高,在2~3cm深度含量最低,之后随深度缓慢升高,在8cm深度达到最大值.各形态铁含量随深度的变化与TFe分级变化趋势一致.但每种形态Fe在不同深度所占百分比有显著变化,Fecarb占TFe分级百分比逐渐升高,最终占最大比例,Feox1和Feox2占TFe分级的百分比随着深度而缓慢降低,Femag和Feprs所占比例相对稳定.Fecarb的形成条件较为苛刻,只发生在富铁、缺硫、且碳酸盐含量很高的亚氧和无氧沉积环境中[23],1#沉积物随着深度的增加,Fecarb比Feox1、Feox2增加的幅度要大,说明该区域内铁及碳酸盐含量下层高于上层,这是因为附近分布着太滆运河沙塘港武进港和直湖港,富营养化区域水体自净能力差,河流输入了大量的污染物导致沉积物表层磷铁含量不断累积,经过时间推移表层的营养物质被覆盖到下层,因此外源污染物的长期输入造成藻型湖区表层沉积物铁含量随深度增加而增加,从而各形态铁尤其是Fecarb含量随深度增加而增加.
2#剖面TFe分级含量整体趋势是减小,首先升高至3.5cm深度锐减,4cm处又升到最大值47mg/g,4.5cm处铁含量再次下降至22mg/g后趋于平缓,各形态铁含量均与TFe分级变化一致.Fecarb与Feprs所占TFe分级比例先减小后增大,最终分别占TFe分级的29%和35%, Feox1和Feox2先增大后减小,Femag所占比例相对稳定.2#湖心区受污染程度轻,是沉积物剖面上层铁含量高于下层的主要原因.沉积物-水界面往下,周围环境由好氧到厌氧转变显著,出现厌氧情况时,FeO(OH)被还原溶解,导致沉积物Fe3+溶解进而转化为Fe2+, Fecarb、Feprs占TFe分级比例增减趋势与Feox1、Feox2相反,因为Feox1和Feox2中的水铁矿、纤铁矿、针铁矿、赤铁矿等均是以Fe3+形式存在的铁氧化物,缺氧时其氧化溶解有助于形成以Fe2+形式存在的晶型Fecarb中的菱铁矿和铁白云石以及层状硅酸盐铁Feprs,Fe(III)的还原性溶解及再氧化生成自生Fe(III)氧化物是沉积物中Fe循环的主要路径.
3#剖面TFe分级含量整体趋势较平缓,在3cm深度缓慢升高,在5cm深度达到最高值,之后缓慢降低,于10cm深度降到最低值.Fecarb含量变化与
TFe分级一致,除Feox2随着深度增加含量有着明显的大幅增加外,其余形态均随着深度而减小,且各形态所占比例的变化趋势和含量呈一致.3#草型湖区浮游植物和沉水植物茂盛,生物量较大,对污染物缓冲作用强,水体具有较强的自净能力,所以沉积物表层磷铁累积量相对小,沉积物-水界面铁含量变化不显著.而晶型铁氧化物Feox2含量的大幅增加,可能与Feox1中无定型铁氧化物水铁矿在草型湖区纯度较高,很容易向更稳定的针铁矿或赤铁矿转化有关.
2.2.3 不同湖区沉积物中各形态铁含量分布特征 太湖3种类型湖区的柱状沉积物中,各铁形态的含量依次为Feox2>Fecarb>Feox1>Feprs>Femag>可吸附性Fe(II),Fecarb、Feox1、Feox23种铁形态含量最高,分别占TFe分级的18.25%~39.51%, 12.45%~27.76,26.55%~32.95%,合计占TFe的72.56%~84.91%,其次为Feprs,约占TFe的11.94%~23.98%.太湖表层沉积物中层状硅酸盐铁Feprs的平均含量(4.92mg/g)明显低于世界陆架沉积物(150μmol/g即8.40mg/g),全球河流颗粒物中的含量(216.17μmol/g即12.11mg/g),以及长江颗粒物中Feprs的含量(307.14μmol/g即17.20mg/g)[24-25],太湖表层沉积物中铁形态大部分是以Fecarb、Feox1、Feox2等高活性铁形式存在,低活性硅酸盐铁含量较低.Femag含量很低,占TFe分级的2.34%~3.45%,磁铁矿是 Fe(II)和 Fe(III)混合价态的铁氧化物,在沉积物中的含量普遍较低,主要来自矿物岩碎屑或火山岩碎屑,以及细粒径的海洋自生磁铁矿,低含量的Femag说明生物控制的磁铁矿形成机制在太湖表层沉积物中不占重要地位.海洋沉积物的厌氧环境中,以自生菱铁矿(晶型FeCO3)和铁白云石[Ca(Fe2+,Mg2+, Mn2+)(CO3)2]形态存在的碳酸盐铁(II)Fecarb发生在富铁、再悬浮频繁的河口、三角洲和陆架泥质沉积物中,Fe(III)氧化物的还原主要有2个相互竞争的路径完成,即微生物(异化)还原和化学(硫化物)还原[26-27],在海洋沉积物的含氧环境中活性Fe(III)氧化物含量高、有机质含量相对较低的情况下,铁异化还原是有机质矿化的重要路径,有利于晶型碳酸盐铁(菱铁矿)的形成.将图3不同湖区沉积物有机质剖面与图2对比,有机质含量与3个湖区沉积物剖面中Fecarb形态含量呈一定的负相关性,更进一步证明了太湖湖区表层沉积物有机质含量对沉积物中碳酸盐铁的影响,有机质含量低说明有机质矿化程度高,从而铁异化还原程度高,有利于晶型Fecarb的形成.湖心区表层(0~3cm深度)沉积物有机质含量低于藻型湖区,因而其Fecarb含量相对较高;草型湖区由于水生植物丰富,其死亡后沉降到沉积物表面造成草型湖区有机质含量反而高于藻型湖区[26],所以晶型碳酸盐铁Fecarb含量草型湖区>藻型湖区>湖心.Feox1易还原(无定形)铁氧化物和Feox2可还原(晶型)铁氧化物是太湖表层沉积物中所占比例最高的铁形态,主要成分是高活性铁(III)氧化物,来源于沉积物中铁的原生矿物及铁硅酸盐矿物风化后再结晶的产物,如赤铁矿和针铁矿.其中Feox1平均含量(6.16mg/g)比富含铁的Mississippi三角洲沉积物含量(145μmol/g即8.12mg/g)[28]低,但Feox2平均含量(8.18mg/g)比Mississippi三角洲沉积物含量(72.7μmol/g即4.07mg/g)高,说明铁单矿物是太湖沉积物中铁主要的存在形式,太湖底泥中较高的活性铁(III)是控制内源磷释放的关键因子,太湖具有较高的释放风险和生物可用性.

图3 太湖研究点位沉积物有机质含量垂直剖面Fig.3 Vertical profiles of TOC in the Surface sediments of different regions from the investigated locations of Taihu
2.3 不同提取态磷形态分布特征
藻型湖区竺山湾柱状沉积物中占TP提取含量较高的是MgCl2-P、NaAc-P、NH2OH·HCl-P,分别占总提取磷的35.28%、31.97%和22.55%,而湖心区和草型湖区除这3种磷形态,Na2S2O4-P也占了较高的比例,湖心区和草型湖区4种形态磷分别占TP提取的17.09%,18.61%,47.66%, 13.41%和25.33%,20.79%,28.41%,19.10%,综上太湖3个湖区沉积物中各结合态磷含量占TP提取的百分比平均值大小为NH2OH·HCl-P(32.87%)> MgCl2-P(25.90%)>NaAc-P(23.79%)>Na2S2O4-P(13.31%)>浓HCl-P(3.43%)>(NH4)2C2O4-P(0.69%),虽然3个湖区表层沉积物中吸附性Fe(Ⅱ)占总铁的比例极低,但其分级提取的磷含量却很高,这可能由于氯化镁不仅能提取吸附性Fe(Ⅱ),还能提取其他交换态吸附性金属离子,其结合态的磷含量较高因而提高了这一部分提取态磷所占比例.根据杨宏伟等[18]总结的沉积物中磷的连续浸提法与铁分级提取方法对比得出,提取得到的MgCl2-P、NaAc-P、Na2S2O4-P、浓HCl-P中包括了部分的可由磷分级方法提出的可交换态Pex、钙结合态磷中的Paut、闭蓄态磷Pobs以及有机磷Porg,并且提取态磷含量MgCl2- P(25.90%)> NaAc-P(23.79%)>Na2S2O4-P(13.31%)与马旭阳等[29]通过磷分级方法得到的PCa(81.96%~ 97.74%)>Pex(0.36%~7.41%)>Pobs(0.00%~ 0.92%)相一致;此外通过表2可知,TP提取同总铁总磷有着一样的变化趋势,3个点TP提取占TP的百分比分别是43.06%,22.75%,20.20%,这与张路等[30]得到的位于太湖重污染湖区Fe-P约占测定总磷含量的50%,其他样点的Fe-P相对含量均小于25%的结论相一致;而沉积物中Pex、PAl、PFe化学性质活泼,易从沉积物中溶解释放而被生物利用,一般将三者之和称为活性磷Bio-P[14],因此通过铁分级方法提取的磷形态主要是活性磷中的部分Pex和PFe,其次为部分无机磷(PCa和Pobs)和有机磷Porg,而对水体磷负荷影响最大最容易释放的就是活性磷Bio-P,尤其是在太湖这种Pca不易释放的碱性水体中,高含量Bio-P的释放导致了严重的水体富营养化现象.
从铁形态分级提取得到的磷铁含量垂直剖面(图4)可以看出,随着剖面深度的增加,3个采样点磷形态变化和相对的铁形态变化类似,1#剖面Fe分级提取的磷铁含量均随着剖面深度的增加而增加,且在剖面-3.5~-4.5cm处达到最小值,之后逐渐升高,在-8~-10cm处达到最大值;2#剖面磷铁含量随着沉积物剖面深度整体降低,且在-3cm处突然降低于-3.5cm处达到一个极小值,-4cm处升到极大值,之后再降低之后平稳;3#剖面磷铁含量整体呈下降趋势,除了第4步氧化还原铁Feox2和Na2S2O4-P含量先升高后降低之后保持稳定外,其余4步的磷铁含量均在-2~3cm处先降低到极小值后,在-3~4cm处升到极大值,之后含量再次降低并保持平稳.由此可见,铁形态分级提取得到的磷铁具有极高的同步性,这是由于在提取不同形态铁的同时,影响了与这一形态铁相结合的磷形态,或者是当水动力条件和理化因子发生改变时,导致铁会以活性铁形式从沉积物中释放出Fe3+、Fe2+,与水体中的磷酸根阴离子发生络合或者吸附反应,从而影响控制与之相关的磷形态,采用铁分级方法提取出的磷是与铁形态最相关的磷形态,因此二者的变化规律具有很好的同步性.王超等[19]采用磷、铁分级方法也获得沉积物中交换态磷Ex-P、铝磷Al-P与可交换态铁F1、无定形的铁锰氧化物和水化氧化物结合态之间同步变化规律.马旭阳[29]对黄河沉积物中铁与磷的形态分布及相关分析中也发现过,黄河沉积物中Fe-6(残渣态Fe)与Paut、PDe之间呈极显著正相关(P<0.01),相关系数为0.558,0.618.不同磷、铁形态之间的同步变化说明沉积物中铁对磷的影响,为验证磷铁经典耦合机制提供了依据.

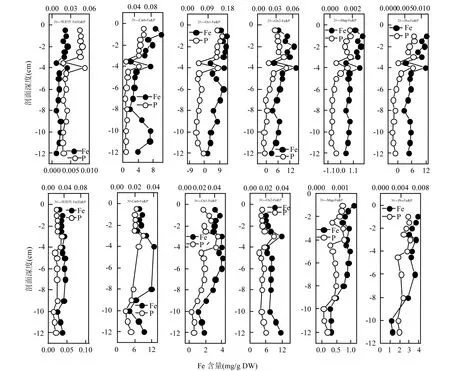
图4 太湖研究点位沉积物Fe分级形态提取磷铁含量垂直剖面Fig.4 Vertical profiles of Fe and P of sequential extraction for iron in the sediments from the investigated locations of Taihu
2.4 沉积物中磷与铁形态的相关性
2.4.1 w(TFe)/w(TP)评价太湖不同湖区沉积物中磷的释放风险 Jensen等[31]表明,w(∑Fe)/ w(∑P)是判断沉积物中磷释放潜力的指标,若沉积物中w(∑Fe)/w(∑P)大于15或20,则铁控制磷释放,磷释放受到其抑制.太湖藻型、过渡型、草型湖区沉积物中w(∑Fe)/w(∑P)分别为33.27、43.23、55.08,说明太湖3种典型湖区沉积物中磷的释放主要受铁控制,但此外也会受到周边环境、工农业生产水平等因素影响.
2.4.2 沉积物中不同形态铁和磷之间的相关性分析 在对太湖不同湖区沉积物进行铁的不同形态分级分析时,同时分析了不同浸提液提取的磷铁含量及其相关性,从表3可以看出,太湖不同湖区沉积物磷铁关系密切,铁对磷的影响较大.除草型湖区对污染物缓冲作用强而导致Feox2大幅增加,因而与其他提取态磷铁含量呈负相关外,其余不同湖区不同形态铁之间相关性比较显著,不同提取态磷含量也多呈正相关,并且磷铁含量的相关系数都较高,第1步至第6步提取的分别是可吸附性Fe(Ⅱ),Fecarb,Feox1,Feox2,Femag,Feprs及同步提取的MgCl2-P,NaAc-P,NH2OH·HCl-P, Na2S2O4-P, (NH4)2C2O4-P,浓HCl-P磷含量随沉积物剖面深度的变化都属于显著相关和极显著相关(P>0.05,不显著相关;P<0.05,显著相关;P<0.01极显著相关),其中1#剖面Fecarb及NaAc-P相关系数达到0.897(P<0.001),2#湖心区连二亚硫酸钠和浓HCl提取的Feox2、Feprs及磷含量相关系数达到0.898和0.913(P<0.001),3#剖面Feox1和盐酸羟氨-P相关系数为0.830(P<0.001).

表3 研究点位表层沉积物Fe分级形态提取磷铁相关性Table 3 The relationships between different Fe and P fractions in the surface sediments from the investigated locations
太湖3个湖区沉积物中可吸附性Fe(Ⅱ)与MgCl2-P之间呈显著正相关关系,相关系数分别为0.741(P<0.01)、0.919(P<0.01)和0.562(P<0.05),说明沉积物中部分由MgCl2所提取出的部分Pex的释放受可吸附性Fe(II)的限制.Pex是非常活泼的形态,当水动力条件和理化因子发生改变时释放出PO43-进入水体,而以被吸附形式存在的可吸附性Fe(II)也会解吸进入水体,与其他离子进行反应.沉积物磷循环与铁循环密切相关,Fe2+会与PO43-产生FePO4沉淀或吸附在FeO(OH)表面, 使Pex含量降低,但是在太湖这种碱性环境中,OH-与PO43-竞争表面吸附点位,导致部分Pex释放,所以沉积物中可吸附性Fe(II)与MgCl2-P之间存在显著正相关关系.
太湖不同湖区沉积物中Feprs与浓HCl-P呈显著正相关关系,相关系数为0.717(P<0.01), 0.913(P<0.01),0.713(P<0.05).这部分提取的Feprs是除Femag和Fecarb以外的表硅酸盐矿物,属于低活性硅酸铁,浓HCl灼烧能提取出部分有机磷Porg,Porg在矿化过程中能够形成有机体胶膜,覆盖在粘粒矿物、氧化铁(或氢氧化铁)以及碳酸钙等矿物表面,从而影响铁元素的释放,因此二者呈显著正相关关系.
不同湖区沉积物中Fecarb及NaAc-P,Feox1与NH2OH·HCl-P,Feox2与Na2S2O4-P均呈现显著相关(P<0.01),高活性铁(III)氧化物Feox1、Feox2和碳酸盐铁(Ⅱ)是占铁分级总铁Fe分级中比例最大的三种形态铁,碳酸盐结合态铁对环境变化比较敏感,特别是当水体的酸碱条件发生改变时, 随着碳酸盐的分解,铁会以活性铁形式从沉积物中释放出来, 进而与磷酸根阴离子发生络合或吸附反应,而同步提取出的磷形态也是除MgCl2-P外3种含量最高的提取态磷,同时也是对水体磷负荷影响最大最容易释放的就是活性磷Bio-P及Fe-P,说明太湖底泥中高活性铁(III)是控制磷释放的关键因子,高活性形态的铁导致活性磷的释放,水体内源磷负荷加重,太湖具有较高的释放风险和生物可用性.
3 结论
3.1 太湖沉积物样品中TFe分级含量藻型湖区30.29mg/g>过渡型湖区29.06mg/g>草型湖区24.29mg/g,各形态铁以高活性铁(III)氧化物Feox1、Feox2和碳酸盐铁(II)Fecarb所占比例最大,可还原(晶型)铁氧化物Feox2是沉积物中铁的主要存在形式;有机质含量与3个湖区沉积物剖面中Fecarb形态含量呈一定的负相关性,这证明了太湖湖区表层沉积物有机质含量对沉积物中碳酸盐铁的影响.
3.2 太湖不同湖区沉积物中各结合态磷以NH2OH·HCl-P所占比例最大,氯化镁可能提取了其他交换态吸附性金属离子结合的磷而提高了MgCl2-P所占比例,其余提取态磷所占比例同提取态铁一致.通过铁分级方法提取的磷形态主要是活性磷中的部分Pex和PFe,其次为部分无机磷(PCa和Pobs)和有机磷Porg,最易释放的活性磷Bio-P导致了水体内源磷负荷加重.
3.3 通过判断沉积物中磷释放潜力的指标w(∑Fe)/w(∑P)得出太湖3种典型湖区沉积物中磷的释放主要受铁控制;3种不同湖区Fe形态分级得到的磷铁呈现显著正相关性(P<0.05),占Fe分级中比例最大的高活性铁(III),控制着对水体磷负荷影响最大最容易释放的活性磷Bio-P及Fe-P,说明太湖沉积物中铁是控制磷释放的关键因子,高含量高活性的磷铁证明太湖具有较高的释放风险和生物可用性.
参考文献:
[1] 高 丽,杨 浩,周健民.湖泊沉积物中磷释放的研究进展 [J].土壤, 2004,36(1):12-15.
[2] Downing J A, Cauley Mc E. The nitrogen: phosphorous relationship in lakes [J]. Limnology and Oceanography, 1992, 37(5):36-945.
[3] Jin L V, Wu H J, Chen M Q. Effects of nitrogen and phosphorus on phytoplankton composition and biomass in 15subtropical, urban shallow lakes in Wuhan, China [J]. Limnologica Ecology and Management of Inland Waters, 2011,41(1):48-56.
[4] Christophoros C, Fytianos K. Conditions affecting the release of phosphorus from surface lake sediments [J]. Journal of Environmental Quality, 2006,35(5):1181–1192.
[5] Bostrom B, Andersen J M, Fleischer S, et al. Exchange of phosphorus across the sediment-water interface [J]. Hydrobiologia, 1988,170(3):229-244.
[6] EINSELE W. Uber dieBeziehungen des EisenkreislaufszumPhosphatkreislaufim Eutrophen See [J]. Arch. Hydrobiol., 1936, 29:664-686.
[7] Mortimer C. The exchange of dissolved substances between mud and water in lakes [J]. J. Ecol., 1941,29:280-329.
[8] Rozan T F, Taillefert M, Trouwborst R E, et al. Iron-sulfurphosphorus cycling in the sediments of a shallow coastal bay: Implications for sediment nutrient release and benthic macroalgal blooms [J]. Limnology and Oceanography, 2002,47(5):1346-1354.
[9] Jensen H S, Kristensen P, Jeppesen E, et al. Iron: phosphorus ratio in surface sediment as an indicator of phosphate release from aerobic sediments in shallow lakes [J]. Hydrobiologia, 1992, 235(1):731-743.
[10] Lovely D R. Dissimilatory Fe (Ⅲ) and M n (Ⅳ) reduction [J]. Microbiol. Rev., 1991,55:259-287.
[11] 熊 毅,陈家坊,马毅杰,等.土壤胶体(第二册) [M]. 北京:科学出版社, 1985:245-268.
[12] 邹元春,吕宪国,等.三江平原多级沟渠系统沉积物中铁的分布特征 [J]. 环境科学, 2009,30(3):889-893.
[13] 杨宏伟,吴雅丽,等.黄河干流表层沉积物铁形态的分布特征及相关性分析 [J]. 中国环境科学, 2015,35(12):3663-3669.
[14] 王 超,邹丽敏,王沛芳,等.典型城市浅水湖泊沉积物中磷与铁的形态分布及相关关系 [J]. 环境科学, 2008,29(12):3400-3404.
[15] 朱广伟.太湖水质的时空分异特征及其与水华的关系 [J]. 长江流域资源与环境, 2009,18(5):439-445.
[16] S. W. Poulton, D. E. Canfield . Development of a sequential extraction procedure for iron:implications for iron partitioning in continentally derived particulates [J]. Chemical Geologym, 2005, 214:209–221.
[17] 王振华.湖泊沉积物铁铝对磷赋存形态及其转化的影响 [D].哈尔滨:东北农业大学, 2012.
[18] 杨宏伟,郭博书,李经纬.内蒙古沙漠与沙尘粒子中磷形态分布特征及其环境意义 [J]. 环境化学, 2012,31(7):990- 997.
[19] 鲁如坤.土壤农业化学分析方法 [M]. 南京:河海大学出版社, 2000.
[20] 鲍士旦.土壤农化分析 [M]. 北京:中国农业出版社, 2005.
[21] 袁和忠,沈 吉,等.太湖水体及表层沉积物磷空间分布特征及差异性分析 [J]. 环境科学, 2010,31(4):954-959.
[22] Enfeng Liu. Gavin F. Comprehensive evaluation of heavy metal contamination in surface and core sediments of Taihu Lake, the third largest freshwater lake in China [J]. Environ. Earth. Sci., 2012,67:39–51.
[23] Aller R C, Heilburun C, Panzeca C, et al. Coupling between sedimentary dynamics,early diagenetic processes, and biogeochemical cycling in the Amazon-Guianas mobile mudbelt: coastal French Guiana [J]. Marine Geology, 2004,208:331-360.
[24] Raiswell R, Canfield D E, Sources of iron for pyrite formation in marine sediments [J]. American Journal of Science, 1998,298: 219-245.
[25] Poulton S W, Raiswell R. The low-temperature geochemical cycle of iron:from continental fluxes to marine sediment deposition [J]. American Journal Science, 2002,302:774-805.
[26] Thamdrup B. Bacterial manganese and iron reduction in aquatic sediments [J]. Advances in Microbiology and Ecology, 2000,16: 41–84.
[27] Lovley D R, Holmes D E, Nevin K P. Dissimilatory Fe(III) and Mn(IV) reduction [J]. Advances in Microbial Physiology, 2004,49: 219-286.
[28] Canfield D E. Reactive iron in marine sediments. Geochimicaet Cosmochimica Acta, 1989, 53:619-632.Thamdrup B. Bacterial manganese and iron reduction in aquatic sediments [J]. Advances in Microbiology and Ecology, 2000,16:41–84.
[29] 马旭阳.黄河水体沉积物中铁与磷的形态分布及相关分析 [D].呼和浩特:内蒙古师范大学, 2015.
[30] 张 路,范成新,等.太湖及其主要入湖河流沉积磷形态分布研究 [J]. 地球化学, 2014,33(4):423-432.
[31] Jensen H S, Kristensen P, Jeppesen E, et al. Iron: Phosphorus ratio in surface sediment as an indicator of phosphate release from aerobic sediments in shallow lakes [J]. Hydrobiologia, 1992,235/ 236:731–743.
Distribution of iron forms and their correlations analysis with phosphorus forms in the sedimentary profiles of Taihu Lake.
YANG Wen-bin1*, TANG Hao1,2, HAN Chao2, DING Shi-ming2(1.College of Environmental Science and Engineering, Anhui Normal University, Wuhu 241003, China;2.State Key Laboratory of Lake Science and Environment, Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences, Nanjing 210008, China). China Environmental Science, 2016,36(4):1145~1156
Abstract:Occureneces and distributions of iron forms in the sediment cores from three typically zones of Lake Taihu, i.e. phytoplankton dominated zone, macrophyte dominated zone, and phytoplankton-macrophyte transition zone, were investigated using the sequential extraction procedure. Generally, the total iron contents decreased in the order: phytoplankton dominated zone (31.57±8.51mg/g)> phytoplankton- macrophyte transition zone (30.34± 11.97mg/g)> macrophyte dominated zone (25.25±4.59mg/g), while the contents of different iron forms in the interest sites followed the variations: reducible oxides Feox2>carbonate associated Fe Fecarb>easilyreducible oxidesFeox1>poorly reactive sheet silicate FeFeprs>magnetite Femag>Absorbed Fe(Ⅱ), Fecarb、Feox1、Feox2weremeasured to be7.79mg/g, 6.16mg/g, 8.18mg/g, accounting for 28.56%, 21.54%, 29.53% of total iron respectively, suggesting those highly reactive iron Fe(III) were the dominated iron forms. The concents of different extracted phosphorus in sediment decreased in the order: NH2OH·HCl-P>MgCl2-P>NaAc-P>Na2S2O4-P>Concentrated HCl-P>(NH4)2C2O4-P. Three dominated phosphorus fractions including MgCl2-P、NaAc-P、NH2OH⋅HCl-Pwere measured to be 0.067mg/g, 0.061mg/g, 0.068mg/g, accounting for 35.28%、31.97% and 22.55% of the total extracted phosphorus.Significantly positive relationships were observed between the extracted phosphorus and iron fractions using the sequential extraction (P<0.05), further confirming the concomitant release of phosphorus from reduction dissolution ofFe (oxyhydr) oxides in sediments.
Key words:sequential extraction for iron;phytoplankton dominated zone;macrophyte dominated zone;phytoplanktonmacrophyte transition zone;correlativity;Taihu Lake
作者简介:杨文斌(1968-),男,安徽长丰人,教授,博士,主要从事水环境生态修复研究.发表论文20余篇.
基金项目:安徽省自然科学基金项目(1208085MD60);国家自然科学基金项目(31070338)
收稿日期:2015-09-10
中图分类号:X171
文献标识码:A
文章编号:1000-6923(2016)04-1145-12
