银黄清肺胶囊含药血清体外抗呼吸道合胞病毒实验研究
2016-03-21卢芳国屈金艳范伏元那婧婧李湘兰湖南中医药大学湖南长沙4008湖南安邦制药有限公司湖南长沙40008湖南中医药大学第一附属医院湖南长沙40007
彭 志,卢芳国,屈金艳,李 玲,范伏元*,那婧婧,李湘兰(.湖南中医药大学,湖南长沙4008;.湖南安邦制药有限公司,湖南长沙40008;.湖南中医药大学第一附属医院,湖南长沙40007)
银黄清肺胶囊含药血清体外抗呼吸道合胞病毒实验研究
彭志1,卢芳国2,屈金艳3,李玲2,范伏元3*,那婧婧1,李湘兰1
(1.湖南中医药大学,湖南长沙410208;2.湖南安邦制药有限公司,湖南长沙410008;3.湖南中医药大学第一附属医院,湖南长沙410007)
〔摘要〕目的研究银黄清肺胶囊含药血清体外抑制呼吸道合胞病毒(RSV)的作用。方法采用观察CPE及MTT法,观察在银黄清肺胶囊含药血清干预下,感染RSV Hep-2细胞的CPE及光密度值,从而比较不同给药方式(预防给药、治疗给药、直接杀灭)及不同药物剂量下银黄清肺胶囊对RSV的抑制作用。结果在三种给药方式中,与相应浓度空白血清比较,各浓度银黄清肺胶囊与利巴韦林片含药血清OD值均明显增高(P<0.05);其中稀释度为3.13%的利巴韦林片含药血清和稀释度为6.25%的银黄清肺胶囊含药血清相比本组其他浓度含药血清OD值均明显增高(P<0.05)。结论银黄清肺胶囊含药血清对RSV有直接灭活作用,对RSV侵入Hep-2细胞有阻断作用,对RSV在Hep-2细胞内增殖有抑制作用。其中稀释度为3.13%的利巴韦林含药血清和稀释度为6.25%的银黄清肺胶囊含药血清相比本组其他浓度含药血清体外抗RSV活性强。
〔关键词〕呼吸道合胞病毒;银黄清肺胶囊;含药血清;抗病毒;葶苈子;炙麻黄;苦杏仁
Experimental Research of Yinhuang Qingfei Capsules Containing Serum on the Respiratory Syncytial Virus in Vitro
PENG Zhi1,LU Fangguo2,QU Jinyan3,LI Ling2,FAN Fuyuan3*,NA Jingjing1,LI Xianglan1
(1. Hunan University of Chinese Medicine, Changsha, Hunan 410208, China; 2. Hunan Anbang Pharmaceutical Co. Ltd., Changsha, Hunan 410208, China; 3. The First Affiliated Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410208, China)
〔Abstract〕Objective To study Yinhuang Qingfei capsules containing serum on the respiratory syncytial virus in vitro. Methods The cytopathic effect(CPE)and optical density(OD)of respiratory syncytial virus(RSV)infection Hep-2 cells, which were intervened by Yinhuang Qingfei capsules, were by CPE and MTT methods. The inhibition effects of Yinhuang Qingfei capsules on RSV with different doses and different administration methods(drug prevention, treatment, directly kill)were observed. Results Compared with the corresponding concentration of blank serum, the serum OD values in Yinhuang Qingfei capsule and ribavirin tablets containing serum groups were significantly increased(P<0.05); Compared with other oncertrations of the same groups, the OD valiues of ribavirin with 3.125%dilution and Yinhuang Qingfei with 6.125%dilution were increased obviuosly(P<0.05). Conclusion Yinhuang Qingfei capsule showed directly inactivation effect on RSV, blocking effect on RSV invade Hep-2 cells, proliferation inhibition on RSV in Hep-2 cell, and the ribavirin with 3.125%dilution and Yinhuang Qingfei with 6. 25%dilution showed strongest anti-RSV effect in vitro.
〔Keywords〕respiratory syncytial virus, Yinhuang Qingfei capsule; drug serum; antiviral; pepperweed seed; prepared ephedra; bitter almond kernel
呼吸道合胞病毒(respiratory syncytial virus, RSV)主要引起婴幼儿下呼吸道感染,即喘息性毛细支气管肺炎,较大儿童和成人主要引起上呼吸道感染。有文献报道,90%以上的毛细支气管炎和多数病毒性肺炎由RSV引起[1]。RSV的传染性很强,且感染后不能获得持久免疫力,因此,重复感染十分常见[2]。由于RSV致病机制复杂,尚无安全有效的RSV疫苗问世,现RSV感染缺乏有效的预防和治疗措施,美国FDA迄今共批准过两个用于治疗RSV感染的药物,即利巴韦林及RSV特异性免疫球蛋白,但由于利巴韦林毒副作用的争议及RSV特异性免疫球蛋白昂贵的价格使其在临床上的推广应用受到限制,目前RSV感染仍以支持疗法为主。近年来对中药及中药复方的研究显示,中药治疗体内外病毒感染性疾病疗效确切,毒副作用小,作用靶点多,耐药发生率低,有独特不可替代的优势[3-5]。银黄清肺胶囊是由葶苈子、炙麻黄、苦杏仁、浙贝母等药物组成的中药复方,具有清肺化痰,止咳平喘功效,临床用于治疗喘息性毛细支气管炎急性发作疗效显著,为探讨其作用机制,本文将其体外抗RSV实验结果报道如下。
1 材料与方法
1.1材料
1.1.1药物银黄清肺胶囊由湖南安邦制药有限公司生产,批号:121202,规格:0.15 g/粒。因成人口服用药剂量为1.35 g/d,按成人体质量60 kg,实验大鼠体质量240 g换算,参照常用实验大鼠与人的体表面积比值(R)表计算,每只大鼠每日给药剂量为0.15 g(即大鼠给药量为0.66 g/kg)。利巴韦林片由江西江仁药业有限公司生产,批号:0601001,规格:0.1 g/片。成人口服用药剂量为0.45 g/d,参照常用实验大鼠与人的体表面积比值(R)表计算,每只大鼠每日给药剂量为0.05 g(即大鼠给药量为0.22 g/ kg)。用蒸馏水充分溶散,制成混悬液待用。
1.1.2病毒及细胞RSV购自湘雅中心实验室,Hep-2细胞购自中国典型培养物保藏中心。
1.1.3实验动物SPF级大鼠,雌雄各半,(220± 20)g,购自湖南斯莱克实验动物有限公司,许可证号:SYXK(湘)2013-0005,饲养于湖南中医药大学动物实验室,室内清洁,自然采光,通风良好。
1.1.4试剂及设备DMEM干粉、胎牛血清均购自Gibco公司;青霉素、链霉素均购自碧云天公司;L-谷胺酰胺购自Amresco公司;MTT(细胞增殖及细胞毒性检测试剂盒)、胰酶消化液均购自碧云天公司;二甲基亚砜、台盼蓝Trypan Blue均购自Sigma公司;DG5033A酶标仪(南京华东电子集团医疗设备有限责任公司);XDS-100倒置荧光电子显微镜(上海光学仪器厂)。
1.2方法
1.2.1含药血清的制备[6]24只大鼠适应性喂养3 d后,根据随机数字表法随机分为银黄清肺胶囊组,利巴韦林组,空白组3组,每组8只。银黄清肺胶囊组、利巴韦林组分别以0.66、0.22 g/kg的剂量灌胃,空白组每天灌胃等体积蒸馏水。每天2次,连续7 d,在第8天末次给药1 h后,予10%水合氯醛麻醉,3 min后经腹主动脉采血,静置30 min后,1 000 r/min,离心10 min,取上清液,经0.22 μm滤膜滤过,56℃水浴灭活补体30 min,于超净工作台分装,置于-20℃冰箱冻存。
1.2.2RSV感染性的测定实验用组织培养感染量(100TCID50)测定药物对病毒的作用。用细胞维持液将病毒做连续10倍稀释,稀释病毒液成10-1、10-2、10-3、10-4、10-5、10-6、10-7、10-8、10-9、10-10共10个稀释度。将生长良好的Hep-2细胞调整浓度至1×105个/mL,每孔100 μL,接种于细胞培养96孔板内,待细胞长成单层后,弃去细胞培养液,接种递次稀释的病毒液,每个浓度接种3复孔,每孔100 μL,同时设置正常细胞对照组(只加维持液),每孔100 μL,再置37℃、5%CO2培养箱中孵育2 h,弃去含病毒的维持液,病毒感染孔及正常对照孔均加入正常细胞维持液,每孔100 μL,置37℃、5%CO2培养箱中培养。镜下观察细胞形态,连续5 d。记录各孔细胞病变(CPE)程度。判定CPE指标[7]:“0”表示无明显CPE,“l”表示CPE为l%~25%,“2”表示CPE为26%~50%,“3”表示CPE为5l%~75%,“4”表示CPE为76%~100%。用Reed-Muench法计算TCID[8]。
1.2.3含药血清对Hep-2细胞毒性测定用细胞维持液将含药血清及空白组血清均以2倍浓度梯度稀释成5个浓度(50%,25%,12.5%,6.25%,3.13%),待细胞长满细胞培养瓶时,将细胞消化、稀释,使细胞密度调整为1×l05个/mL,依次接种于细胞培养96孔板中,每孔100 μL,置于37℃、5%CO2培养箱内培养,待细胞长成单层后,弃去细胞培养液,加入各浓度含药血清稀释液,每孔100 μL,每浓度3个复孔,将培养板置于37℃、5%CO2培养箱内培养48 h后,MTT法于酶标仪550 nm波长处读取吸收度OD值,计算最大无毒浓度。
1.2.4含药血清体外抗RSV毒性测定将各组血清(银黄组、利巴韦林组、空白组)在最大无毒范围内以无血清DMEM进行2倍浓度梯度稀释,最终各5个浓度(12.5%,6.25%,3.13%,1.56%,0.78%)。病毒攻击量为100TCID50。选用96孔细胞培养板,待细胞长成单层后,分3种加药方式:Ⅰ组(预防给药组)先将各稀释浓度的含药血清加至已长满细胞的96孔板,每孔100 μL,每浓度3个复孔,培养24 h后,弃去上清,加入病毒100 μL/孔,37℃、5%CO2培养箱内吸附2 h后,吸去病毒液,用PBS液洗涤2次,加入2%胎牛血清维持液100 μL/孔,37℃、5%CO2培养箱内培养48 h后,记录细胞病变结果。同时设正常对照及病毒对照组,用活细胞染色计数法(MTT)于酶标仪在550 nm波长处读取吸光度OD值,参照文献[9]进行;Ⅱ组(治疗给药组)先将稀释病毒液加入已长满细胞的96孔板,每孔100 μL,每浓度3个复孔,37℃、5%CO2培养箱内吸附2 h后,吸去病毒液,用PBS液洗涤2次,再加入各稀释浓度的含药血清培养48 h,用MTT法于酶标仪在550 nm波长处读取吸光度OD值;Ⅲ组(直接杀灭组)将各稀释浓度含药血清分别与稀释病毒液混匀后放入37℃、5%CO2培养箱内作用1 h后,加入已长满细胞的96孔板中,每孔100 μL,每浓度3个复孔,37℃、5%CO2培养箱内培养48 h,用MTT法于酶标仪在550 nm波长处读取吸光度OD值。
1.3统计学方法
2 结果
2.1RSV感染性的测定
结果测得RSV的TCID50为l0-8。
2.2含药血清对Hep-2细胞毒性测定结果
依Reed—Muench法计算出银黄清肺胶囊含药血清和空白组血清在检测的浓度范围内对Hep2细胞无毒。利巴韦林分散片含药血清在检测的浓度范围内对Hep2细胞的最大无毒浓度为含药血清原液的12.5%。结果见图1。
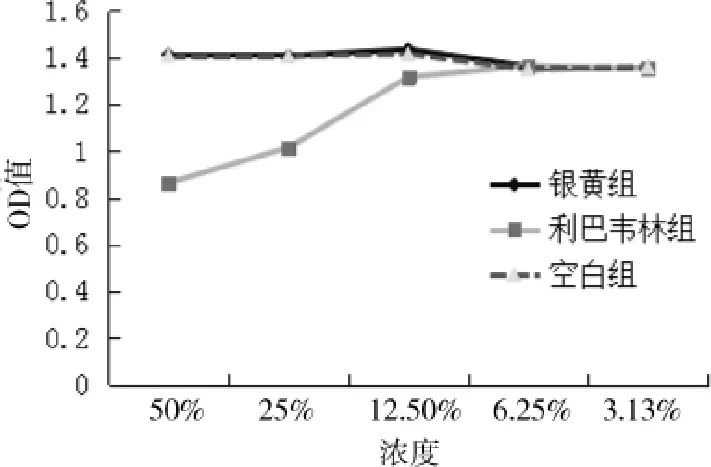
图1 含药血清对Hep-2细胞毒性测定结果折线图
2.3含药血清体外抗RSV毒性测定
2.3.1Ⅰ组与正常对照组比较,各浓度空白对照组Hep-2细胞的OD值明显降低(P<0.05);与相应浓度的空白对照组比较,各浓度银黄清肺胶囊含药组血清及利巴韦林含药血清Hep-2细胞的OD值明显升高(P<0.05);稀释度为3.13%的利巴韦林含药血清和稀释度为6.25%的银黄清肺胶囊含药血清相比本组其他浓度含药血清OD值明显升高(P<0.05)。空白组的血清不同浓度Hep-2细胞OD值差异无统计学意义(F=0.053,P>0.05);利巴韦林片含药血清不同浓度Hep-2细胞OD值差异有统计学意义(F=11.494,P<0.05),银黄清肺胶囊含药血清不同浓度Hep-2细胞OD值差异有统计学意义(F=17.456,P<0.01)。见表1。
表1 预防给药含药血清对RSV感染Hep-2细胞活性的影响 (±s,n=3)
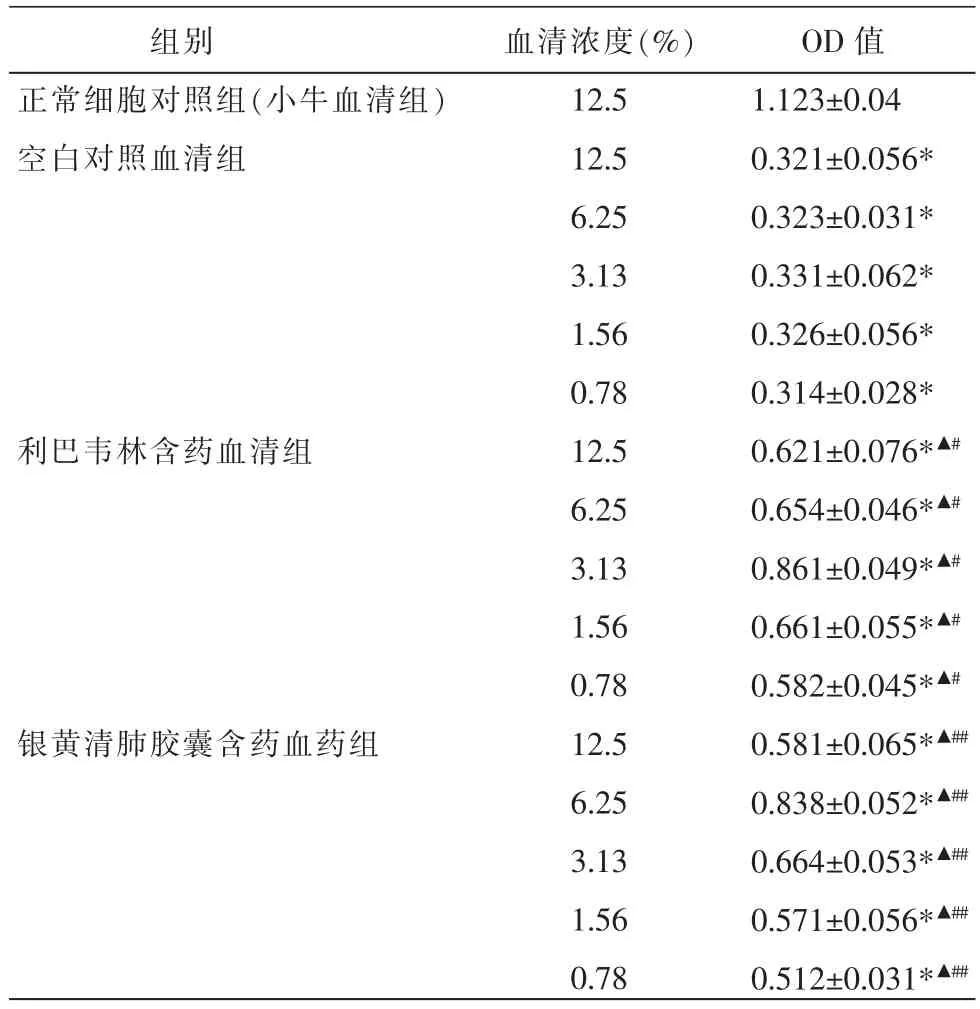
表1 预防给药含药血清对RSV感染Hep-2细胞活性的影响 (±s,n=3)
注:与正常对照组比较,*P<0.05;与空白对照组比较,▲P<0.05;组内不同浓度两两比较,#P<0.05,##P<0.01。
组别正常细胞对照组(小牛血清组)空白对照血清组利巴韦林含药血清组银黄清肺胶囊含药血药组血清浓度(%)12.5 12.5 6.25 3.13 1.56 0.78 12.5 6.25 3.13 1.56 0.78 12.5 6.25 3.13 1.56 0.78 OD值1.123±0.04 0.321±0.056* 0.323±0.031* 0.331±0.062* 0.326±0.056* 0.314±0.028* 0.621±0.076*▲#0.654±0.046*▲#0.861±0.049*▲#0.661±0.055*▲#0.582±0.045*▲#0.581±0.065*▲##0.838±0.052*▲##0.664±0.053*▲##0.571±0.056*▲##0.512±0.031*▲##
2.3.2Ⅱ组与正常对照组比较,各浓度空白对照组的Hep-2细胞的OD值明显降低(P<0.05);与相应浓度的空白对照组比较,各浓度银黄清肺胶囊含药组血清及利巴韦林含药血清Hep-2细胞的OD值明显升高(P<0.05);稀释度为3.13%的利巴韦林含药血清及稀释度为6.25%的银黄清肺胶囊含药血清相比本组其他浓度含药血清OD值明显升高(P<0.05)。空白组血清不同浓度Hep-2细胞OD值差异无统计学意义(F=0.256,P>0.05);利巴韦林片含药血清不同浓度Hep-2细胞OD值差异有统计学意义(F=23.913,P<0.05);银黄清肺胶囊含药血清不同浓度Hep-2细胞OD值存在显著差异(F=66.866,P<0.01)。见表2。
2.3.3Ⅲ组与正常对照组比较,各浓度空白对照组的Hep-2细胞的OD值明显降低(P<0.05);与相应浓度的空白对照组比较,各浓度银黄清肺胶囊含药组血清及利巴韦林片含药血清Hep-2细胞的OD值明显升高(P<0.05);稀释度为3.13%的利巴韦林含药血清及稀释度为6.25%的银黄清肺胶囊含药血清相比本组其他浓度含药血清OD值明显升高(P<0.05)。空白组的血清不同浓度Hep-2细胞OD值差异无统计学意义(F=0.115,P>0.05);利巴韦林片含药血清不同浓度Hep-2细胞OD值差异有统计学意义(F=22.266,P<0.05);银黄清肺胶囊含药血清不同浓度Hep-2细胞OD值差异有统计学意义(F=60.480,P<0.01)。见表3。
表2 治疗给药含药血清对RSV感染Hep-2细胞活性的影响 (±s,n=3)

表2 治疗给药含药血清对RSV感染Hep-2细胞活性的影响 (±s,n=3)
注:与正常对照组比较,*P<0.05;与空白对照组比较,▲P<0.05;组内不同浓度两两比较,#P<0.05,##P<0.01。
组别正常细胞对照组(小牛血清组)空白对照血清组利巴韦林含药血清组银黄清肺胶囊含药血药组血清浓度(%)12.5 12.5 6.25 3.13 1.56 0.78 12.5 6.25 3.13 1.56 0.78 12.5 6.25 3.13 1.56 0.78 OD值1.083±0.094 0.336±0.008* 0.358±0.083* 0.333±0.040* 0.328±0.036* 0.324±0.021* 0.593±0.029*▲#0.663±0.064*▲#0.915±0.033*▲#0.682±0.027*▲#0.589±0.066*▲#0.561±0.039*▲##0.932±0.019*▲##0.597±0.034*▲##0.521±0.026*▲##0.497±0.058*▲##
表3 直接抑制给药含药血清对RSV感染Hep-2细胞活性的影响 (±s,n=3)
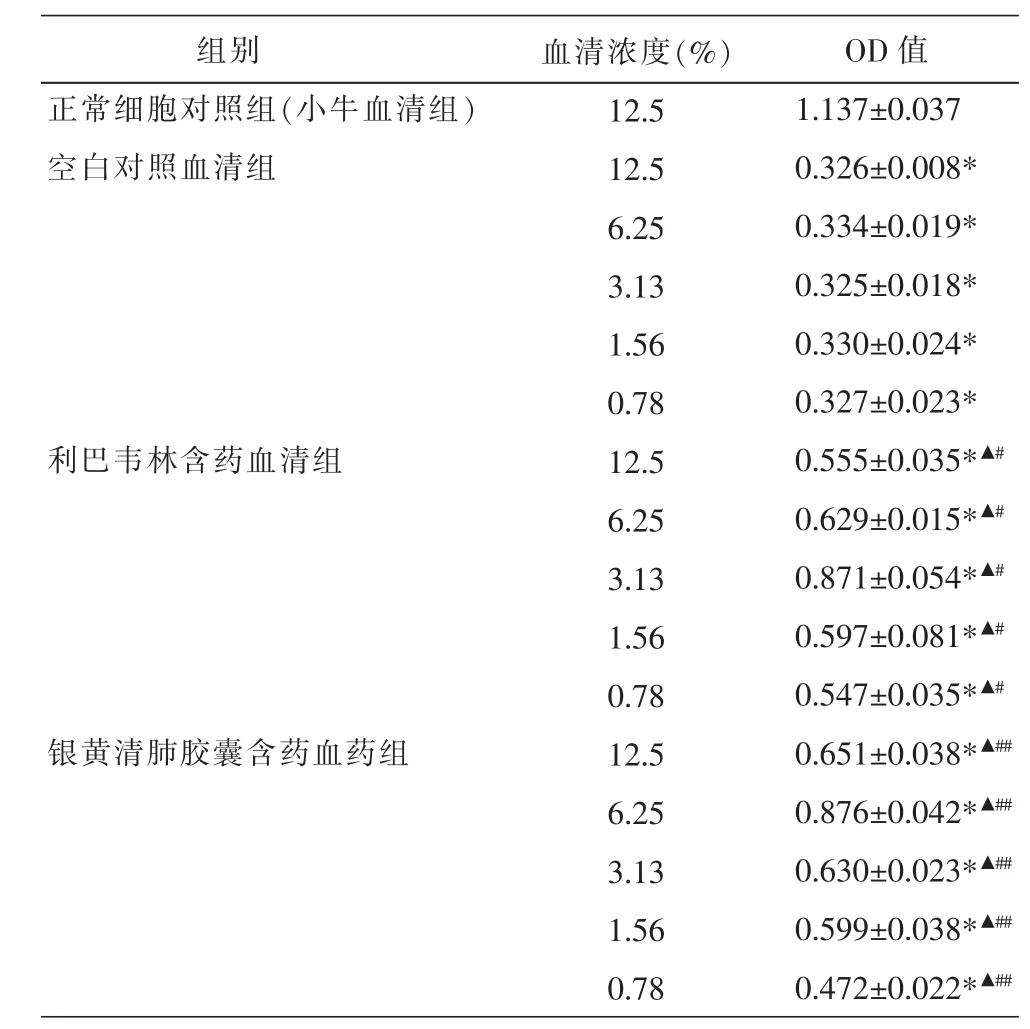
表3 直接抑制给药含药血清对RSV感染Hep-2细胞活性的影响 (±s,n=3)
注:与正常对照组比较,*P<0.05;与空白对照组比较,▲P<0.05;组内不同浓度两两比较,#P<0.05,##P<0.01。
组别正常细胞对照组(小牛血清组)空白对照血清组利巴韦林含药血清组银黄清肺胶囊含药血药组血清浓度(%)12.5 12.5 6.25 3.13 1.56 0.78 12.5 6.25 3.13 1.56 0.78 12.5 6.25 3.13 1.56 0.78 OD值1.137±0.037 0.326±0.008* 0.334±0.019* 0.325±0.018* 0.330±0.024* 0.327±0.023* 0.555±0.035*▲#0.629±0.015*▲#0.871±0.054*▲#0.597±0.081*▲#0.547±0.035*▲#0.651±0.038*▲##0.876±0.042*▲##0.630±0.023*▲##0.599±0.038*▲##0.472±0.022*▲##
3 讨论
既往研究发现,在一定细胞浓度范围内,光密度值与活细胞数成正比[10]。此次实验结果表明:银黄清肺胶囊含药血清对呼吸道合胞病毒有直接灭活作用,能阻断RSV侵入Hep-2细胞,同时能抑制呼RSV在Hep-2细胞内增殖。其中直接灭活呼吸道合胞病毒,可能是由于其具有直接杀伤病毒作用,或者药物成分与病毒表面某特征性部位相结合,使病毒难以进入细胞内复制。阻断RSV侵入可能是通过与细胞表面受体结合而实现,抑制RSV增殖则可能是由于抑制了病毒核酸的复制或阻断了病毒蛋白的合成。三种给药方式中,银黄清肺胶囊含药血清当稀释度为6.25%时OD值最高,体外抗RSV活性最强,可能与高浓度组含药血清浓度高,对细胞有一定毒性作用;低浓度组含药血清浓度低,抗病毒效力弱有关。既往研究发现防治病毒性肺炎的药物都是从以下两方面入手的:一是作用于病毒复制、转录、翻译等环节,直接影响病毒生活周期以抗病毒;二是修饰宿主细胞膜受体、调整机体状态,阻止病毒表达进入宿主细胞,或对病毒感染产生的次生变化进行调整[11]。但由于银黄清肺胶囊药物组成较多,作用靶点多,环节复杂,其详尽作用机制目前还不够明确,有待进一步研究。
参考文献:
[1] Moler FW, Steinhart CM, Ohmit SE, et al. Effectiveness of ribavirin in otherwise well infants with respiratory syncytial virus-associated respiratory failure[J]. Pediatr,1996,128(3):422-8.
[2] Pocket RD, Cambell D, Carroll S, et al. virus, respiratory syncytial virus and non-rotaviral gastroenteritis analysis of hospital readmissions in England and Wales[J]. Acta Paediatrica,2013,102 (4):e158-e163.
[3]吕伟伟,朱童娜,邱欢,等.疏风解毒胶囊抗病毒及抗菌的体外药效学实验研究[J].中药新药与临床药理,2013,5(24):234-238.
[4]张颖,刘兰林,郑李锐,等.近10年中医药治疗流感病毒性肺炎实验研究进展[J].江西中医药,2013,44(8):78-80.
[5]艾碧琛,贺又舜.甘露消毒丹抗病毒作用的临床与实验研究现状[J].中华中医药学刊,2013,31(8):1 665-1 667.
[6]李仪奎,吴健宇.血清药理学中采血时间的通法方案[J].中国药理学通报,1999,5(6):569.
[7]阎祖炜,朱欣,李闻文,等.MTT法、CPE观察法用于药物细胞毒性实验的比较与分析[J].实用预防医学,2010,14(5):1 552.
[8]黄祯祥,洪涛,刘崇柏,等.医学病毒学基础及实验技术[M].北京:科学出版社,1990.130-141.
[9]王毅军,奚肇庆,冯旰珠,等.痰热清对呼吸道合胞病毒体外抑制作用研究[J].河北医药,2010,32(24):3 447-3 448.
[10]汪志荣,高琼,马传鑫,等.MTT法测定大肠杆菌活菌数研究[J].环境科学学报,2001,31(12):2 642-2 650.
[11]梁建卫.清肺解毒法治疗小儿呼吸道合胞病毒肺炎的临床研究[D].南京:南京中医药大学,2007,4:62-63.
(本文编辑杨瑛)
〔通讯作者〕*范伏元,男,教授,硕士研究生导师,E-mail:ffy023@163.com。
〔作者简介〕彭志,女,在读硕士研究生,研究方向:中医呼吸内科。
〔基金项目〕国家自然基金课题(81473468,81072751);湖南省自然科学基金项目(13JJ6062);湖南省教育厅科学研究重点项目(13A066);湖南省高校科技创新团队“感染性疾病中医药防治研究”资助项目;湖南省战略性新兴产业科技攻关类项目(2014CK1022)。
〔收稿日期〕2015-06-02
〔中图分类号〕R285.5
〔文献标识码〕A
〔文章编号〕
doi:10.3969/j.issn.1674-070X.2016.02.011
