Fe3O4/羧甲基壳聚糖磁性载药微球的制备及释药性能
2016-01-05韩利华赵由春陈春江王家喜尚宏周
韩利华 ,赵由春,高 扬,陈春江,王家喜,尚宏周
(1.唐山三友硅业有限责任公司,河北 唐山 063305;2.河北工业大学化工学院,天津 300130;3.华北理工大学化工学院,河北 唐山 063009)
Fe3O4/羧甲基壳聚糖磁性载药微球的制备及释药性能
韩利华1,2,3,赵由春1,高扬3,陈春江1,王家喜2,尚宏周3
(1.唐山三友硅业有限责任公司,河北 唐山 063305;2.河北工业大学化工学院,天津 300130;3.华北理工大学化工学院,河北 唐山 063009)
摘要:通过乳化交联法制备了负载有抗癌药物5-氟尿嘧啶的Fe3O4/羧甲基壳聚糖磁性载药微球。利用红外光谱(IR)和扫描电镜(SEM)对载药微球的结构与形貌进行了表征,研究了影响载药微球载药和释药性能的因素。IR测试显示载药微球中含有磁性Fe3O4;SEM照片显示载药微球尺寸均一,表面光滑。确定制备磁性载药微球的最佳条件为:5-氟尿嘧啶0.5 g、磁性Fe3O40.2 g、戊二醛8 mL;磁性载药微球在温度为35~40 ℃、pH值为5.2的缓冲溶液中释药量达到峰值,适用于人体十二指肠肿瘤的治疗。
关键词:羧甲基壳聚糖;磁性Fe3O4;载药微球;5-氟尿嘧啶;释药性能
近年来,靶向给药作为一种新型药物输送方式引起了人们的广泛关注[1-3]。磁性靶向给药系统一般由药物和磁性复合微球组成,通过注射进入体内,可在外加磁场的作用下将药物输送到特定的病变部位释放,能大幅降低药物的使用剂量和毒副作用,提高治疗效率[4],在肿瘤治疗领域具备潜在的应用价值。但这一过程要求药物载体的磁性可随磁场的去除而消失,并可被安全地排出体外,因此药物载体必须无毒、无害且具有一定的生物相容性。壳聚糖具有良好的生物相容性和较强的药物缓释能力[5],改性成为羧甲基壳聚糖后其水溶性明显提高,有利于更好地进入肿瘤细胞中,减轻患者对药物的不耐受性,是理想的药物载体。
作者在此选用羧甲基壳聚糖和磁性Fe3O4为药物载体,以对肠道肿瘤、乳腺肿瘤、胰腺肿瘤等都具备较好疗效的5-氟尿嘧啶为负载药物,通过乳化交联法制备Fe3O4/羧甲基壳聚糖磁性载药微球,并对影响其载药和释药性能的因素进行研究,以确定最佳的载药、释药条件。
1实验
1.1 试剂与仪器
壳聚糖(脱乙酰度96.12%),浙江金壳化学有限公司;5-氟尿嘧啶(分析纯),江苏美达化学品有限公司;液体石蜡、Span-80(化学纯)、戊二醛(分析纯),天津光复精细化工研究所;FeCl3·6H2O、PEG-4000、氯乙酸、石油醚、冰醋酸、醋酸钠、氢氧化钠(分析纯),天津永大化学试剂有限公司;FeSO4·7H2O、乙醇、磷酸二氢钠、磷酸氢二钠、碳酸氢钠(分析纯),天津天力化学试剂有限公司;盐酸(分析纯),天津凯信化学工业有限公司。
Nicolet380型红外光谱仪,美国尼高力公司;S-4800型场发射扫描电子显微镜,日本日立公司;UV1901型紫外可见分光光度计,北京普析通用仪器公司;PHS-3C型酸度计,赛多利斯科学仪器有限公司;再生纤维素管式透析袋(截留量14 000),美国Viskase。
1.2 Fe3O4/羧甲基壳聚糖磁性载药微球的制备
以FeCl3·6H2O、FeSO4·7H2O、PEG-4000等为原料,依据文献[6]采用化学共沉淀法制备得到磁性Fe3O4。
以壳聚糖、氯乙酸等为原料,依据文献[7]制备得到羧甲基壳聚糖。
将1.2 g羧甲基壳聚糖、一定质量的磁性Fe3O4和一定质量的5-氟尿嘧啶溶于40 mL去离子水中,搅拌至完全溶解,静置至泡沫消失,即得水相溶液。在80 mL液体石蜡中加入2.4 mL Span-80,搅拌均匀,即得油相溶液。将水相缓慢加入到油相中,搅拌,乳化1.5 h后,滴加一定量的交联剂戊二醛,35 ℃继续搅拌2.5 h。将产物与乳液分离,用石油醚、乙醇、去离子水各冲洗3次,抽滤,40 ℃真空干燥,即得Fe3O4/羧甲基壳聚糖磁性载药微球。
微球的载药性能主要通过载药量和包封率来表征,载药量和包封率按式(1)、式(2)计算:
载药量=(m药物/m微球)×100%
(1)
包封率=(m包载药物/m加入药物)×100%
(2)
式中:m药物为微球中药物的质量,g;m微球为微球的质量,g;m包载药物为微球中药物包封的质量,g;m加入药物为加入的总药量,g。
通过改变5-氟尿嘧啶、磁性Fe3O4和戊二醛的用量制备Fe3O4/羧甲基壳聚糖磁性载药微球,并测定其载药量和包封率,优化Fe3O4/羧甲基壳聚糖磁性载药微球的制备条件。
1.3 Fe3O4/羧甲基壳聚糖磁性载药微球的药物释放
以冰醋酸、醋酸钠、磷酸二氢钠、磷酸氢二钠、碳酸氢钠和氢氧化钠为原料分别配制pH值为5.2、7.4和9.2的缓冲溶液。分别在10 mL pH值为5.2、7.4和9.2的缓冲溶液中加入0.1 g Fe3O4/羧甲基壳聚糖磁性载药微球,将装有缓冲溶液的透析袋放入100 mL烧杯中,并加入40 mL与透析袋内pH值相同的缓冲溶液,测定不同时间烧杯中液体的吸光度。
将0.1 g Fe3O4/羧甲基壳聚糖磁性载药微球加入到10 mL pH值为5.2的缓冲溶液中,将装有缓冲溶液的透析袋放入150 mL烧杯中,加入90 mL pH值为5.2的缓冲溶液。将烧杯分别放在不同温度的恒温水浴中72 h,取烧杯中液体测定吸光度。
1.4 5-氟尿嘧啶标准曲线的绘制
用紫外可见分光光度计测定不同条件下5-氟尿嘧啶在266 nm的吸光度,绘制5-氟尿嘧啶的标准曲线。
1.5 测试表征
将羧甲基壳聚糖粉末、磁性Fe3O4粉末及Fe3O4/羧甲基壳聚糖磁性载药微球粉末溴化钾压片后进行红外光谱测试。将Fe3O4/羧甲基壳聚糖磁性载药微球表面喷金处理,用扫描电镜观察其形貌。
2结果与讨论
2.1 红外光谱分析
图1为羧甲基壳聚糖、Fe3O4/羧甲基壳聚糖磁性载药微球和磁性Fe3O4的红外光谱。

图1 羧甲基壳聚糖(a)、Fe3O4/羧甲基壳聚糖磁性载药微球(b)和磁性Fe3O4(c)的红外光谱Fig.1 IR Spectra of carboxymethyl chitosan(a),Fe3O4/carboxymethyl chitosan magnetic drug carrying microspheres(b) and magnetic Fe3O4(c)
由图1a可知,3 437 cm-1为O-H和N-H的伸缩振动峰,1 628 cm-1为-NH2的弯曲振动峰,1 324 cm-1为-COOH中C-O的伸缩振动峰,1 072 cm-1为β-1,4糖苷键的伸缩振动峰。由图1c可知,577 cm-1处有明显的Fe-O特征峰[8]。由图1b可知,Fe3O4/羧甲基壳聚糖磁性载药微球中上述特征峰全部存在,但某些峰的位置和强度发生了不同程度的变化。-NH2的弯曲振动峰偏移到了1 610 cm-1,且峰形变宽,强度减弱,说明-NH2与戊二醛中的-CHO发生了交联反应;577 cm-1的Fe-O特征峰偏移到了554 cm-1处,说明磁性Fe3O4被成功负载于羧甲基壳聚糖微球中。
2.2 Fe3O4/羧甲基壳聚糖磁性载药微球的形貌分析(图2)

图2 Fe3O4/羧甲基壳聚糖磁性载药微球的SEM照片(×6000)Fig.2 SEM Image of Fe3O4/carboxymethyl chitosan magnetic drug carrying microspheres(×6000)
从图2可以看出,载药微球具有较好的球型结构,且尺寸较均一,粒径在3.0~4.5μm之间,微球表面比较光滑。这样的结构有利于药物的均匀负载和释放。
2.3 磁性羧甲基壳聚糖微球的载药性能
2.3.15-氟尿嘧啶用量对载药量和包封率的影响(图3)
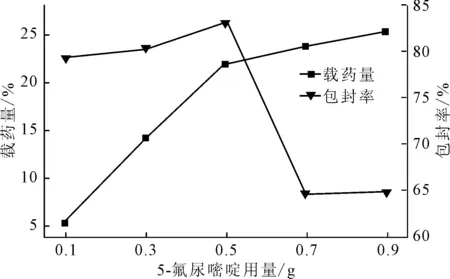
图3 5-氟尿嘧啶用量对载药量和包封率的影响Fig.3 Effect of 5-fluorouracil dosage on drug loading efficiency and encapsulation rate
从图3可以看出,载药量随5-氟尿嘧啶用量的增加而显著上升,但包封率却先升后降;当5-氟尿嘧啶用量为0.5 g时,包封率达到最大;当5-氟尿嘧啶用量从0.5 g增加到0.7 g时,包封率显著下降,继续增加用量,包封率无明显变化。综合考虑,确定最佳的5-氟尿嘧啶用量为0.5 g。
2.3.2磁性Fe3O4用量对载药量和包封率的影响(图4)
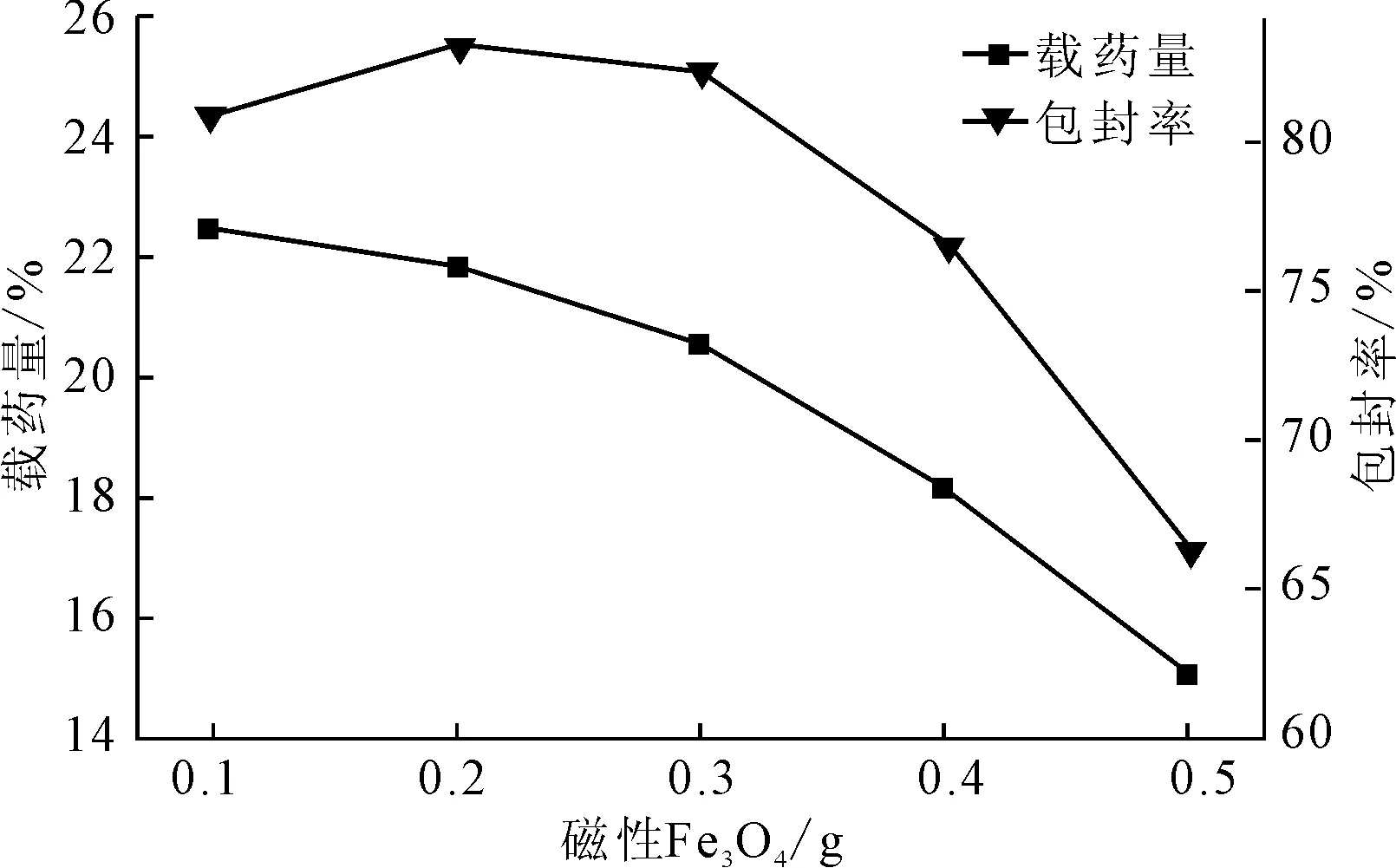
图4 磁性Fe3O4用量对载药量和包封率的影响Fig.4 Effect of magnetic Fe3O4 dosage on drug loading efficiency and encapsulation rate
从图4可以看出,随着磁性Fe3O4用量的增加,载药量持续下降,包封率则是先升后降;当磁性Fe3O4用量达到0.2 g时,包封率最高;继续增加用量,包封率下降明显。因此,确定最佳的磁性Fe3O4用量为0.2 g。
2.3.3交联剂用量对载药量和包封率的影响(图5)
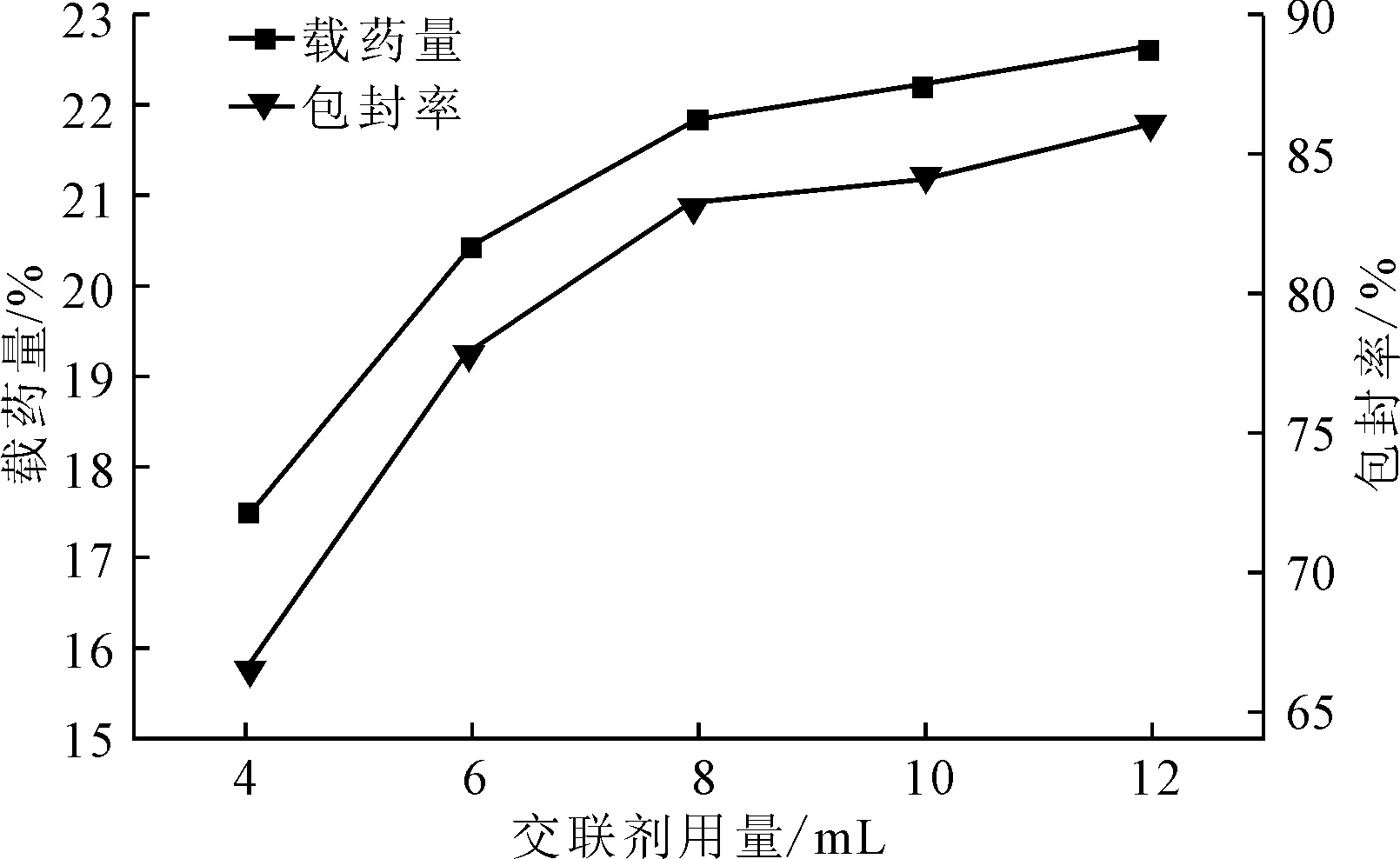
图5 交联剂用量对载药量和包封率的影响Fig.5 Effect of crosslinking agent dosage on drug loading efficiency and encapsulation rate
从图5可以看出,交联剂戊二醛的用量从4 mL增加到12 mL,载药量和包封率都呈上升趋势。说明交联剂加入的越多,交联程度越高,包裹的药物越多,包覆越紧密。但戊二醛的用量从8 mL增加到12 mL时,载药量和包封率的增速均放缓,说明戊二醛的用量在达到8 mL后,继续增加用量对载药量和包封率的提升效果不再明显。因此,戊二醛用量为8 mL即可。
2.4 Fe3O4/羧甲基壳聚糖磁性载药微球的释药性能
图6为Fe3O4/羧甲基壳聚糖磁性载药微球在不同pH值和不同温度下的释药百分率。
从图6a可以看出,pH值为5.2和7.4时,释药百分率在0~72 h内缓慢增加,72 h时达到最大值,72 h
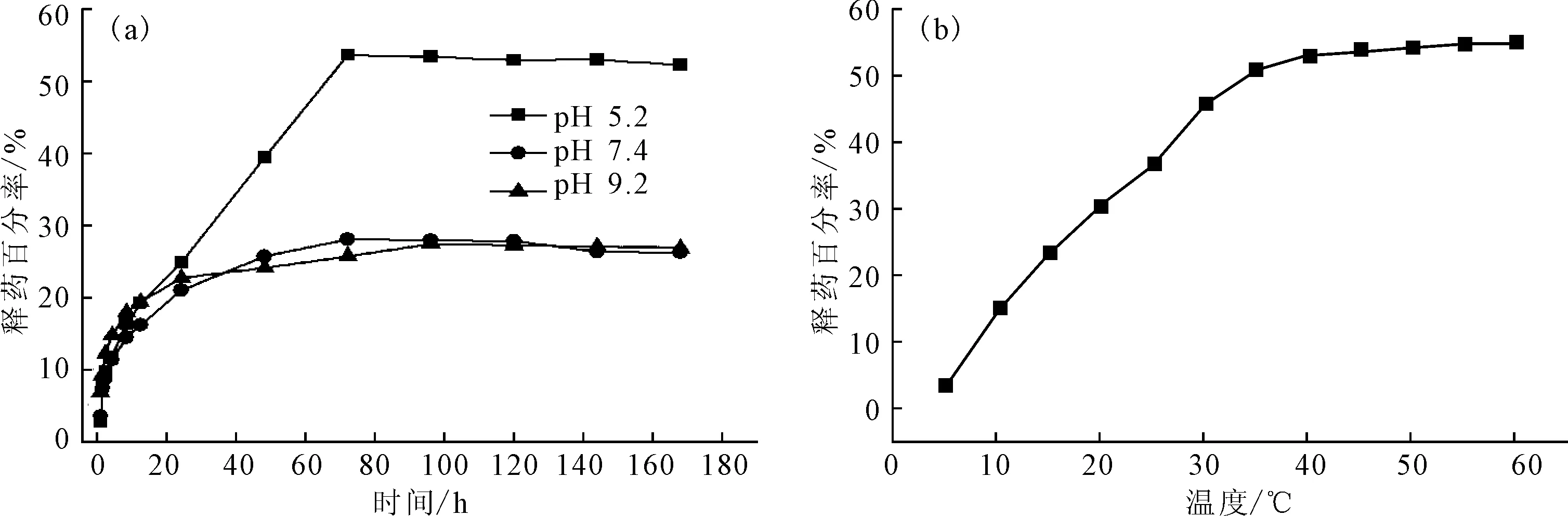
图6pH值(a)和温度(b)对磁性载药微球释药性能的影响
Fig.6Effect of pH value(a) and temperature(b) on drug release properties of magnetic drug carrying microspheres
后释药百分率无明显变化;pH值为9.2时,释药百分率在96 h达到最大值。磁性载药微球的最大释药百分率在pH值为5.2时最高,为53.80%,远高于pH值为7.4和9.2的释药百分率。人体十二指肠的pH值为5.8[9],因此,Fe3O4/羧甲基壳聚糖磁性载药微球适用于人体十二指肠肿瘤的治疗。从图6b可以看出,磁性载药微球的释药百分率在35~40 ℃达到最大值,符合人体的体温范围,说明磁性载药微球在人体体温下可达到最大的药物释放量,在人体抗癌靶向给药领域具有潜在的应用价值。
3结论
通过乳化交联法制备了Fe3O4/羧甲基壳聚糖磁性载药微球,并将抗癌药物5-氟尿嘧啶负载于微球上。结果表明,载药微球的载药性能受投药量、磁性Fe3O4用量及交联剂用量等多种因素影响,在5-氟尿嘧啶用量为0.5 g、磁性Fe3O4用量为0.2 g、戊二醛用量为8 mL时,载药微球的载药量和包封率最佳。磁性载药微球在温度为35~40 ℃、pH值为5.2的缓冲溶液中药物释放量最大。该载药微球在人体十二指肠肿瘤的治疗领域具有广阔的应用前景。
参考文献:
[1]KATRINE D M,CAMILLA S,STEFANIA B,et al.Development of anexvivoretention model simulating bioadhesion in the oral cavity using human saliva and physiologically relevant irrigation media[J].International Journal of Pharmaceutics,2013,448(2):373-381.
[2]MENNINI N,FURLANETTO S,CIRRI M,et al.Quality by design approach for developing chitosan-Ca-alginate microspheres for colon delivery of celecoxib-hydroxypropyl-β-cyclodextrin-PVP complex[J].European Journal of Pharmaceutics and Biopharmaceutics,2012,80(1):67-75.
[3]PATIL S P,BABBAR A,MATHUR R,et al.Mucoadhesive chitosan microspheres of carvedilol for nasal administration[J].Journal of Drug Targeting,2010,18(4):321-331.
[4]ZHANG H B,KAJIYOSHI K.Hydrothermal synthesis and size-dependent properties of multiferroic bismuth ferrite crystallites[J].Journal of the American Ceramic Society,2010,93(11):3842-3849.
[5]SIVKUMARM M,MANJUBALA I,RRO P K.Preparation,characterization andinvitrorelease of gentamicin from coralline hydroxyapatite-chitosan composite microspheres[J].Carbohydrate Polymer,2002,49(3):281-288.
[6]NAKAMURA M,KATAGIRI K,KOUMOTO K.Preparation of hybrid hollow capsules formed with Fe3O4and polyelectrolytesviathe layer-by-layer assembly and the aqueous solution process[J].Journal of Colloid and Interface Science,2010,341(1):64-68.
[7]TRONG M D,CHIA F K,WEN Y C.Synthesis and properties of chitosan-modified poly(vinyl acetate)[J].Journal of Applied Polymer Science,2002,86(12):3057-3063.
[8]符晓兰,卞学海,赵亚萍,等.纳米Fe3O4颗粒及其磁流体的制备与研究[J].东华大学学报,2011,37(3):341-345,361.
[9]EKARAT J,VIVCENZO D M,EMANUELA R,et al.Application of biorelevant dissolution tests to the prediction ofinvivoperformance of diclofenac sodium from an oral modified-release pellet dosage form[J].European Journal of Pharmaceutical Sciences,2009,37(3):434-441.
Preparation and Drug Release Properties of Fe3O4/Carboxymethyl Chitosan Magnetic Drug Carrying Microspheres
HAN Li-hua1,2,3,ZHAO You-chun1,GAO Yang3,CHEN Chun-jiang1,WANG Jia-xi2,SHANG Hong-zhou3
(1.TangshanSanyouSiliconIndustryCo.,Ltd.,Tangshan063305,China;2.SchoolofChemical
EngineeringandTechnology,HebeiUniversityofTechnology,Tianjin300130,China;3.CollegeofChemical
Engineering,NorthChinaUniversityofScienceandTechnology,Tangshan063009,China)
Abstract:Fe3O4/Carboxymethyl chitosan magnetic drug carrying microspheres were prepared by emulsion crosslinking method,in which 5-fluorouracil were loaded.Structure and morphlogy of the drug carrying microspheres were characterized by infrared spectroscopy(IR) and scanning electron microscopy(SEM).The factors affecting the drug loading and release properties of the drug carrying microspheres were investigated.IR Test showed that the drug carrying microspheres contained magnetic Fe3O4.SEM Image indicated that drug carrying microspheres were homogeneous in size and surface was smooth.The optimal preparation conditions of magnetic drug carrying microspheres were as follows:0.5 g 5-fluorouracil,0.2 g magnetic Fe3O4,8 mL glutaraldehyde.Releasing content of magnetic drug carrying microspheres reached a peak at 35~40 ℃,pH value 5.2 buffer solution,which was applicable to the treatment of human duodenum tumor.
Keywords:carboxymethyl chitosan;magnetic Fe3O4;drug carrying microspheres;5-fluorouracil;drug release property
中图分类号:O 646.8
文献标识码:A
文章编号:1672-5425(2015)05-0033-04
doi:10.3969/j.issn.1672-5425.2015.05.008
作者简介:韩利华(1972-),男,博士,教授,主要从事应用化学及环境技术的研究,E-mail:tshlh@heuu.edu.cn。
收稿日期:2015-01-26
基金项目:河北省自然科学基金资助项目(B2014209200)
