高效液相色谱法测定饲料中左旋咪唑
2015-12-16吴荔琴林海丹李小云邓国东伍宏凯蓝棋浩
吴荔琴, 林海丹*, 李小云, 邓国东, 伍宏凯, 蓝棋浩
(1.广东省兽药饲料质量检验所,广东广州 510230;2.广东省动物卫生监督总所,广东广州510230)
左旋咪唑(LMS)属咪唑并噻唑类抗蠕虫药,临床常用其盐酸盐或磷酸盐。左旋咪唑具有广谱、高效的特点,但该药具有潜在的基因毒性,用药后对消化系统、神经系统、心血管系统、血液及造血系统、泌尿系统和皮肤均有不同程度的毒副作用。左旋咪唑在国内外养殖业中应用极为广泛,当长期、超量用药或不执行休药期规定时,或盲目用药、重复用药、配伍不当时,均可产生残留,直接危害人体健康。本研究建立了检测配合饲料和浓缩饲料中左旋咪唑的高效液相色谱方法,该方法灵敏、高效、简便。
1 材料与方法
1.1 仪器与设备 高效液相色谱仪,Aglient1100型,配UV检测器,美国Aglient公司;分析天平,感量0.00001 g,CPA-225D型,德国赛多利斯公司;氮吹仪,GM-2100型,日本EYELA公司;超声波清洗器,SB-5200DTDN型,宁波新芝公司;振荡器,KS501型,马来西亚IKA公司;离心机,5804R型,德国Eppendof公司;有机滤膜,孔径为0.45 μm,天津市腾达过滤器件厂。
1.2 药品与试剂 左旋咪唑标准品,德国Dr.Ehrenstorfer GmbH公司,纯度≥98.5%;乙腈、甲醇,均为色谱纯,德国Merck公司;氢氧化钠、乙酸乙酯、磷酸二氢钠、正己烷等均为国产分析纯试剂;水为超纯水,利用美国Millipore超纯水仪自制。
1.3 标准溶液制备 标准储备液:准确称取左旋咪唑标准品10 mg(精确至 0.00001 g),于10 mL容量瓶中,用甲醇溶解并定容至刻度,配制成1000 μg/mL标准储备液。
标准工作液:准确量取标准储备液1 mL,于10 mL容量瓶中,用流动相稀释并定容至刻度,配制成100 μg/mL标准工作液。
1.4 溶液配制 5 mol/L氢氧化钠溶液:称取氢氧化钠40 g,加水至200 mL,摇匀。0.02 mol/L磷酸二氢钠溶液:称取磷酸二氢钠3.14 g,加水至1000 mL,摇匀。流动相:0.02 mol/L磷酸二氢钠-乙腈溶液(75∶25,V/V)。
1.5 样品制备
1.5.1 样品提取 称取适量饲料样品 (配合饲料2 g、浓缩饲料1 g)于 50 mL离心管中,加适量水(配合饲料试样10 mL、浓缩饲料5 mL),加5 mol/L氢氧化钠溶液0.2 mL,涡旋混匀1 min,超声20 min,加入20 mL乙酸乙酯,振荡30 min,6500 r/min离心5 min,取上清液5 mL于试管中,50℃氮气吹干,备用。
1.5.2 样品净化 残留物用2 mL流动相溶解,加入正己烷2 mL,涡旋1 min,静置分层,取下层溶液过滤膜上机测定。
1.6 色谱条件 色谱柱:SCX柱,柱长250 mm,内径 4.6 mm,粒径 5 μm;流动相:0.02 mol/L 磷酸二氢钠乙腈-溶液(75∶25,V/V);流速:1.0 mL/min;波长:215 nm;进样量:20 μL。
1.7 检测限和定量限的测定 按照信噪比S/N≥3时的添加浓度为检测限,S/N≥10时的添加浓度为定量限,测定方法的检测限和定量限。
1.8 添加回收率和精密度测定 选择空白配合饲料、浓缩饲料样品作为测试对象,进行加标回收率实验。称取适量饲料样品于50 mL离心管中,加入适量标准储备液,使配合饲料的添加浓度分别为 0.5、75、150、300 mg/kg, 浓缩饲料的添加浓度分别为 1、300、600、1200 mg/kg。 每个添加浓度设6个平行,进行3次重复。当样品上机液的浓度超过线性范围时,需稀释后重新测定,直至上机液浓度在线性范围内。
2 结果与分析
2.1 标准曲线 准确移取左旋咪唑标准工作液适量,用流动相逐级稀释配制成浓度为0.1、0.5、1、5、10、20、50 μg/mL 的系列标准溶液, 过 0.45 μm滤膜后上机测定。以左旋咪唑药物峰为纵坐标,标准溶液浓度为横坐标,绘制标准曲线。得到的回归方程为Y=127.5C+1.973,r=1.0000。结果显示,左旋咪唑浓度为0.1~50 μg/mL时呈现良好的线性关系(图1)。
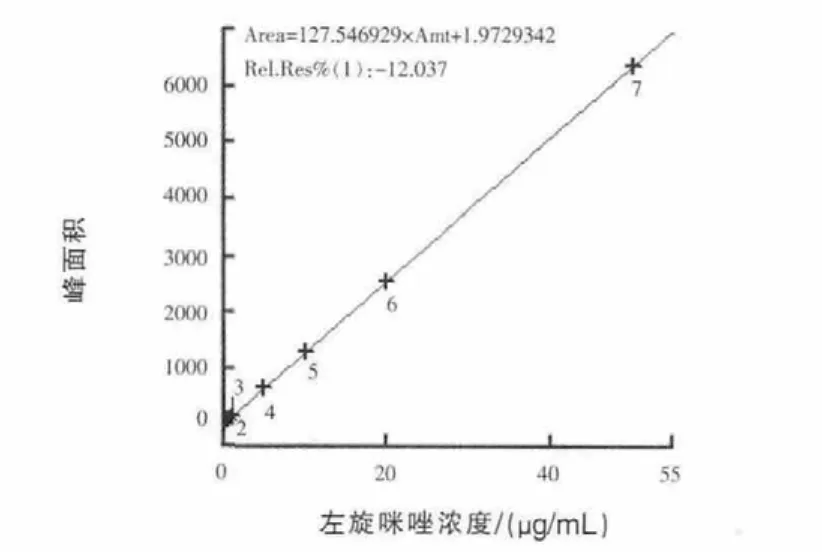
图1 左旋咪唑标准曲线
2.2 检测限和定量限 按照信噪比S/N≥3要求确定方法的检测限,按照信噪比S/N≥10要求确定方法的定量限。结果表明,在配合饲料中的检测限为0.2 mg/kg,定量限为0.5 mg/kg;在浓缩饲料中的检测限为0.4 mg/kg,定量限为1 mg/kg。
2.3 回收率和精密度 配合饲料浓度为0.5~300 mg/kg时,回收率为80.5%~102%,批内变异系数为0.6%~6.0%,批间变异系数为2.1%~4.8%;浓缩饲料浓度为1~1200 mg/kg时,回收率为80.1%~107%,批内变异系数为0.7%~9.8%,批间变异系数为2.0%~9.1%。配合饲料及浓缩饲料中左旋咪唑添加回收率测定结果见表1和表2;左旋咪唑标准溶液色谱图见图2;代表性配合饲料和浓缩饲料空白添加样品溶液色谱图见图3和图4。
3 讨论
3.1 液相色谱条件的优化 测定左旋咪唑常用C18色谱柱进行分离(林维宣等,2011;曾建亭等和曾勇等,2010),流动相为0.02 mol/L磷酸二氢钠(加二乙胺,用磷酸调pH值至7.5)-乙腈溶液(75∶25,V/V),紫外吸收波长为 210 nm(曾勇等,2010)。经测试,该条件下,样品的基线峰波动较大,杂质干扰较多。左旋咪唑是极性较强的化合物,本方法采用强离子交换色谱柱 (SCX,250 mm×4.6 mm,粒直径5 μm),流动相为0.02 mol/L磷酸二氢钠-乙腈溶液,基线平稳,杂质干扰少。当流动相比例为75∶25(V/V)时,能把样品溶液中杂质峰和目标药物峰较好地分离。二极管阵列扫描最大吸收波长为215 nm。其他液相条件为进样量20 μL,柱温30℃。在该液相条件下,左旋咪唑最大吸收波长为215 nm,见图5。
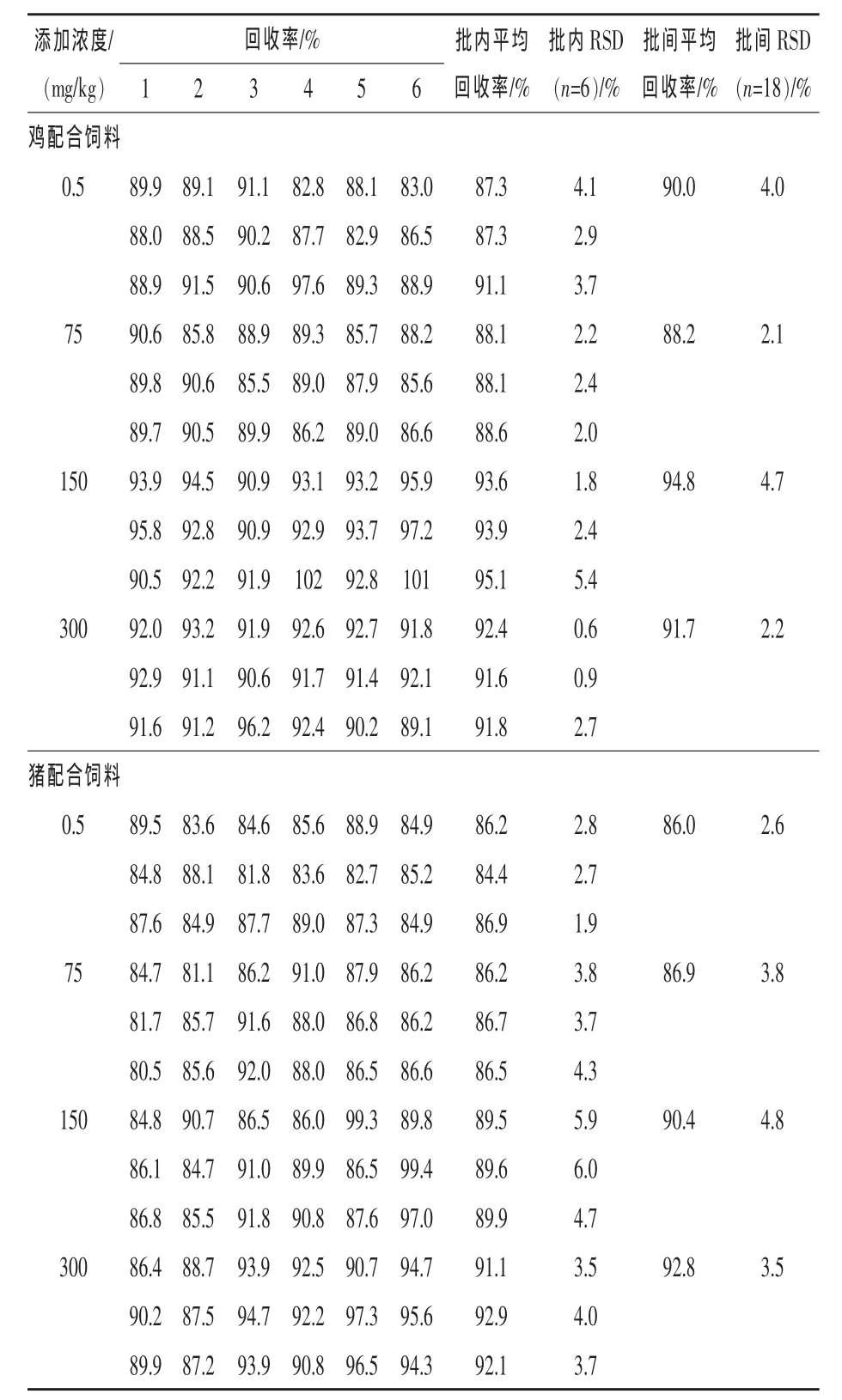
表1 配合饲料中左旋咪唑添加回收率测定结果

图2 左旋咪唑标准溶液色谱图(20 μg/mL)
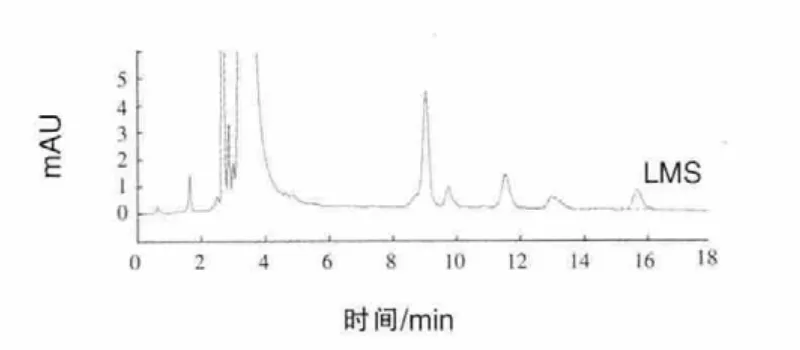
图3 配合饲料空白添加色谱图(0.5 mg/kg)
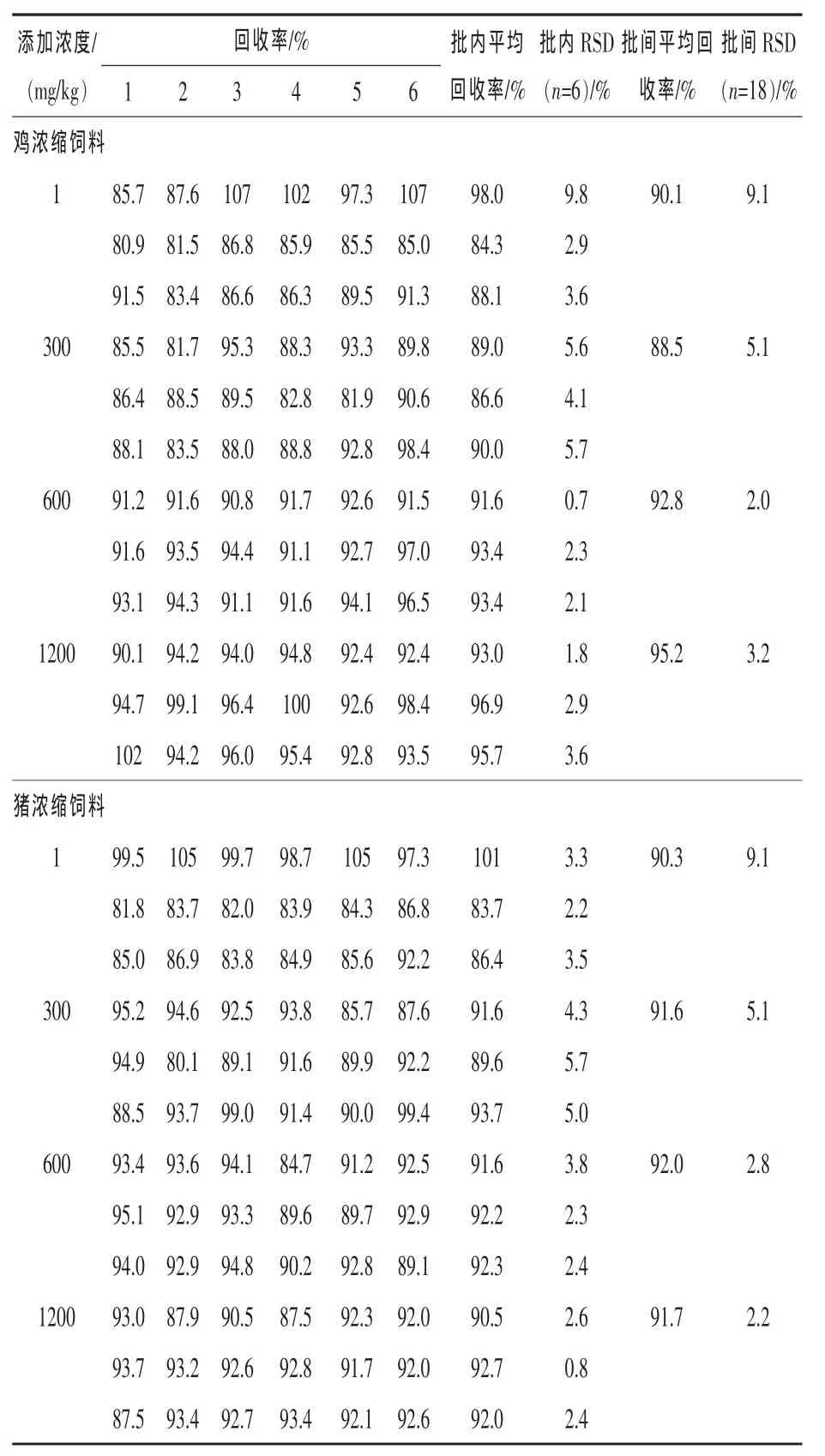
表2 浓缩饲料中左旋咪唑添加回收率测定结果

图4 浓缩饲料空白添加色谱图(1 mg/kg)
3.2 提取方法的确定 根据左旋咪唑的化学性质,在碱性条件下,左旋咪唑有一定的质子化倾向,可以促进目标物质从饲料中提取。当溶液为碱性时,左旋咪唑的电离受到抑制,在水相溶解度降低,易溶于卤代烷、醚、酯类等弱极性有机溶剂。因此,饲料中左旋咪唑的提取思路是:先在饲料中加入一定量的水和氢氧化钠溶液,使饲料和目标药物分散于碱性水溶液中,再用有机溶剂进行提取。
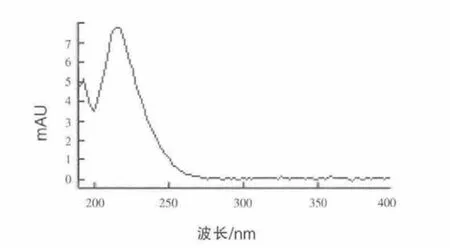
图5 左旋咪唑光谱图
3.2.1 加碱量的确定 碱性环境的强弱会影响有机溶剂的提取效果。在加水后的饲料样品中,若碱性环境太弱,左旋咪唑质子化程度低,降低其在乙酸乙酯中的溶解度;但随着氢氧化钠溶液剂量的增加(当pH值大于13),饲料中的脂肪成分会与多余的氢氧化钠发生反应,生成脂肪酸钠,黏性越来越大,导致样品不能与乙酸乙酯充分反应,降低乙酸乙酯的提取效果。在配合饲料和浓缩饲料中分别加入 5 mol/L 的氢氧化钠 0.1、0.2、0.3、0.5 mL,经比较发现,加入浓度为5 mol/L的氢氧化钠溶液0.2 mL时,回收率最高。
3.2.2 提取剂的选择 常用提取剂有:二氯甲烷、三氯甲烷、正己烷、异辛烷和乙酸乙酯。考虑有机溶剂的毒性,比较提取过程中操作的难易程度和回收率的高低。结果显示,回收率较高的是二氯甲烷和乙酸乙酯,均达到90%以上,但二氯甲烷麻醉性强,且太易挥发,分层后位于下层,不便于取出,因此选择乙酸乙酯作为提取剂。
3.3 净化方式的选择 饲料样品经乙酸乙酯提取后,脂溶性杂质较多的保留在样品中,同时左旋咪唑是极性较强的化合物,在酸性水溶液中可用极性较低的有机溶剂进行除脂,因此选择常用有机溶剂正己烷进行除脂。取5 mL乙酸乙酯提取液,置于50℃水浴中氮气吹干,再用2 mL流动相定容,并加入一定量的标准溶液,加入2 mL正己烷,涡旋1 min,静置,取下层溶液过滤膜,上高效液相色谱仪测定,观察正己烷的除脂效果,测定定容液的pH值,并计算回收率。结果显示,正己烷能有效除脂,定容液的pH值为5.8~6.0,样品的平均回收率为99.5%。结果说明,碱化乙酸乙酯经氮气吹干后对流动相定容液的pH值略有影响,由原来的4.78提高到了6.0,但仍为酸性条件,因此左旋咪唑是以离子形式存在于样品复溶液中,正己烷的除脂操作并不会减少左旋咪唑的含量。
3.4 同类药物的干扰 兽医临床常用的苯并咪唑类抗线虫药有:甲苯咪唑、阿苯达唑以及芬苯达唑。应用本方法色谱条件对上述三种药物和左旋咪唑的混合标准溶液进行测定。甲苯咪唑、阿苯达唑以及芬苯达唑的出峰时间分别为3.636、3.885、4.142 min,与左旋咪唑的出峰时间(15.361 min)相距较远,不会干扰左旋咪唑的测定。
3.5 添加浓度的确定 根据《中华人民共和国兽药典 兽药使用指南》(中国兽药典委员会,2010)左旋咪唑内服一次量,每千克体重,猪7.5 mg,禽25 mg,该药物常用于生长猪或生长鸡,根据饲喂畜禽的体重、日采食量,添加剂量约为150 mg/kg才有治疗作用。根据《饲料中兽药及其他化学物监测试验规程》(全国饲料工业标准化技术委员会,2008),按照方法定量限及该药物在临床使用的有效剂量,确定配合饲料的添加浓度分别为0.5(定量限)、75、150、300 mg/kg。 浓缩饲料添加比例与配合饲料相比为8∶2,因此浓缩饲料的添加浓度分别为 1(定量限)、300、600、1200 mg/kg。回收率实验中,当样品的上机液浓度超过线性范围时,需稀释后重新测定,直至上机液浓度在线性范围内。
4 结论
本研究建立了饲料中左旋咪唑的高效液相色谱检测方法,采用碱性环境下乙酸乙酯提取,用正己烷除脂。该方法的回收率为80%~110%,批内变异系数和批间变异系数均小于10%,说明本方法能满足饲料中左旋咪唑测定的要求。
[1]林维宣,田苗,隋凯,等.高效液相色谱法测定牛乳中左旋咪唑[J].中国乳品工业,2011,29(1):24~26.
[2]全国饲料工业标准化技术委员会.GB/T 23182-2008[S].饲料中兽药及其他化学物监测试验规程.北京:中国标准出版社,2008-12-31.
[3]曾建亭,钟小燕.HPLC法测定盐酸左旋咪唑片的含量及溶出度[J].中国热带医学,2010,10(5):628~629.
[4]曾勇,金秀娥,卢芳,等.猪鸡组织中左旋咪唑残留的HPLC检测方法研究[J].中国兽药杂志,2010,44(8):17~21.
[5]中国兽药典委员会.中华人民共和国兽药典 兽药使用指南[M].北京:中国农业出版社出版,2010.1:142~143.
