接骨草的化学成分与药理活性研究进展
2015-12-08姚元枝伍贤进黎晓英
姚元枝, 伍贤进, 黎晓英, 虢 慧, 魏 麟
(怀化学院生物与食品工程学院民族药用植物资源研究与利用湖南省重点实验室 湘西药用植物与民族植物学湖南省高校重点实验室,湖南怀化418008)
接骨草的化学成分与药理活性研究进展
姚元枝, 伍贤进, 黎晓英, 虢 慧, 魏 麟*
(怀化学院生物与食品工程学院民族药用植物资源研究与利用湖南省重点实验室 湘西药用植物与民族植物学湖南省高校重点实验室,湖南怀化418008)
接骨草Sambucus chinensis Lindl.为忍冬科接骨木属植物,为我国传统中草药,含有黄酮、三萜、甾体和苯丙素类等多种化合物,具有抗肝炎、抗菌消炎、活血化瘀、镇痛等广泛的药理活性,开发利用价值很高。本文综述了接骨草化学成分和药理作用的研究进展,并对未来的研究做了展望。
接骨草;化学成分;药理活性;研究进展
接骨草是忍冬科接骨木属接骨草Sambucus chinensis Lindl.的全草,别名陆英、蒴藋、八棱麻、臭草、七叶金、走马风、公道老、马鞭梢、水英、秧心草等,为多年生高大草本或亚灌木植物,生于海拔300~2 600米的阴湿肥沃地,分布于我国大部分地区,资源丰富。该植物始载于《神农本草经》[1],味苦寒、无毒,今记载于 《中华本草》[2],为我国传统中草药,全株皆可入药,具有疏肝健脾、祛风除湿[3]、 活血散瘀[4]、抗炎[5]、 镇痛[6]、 抗氧化[7]、抗病毒[8]和抗肿瘤[9]等功效。在民间,接骨草因具有接骨功效而得名,并广泛用于治疗跌打损伤。近年来研究发现,其治疗黄疸型和病毒性肝炎的效果显著,而且无毒性[10],因此引起了国内外学者的广泛重视。目前对接骨草的研究主要集中在化学成分和药理活性等方面。
1 化学成分
接骨草化学成分的研究始于20世纪70年代,迄今为止,其中已有55个化合被分离鉴定,主要为黄酮、三萜、甾体、酚酸、挥发油和苯丙素类等[11]成分,具体见表1。

表1 接骨草化学成分

续表1
1.1 黄酮类化合物 从接骨草中已经分离鉴定黄酮类化合物8种 (表1和图1),以黄酮醇类为主,如化合物1~2、4~8。该类化合物的母核由两个有羟基的苯环通过中央三碳原子连接形成,且母核山柰酚中羟基的氢原子易被糖苷的半缩醛羟基取代,从而形成多种不同黄酮类化合物。化合物7~8由廖琼峰等[14]首次分离得到。文献 [21-23]
报道接骨草生药及其制剂的黄酮含有量,并用加热回流[24]、微波[7]及超声波[8]提取其中的黄酮类化合物,发现超声提取得率较高,达4.143%。另外,化合物1-3具有较好抗炎功效。
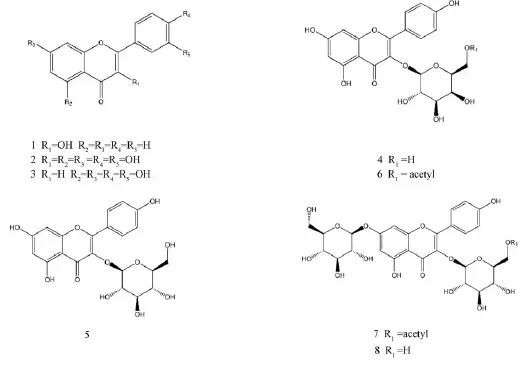
图1 接骨草中黄酮类化合物结构
1.2 三萜类化合物 目前,从接骨草中提取分离得到11种三萜类化合物 (表1和图2),其结构是由六个异戊二烯单位聚合形成的五环三萜,主要有熊果烷型、齐墩果烷型和木栓烷型。其中,化合物9~13由陶佳颐等[15]首次提取获得。严建良等[25]采用水沉纯化和活性炭脱色法提取得到化合物14和15,并且前者的含有量远高于后者[26]。采用不同提取工艺及分离方法[27-30]获得化合物14,并由邹盛勤[31]推定了其分子骨架、官能团位置和结构。化合物14在叶中的含有量为0.4%~0.5%[32],并随叶片的发育有增高趋势,而花中为0.83%[28]。化合物15在叶中的含有量是茎的7倍[33]。化合物16由杨燕军等[19]首次鉴定。陈武等[16]利用乙醇回流法提取获得化合物17~18。化合物19为Inoue等[17]首次分离得到。
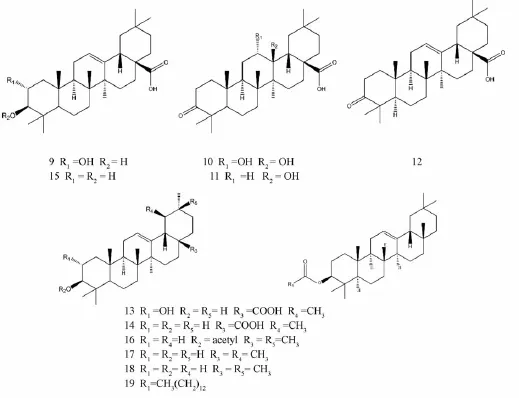
图2 接骨草中三萜类化合物的结构
1.3 甾体类 目前,从接骨草中提取分离得到5种甾体类(表1及图3),化合物母核为环戊烷骈多氢菲结构,以C-21甾为母核,其中化合物21的C-3位连糖苷,而化合物20连羟基,其他化合物也因取代基不同而有所差异。杨德泉[34]采用薄层扫描法测定β-谷甾醇的含有量,发现叶中比茎要高,而且均在开花期间最高 (0.419%),故建议药材宜以采收叶为主,应在开花时采收为佳。
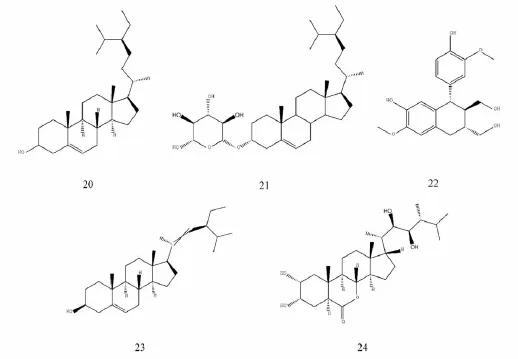
图3 接骨草中甾体类化合物的结构
1.4 挥发油类 采用GC-MS联用技术分离了接骨草中34种挥发油成分,已鉴定了其中的26种成分[20](表1及图4),多为环类或长链烷烃、酸、酯等化合物,同时报道了其相对含有量,以化合物25最高 (35.651%),34次之(30.507%),33较少 (13.613%),另外8种迄今未见报道。化合物39为杨燕军等[19]从接骨草中首次获得。
1.5 苯丙素类 从接骨草中分离得到绿原酸和东莨菪素(图5),后者属于香豆素,由李胜华等[12]首次分离得到,但无后续报道。目前,相继报道了绿原酸的含有量[35-38]在花、叶中最高[39-40],并以5月[37]或7月[41]为高。
1.6 酚酸类 接骨草中酚酸类成分有3种,分别为咖啡酸、阿魏酸和对香豆酸 (图5),均以肉桂酸为母核,因苯环上取代基不同而形成不同的化合物,但未见进一步的研究报道。
2 药理活性
2.1 抗肝炎作用 接骨草生药提取液及其制剂对小鼠多种急性实验性肝损伤有明显的保护作用,并用于临床,效果很好。文献 [42]报道接骨草生药75%乙醇提取物经大孔吸附树脂纯化后,可对抗CCl4导致小鼠肝损伤,保肝降酶功效的活性有效部分主要集中在30%乙醇洗脱液。而且对CCl4、D-Gal、ConA所致急性实验性肝损伤有明显的保护作用,通过提高正常小鼠单核-巨噬细胞吞噬功能,增加血清中异物清除速率,提高肝脾网状内皮系统吞噬指数,来实现增强小鼠的非特异性免疫功能[43]。有用接骨草颗粒作用于CCl4、D-Gal、ConA所致肝损伤,保护效果很明显的报道[44],进一步发现[45]其能有效地对抗CCl4所致的脂质过氧化、保护线粒体、提高细胞膜及微粒体膜钙泵的活性,呈显著剂效关系,但对其余两种的作用机理尚无进一步研究。也有报道[46]用接骨草冲剂对CCl4、D-Gal和ANIT小鼠急性肝损伤具有一定的保肝、退黄以及减轻肝脏病理损伤作用。
王明时等[47]认为,接骨草中含有量最高的熊果酸是治疗肝炎的主要有效成分,这一结论在陈武等[48]的研究中得到进一步证实,但也有研究[49]表明其中的齐墩果酸能有效治疗传染性黄疸肝炎,从而对急性肝损伤有显著保护效果,有效率达93.5%。因此,接骨草中抗肝炎的主要成分可能是三萜类化合物熊果酸和齐墩果酸,但是否与其它抗氧化活性成分如黄酮、苯丙素及甾体类等化合物有关,有待作进一步研究。
2.2 抗炎镇痛作用 接骨草水、醇提取物或有机溶剂萃取物均具有较好的抗炎及镇痛作用。研究表明[5]服用临床常用剂量接骨草时较安全,其水及醇提物对急性炎症 (二甲苯致小鼠耳廓肿胀、醋酸致小鼠扭体)及中枢性疼痛 (热板致小鼠足痛)均有明显的抑制作用。接骨草水煎剂有很好的镇痛作用,但比盐酸曲马多稍弱[6]。用不同有机溶剂萃取接骨草醇提取物,发现正丁醇和氯仿部位都能抑制醋酸刺激腹腔黏膜引起的疼痛反应,但前者镇痛效果好于后者[50]。翁进[49]报道,接骨草中的麻醉成分具有止痛效果,其特点为无耐受性及成瘾性,但脂溶性成分无镇痛作用,推测水溶性成分中可能含有。另外,酚性生物碱也可能有
镇痛作用[51]。
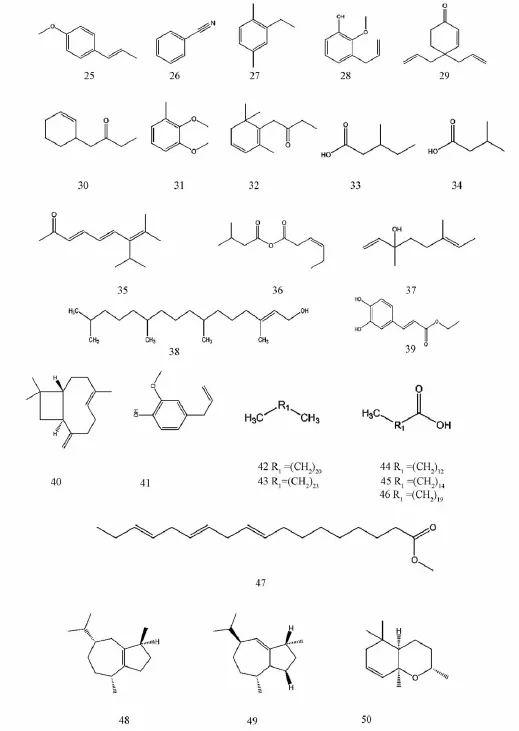
图4 接骨草中挥发油类化合物的结构
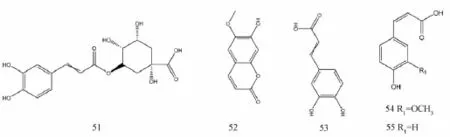
图5 接骨草中苯丙素类和酚酸类化合物的结构
2.3 活血化瘀作用 目前认为,接骨草的活血化瘀作用与含有量较高的熊果酸有关。研究发现[52],接骨草全草水煎剂、熊果酸均能延长小鼠出血时间和凝血时间,它可能抑
制凝血因子、血小板和毛细血管功能,具有较好的抗凝作用。进一步研究表明[53],接骨草水煎剂与熊果酸能降低全血黏度、红细胞沉降率值,并具有明显的量效关系。陈东波[4]等报道,接骨草煎剂能明显降低大鼠体外血栓形成过程中血栓重量,从而抑制其血栓的形成。该植物已广泛用于治疗扭伤、腰肌劳损、骨折等症,又能作兽药治牛跌伤[54],这与其抗炎镇痛及活血化瘀的药理活性有关,但其作用机理及有效成分不能确定,将直接影响该药的开发利用。
2.3 抗菌消炎作用 接骨草针剂可用于治疗急性菌痢、急性化脓性扁桃腺炎、多发性疖肿等炎症,所以有一定的消炎和清热解毒作用[45]。有研究认为[55],齐墩果酸能抑制血管通透性增高,使组织释放PGE量下降,抑制肉芽组织增生,有较好的抗炎作用,其机理可能是激活垂体-肾上腺皮质系统,抑制PGE的合成或释放。接骨草抗菌消炎和清热解毒的物质基础及机理不是很清楚,可能与接骨草中黄酮、三萜及绿原酸等主要有效成分有关。另外,β-谷甾醇也具有明显的消炎作用,并且不依赖垂体-肾上腺系统。
2.4 其他药理作用 王朝元等[56]报道,绿原酸可通过调控成骨细胞增殖和分化来实现成骨作用,是接骨草的主要活性成分之一,但有待作进一步探讨,并且熊果酸还有明显降脂作用[43]。另外,接骨草中黄酮类成分表现出很好的抗氧化活性,对Fenton体系产生的·OH自由基有一定清除作用,并且对水杨酸体系中·OH自由基的清除效果比芦丁好,与Vc相当[7]。
2.5 毒性评价 翁进等[49]用小鼠灌胃检测接骨草水煎浓缩液的毒性,发现小鼠最大耐受量为500 g/kg,比成人临床用量高100倍,小鼠灌胃给药LD50为820 g/kg,腹腔注射LD50为119 g/kg。同时发现,小鼠死亡前都有烦躁不安、大小便失禁、抽搐等症状,这说明过量的接骨草制剂对神经系统有一定毒性。王文静[5]等给小鼠灌服接骨草水提物及醇提物,采用最大给药量评价其毒性,结果发现小鼠灌胃给予接骨草分别为临床人用量的720、750倍左右时,仍无明显不良反应。虽然接骨草煎剂副作用很小,但使用时仍有少数患者会产生轻度头晕、盗汗、瘙痒、手足发麻等不良症状,停药后便恢复正常[57]。因此,该植物产生毒性的机理、生药及制剂的安全用药还需作进一步研究。
3 展望
我国接骨草资源十分丰富,随着对该植物化学成分的不断深入研究,其现代药理研究也取得了较大进展,特别是三萜类抗肝炎的突出作用尤为引人关注。但是,治疗骨折、抗肝炎、活血化瘀、镇痛等药效物质基础及药用机理研究还不够完善,尤其在有效成分的基因克隆及表达方面的研究颇少。所以,建立多种简单、有效、可复制性强的药理学模型和临床药效学模型,以进一步对接骨草有效部位及成分进行分离分析,特别是对抗肝炎、治疗骨折、活血化瘀及镇痛等作用的有效成分及机制研究是现阶段亟需解决的问题。在此基础上,建立稳定、可靠的接骨草生药及其制剂质量控制标准,这不但能为开发出相关药物奠定基础,也能为更合理地进一步利用该资源提供必要的科学依据。
[1] 明·李时珍.本草纲目[M].北京:人民卫生出版社,1985:1082,1084,2456.
[2] 国家中医药管理局 《中华本草》编委会.中华本草[M].上海:上海科学技术出版社,1999:541-544.
[3] 曹梦晔,高 昂,巩 江,等.接骨木属植物药用研究概况[J].宁夏农林科技,2011,52(4):59-60,62.
[4] 陈东波,黄清松,曾繁涛.陆英煎剂对大鼠体外血栓形成的影响[J].辽宁医学院学报,2013,34(5):13-15.
[5] 王文静,王 军,饶高雄.接骨草的两种提取物对小鼠的抗炎镇痛作用[J].华西药学杂志,2011,26(3):247-249.
[6] 吴丽霞,吴铁松,郑 敏.陆英煎剂对小鼠镇痛作用的实验研究[J].今日药学,2012,22(8):481-483.
[7] 李 伟.接骨草黄酮类物质超声提取工艺优化及其抗氧化活性[J].中药材,2011,34(11):1789-1791.
[8] 蔡凌云.接骨草黄酮成分的初步研究[J].凯里学院学报,2010,28(6):62-64.
[9] 廖琼峰.陆英药效物质基础研究[D].沈阳:沈阳药科大学,2005.
[10] 杨 威,王茜莎,王敏伟,等.陆英提取物对急性实验性肝损伤的保护作用[J].沈阳药科大学学报,2006,23(8):524-528.
[11] 中国医学科学院药物研究所.中草药有效成分的研究:第一分册[M].一版.北京:人民卫生出版社,1972:39.
[12] 李胜华,李爱民,伍贤进.接骨草化学成分研究[J].中草药,2011,42(8):1502-1504.
[13] Zhang TH,Zhu M,Chen X H,et al.Simultaneous analysis of seven bioactive compounds in Sambucus Chinensis Lindl.by HPLC[J].Anal Lett,2010,43(16):2525-2533.
[14] 廖琼峰,谢社平,陈晓辉,等.陆英的化学成分研究[J].中药材,2006,29(9):916-917.
[15] 陶佳颐,方唯硕.陆英中化学成分的研究[J].中国中药杂志,2012,37(10):1399-1401.
[16] 陈 武,李开泉,熊筱娟,等.陆英抗肝炎活性成分的化学研究[J].宜春医专学报,2000,12(4):239-241.
[17] Inoue T,Hirashima H.Studies on the constituents of Sambucus speciesⅡ.Constituents of the leaves of Sambucus sieboldiana Blume ex Graebn.var.Miquelii(Nakai)Hara[J].Yakugaku Zasshi,1973,93(11):1530-1533.
[18] Inoue T,Nakahata F.Studies on the constituents of Sambucus Chinensis Lindl.[J].Chem Pharm Bull,1969,17(1):124-127.
[19] 杨燕军,林洁红.陆英化学成分的研究 (I)[J].中药材,2004,27(7):491-492.
[20] 蒋道松,裴 刚,周朴华,等.八棱麻挥发性成分分析[J].中药材,2003,26(2):102-103.
[21] 涂剑平,汪 玢,何 京,等.分光光度法测陆英中总黄酮含量时NaOH的用量研究[J].江西医学院学报,2005,45
(4):140-142.
[22] 何 京,汪 玢,涂剑平,等.陆英糖浆质量标准研究[J].时珍国医国药,2006,17(12):2536-2537.
[23] 汪 玢,张 宁,何 京,等.陆英片中总黄酮的含量测定[J].江西医学院学报,2006,46(1):148-150.
[24] 周 文,黎 莉,戴立珍,等.正交实验法优选陆英总黄酮的提取工艺[J].亚太传统医药,2009,5(11):30-32.
[25] 严建良,吴安明,何杨虎.陆英中三萜酸类成分提取工艺研究[J].江西中医药,2012,43(6):70-72.
[26] 邹盛勤,陈 武.陆英中乌索酸和齐墩果酸动态含量的研究[J].安徽农业科学,2005,33(4):642-643,666.
[27] 马 延,王 瑾,席鹏洲,等.响应面法优化陆英中熊果酸的提取工艺[J].西北农业学报,2012,21(6):156-161.
[28] 李爱民,姚元枝,陈 镇,等.超声波提取接骨草花中乌索酸的工艺研究[J].食品工业科技,2012,33(9):234-237.
[29] 李开泉,邹盛勤,陈 武,等.陆英中乌索酸提取工艺的正交优选[J].中草药,2003,34(9):791-792.
[30] 李开泉,陈 武,张绍良,等.以陆英为原料提取乌索酸的工艺研究[J].中成药,2003,25(5):356-358.
[31] 邹盛勤,张西安.陆英提取物乌索酸的紫外和红外光谱研究[J].河南师范大学学报:自然科学版,2005,33(1):73-76.
[32] 李爱民,李 媛.接骨草叶结构及乌索酸的含量测定[J].贵州科学,2011,29(3):32-34.
[33] 杨德泉.土家药水边麻叶与茎中齐墩果酸的含量测定[J].中国民族医药杂志,2004,10(12):188-189.
[34] 杨德泉.薄层扫描法测定土家药陆英不同采收期叶与茎中β-谷甾醇的含量[J].中国民族医药杂志,2005,11(3):26-27.
[35] 刘立荣.HPLC法测定陆英中绿原酸的含量[J].科技创新导报,2012(35):219.
[36] 刘传安,邹盛勤.RP-HPLC法测定陆英叶中绿原酸含量的研究[J].安徽农业科学,2005,33(12):2334-2335.
[37] 廖琼峰,谢社平,陈晓辉,等.不同采收期陆英中绿原酸含量的动态研究[J].中药新药与临床药理,2006,17(3):198-200.
[38] 杨红兵,石 磊,肖 萍,等.陆英的质量研究Ⅱ[J].湖北中医学院学报,2010,12(1):26-27.
[39] 姚元枝,李爱民,全妙华,等.接骨草的绿原酸含量测定及方法学考察[J].怀化学院学报,2013,32(11):9-11.
[40] 姚元枝,李爱民,全妙华,等.HPLC测定接骨草中的绿原酸[J].光谱实验室,2014,31(4):472-476.
[41] 李爱民,姚元枝,郭 瑛,等.超声波提取接骨草叶中绿原酸的工艺优化[J].食品工业科技,2013(17):323-240.
[42] 朱少璇,廖琼峰,王茜莎,等.陆英不同工艺提取物对四氯化碳致小鼠肝损伤的影响实验研究[J].中药材,2008,31(8):1216-1219.
[43] 杨 威,王茜莎,王敏伟,等.陆英提取物对急性化学性肝损伤的保护作用[J].沈阳药科大学学报,2006,23(8):524-528.
[44] 杨 威,王茜莎,王敏伟,等.陆英颗粒对急性实验性肝损伤的保护作用研究[J].中药材,2005,28(12):1085-1088.
[45] 曾琳玲,杨 威,王茜莎,等.陆英颗粒对CCl4致小鼠急性肝损伤保护作用研究[J].中国实用医药,2007,2(22):12-14.
[46] 肖小华,徐丽瑛,方 铝,等.陆英冲剂保肝作用研究[J].实用中西医结合临床,2004,4(1):66-67.
[47] 王明时,李景荣,徐丽仙,等.陆英抗肝炎活性成分的化学研究[J].南京药学院学报,1985,16(3):15-17.
[48] 陈 武,李开泉,熊筱娟,等.陆英抗肝炎活性成分的研究[J].南昌大学学报:理科版,2001,25(2):165-167.
[49] 翁 进,郑尚忠,张文清.陆英的临床应用及其有效成份浅析[J].福建药学杂志,1994,6(1):33-34.
[50] 袁志军,易增兴.陆英的不同提取分离物对小鼠镇痛作用的影响[J].中外医疗,2011(36):17.
[51] 周林华.陆英不同提取物镇痛作用的研究[J].华章,2011(34):367.
[52] 易增兴,熊筱娟,李四玲.陆英及其提取物乌索酸对小鼠出血和凝血时间的影响[J].宜春学院学报,2011,33(8):77-78.
[53] 黄电波,黄清松.陆英与乌索酸对大鼠全血黏度和红细胞沉降率的影响[J].实用临床医学,2012,13(6):10-12.
[54] 江苏新医学院.中药大辞典:下册[M].上海:上海人民出版社,1977:2456.
[55] 戴 岳.齐墩果酸的抗炎作用[J].中国药理学与毒理学杂志,1989,3(2):96-99.
[56] 王朝元,易继凌,宋 超,等.绿原酸对体外培养成骨细胞活性的影响[J].中南民族大学学报,2013,32(2):46-50.
[57] 南京药学院 《中草药学》编写组.中草药学 (下)[M].南京:江苏科技出版社,1980:1075-1076.
R284.1;R285.5
A
1001-1528(2015)12-2726-07
10.3969/j.issn.1001-1528.2015.12.033
2015-01-26
国家自然科学基金项目 (30870230);湖南省科技计划重点项目 (2015SK2013,2013FJ6090);湖南省高校创新平台开放基金项目 (12K132);民族药用植物资源研究与利用湖南省重点实验室开放基金项目 (YYZW2015-8,ZDSYSJJ2013-2);湖南省 “十二五”植物学重点建设学科资助 (201142)
姚元枝 (1965—),女,副教授,研究方向为药用植物有效成分与资源。Tel:(0745)2851037,E-mail:yaoyuanzhi93@ 163.com
*通信作者:魏 麟(1974—),男,博士,副教授。E-mail:hhweilin@163.com
