TBAB/KCl对构筑阴离子蠕虫状胶束的影响
2015-12-07韩一秀韦勇强梅拥军
韩一秀 周 洪 韦勇强 梅拥军 王 航
(中国民航局第二研究所, 成都 610041)
TBAB/KCl对构筑阴离子蠕虫状胶束的影响
韩一秀 周 洪 韦勇强 梅拥军*王 航
(中国民航局第二研究所, 成都 610041)
采用流变测试技术考察了两种阴离子表面活性剂油酸钠(NaOA)和芥酸钠(NaOEr)在四丁基溴化铵(TBAB)和KCl诱导下构筑蠕虫状胶束的行为. 随着KCl浓度增加, NaOA水溶液粘度增加, 而加入TBAB使NaOA-KCl样品的粘度持续降低. 与之相反, TBAB浓度的增加却使NaOEr-KCl样品的粘度大幅度增强. 此外, NaOEr分子比NaOA表现出更强的形成胶束的能力, 构成粘弹性蠕虫状胶束所需表面活性剂浓度和盐浓度更少. 本文采用TBAB和KCl两种盐协同诱导NaOEr, 制备了具有强粘弹性的阴离子蠕虫状胶束, 探讨了盐TBAB/KCl对长链阴离子表面活性剂构筑蠕虫状胶束的影响机理.
阴离子表面活性剂; 芥酸钠; 四丁基溴化铵; 蠕虫状胶束; 流变性
1 引 言
两亲结构特点使表面活性剂分子在水溶液中有自发聚集的倾向, 在特定的电解质、温度、剪切等条件下, 表面活性剂自组装形成长的柔性蠕虫状胶束.1–4当表面活性剂达到临界交叠浓度(C*)以上,蠕虫状胶束互相缠绕形成瞬时三维网络状结构, 宏观上表现出类似聚合物溶液的流变性.5由于蠕虫状胶束具有自组装结构, 它受到机械剪切后能快速恢复胶束结构和溶液流变性, 因而蠕虫状胶束也被称作“living”聚合物.6这一独特流变特性使蠕虫状胶束作为流变控制剂, 在流体减阻、三次采油、清洁压裂液、日常洗护用品等领域存在潜在的应用价值.7,8
关于蠕虫状胶束的研究集中在由尾基链长为C16的阳离子表面活性剂构成的体系, 相比之下, 阴离子表面活性剂体系受到的关注较少.6,8–12据报道,阴离子表面活性剂比阳离子表面活性剂更易降解,应用在三次采油时, 由于地层岩石表面多带负电,还能有效降低吸附损失.13,14根据堆积参数理论, 堆积参数P = V/al, V代表表面活性剂的疏水尾基的体积, a代表头基的横截面积, l代表疏水链长, 只有当1/3 ≤ P ≤ 1/2时才能形成蠕虫状胶束.15可见表面活性剂的分子结构是影响胶束形态的重要因素. 由于离子表面活性剂亲水头基间存在强烈的静电排斥作用不利于形成蠕虫状胶束, 往往通过加入带相反电荷的无机或有机反离子来屏蔽静电排斥作用, 才能有效促进胶束形成和增长.16
目前报道的阴离子蠕虫状胶束多数是由无机盐诱导疏水基碳链长度不大于C18的阴离子表面活性剂构成, 比如, 油酸钾-KCl,17十二烷基三乙氧基硫酸钠-NaCl,18油酸钠(NaOA)-KCl,13NaOA-NaBr,19十六烷基硫酸钠-Bola盐20等体系. 除了无机盐之外,季铵盐是阴离子表面活性剂胶束体系里最常见的有机盐添加剂.21,22不对称型季铵盐——苄基三甲基溴化铵利用超强疏水性分别诱导NaOA和芥酸钠(NaOEr)形成蠕虫状胶束.19,23Nakamura和Shikata24考察了不同大小的季铵根离子与不同链长的烷基硫酸钠的相互作用, 发现季铵根离子大小与表面活性剂链长存在一定匹配性, 表面活性剂的链长越长形成粘弹性蠕虫状胶束所需要的季铵根离子越大.24以上报道限于非对称型季铵根离子, 即四个支链不完全相同, 由于有一个较长的支链存在, 在促进胶束增长时疏水缔合作用占主导. 对称型季铵盐(TAA+)存在时, 硫酸根型阴离子表面活性剂往往有浊点出现.21,25不仅如此, 油酸钠和十二烷基硫酸钠只能形成球型胶束, TAA+的位阻效应阻碍胶束在一维线型方向增长.13,26对称型季铵根离子能否克服位阻效应诱导阴离子表面活性剂形成蠕虫状胶束尚无定论. 超长链(C22)表面活性剂由于在制备蠕虫状胶束时表现出有利趋势, 而使此类表面活性剂成为新研究热点.23,27
本文考察了两种阴离子表面活性剂NaOA和NaOEr在水溶液中的胶束聚集和增长行为, 研究了正四丁基溴化铵(TBAB)和KCl的浓度变化对胶束形态变化及溶液流变行为的影响, 探讨了对称性季铵盐TBAB与表面活性剂的相互作用机理及促进胶束增长的驱动力.
2 实验部分
2.1 试 剂
NaOA(99%)购于国药集团, NaOH (99%)、TBAB(97%)和KCl(98%)购于成都科龙化工, 芥酸钠参照文献在实验室自制,23所用芥酸(95%)购买于西普化工. 所有试剂使用前未经过进一步纯化, 超纯水由Millipore Milli-Q制备. 为了控制表面活性剂水解, 样品均用pH为10左右的纯水溶液配制.28本实验所用表面活性剂和有机反离子结构如图1所示.
2.2 分析测试方法
流变测试采用TA流变仪(AR2000ex)进行, 采用椎板(半径40 mm, 锥角1°)传感器测量, 使用仪器自带样品盖以减小样品中水分挥发. 每个样品在测试前均放置在测试温度下稳定24 h. 稳态流变测试采用应力控制模式, 剪切速率在10–3–103s–1. 频率实验采用振荡模式(OSC), 首先在固定频率1 Hz下进行应力谱测试, 确定体系的线性粘弹区后选择确定的应力值, 在线性粘弹区展开动态流变测试, 频率范围在0.01–100 rads–1. 如无特殊说明所有流变测试均在50 °C下进行.
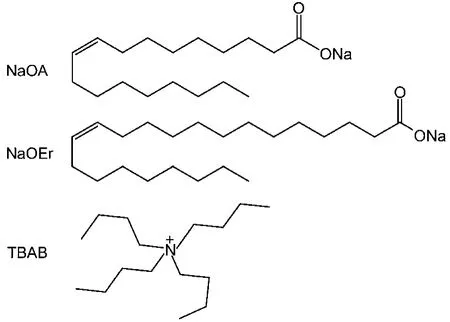
图1 NaOA, NaOEr和TBAB的分子结构式Fig.1 Molecular structures of NaOA, NaOEr, and TBAB
3 结果与讨论
3.1 盐浓度对NaOA溶液流变性的影响
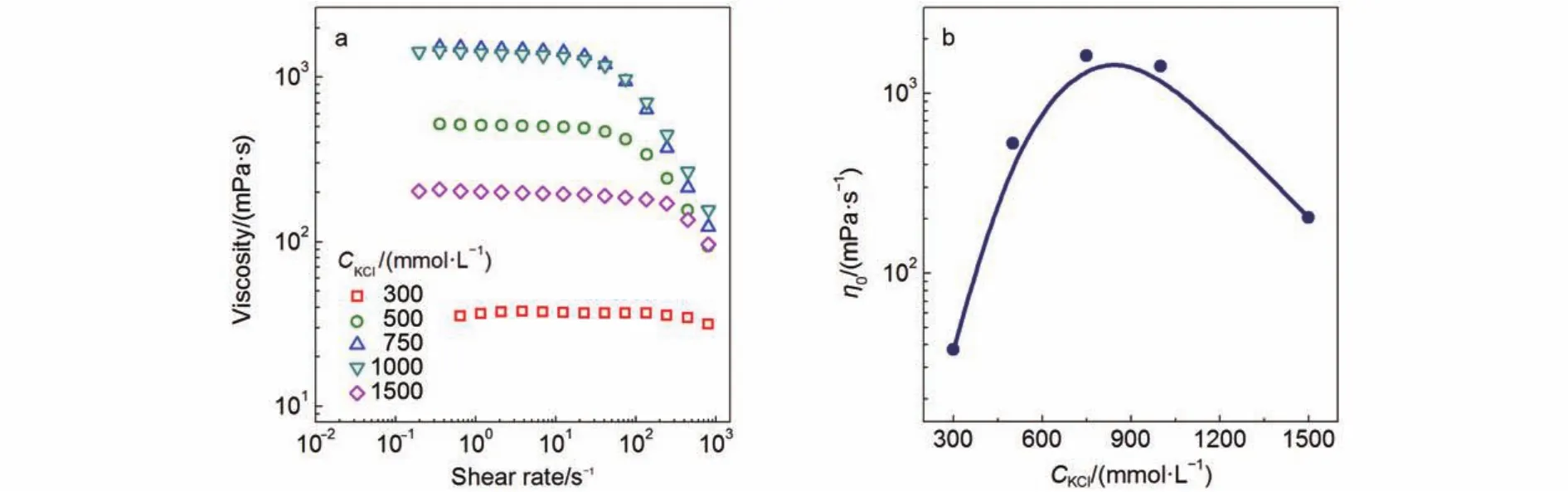
图2 KCl浓度变化对250 mmolL–1NaOA溶液稳态流变(a)及零剪切粘度η0(b)的影响Fig.2 Effect of KCl concentration on steady rheology (a) and zero-shear viscosity η0(b) of 250 mmolL–1NaOA solution
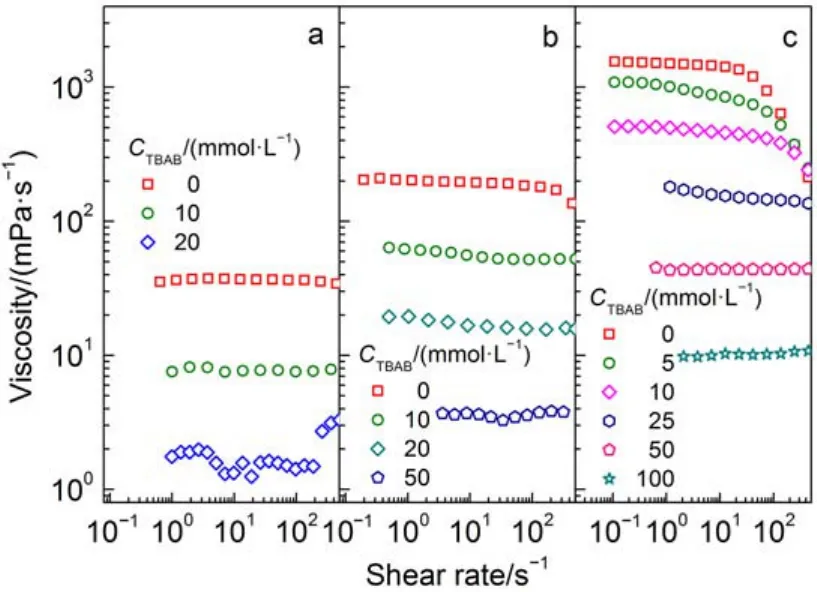
图3 TBAB浓度变化对样品稳态流变的影响Fig.3 Effect of TBAB concentration on steady rheology of samples
由图3的稳态流变曲线所得的η0汇总于图4. 三个KCl浓度的NaOA胶束溶液, 其η0均随TBAB浓度增加而降低. KCl浓度为750 mmolL–1时样品的初始粘度最大, 这条曲线下降相对平缓, TBAB浓度从0 mmolL–1增加到100 mmolL–1, 样品的η0降低两个数量级. TBA+通过三种作用影响胶束增长: 静电屏蔽、空间位阻和疏水缔合. TBA+的正电荷被四个支链相对分散后对表面活性剂头基的静电屏蔽作用被削弱, 样品“250 mmolL–1NaOA + 750 mmolL–1KCl”中盐浓度过量, 静电屏蔽比较充分, TBA+的静电屏蔽贡献更加不明显. 由粘度逐渐减小的结果表明, TBA+的位阻效应起主要作用, 位阻效应影响了表面活性剂聚集.
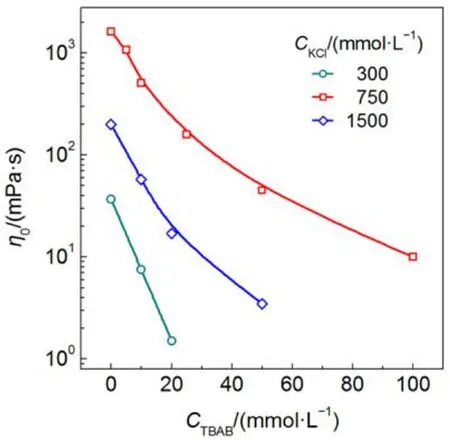
图4 TBAB浓度变化对不同KCl含量下250 mmolL–1NaOA胶束溶液η0的影响Fig.4 Effect of TBAB concentration on η0of 250 mmolL–1NaOA solution at different KCl contents
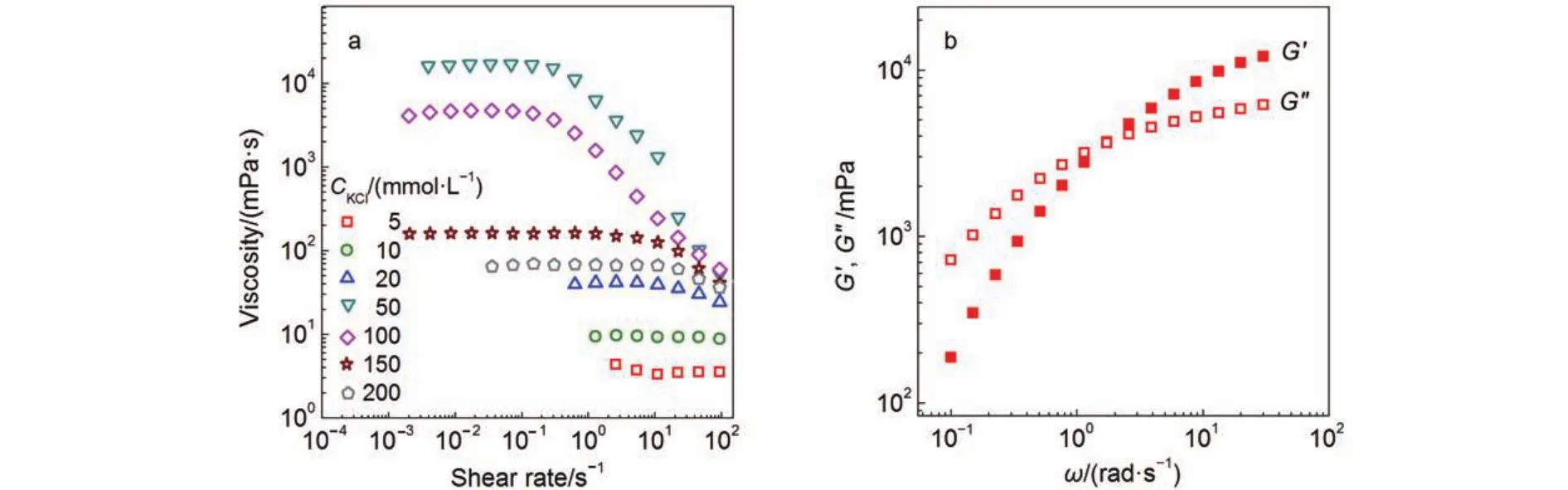
图5 KCl浓度变化对“50 mmolL–1NaOEr + 14 mmolL–1TBAB”溶液稳态流变的影响(a), 以及样品“50 mmolL–1NaOEr + 14 mmolL–1TBAB + 50 mmolL–1KCl”的动态流变(b)Fig.5 Effect of KCl concentration on the steady rheology of “50 mmolL–1NaOEr+14 mmolL–1TBAB” solution (a), and dynamic rheology of sample “50 mmolL–1NaOEr + 14 mmolL–1TBAB+50 mmolL–1KCl” (b)
三个样品体系的η0下降幅度略有不同, 随着NaOA-KCl样品初始粘度的降低, 下降曲线变得更加陡峭. KCl浓度为300 mmolL–1时样品的初始粘度最低, TBAB浓度仅增加20 mmolL–1时样品的η0就降低1.5个数量级. 可见TBAB浓度增加对初始粘度低的样品或者胶束长度短的样品的破坏作用更明显, 换言之, 粘度偏高的胶束体系更能承受TBAB带来的不利影响. 由图3的稳态流变数据可知, 该样品以分散的短棒状胶束或者球型胶束为主, 加入TBA+后, 位阻效应得到充分发挥, 表面活性剂分子更加分散, 长的棒状胶束迅速瓦解成球型胶束, 粘度消失. 样品“250 mmolL–1NaOA + 750 mmolL–1KCl”的稳态流变表明溶液中形成了缠绕的网络状结构, 胶束分布较为密集, 表面活性剂聚集程度提高, TBA+的位阻效应得到部分抑制. 此外, 位阻效应产生的影响为, 蠕虫状胶束先变在长度上有所减少,由长的柔性蠕虫状胶束变成短棒状胶束, 最后变成球型胶束. 因此其粘度转变也是一个循序渐进的过程.
3.2 盐浓度变化对NaOEr溶液流变性的影响
由于NaOEr具有超长疏水链, 水溶性较差, 在50°C不溶, 不能形成稳定均相的KCl-NaOEr胶束溶液.可采用季铵盐来提高阴离子表面活性剂的溶解性,32加入少量TBAB便能有效改善NaOEr的溶解性, 加入14 mmolL–1TBAB时50 mmolL–1NaOEr样品在50 °C下呈均相澄清状态. 以“14 mmolL–1TBAB + 50 mmolL–1NaOEr”为对照样, 考察加入KCl对样品稳态流变的影响, 结果如图5a所示. 未加入KCl时“14 mmolL–1TBAB + 50 mmolL–1NaOEr”样品的粘度与水的粘度接近, 可见TBAB仅起到促进NaOEr溶解的作用, 不会对胶束形态有明显影响. 随着KCl的加入样品的稳态流变持续升高, 浓度为50 mmolL–1时稳态流变达到最大, 平台处粘度值达到104mPas. 解决了溶解问题后, NaOEr体系与NaOA体系一样, 在KCl的静电屏蔽作用诱导下形成了蠕虫状胶束. 然而, 在相同的温度下NaOA体系最大粘度出现在250 mmolL–1NaOA处, 仅为103mPas, 所需KCl浓度为750 mmolL–1. 显然,NaOEr体系需要的表面活性剂和盐浓度都远远偏低于NaOA体系, 表现出形成胶束的高效率, 这表明表面活性剂链长增加是促进分子缔合和胶束增长的主要因素.
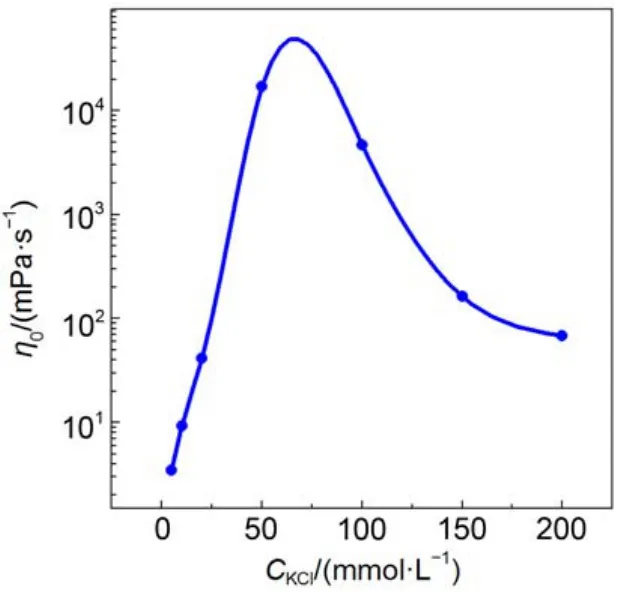
图6 KCl浓度变化对“50 mmolL–1NaOEr + 14 mmolL–1TBAB”体系η0的影响Fig.6 Effect of KCl concentration on η0of “50 mmolL–1NaOEr + 14 mmolL–1TBAB” solution
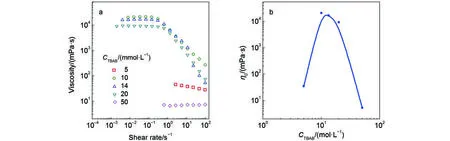
图7 TBAB浓度变化对“50 mmolL–1NaOEr + 50 mmolL–1KCl”溶液稳态流变的影响Fig.7 Effect of TBAB concentration on the steady rheology of the “50 mmolL–1NaOEr + 50 mmolL–1KCl” solution
以上研究表明, 两种盐浓度变化时η0随盐浓度(CS)变化趋势是一致的, 盐浓度增加都能促进体系粘度增加, 引起“盐浓度效应”. 此外, 不管是KCl还是TBAB, 两种混合体系达到最大粘度所需的总盐浓度接近, 比值CS/CD均略大约1, 所达到的粘度最大值非常接近. 因此, 在相同的表面活性剂浓度下, 给予充分的电解质诱导, 胶束所能达到的缠绕结构应该是类似的.
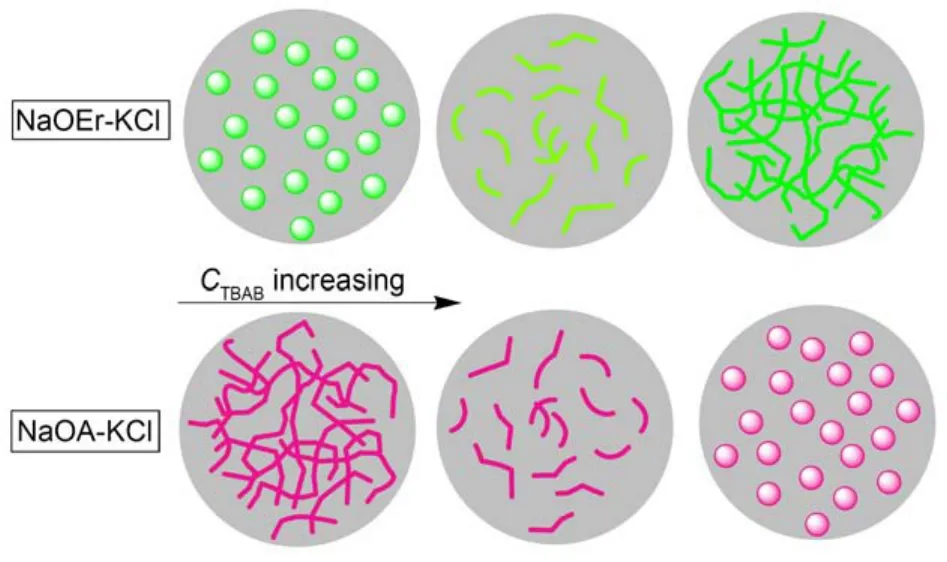
图8 加入TBAB分别对NaOA-KCl和NaOEr-KCl胶束形态的影响示意图Fig.8 Influence of adding TBAB on the morphology of micelles constructed by NaOA-KCl and NaOEr-KCl
TBAB的加入引起NaOA-KCl体系的粘度急剧下降, 却使NaOEr-KCl溶液的粘度大幅度增加. 粘度变化规律的不同反应出胶束形态的差异, TBAB对两种体系胶束形态的影响示意图如图8所示. TBA+的四个疏水支链由于空间位阻作用只能有一个或者两个插入胶束内部, 其余的支链留在胶束表面, TBA+带来的隔离位阻影响NaOA分子之间的疏水缔合作用, 从而不利于胶束增长. 从堆积参数角度解释, 引入TBA+相当于增加了表面活性剂头基横截面积, 从而不利于蠕虫状胶束形成. 与NaOA相比, NaOEr分子间的疏水缔合作用增强, 表面活性剂分子的紧密排列使TBA+的空间位阻影响被削弱, 反而使TBA+疏水缔合作用得以发挥. 表面活性剂链长是导致两个体系流变性差异的关键因素, NaOEr的链长增加引起疏水缔合作用增强, 宏观上引起两种溶液流变性能的巨大差异.
4 结 论
TBAB/KCl对NaOEr和NaOA构筑蠕虫状胶束产生不同的影响. 由于位阻效应, TBAB不能诱导NaOA形成蠕虫状胶束, 还会破坏NaOA-KCl体系形成的蠕虫状胶束. 由于NaOEr具有超强疏水缔合作用, 不仅减弱了TBAB位阻效应的影响, 还使TBAB的疏水缔合作用得到充分发挥, 利用其疏水作用与KCl协同诱导NaOEr构筑了具有强粘弹性的蠕虫状胶束. 结果证实, 具有位阻效应的对称型季铵盐TBAB同样能诱导阴离子表面活性剂形成蠕虫状胶束, 这种季铵盐可以与超长链阴离子表面活性剂协同作用.
(1)Khatory, A.; Kern, F.; Lequeux, F.; Appel1, J.; Porte, J. G.; Morie, N.; Ott, A.; Urbach, W. Langmuir 1993, 9, 933. doi: 10.1021/la00028a010
(2)Bharti, B.; Xue, M.; Meissner, J.; Cristiglio, V.; Findenegg, G. H. J. Am. Chem. Soc. 2012, 134, 14756. doi: 10.1021/ja307534y
(3)Morita, C.; Imura, Y.; Ogawa, T.; Kurata, H.; Kawai, T. Langmuir 2013, 29, 5450. doi: 10.1021/la400604m
(4)Pei, X. M.; Zhao, J. X.; Wei, X. L. Acta Phys. -Chim. Sin. 2011, 27, 913. [裴晓梅, 赵剑曦, 魏西莲. 物理化学学报, 2011, 27, 913.] doi: 10.3866/PKU.WHXB20110420
(5)Dreiss, C. A. Soft Matter 2007, 3, 956. doi: 10.1039/b705775j
(6)Cates, M. E.; Candau, S. J. J. Phys.: Condens. Matter 1990, 2, 6869. doi: 10.1088/0953-8984/2/33/001
(7)Mohsenipour, A. A.; Pal, R. Ind. Eng. Chem. Res. 2013, 52, 1291. doi: 10.1021/ie3024214
(8)Yang, J. Curr. Opin. Colloid Interface Sci. 2002, 7, 276. doi: 10.1016/S1359-0294(02)00071-7
(9)Wilmsmeyer, K. G.; Zhang, X.; Madsen, L. A. Soft Matter 2012, 8, 57. doi: 10.1039/C1SM06634J
(10)Oelschlaeger, C.; Suwita, P.; Willenbacher, N. Langmuir 2010, 26, 7045. doi: 10.1021/la9043705
(11)Yusof, N. S. M.; Khan, M. N. J. Phys. Chem. B 2012, 116, 2065. doi: 10.1021/jp210467p
(12)Yusof, N. S. M.; Khan, M. N.; Ashokkumar, M. J. Phys. Chem. C 2012, 116, 15019. doi: 10.1021/jp304854h
(13)Kalur, G. C.; Raghavan, S. R. J. Phys. Chem. B 2005, 109, 8599. doi: 10.1021/jp044102d
(14)Maitland, G. C. Curr. Opin. Colloid Interface Sci. 2000, 5, 301. doi: 10.1016/S1359-0294(00)00069-8
(15)Israelachvili, J. N.; Mitchell, D. J.; Ninham, B. W. J. Chem. Soc. Faraday Trans. 2 1976, 72, 1525. doi: 10.1039/f29767201525
(16)Couillet, I.; Hughes, T.; Maitland, G.; Candau, F.; Candau, S. J. Langmuir 2004, 20, 9541. doi: 10.1021/la049046m
(17)Molchanov, V. S.; Shashkina, Y. A.; Philippova, O. E.; Khokhlov, A. R. Colloid J. 2005, 67, 606. doi: 10.1007/s10595-005-0139-8
(18)Parker, A.; Fieber, W. Soft Matter 2013, 9, 1203. doi: 10.1039/C2SM27078A
(19)Han, Y.; Wei, Y.; Wang, H.; Mei, Y.; Zhou, H. J. Surfact Deterg. 2013, 16, 139. doi: 10.1007/s11743-012-1364-x
(20)Zhao, J. X.; Yang, D. P. Acta Phys. -Chim. Sin. 2012, 28, 1218. [赵剑曦, 杨铎平. 物理化学学报, 2012, 28, 1218.] doi: 10.3866/PKU.WHXB201202211
(21)Kumar, S.; Bhadoria, A. J. Chem. Eng. Data 2012, 57, 521.doi: 10.1021/je200909j
(22)Bales, B. L.; Tiguida, K.; Zana, R. J. Phys. Chem. B 2004, 108, 14948. doi: 10.1021/jp040289x
(23)Han, Y.; Feng, Y.; Sun, H.; Li, Z.; Han, Y.; Wang, H. J. Phys. Chem. B 2011, 115, 6893. doi: 10.1021/jp2004634
(24)Nakamura, K.; Shikata, T. Langmuir 2006, 22, 9853. doi: 10.1021/la061031w
(25)Zana, R.; Benrraou, M.; Bales, B. L. J. Phys. Chem. B 2004, 108, 18195. doi: 10.1021/jp040507m
(26)Benrraou, M.; Bales, B. L.; Zana, R. J. Phys. Chem. B 2003, 107, 13432. doi: 10.1021/jp021714u
(27)Han, Y.; Chu, Z.; Sun, H.; Li, Z.; Feng, Y. RSC Adv. 2012, 2, 3396. doi: 10.1039/c2ra20136d
(28)de Mul, M. N. G.; Davis, H. T.; Evans, D. F.; Bhave, A. V.; Wagner, J. R. Langmuir 2000, 16, 8276. doi: 10.1021/la000467n
(29)Zhang, Y.; Han, Y.; Chu, Z.; He, S.; Zhang, J.; Feng, Y. J. Colloid Interface Sci. 2013, 394, 319. doi: 10.1016/j. jcis.2012.11.032
(30)Berret, J. F.; Appell, J.; Porte, G. Langmuir 1993, 9, 2851. doi: 10.1021/la00035a021
(31)Candau, S. J.; Hirsch, E.; Zana, R.; Delsanti, M. Langmuir 1989, 5, 1225. doi: 10.1021/la00089a018
(32)Lin, B.; McCormick, A. V.; Davis, H. T.; Strey, R. J. Colloid Interface Sci. 2005, 291, 543. doi: 10.1016/j.jcis.2005.05.036
(33)Chu, Z.; Feng, Y. Chem. Commun. 2010, 46, 9028. doi: 10.1039/c0cc02415e
(34)Kalur, G. C.; Frounfelker, B. D.; Cipriano, B. H.; Norman, A. I.; Raghavan, S. R. Langmuir 2005, 21, 10998. doi: 10.1021/la052069w
(35)Mackintosh, F. C.; Safran, S. A.; Pincus, P. A. Europhys. Lett. 1990, 12, 697. doi: 10.1209/0295-5075/12/8/005
(36)Kusano, T.; Iwase, H.; Yoshimura, T.; Shibayama, M. Langmuir 2012, 28, 16798. doi: 10.1021/la304275h
Effect of TBAB/KCl on Constructing Anionic Wormlike Micelles
HAN Yi-Xiu ZHOU Hong WEI Yong-Qiang MEI Yong-Jun*WANG Hang
(The Second Research Institute of Civil Aviation Administration of China, Chengdu 610041, P. R. China)
Using rheological measurements, we investigated the wormlike micelles formed by anionic surfactants, sodium oleate (NaOA), and sodium erucate (NaOEr) in the presence of KCl and tetrabutyl ammonium bromide (TBAB). The viscosity of the NaOA solution increased with KCl concentration, but adding TBAB decreased viscosity. In contrast, the apparent viscosity of NaOEr-KCl solution enhances with increasing TBAB concentration. In addition, NaOEr is better than NaOA at encouraging the construction of viscoelastic wormlike micelles, needing less surfactant and a lower salt concentration. We prepared a wormlike micelle system with strong viscoelasticity by using NaOEr, cooperatively induced by KCl and TBAB. Based on these studies, we discussed the complex influence of TBA+on constructing wormlike micelles.
Anionic surfactant; Sodium erucate; Tetrabutyl ammonium bromide; Wormlike micelles; Rheology
O648
10.3866/PKU.WHXB201509112
Received: June 17, 2015; Revised: September 11, 2015; Published on Web: September 11, 2015.
*Corresponding author. Email: yongjun.mei@outlook.com; Tel: +86-28-82909883.
The project was supported by the National Natural Science Foundation of China and Civil Aviation Administration of China (U1233122).
国家自然科学基金-民航联合研究基金(U1233122)资助项目
©Editorial office of Acta Physico-Chimica Sinica
