地下水中溶解性有机物的季节变化特征及成因
2015-11-18何小松席北斗高如泰中国环境科学研究院环境基准与风险评估国家重点实验室北京100012中国环境科学研究院地下水与环境系统创新基地北京100012重庆市市政环卫监测中心技术服务科重庆401121
何小松,席北斗,张 鹏,高如泰,李 丹,张 慧(1.中国环境科学研究院,环境基准与风险评估国家重点实验室,北京 100012;2.中国环境科学研究院,地下水与环境系统创新基地,北京 100012;3.重庆市市政环卫监测中心技术服务科,重庆 401121)
地下水中溶解性有机物的季节变化特征及成因
何小松1,2,席北斗1,2,张 鹏3*,高如泰1,2,李 丹1,2,张 慧1,2(1.中国环境科学研究院,环境基准与风险评估国家重点实验室,北京 100012;2.中国环境科学研究院,地下水与环境系统创新基地,北京 100012;3.重庆市市政环卫监测中心技术服务科,重庆 401121)
为阐明地下水中溶解性有机物(DOM)的分布特征与环境效应,联合三维荧光光谱、平行因子分析及主成分分析,研究了地下水中DOM的来源及随季节和空间变化特征,探究了地下水DOM组成对无机盐分布的影响.结果显示,地下水DOM主要来自微生物源,可鉴别出4种荧光组分,4种组分中,组分1和3为类蛋白组分,组分2和4属于类腐殖质组分.类蛋白组分来源差异较大,组成不稳定,其含量随季节变化明显,春冬季含量低而夏秋季含量高;类腐殖质组分来源相似,组成稳定,随季节变化小.两类荧光组分,尤其是类蛋白组分,是地下水氨氮的主要来源,可以影响地下水pH值.结果表明,三维荧光光谱结合平行因子和主成分分析,可以解析地下水中有机物的组成特征和季节变化规律.
三维荧光光谱;平行因子分析;地下水;溶解性有机物
地下水中有机物含量一般较低,常规技术如BOD5、CODcr检测困难[1].现代光谱技术,如荧光光谱、紫外光谱,可以在有机物浓度极低的情况下无损地分析地下水有机物组成和结构[2].Baker等[2]采用三维荧光光谱,分析了受渗滤液污染地下水有机物的组成特征,发现地下水中有机物的荧光强度与氨氮浓度显著相关;Lapworth等[3]通过地下水溶解性有机物(DOM)三维荧光光谱的研究,指出当地下水有机物来源变化时,其中类色氨酸/类富里酸荧光强度比会发生改变.Stedmon等[4]采用三维荧光光谱和平行因子分析对地下水有机物的组成进行了研究,发现地下水中类腐殖质组分荧光强度稳定,不受外源生活污水注入的影响.
地下水中有机物的组成会随着地下水的流动和季节演替而改变,但是,目前关于空间和季节变化对地下水中有机物组成的影响却鲜有报道.另外,地下水有机物的组成可能会影响无机盐和重金属的浓度和分布状况,因此,当季节变化时,地下水中无机盐等污染物的组成可能也发生改变.基于此,本研究拟选择典型的水文地质单元,基于三维荧光光谱和紫外光谱,结合平行因子分析和主成分分析,建立一种新的有机物荧光信息提取技术,研究地下水中有机物的来源及时空变化特征,揭示地下水有机物组成对其他污染物分布的影响,以其为地下水污染监测和快速诊断提供科学依据.
1 材料与方法
1.1 样品采集

图1 地下水采样点示意及水位等值线Fig.1 The map of the sampling site and water level contour
样品采集于山东寿光市,该市为我国著名的蔬菜之乡,区内主要为大棚种植蔬菜,冬春季种植,6~7月空闲.图1为采样点示意和2012年5月地下水水位等值线,所选研究区中间为居民区,四周为蔬菜大棚,共设置12个地下水采样点,依次标记为S1~S12,每个采样点均有一口农民灌溉用的机井.该地地下水埋深在33~36m间,地下水流向为西南流向东北,于2012年1月、5月、8月及12月,通过机井抽取地下水,将抽取得到的地下水放入加有冰块的采样箱中,24h内运回实验室.
1.2 水质分析
将所采集样品过0.45μm孔径的醋酸纤维素滤膜后,进行常规水质分析.溶解性有机碳(DOC)含量采用总有机碳分析仪 (multi N /C-2100TOC, Analytik Jena GER) 测定采用纳式试剂法进行测定、、Cl-及采用离子色谱仪(ICS-2000, Dionex USA)测定,pH值采用TOLEDO 320Meter测定,电导率(EC)采用METTLER TOLEDO SG3型电导率仪测定.
1.3 光谱扫描
采用优尼科公司生产的4802-UV/Vis型紫外分光光度计,测定样品在254nm下的吸光度,计算地下水样品在254nm下的吸光系数[5].计算公式如下:
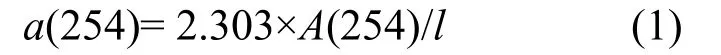
式中:a(254)是254nm处的吸收系数, m-1; A(254)为254nm下的吸光度;l为光程路径, m.
荧光光谱测定仪器为日立公司生产的Hitachi F-7000型荧光光度计,固定激发波长为370nm,激发和发射狭缝宽度5nm,速度240nm/min,扫描发射光谱,计算发射光谱中450nm与500nm处荧光强度的比值,记为f450/500.
三维荧光光谱测定时固定激发和发射波长狭缝宽度均为5nm,激发波长范围设为200~400nm,发射波长范围设为280~500nm,激发和发射光谱增量5nm,扫描速度2400nm/min,然后进行三维荧光光谱扫描,以超纯水在上述条件下扫描所得光谱为空白对照,将所有地下水样品扣除空白后,数据导出至Excel表格进行平行因子分析.
1.4 数据分析
将48个三维荧光数据导出后,采用Bahram等报道的方法去除一次和二次瑞利散射[6],然后在Matlab 7.0b (Mathworks, Natick, MA) 上采用DOMFluor toolbox 软件包进行平行因子分析.通过核一致性分析和对半检验确定荧光组分数,以及每个样品在对应组分的浓度得分值Fmax.
主成分分析和聚类分析在SPSS 16.0进行.相关性分析在SPSS16.0和Excel 2003上进行.图形处理在Origin 8.0 和Matlab 7.0b上进行.
表1是1981—2017年柑橘产量与年平均气温、日平均气温稳定通过0℃积温、日平均气温稳定通过10℃积温、年降水量、降水量天数、年日照时数的相关系数。
2 结果与讨论
2.1 地下水中有机物组成与来源分析
地下水在254nm下的吸收系数a(254)与其苯环化合物的含量有关[5,7].2012年1月12口水井中有机物的a(254)平均值为17.73/m,随后剧烈下降, 5月为3.62/m,8月为3.92/m,但在12月份,地下水有机物的a(254)又增至6.76/m,上述结果显示地下水中苯环化合物的含量较高,可以采用荧光光谱深入分析其组成和结构特性.f450/500与有机物的组成有关,前人的研究显示,陆源有机物的f450/500在1.4左右,而微生物源有机物其值在1.9左右[7].表1显示,春季(1月份)地下水有机物f450/500为1.95,显示其主要来自微生物来源,在夏季和秋季(5月和8月)其微生物源进一步增强,但到冬季(12月)时f450/500为1.77,显示这一时期地下水微生物活动变弱,陆源有机物的相对浓度增加.相对于陆源有机物而言,微生物来源的有机物结构简单,腐殖质化率低,易被微生物利用,这就导致了a(254)在夏秋季节低,而春冬季高.

表1 2012年不同季节地下水有机物基本理化特性Table 1 Basic physicochemical properties of groundwater-derived organic matter at different time
3.2 地下水中有机物的种类组成特征
有机物组成可以反映地下水污染现状和趋势.采用三维荧光光谱,结合平行因子分析法,对四个季节所采集的48个地下水有机物样品的三维荧光光谱进行分析,鉴定出4个荧光组分(图2).4个组分中,组分1有两个荧光峰,对应两个激发波长和一个发射波长,一个激发波长小于240nm,另一个在275nm附近,发射波长均为330nm,根据前人的报道可知[1,9],该组分为与微生物活动有关的类色氨酸组分.组分2有3个荧光峰,其激发波长依次为245、285及315nm,发射波长均为395nm,该组分为陆源腐殖质组分[10].组分3激发/发射波长为<240, 275/350nm,也是与微生物活动有关的类色氨酸组分[11-12].组分4的激发/发射波长为260, 370/450nm,来源于陆源腐殖质物质[13-16].因此,地下水荧光有机物主要为两类物质,一类为类蛋白质物质,包括组分1和3,另一类为类腐殖质物质,包括组分2和4.
2.3 地下水中有机物浓度分布特征
将平行因子分析所得4个荧光组分的浓度得分值Fmax在Matlab上绘图,得各荧光组分在不同采样点、不同季节的浓度分布图.图3显示,对大部分采样点,组分1的Fmax值在4个组分中最高,但地下水水质浓度在不同采样点差异较大,其Fmax值大小不同:春季S3和S7两点浓度最高,夏季除S2、S3、S4、S5及S12外,其他采样点组分1的含量均很高,秋季组分1含量普遍下降,但采样点S5和S12的组分1浓度却升高了.该地区地下水为西南流向东北,因此,这两点组分1浓度的上升可能与地下水的流动有关.冬季该地下水中组分1的浓度进一步下降.除了采样点S5、S6及S7外,组分2一年4季在地下水中的浓度变化不大.采样点S5、S6及S7中,S6点组分2的浓度一直很高,而S5在夏季浓度高而其他季节浓度较低,采样点S7组分2最大浓度值出现在冬季.生物源类色氨酸组分3在春季含量也很低,但夏季除采样点S1~S4外,其余采样点浓度均显著升高,S5和S7在秋季达到浓度最大,上述结果可能与地下水的流向有关,但冬季地下水中组分3浓度又开始下降.除采样点S5、S6外,陆源腐殖质组分4随季节变化不大.采样点S6的组分4从春季到冬季浓度呈增加的趋势,显示S6点可能有陆源腐殖质组分输入.S5点在秋季强度达到最大,这可能与地下水的流动有关.总体而言,大部分采样点类蛋白物质组分的含量随季节变化较大,而类腐殖质物质浓度随季节变化很小,组成相对稳定.
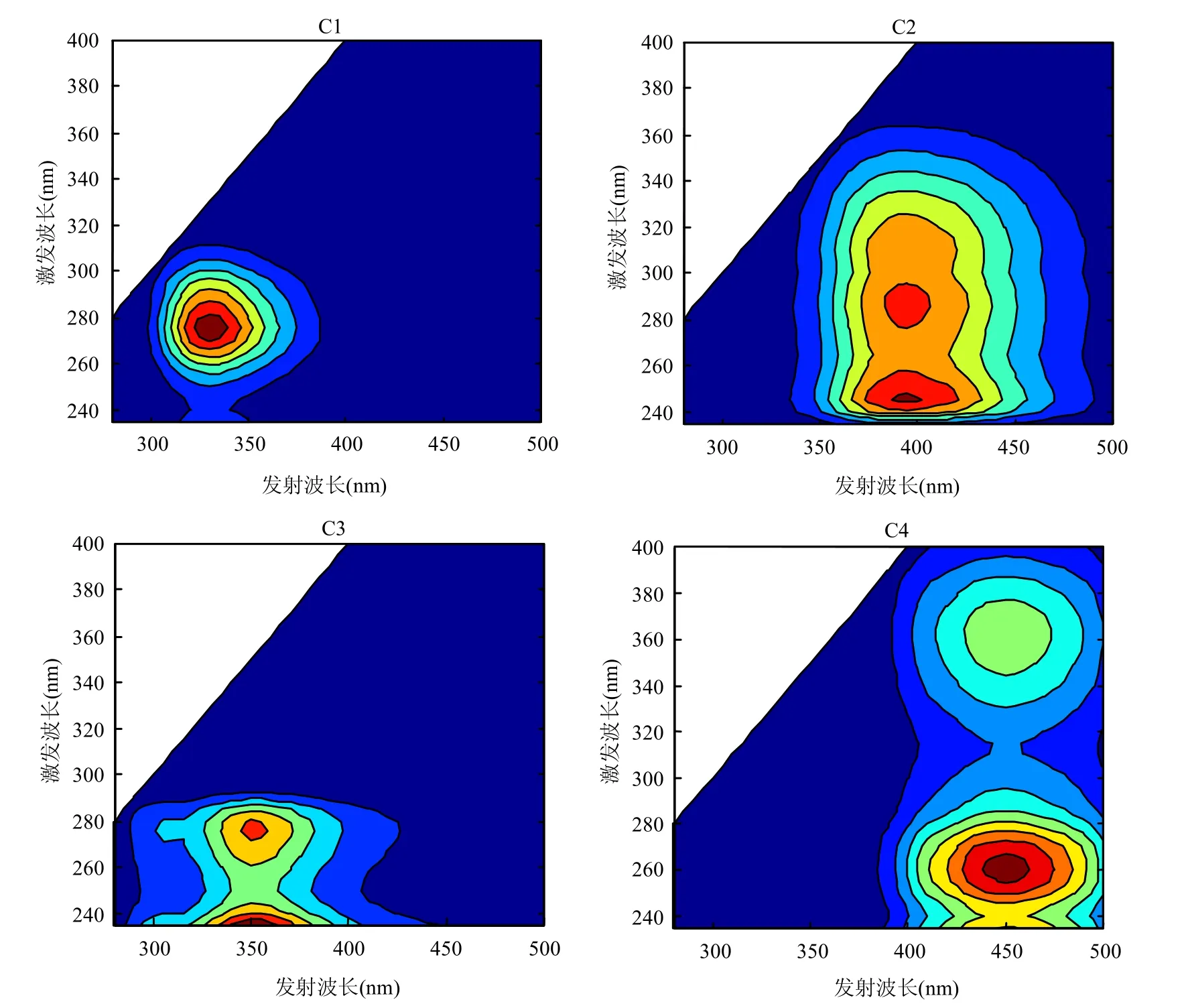
图2 地下水有机物经平行因子分析法鉴定出的4个荧光组分Fig.2 Four fluorescence components identified by PARAFAC analysis in groundwater-derived organic matter
2.4 地下水中有机物的季节分布特征
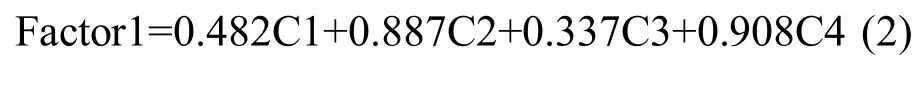
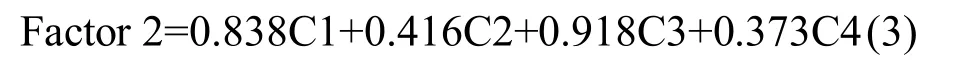
从式(2)可见,因子1中类腐殖质组分2和4的系数(0.887和0.908)远高于类蛋白组分的系数(0.482和0.337),结合图4a,可以发现因子1主要由类腐殖质荧光组分2和4决定.式(3)显示,因子2中类蛋白组分1和3的系数(0.838和0.918)远高于类腐殖质组分2和4的系数(0.416和0.373),结合图4a分析,可以发现因子2主要由类蛋白组分1和3决定.因此,因子1主要代表类腐殖质物质,而因子2主要代表类蛋白物质.所有48个样品在因子1和2上的得分如图4b所示.春季时,所有样品的因子1和2得分聚集在一起,均聚集在因子1和2载荷的负方向.在夏季时,12个样品的浓度得分很分散,且因子2得分值增加,显示夏季地下水DOM中类蛋白组分的含量增加,与夏季样品相比,秋季的不同样品的得分分布离散度进一步增大,部分样品的因子1得分进一步增强,显示秋季DOM中类蛋白组分含量进一步增高,到冬季后,大部分样品的因子1得分下降了,显示冬季微生物活动减弱,地下水中类蛋白组分含量下降.在类腐殖质物质方面,夏季样品S1和S6因子1得分都很高,显示这两个样品类腐殖质组分含量高,这与图3所示结果一致,而秋季样品中S5因子1和2得分都很高,这一样品类腐殖质和类蛋白物质含量都很高,冬季样品中,S6、S7及S12的因子1得分都很高,显示这一时期类腐殖质组分含量高,这与图3分布一致.上述结果表明,平行因子分析法结合主成分分析,可以有效解释地下水中荧光有机物的季节变化特征和规律.

图3 2012年不同季节4个荧光组分的Fmax分布Fig.3 Fmax distribution of four fluorescence components in different seasons
2.5 地下水中荧光有机物空间分布特征及与地下水流向的关系
将不同样品4个时期地下水平行因子组分得分Fmax进行聚类分析,图5显示,当欧几里德距离小于5时,这一聚类结果与图1中地下水采样点的分布一致,即地理位置上相近的采样点首先聚为一类,再和远处采样点聚为一类;此外,这一聚类分析结果还与地下水流向一致,即上游采样点首先聚为一类,然后和中游地下水采样点聚为一类,最后和下游地下水采样点聚为一类.这表明,采用三维荧光光谱,联合平行因子分析和聚类分析,可以确定地下水不同采样点DOM水平分布特征以及地下水的流向.
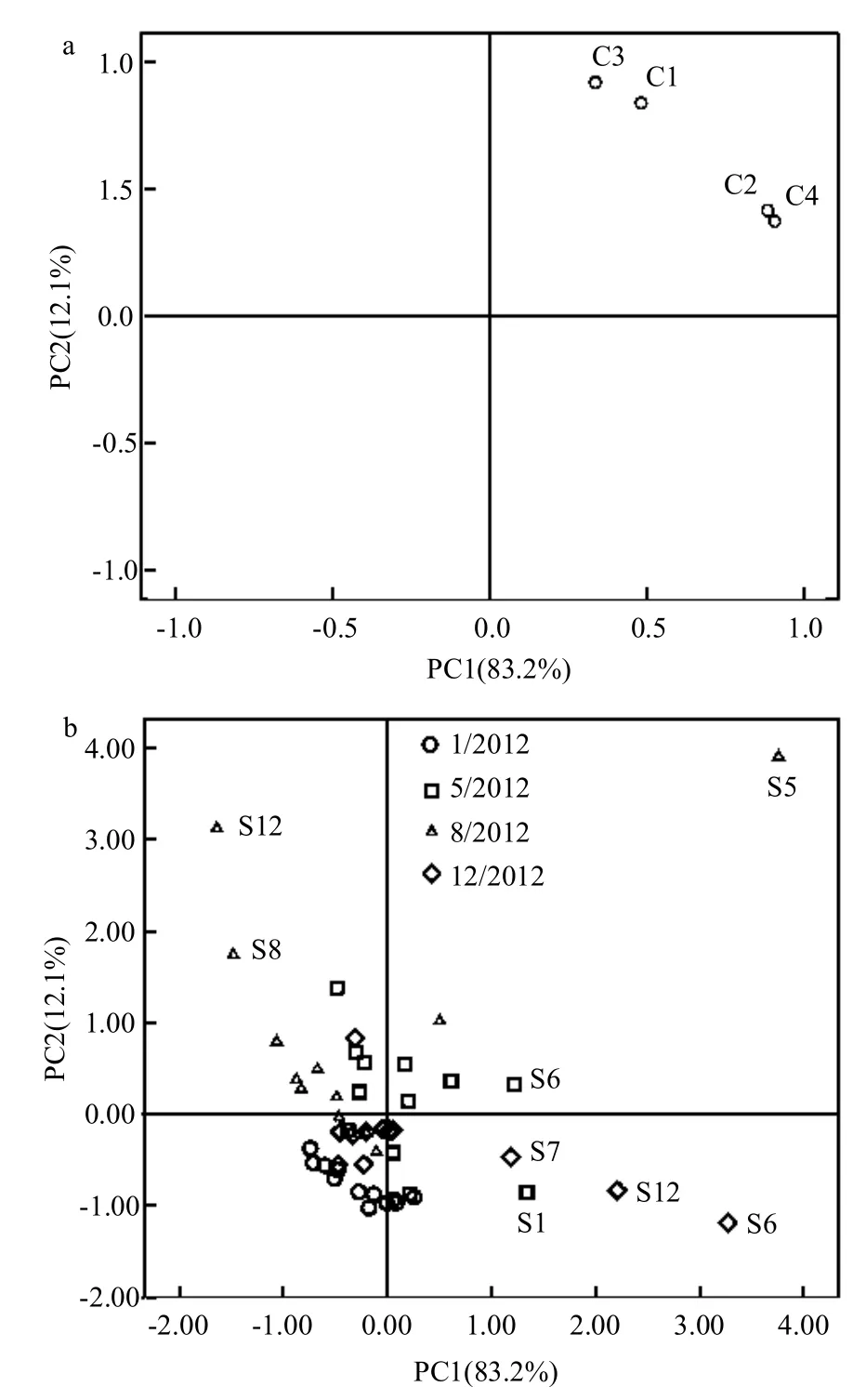
图4 地下水中有机物变化的EEM-PARAFAC-PCA分析Fig.4 EEM-PARAFAC-PCA analysis of the variety of groundwater-derived organic matter
2.6 地下水荧光有机物的环境影响分析
地下水是个复杂的体系,除了含有有机物外,还含有无机盐和重金属,地下水有机物的组成和转化特征可能对无机盐等的组成和地下水其他理化特性具有重要影响.对地下水中不同理化指标进行相关性分析显示(表2),地下水中DOC浓度与氨氮、腐殖质组分2达到显著相关(P<0.05),与腐殖质组分4不相关,而DOC与类蛋白组分1和3均达到极显著正相关(P<0.01),此外,表2还显示,氨氮与荧光组分1、2、3及4均达到极显著正相关.上述结果表明,地下水DOC主要为类蛋白类物质,这些类蛋白物质与氨氮紧密相关,可能是氨氮的重要产生源.此外,表2还显示,地下水中硝氮、亚硝氮、氯离子及硫酸根离子的浓度两两间显著相关(P<0.05)或极显著相关(P<0.01),显示这四种阴离子具有相同的来源和迁移特性.地下水pH值与氨氮浓度达到显著相关,与类腐殖质组分2和4也达到显著相关(P<0.05),与类蛋白组分1和3达到极显著相关(P<0.01),显示地下水中pH主要受氨氮浓度,尤其受类蛋白物质含量的影响,类蛋白物质含量增加会导致氨氮含量增加引起pH值上升.地下水EC与DOC、氨氮显著负相关(P<0.05),与硝氮、亚硝氮、氯离子和硫酸根离子显著正相关(P<0.01),显示地下水中的电导率主要受无极阴离子的影响.地下水中a(254)与氨氮浓度达到极显著负相关(P<0.01),而与硝酸盐氮、亚硝酸盐氮和电导率达到极显著正相关(P<0.01),显示地下水荧光有机物的降解导致氨氮的增加,地下水荧光有机物含量越高,硝酸盐、亚硝酸盐及电导率越高.
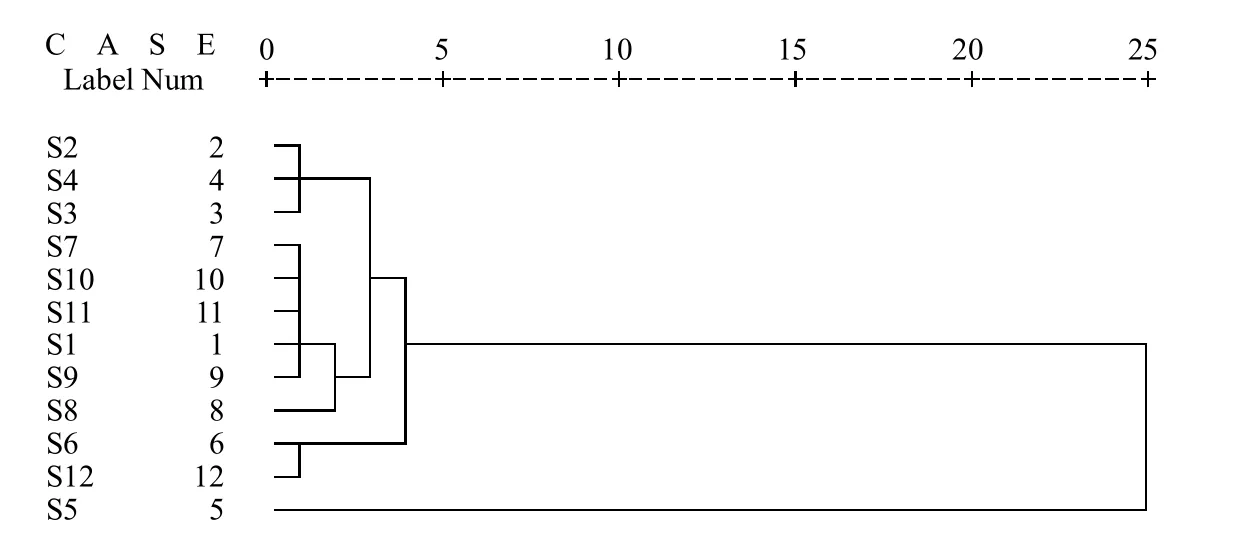
图5 四个季节不同点平行因子得分的聚类分析结果Fig.5 Results obtained from the cluster analysis of the PARAFAC scores of DOM with four seasons
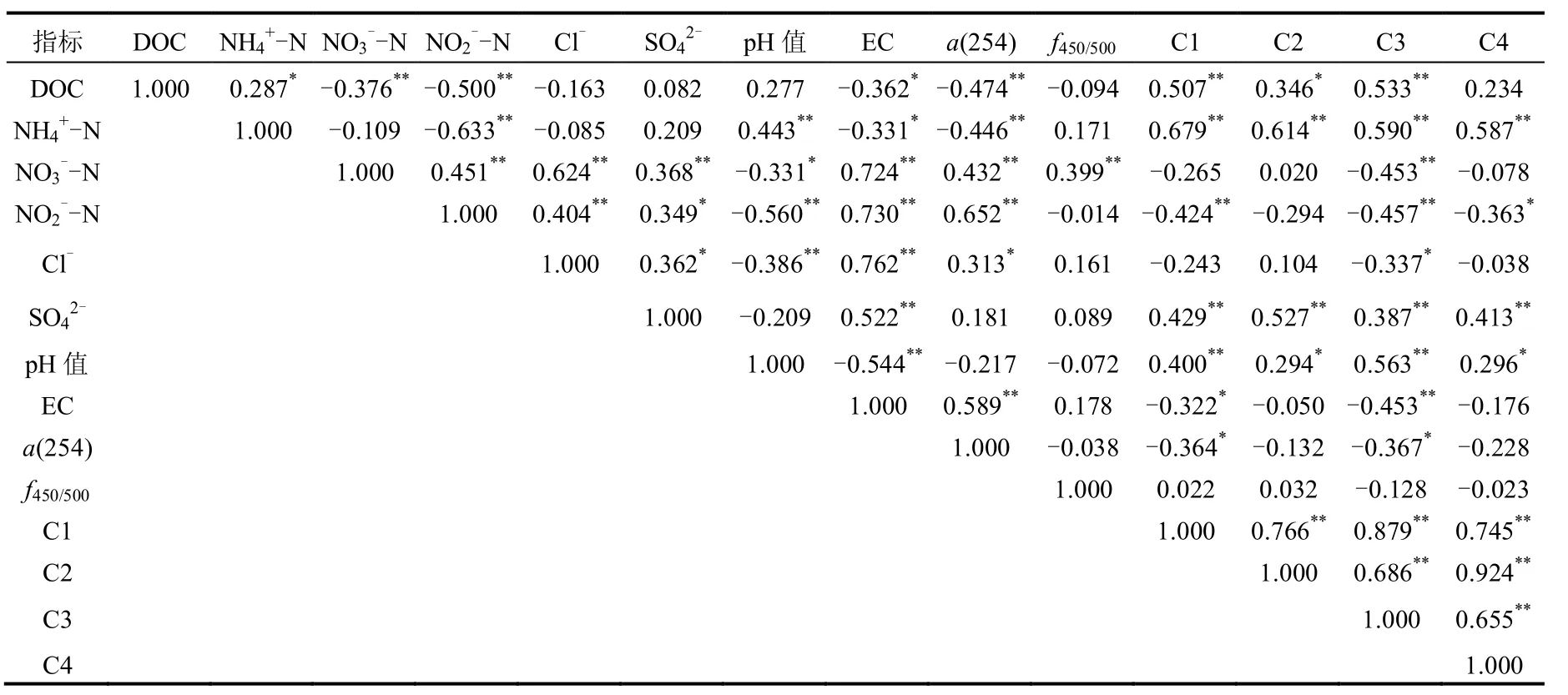
表2 不同指标相关性分析Table 2 Results from correlation analysis of the different parameters


图7 2012年地下水中不同荧光组分Fmax的相关性分析Fig.7 Correlation analysis of the Fmax values of protein-like components or humic-like components
地下水中4个荧光组分浓度两两间均达到极显著相关(P<0.01),表明地下水中4种荧光有机物均有类似的来源.然而,进一步分析发现,在一年四季中,除了秋季类蛋白物质与类腐殖质物质达到显著相关外,其他季节均未达到显著相关,显示类腐殖质和类蛋白物质虽然有类似的来源,但还存在一些微小的差异.表2和图7显示,尽管类蛋白组分1和3,类腐殖质组分2和4有相同的来源,但是其来源在不同季节还是有变化的,变化最大的是类蛋白组分, 其含量除了秋季达到相关外,其他季节均未达到显著相关.类腐殖质组分来源相对稳定,除了夏季外,其他3个季节类腐殖质组分2和4含量均达到极显著正相关,显示类腐殖质组分2和4来源相似性高,影响因素相同.在夏季,不同组分相关性很差,可能与夏季温度高,微生物活动旺盛,不同组分的降解和合成差别较大有关.
3 结论
3.1 地下水有机物主要为微生物来源,在夏季和秋季其微生物来源增强,而在冬季微生物来源减弱.
3.2 地下水中类腐殖质物质来源相似,组成稳定,随季节变化小,而类蛋白物质组分来源差异较大,组成不稳定,随季节变化明显,春冬季含量低而夏秋季含量高.
3.3 采用三维荧光光谱,结合平行因子和主成分分析,可以解析地下水中有机物的季节分布特征和变化规律;采用三维荧光光谱,结合平行因子分析和聚类分析,可以揭示地下水不同采样点的空间分布特征,确定地下水流向.
3.4 地下水中的荧光有机物,尤其是类蛋白有机物,是地下水氨氮的主要来源,可以影响地下水pH值.
[1]Lu J, Chang A C, Wu L. Distinguishing sources of groundwater nitrate by1H-NMR of dissolved organic matter [J]. Environmental Pollution, 2004,132(2):365-374.
[2]Baker A, Curry M. Fluorescence of leachates from three contrasting landfills [J]. Water Research, 2004,38(10):2605-2613.
[3]Lapworth D J, Gooddy D C, Butcher A S, et al. Tracing groundwater flow and sources of organic carbon in sandstone aquifers using fluorescence properties of dissolved organic matter(DOM) [J]. Applied Geochemistry, 2008,23(12):3384-3390.
[4]Stedmon C A, Seredynska-Sobecka B, Boe-Hansen R, et al. A potential approach for monitoring drinking water quality from groundwater systems using organic matter fluorescence as an early warning for contamination events [J]. Water Research, 2011,45(18):6030-6038.
[5]崔东宇,何小松,席北斗,等.牛粪堆肥过程中水溶性有机物演化的光谱学研究 [J]. 中国环境科学, 2014,34(11):2897-2904.
[6]Bahram M, Bro R, Stedmon C, et al. Handling of Rayleigh and Raman scatter for PARAFAC modeling of fluorescence data using interpolation [J]. Journal of Chemomtrics, 2006,20(3/4):99-105.
[7]Chen M, Maie N, Parish K, et al. Spatial and temporal variability of dissolved organic matter quantity and composition in an logographic subtropical coastal wetland [J]. Biogeochemistry,2013,115(1-3):167-183.
[8]McKnight D M, Boyer E W, Westerhoff P K, et al. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity [J].Limnology and Oceanography, 2001,46(1):38-48.
[9]He X S, Xi B D, Wei Z M, et al. Fluorescence excitationemission matrix spectroscopy with regional integration analysis for characterizing composition and transformation of dissolved organic matter in landfill leachates [J]. Journal of Hazardous Materials, 2011,190(1-3):293-299.
[10]Yao X, Zhang Y, Zhu G, et al. Resolving the variability of CDOM fluorescence to differentiate the sources and fate of DOM in Lake Taihu and its tributaries [J]. Chemosphere, 2011,82(2):145-155.
[11]Coble P G. Characterization of marine and terrestrial DOM in seawater using excitation emission matrix spectroscopy [J]. Marine Chemistry, 1996,51(4):325-346.
[12]He X S, Xi B D, Li X, et al. Fluorescence excitation-emission matrix spectra coupled with parallel factor and regional integration analysis to characterize organic matter humification[J]. Chemosphere, 2014,93(9):2208-2215.
[13]Murphy K R, Stedmon C A, Waite T D, et al. Distinguishing between terrestrial and autochthonous organic matter sources in marine environments using fluorescence spectroscopy [J]. Marine Chemistry, 2008,108(1):40-58.
[14]Yamashita Y, Jaffe R. Characterizing the interactions between trace metals and dissolved organic matter using excitationemission matrix and parallel factor analysis [J]. Environmental Science and Technology, 2008,42(19):7374-7379.
[15]Williams C J, Yamashita Y, Wilson H F. Unraveling the role of land use and microbial activity in shaping dissolved organic matter characteristics in stream ecosystems [J]. Limnology and Oceanography, 2010,55(3):1159-1171.
[16]甘淑钗,吴 莹,鲍红艳,等.长江溶解有机质三维荧光光谱的平行因子分析 [J]. 中国环境科学, 2013,33(6):1045-1052.
致谢:本实验的现场采样工作由中国农业大学的许艇教授和毕经纬硕士协助完成,绘图过程得到了中国环境科学研究院潘红卫博士的帮助,在此表示感谢.
The seasonal distribution characteristics and its reasons of dissolved organic matter in groundwater.
HE Xiao-song1,2, XI Bei-dou1,2, ZHANG Peng3*, GAO Ru-tai1,2, LI Dan1,2, ZHANG Hui1,2(1.State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012,China;2.Innovation Base of Ground Water and Environmental System Engineering, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;3.Technical Services Section, Chongqing Municipal and Environmental Sanitation Monitoring Department, Chongqing 401121, China). China Environmental Science, 2014,35(3):862~870
To illuminate the distribution characteristics and environmental influences of dissolved organic matter (DOM)in groundwater, the source, spatial and temporal distribution characteristics of DOM were studied by fluorescence excitation-emission matrix spectra (EEM) combined with parallel factor (PARAFAC) analysis, and the influence of DOM on the distribution of inorganic salts was investigated as well. The results showed that the groundwater DOM was mainly microbial-derived. Four florescence components were identified by EEM spectra coupled with PARAFAC analysis, and components 1 and 3 originated from protein-like materials, while components 2 and 4 were ascribed to humic-like substances. The protein-like components had different sources and their composition was variable and changed with time,i.e., the concentration of them was higher in the summer and fall but lower in the winter and spring. On the other hand, the humic-like components had a similar source, and their composition was stable and showed no obvious change with season. The DOM, especially the protein-like components, was a source of ammonia nitrogen, and had an important influence on the groundwater pH value. The results demonstrated that, EEM spectra coupled with PARAFAC and principle component analysis can be used to analyze the composition and seasonal variation of the DOM in groundwater.
fluorescence excitation-emission matrix spectra (EEM);parallel factor (PARAFAC) analysis;groundwater;dissolved organic matter
X523
A
1000-6923(2015)03-0862-09
何小松(1982-),男,湖南道县人,助理研究员,主要从事固体废物处理处置与地下水污染监测研究.发表论文50篇.
2014-07-31
国家杰出青年基金(51325804);中国博士后科学基金(2012M520349);中央级公益性科研院所基本科研业务专项(2012GQ-14)
* 责任作者, 工程师, zp21@foxmail.com
