甘草属Glycyrrhiza L.植物资源化学及利用研究进展△
2015-09-25郑云枫魏娟花冷康陶伟伟方诗琦彭国平段金廒
郑云枫,魏娟花,冷康,陶伟伟,方诗琦,彭国平,段金廒 *
(1.南京中医药大学 药学院,江苏 南京 210023;2.江苏省中药资源产业化过程协同创新中心,江苏 南京 210023)
·综述·
甘草属Glycyrrhiza L.植物资源化学及利用研究进展△
郑云枫1,2,魏娟花1,冷康1,陶伟伟2,方诗琦1,彭国平1,2,段金廒1,2 *
(1.南京中医药大学 药学院,江苏 南京 210023;2.江苏省中药资源产业化过程协同创新中心,江苏 南京 210023)
甘草作为一种优良的天然植物资源,已被广泛应用于医药、食品、化工、畜牧等领域,国内外相关研究也方兴正艾,但近年来随着生态环境的破坏及无节制的采挖,资源状况日益严峻。本文从中药资源化学的角度出发,对甘草属植物的种类及资源分布进行总结,并针对不同品种甘草的活性成分、药理作用以及应用现状进行综述。旨在为进一步深入研究和开发该类药用植物资源提供参考,并为多层次、精细化的甘草资源综合利用提供依据。
甘草属;资源化学;活性成分;药理作用;综合利用
甘草为豆科(Leguminosae)蝶形花亚科(Papilionatae Taub.)的多年生草本植物,全球均有分布。主产区为亚洲及欧洲,少数分布在美洲及非洲的热带和亚热带地区。我国地处甘草资源中心地带,也是世界上甘草使用量及出口量最大的国家,年消耗量超过3万吨,以新疆、内蒙古、宁夏和甘肃为主产地,华北和西北各省区亦有产出。国内甘草属植物约有8种[1],其中作为法定的药用品种有乌拉尔甘草Glycyrrhizauralensis、光果甘草Glycyrrhizaglabra和胀果甘草Glycyrrhizainflate[2]。
甘草属植物的药用历史悠久,早在古埃及、古希腊时期就被用于治疗咳嗽、胃病及肝脏疾病[3];传统中医药,甘草始载于《神农本草经》,列为上品,具有益气补中、祛痰止咳、缓急止痛、缓和药性和清热解毒的功能,临床应用广泛,素有“十方九草”之说。除了药用价值外,甘草及其提取物在食品、饮料、化妆品等工业中也有着广泛的应用。
甘草属植物化学成分非常复杂,迄今为止从不同品种甘草中分离获得的各类化合物超过400个[4],其中三萜和黄酮为两类主要的活性物质,具有镇痛、止咳、抗炎、抗病毒、抗氧化、抗溃疡、抗肿瘤、抗变态反应及免疫调节等作用[5]。但由于种质遗传差异和分布区域环境的不同,不同品种、不同产地甘草化学成分组成及含量存在显著差异,这直接影响了产品质量的稳定及资源的有效利用。
近年来国内外科研工作者从资源合理开发利用的角度出发,采用中药资源化学研究思路与方法对甘草的植物资源进行了较为系统的研究与评价,取得了一定进展。本文从甘草属植物资源化学的角度对不同品种甘草中所含主要活性成分进行归纳分析,并总结其开发利用、研究的现状,为甘草资源综合利用及产业发展提供一定的依据与参考。
1 资源性化学成分研究
1.1 三萜皂苷类成分
三萜皂苷是甘草属植物中主要成分类型之一,具有抗炎、抗病毒、免疫调节、抗肿瘤等广泛的药理活性,同时它也是一类天然甜味剂。迄今为止从全世界甘草属G.uralensis、G.inflate、G.glabra和G.yunnanensis等植物中已分离获得了50余个三萜皂苷类成分。从已发现的化合物来看,其骨架结构一般为3β-羟基五环三萜齐墩果烷型,可视为β-香树脂醇的衍生物,其基本骨架见图1。
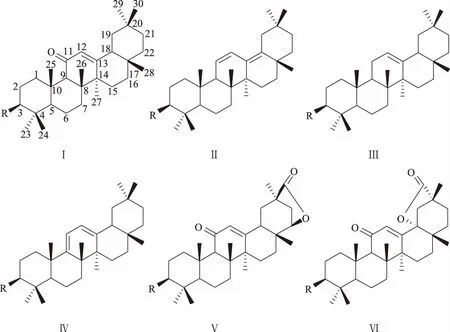
图1 甘草中三萜皂苷类成分的基本骨架
甘草属三萜皂苷结构主要特征:1)糖链:在糖链的组成上,大多数甘草三萜皂苷都含有葡萄糖醛酸基,这是甘草属植物中特有的结构特征,可作为甘草属植物鉴定的依据之一。少数成分中还含有鼠李糖、芹糖、阿拉伯糖或葡萄糖。糖与苷元连接位置多见于C3位羟基,有部分成分中糖链连接于C30的羧基、C21或C22位羟基。糖与糖之间以1→2位相连为主,仅少数成分,如Uralsaponin B以1→3位相连,Glyeurysaponin以1→4相连;2)11-位羰基:多数三萜类成分具有C11-酮基和Δ12双键结构,在化合物碳谱的低场可见δC199附近的羰基信号,同时化合物的紫外光谱最大吸收波长显示在254 nm附近。而在云南甘草中,三萜皂苷类成分主要以共轭双键、孤立双键或酮基存在,常有Δ12或Δ11,13(18)、Δ9(11),12(13)的结构;3)羟基:羟基是该类三萜皂苷中常见的取代基,出现的位置主要在C21、C22、C24、C29或C30位上;4)羧基:大多数化合物在C29或C30见有羧基,少数成分在C29和C30位被醛基或羟基取代;5)内酯环:内酯环常见位置在C30→C22和C29→C18,可以理解为C29和C30羧基与C18和C22的取代羟基脱水后形成。甘草属三萜皂苷类成分的总结见表1。

表1 甘草中三萜皂苷类化合物
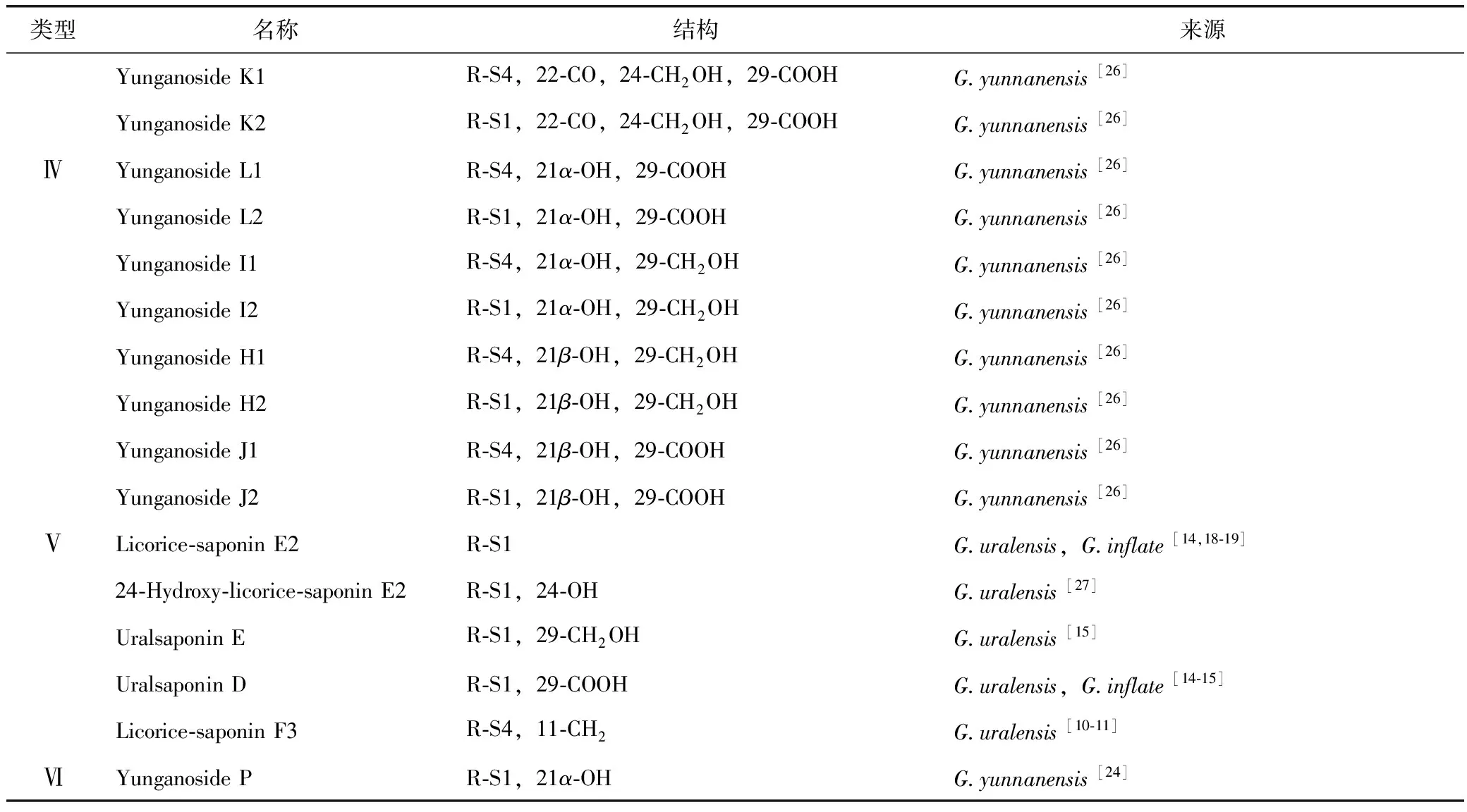
表1(续)
注:S1=-O-[β-D-GluA(1→2)-β-D-GluA];S2=-O-[β-D-GluA(1→3)-β-D-GluA];S3=-O-[β-D-GluA(1→4)-β-D-GluA];S4=-O-[α-L-Rha(1→2)-β-D-GluA(1→2)-β-D-GluA];S5=-COO-β-D-Glc;S6=-O-β-D-GluA;S7=-O-α-L-Rha。
1.2 黄酮类活性成分
甘草属中黄酮类成分复杂,迄今为止从甘草属植物中分离获得的黄酮类成分超过200个,虽然已有学者对该类成分进行了总结[28-29],但针对不同品种甘草所含黄酮活性成分的系统归纳未见报道。根据基本骨架的不同,甘草黄酮类活性成分可以分为以下几类:黄酮类(Flavones)、二氢黄酮(Flavanones)、异黄酮(Isoflavones)、二氢异黄酮(Isoflavanones)、查耳酮(Chalcones)、异黄烷(Isoflavans)、异黄烯(Isoflavenes)等,见图2。
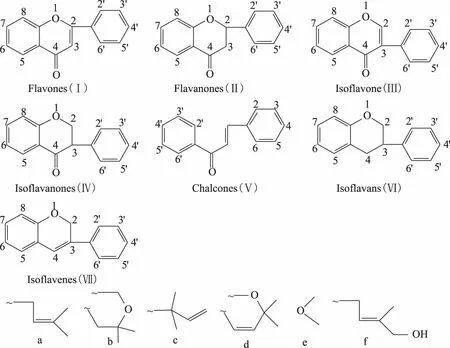
图2 甘草属中黄酮类活性成分的基本骨架及特征取代基
越来越多的研究表明,甘草黄酮在抗氧化、抗肿瘤、抗炎、抗菌及保肝等方面具有良好的活性,引起国内外学者的广泛关注。值得注意的是,不同品种甘草所含黄酮类型成分差异明显,且各类型黄酮成分活性特点也存在不同,如乌拉尔甘草中异黄酮类活性成分含量较高,甘草查尔酮类成分则主要分布于胀果甘草,而异黄烷类活性物质光甘草定在光果甘草中分布较多。但目前甘草资源利用尚未考虑到这些状况,其开发利用的方案还有待进一步的研究与优化。甘草属植物中黄酮类活性成分的总结见表2。

表2 甘草属中黄酮类活性化合物

表2(续)
1.3 香豆素类
甘草中香豆素类成分的典型特征为羰基邻位上有苯环取代,如3-Arylcoumarins(Ⅰ)类,这类成分结构符合C6-C3-C6的规则,有学者在分类时将其归为黄酮类成分。少数成分结构中的取代苯环与母核之间环合成呋喃环,形成Coumestnas(Ⅱ)类结构,见图3。从来源上来分析,香豆素类活性成分主要存在于乌拉尔甘草G.uralensis中,光果甘草G.glabra及粗毛甘草G.aspera中亦有少量分布,见表3。
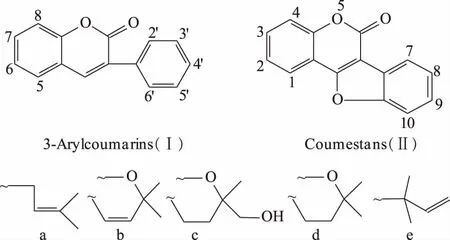
图3 甘草属中香豆素类活性成分基本骨架及特征取代基团

表3 甘草属中香豆素类活性化合物
1.4 二苯乙烯类
甘草属植物中二苯乙烯类化合物较少,主要分布在乌拉尔甘草G.uralensis、光果甘草Glycyrrhiza.glabra、北美甘草G.lepidota、臭甘草G.foetida中。从结构特征上来看,这类化合物具有C6-C2-C6的结构,有些成分中二苯乙烯的α-烯基被还原,形成“戊烯二氢二苯乙烯”结构(类型Ⅱ),见图4。已有研究表明,该类化合物具有良好的抗菌、抗病毒、降血糖及抗炎活性,引起了国内外研究者的关注,见表4。如从臭甘草G.foetida中发现的戊烯二氢二苯乙烯类成分Amorfrutins,不仅具有降血糖及抗炎的作用,而且耐受性极好,具有治疗复杂糖代谢性疾病的前景。
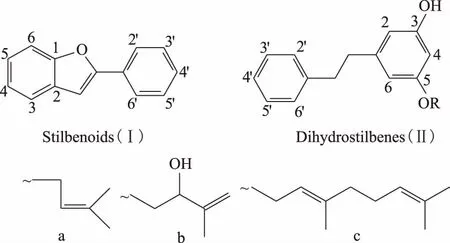
图4 甘草属中二苯乙烯类活性成分基本骨架及特征取代基团

表4 甘草属中二苯乙烯类活性化合物
1.5 多糖
多糖类成分是甘草活性成分之一,其极性较大,结构复杂,鉴定相对困难。从乌拉尔甘草G.uralensis中分离获得的由鼠李糖、葡聚糖、阿拉伯糖和半乳糖组成的多糖组分具有抗肿瘤、免疫促进及抗病毒等活性[81-82]。经研究确定其核心结构包含有3种类型[83-85]:1)以葡萄糖为主链,通过α-(1,4)键连接的单一葡萄糖结构;2)以1,3-D-半乳糖组成一个主链,在主链半乳糖某单元的6位带有一个由1,6-半乳糖残基组成的侧链分支;3)以1,3-D-半乳糖组成一个主链,在主链所有半乳糖单元6位带有一个由α-1,5-连接的L-阿拉伯糖残基组成的侧链。进一步分析其高级结构还发现[86],该类甘草多糖的糖链间可呈现环状、柱状、螺旋状、平面网状及立体网状等多种复杂空间结构,并推测这种空间的构象与甘草多糖的药理活性及作用特点有密切关系。
从光果甘草G.glabra地上部分茎中分离获得一种酸性甘草多糖,确定其分子组成为L-阿拉伯糖∶D-半乳糖∶L-鼠李糖∶D-半乳糖醛酸∶D-葡萄醛酸=22∶10∶1∶2∶1。碳粒廓清实验表明,此多糖具有显著的激活网状内皮系统功能的活性[87]。在胀果甘草G.inflata中得到一种多糖成分GIP-2,相对分子量大于2000 KDa,分子组成为葡萄糖∶阿拉伯糖∶半乳糖=3.3∶11.7∶1.0[88]。
2 甘草资源的多途径利用
2.1 在医药领域中的应用
2.1.1 抗病毒 甘草具有良好的抗病毒作用,如抗乙型肝炎病毒(HBV)。研究发现[89],甘草酸能够通过改变与HBV有关的抗原表达及抑制乙肝表面抗原(HbsAg)的分泌而对乙型肝炎有治疗作用,其作用机制与神经氨酸酶[90]、高迁移率族蛋白1(HMGB-1)[91]及磷脂酶A2[92]等多个关键靶点活性有关。对现有知识产权及临床应用状况分析发现,甘草酸及其衍生物是目前用于研制治疗HBV的常用药物,如18α-甘草酸是由18β-甘草酸在强碱催化条件下转化而成,其具有比甘草酸更好的抗病毒和抗炎作用,目前已被开发成新药应用于临床[93]。
此外,甘草酸具有抑制免疫缺陷病毒(HIV)增殖,激活机体疫功能的作用[94],对SARS冠状病毒、水痘、带状疱疹病毒也有抑制活性[95]。另有研究发现,甘草黄酮类成分Licochalcone A、Isolicoflavonol、Glycycoumarin、Glycyrhisoflavone和Licopyrancoumarin等对HIV也有一定的抑制作用[96]。
2.1.2 抗炎、抗变态反应 甘草酸及黄酮类成分是甘草抗炎、抗变态反应的主要活性物质。甘草酸在结构及功能上与糖皮质激素相似,可作为皮质激素的替代治疗。同时甘草酸可以多靶点地抑制补体系统,抑制炎性细胞因子和炎症介质生成[97],临床已用于皮炎、药疹、结缔组织病以及与自身免疫相关的疾病。甘草黄酮类成分异甘草素、甘草素、甘草查耳酮A、光甘草定、甘草醇等能够抑制炎性细胞浸润,降低炎症介质释放,减轻中性粒细胞的氧化损伤等[98]。由甘草提取物制成的黏附贴片,目前已用于治疗反复发作的炎性口腔溃疡,能够显著减轻疼痛、炎症和细胞坏死[99]。
2.1.3 抗病原微生物 甘草黄酮类成分甘草查尔酮A、甘草查尔酮B、甘草西定、光甘草定和光甘草素对大肠杆菌、绿脓杆菌、金黄色葡萄球菌、枯草杆菌、酵母菌和真菌均有显著的抑制作用[100],是一类活性强而广的抗菌抗原虫类物质。其中,甘草查尔酮A活性作用最强,可以作为开发抗呼吸道感染的潜药。
2.1.4 抗消化性溃疡 传统甘草即有治疗胃病的应用。早在1960年,日本就采用精制后含黄酮及16%甘草酸成分的提取物FM100(商品名为Aspalon)治疗消化性溃疡;而国内也有甘酮酸(主要含有甘草黄酮及甘草酸)、甘草酸(Glycyrrhizic acid)、甘草锌(Licorzine)、甘珀酸钠(Carbenoxolone sodium)和甘草酸铋盐等多种甘草酸及衍生物制剂,用于抗消化性溃疡。生物学研究发现,甘草酸类及甘草总黄酮(含甘草苷、异甘草苷、甘草素、异甘草素等黄酮类化合物)具有解痉、抑制胃酸分泌、降低胃蛋白酶活性、增加胃黏膜血流量及促进溃疡愈合的作用,能显著提高大鼠实验性胃溃疡的抑制率和治愈率[101]。
2.1.5 用于止咳祛痰 止咳祛痰是甘草主要功能之一,早已被中西医临床广为应用。其主要活性组分是三萜类成分甘草酸及甘草次酸,服用后能作用于发炎的咽部粘膜,缓和炎性刺激而镇咳。甘草流浸膏、甘草片、复方甘草合剂对急、慢性支气管炎、支气管哮喘、咽喉炎等症引起的哮喘均有一定疗效。
2.1.6 解毒作用 甘草有“解百毒”之功能,甘草酸被认为是其主要有效成分。研究表明,甘草及其各类制剂对多种药物中毒、动物毒素中毒、细菌毒素中毒及其机体代谢产物中毒均有一定的解毒作用,能缓解中毒症状,降低中毒动物死亡率。
2.1.6 其他活性 研究发现,甘草提取物具有一定的降糖、降胆固醇和神经保护作用[102-103],可有效预防糖尿病的血管并发症和内皮机能紊乱,缓解高胆固醇血症,增强记忆等。甘草多糖还具有增强免疫功能作用,能有效提高机体的抵抗力[104]。
2.2 在食品工业中的应用
甘草具有较高的营养价值及保健作用,已被广泛使用于食品工业中。甘草酸作为一种天然的甜味剂,甜度可达蔗糖的200倍,可以替代糖及人工甜味剂用于各类食品中。我国《食品添加剂卫生标准》(GB 2760-1996)规定:甘草酸可按生产需要适量用于肉类罐头、调味料、糖果、饼干、蜜饯、凉果、饮料中。美国香味料和萃取物制造者协会(FEMA)规定:甘草酸的最高用量,在饮料中为130 mg·kg-1;在糖果中为460 mg·kg-1;在焙烤食品中为75 mg·kg-1;在胶姆糖中为3200 mg·kg-1。
此外,从甘草中提取出的黄酮类物质,具有良好的抗氧化活性,在中国及日本已被批准为天然抗氧剂,可用于食用油脂、油炸食品、饼干、方便面、速煮米、干果罐头、干鱼制品和腌制肉制品。
2.3 在日用化工中的应用
甘草具有美白、抗衰老的功能,在化妆品领域被称为“美白皇后”。研究发现,甘草黄酮具有良好的抗氧化活性,甘草素、异甘草素、甘草查耳酮A等多种类型黄酮能够抑制脂质过氧化反应的产物丙二醛的生成,清除体内自由基及提高超氧化物歧化酶活性,防止皮肤老化;同时甘草黄酮还可以通过抑制酪氨酸酶和多巴色素互变异构酶(TRP-2)的活性[105],有效抑制黑色素生成。甘草酸类也是化妆品中常添加的一类物质,它不仅有抗炎、抗过敏和防止皮肤病的作用,同时还具有表面活性剂性质,能够辅助制备变凝性化妆水剂或乳液。目前,甘草提取物已用于制成护肤霜、祛斑霜、珍珠霜等各类化妆品。
欧美国家利用甘草的抗炎、解毒作用及发泡性质,将其作为天然添加剂用于制造沐浴液、牙膏及洗漱液等日用品。
2.4 其他用途
甘草地上部分茎叶中粗蛋白、粗脂肪含量高,粗纤维含量较低,饲喂效果与紫花苜蓿相似,可以作为干旱、半干旱地区优良的冬春牧草或辅助性草料。甘草提取后的废渣可用于生产绝缘人造板、食用菌培养基和肥料等,还可从中提取获得纤维素类物质,并通过转化获得医药原料—羧甲基纤维素[106]。甘草种子富含蛋白质和脂肪,中东及欧洲一些地区将其烘焙后,作咖啡代用品。民间还用刺果甘草G.Pallidiflora的种子与皂刺相配,制成煎汤,具有催乳功能,用于治疗奶汁缺少等症。
3 结语
据统计,全世界甘草属植物有10余种,分布较为广泛,以欧亚大陆种类最为丰富,北美、南美、澳大利亚以及北非也有分布。但随着环境的破坏及无节制的采挖,多数种类分布区域已比较狭窄,有的已经濒临灭绝,只有少数品种如乌拉尔甘草G.uralensis等属于广布种。因此如何保护及高效利用甘草资源已成为急需解决的关键问题。
目前针对甘草属植物已开展了深入研究,发现了包括三萜类、黄酮类、香豆素类、多糖等多种类型成分,对其中甘草酸、甘草黄酮及多糖类成分开展了多途径的药理作用研究,并已应用在医药、食品工业、日用化工等领域。但从现有的研究及应用看,尚需基于中药资源化学的研究思路与方法[107],针对资源性成分的多层次利用价值、利用效率、加工过程生物转化与化学转化,以及资源产业化过程废弃物再利用等方面进行深入细致的研究,以实现甘草资源产业链的发展与延伸:1)充分考虑不同来源甘草化学成分的差异,制定个性化的提取、分离和工艺制备方案,以实现不同品种甘草资源的合理化利用;2)采用新技术提高有效成分提取率,通过化学反应、生物转化等方式促使天然化学成分的转化和半合成,以有效提高资源性成分利用效率;3)针对甘草种植、采收、生产过程中产生的各类废弃物,开展精细化综合利用研究,以实现甘草资源的高效利用,提升资源的附加值。
[1] 中国科学院中国植物志编辑委员会.中国植物志:42卷(第2分册)[M].北京:科学出版社,1998:167-176.
[2] 中国药典委员会.中华人民共和国药典:一部[S].北京:中国医药科技出版社,2010:80.
[3] Shibata S.A Drug over the Millennia:Pharmacognosy,Chemistry,and Pharmacology of Licorice[J].Yakugaku Zasshi,2000,120(10):849-862.
[4] 向诚,乔雪,叶敏,等.利用数据库对甘草属植物化学成分的分类和分布分析[J].药学学报,2012,47(8):1023-1030.
[5] 高雪岩,王文全,魏胜利,等.甘草及其活性成分的药理活性研究进展[J].中国中药杂志,2009,34(21):2695-2700.
[6] 陶伟伟,段金廒,杨念云,等.乌拉尔甘草皂苷类成分研究[J].中草药,2013,44(12):1552-1557.
[7] Kitagawa I,Sakagami M,Hashiuchi F,et al.Apioglycyrrhizin and araboglycyrrhizin,two new sweet oleanene-type triterpene oligoglycosides from the root ofGlycyrrhizainflata[J].Chem Pharm Bull,1989,37(2):551-553.
[8] Kitagawa I,Hori K,Sakagami M,et al.Saponin and sapogenol.XLIX.On the constituents of the roots ofGlycyrrhizainflateBatalin from Xinjiang,China.Characterization of two sweet oleanane-type triterpene oligoglycosides,apioglycyrrhizin and arboglycyrrhizin[J].Chem Pharm Bull,1993,41(8):1350-2357.
[9] 蔡立宁,张如意,张志亮,等.黄甘草皂苷的结构[J].药学学报,1991,26(6):447-450.
[10] Kitagawa I,Zhou J L,Sakagami M,et al.Licorice-saponins F3,G2,H2,J2 and K2,five new oleanene-triterpene oligoglycosides from the root ofGlycyrrhizauralensis[J].Chem Pharm Bull,1991,39(1):244-246.
[11] Kitagawa I,Hori K,Sakagami M,et al.Saponin and sapogenol.XLVII.On the constituents of the roots ofGlycyrrhizauralensisFischer from northeastern China.licorice-saponins D3,E2,F3,G2,H2,J2,and K2[J].Chem Pharm Bull,1993,41(8):1337-1345.
[12] 张如意,张建华,汪茂田.乌拉尔甘草中皂苷的研究[J].药学学报,1986,21(7):510-515.
[13] 曾路,楼之岑,张如意.国产甘草的质量评价[J].药学学报,1991,26(10):788-793.
[14] Tao W W,Duan J A,Zhao R H,et al.Comparison of three officinal Chinese pharmacopoeia species of Glycyrrhiza based on separation and quantification of triterpene saponins and chemometrics analysis[J].Food Chem,2013,141(3):1681-1689.
[15] Zheng Y F,Qi L W,Cui X B,et al.Oleanane-type Triterpene Glucuronides from the Roots ofGlycyrrhizauralensisFischer[J].Planta Med,2010,76(13):1457-1463.
[16] 张慧,王世盛,李伟,等.乌拉尔甘草中的一个新三萜皂苷成分[J].世界科学技术—中医药现代化基础研究,2009,11(2):253-256.
[17] Jinwei L,Nakajima J,Kimura N,et al.Oleanane-type triterpene glycosides fromGlycyrrhizauralensis[J].Nat Prod Commun,2007,2(6):243-248.
[18] Kitagawa I,Zhou J L,Sakagami M,et al.Licorice-saponins A3,B2,C2,D3 and E2,five new oleanene-type triterpene oligoglycosides from Chinese Glycyrrhizae Radix[J].Chem Pharm Bull,1988,36(9):3710-3713.
[19] Kitagawa I,Hori K,Taniyama T,et al.Saponin and sapogenol.XLVII.On the constituents of the roots ofGlycyrrhizauralensisFischer from northeastern China.licorice-saponins A3,B2,and C2[J].Chem Pharm Bull,1993,41(1):43-49.
[20] Shibano M,Nukui H,Kita S,et al.Studies on index compounds for HPLC analysis ofGlycyrrhizamacedonica[J].Nat Med,1999,53(4):166-172.
[21] 曾路,张如意,王动,等.云南甘草次皂苷和云南甘草皂苷元的结构鉴定[J].药学学报,1990,25(10):750-757.
[22] Gao D Y,Zhang R Y,Yao B.Structure identification of yunnanglysaponin A and B[J].J Chin Pharm Sci,1994,3(1):1-5.
[23] Ohtani K,Ogawa K,Kasai R,et al.Oleanane glycosides from Glycyrrhiza yunnanensis roots[J].Phytochemstry,1992,31(5):1747-1752.
[24] Ji S,Wang Q,Qiao X,et al.New triterpene saponins from the roots ofGlycyrrhizayunnanensisand their rapid screening by LC/MS/MS[J].J Pharm Biomed,2014,90(1):15-26.
[25] Kitagawa I,Hori K,Uchida E,et al.On the constituents of the roots ofglycyrrhizauralensisFischer from Xinjiang,China.Chemical structures of licorice-saponin L3 and isoliquiritin apioside[J].Chem Pharm Bull,1993,41(9):1567-1572.
[26] Ohtani K,Kasai R,Yang C R,et al.Oleanane glycosides from roots ofGlycyrrhizayunnanensis[J].Phytochemistry,1994,36(1):139-145.
[27] 朱绪民,邸迎彤,彭树林,等.乌拉尔甘草中的化学成分[J].中草药,2003,34(3):198-201.
[28] 邢国秀,李楠,王童,等.甘草中黄酮类化学成分的研究进展[J].中国中药杂志,2003,28(7):593-597.
[29] 张波,官月平,田庆来.乌拉尔甘草中黄酮类化学成分的研究进展[J].中成药,2006,28(9):1362-1365.
[30] 朱大元,宋国强,蒋福祥,等.甘草化学成分的研究-异甘草黄酮醇及甘草香豆素的结构[J].化学学报,1984,42(10):1080-1084.
[31] Fukai T,Marumo A,Kaitou K,et al.Anti-Helicobacter pylori flavonoids from licorice extract[J].Life Sci,2002,71(12):1449-1463.
[32] Manfredi K P,Vallurupalli V,Demidova M,et al.Isolation of an anti-HIV diprenylated bibenzyl fromGlycyrrhizalepidota[J].Phytochemistry,2001,58(1):153-157.
[33] Jayaprakasam B,Doddaga S,Wang R,et al.Licorice flavonoids inhibit eotaxin-1 secretion by human fetal lung fibroblasts in vitro[J].J Agric Food Chem,2009,57(3):820-825.
[34] Kuroda M,Mimaki Y,Honda S,et al.Phenolics fromGlycyrrhizaglabraroots and their PPAR-gamma ligand-binding activity[J].Bioorg Med Chem,2010,18(2):962-970.
[35] Kumar S,Pathania A S,Saxena A K,et al.The anticancer potential of flavonoids isolated from the stem bark ofErythrinasuberosathrough induction of apoptosis and inhibition of STAT signaling pathway in human leukemia HL-60 cells[J].Chem Biol Interact, 2013,205(2):128-137.
[36] Kim Y W,Ki S H,Lee J R,et al.Liquiritigenin,an aglycone of liquiritin in Glycyrrhizae radix,prevents acute liver injuries in rats induced by acetaminophen with or without buthionine sulfoximine[J].Chem Biol Int,2006,161(2):125-138.
[37] Adianti M,Aoki C,Komoto M,et al.Anti-hepatitis C virus compounds obtained fromGlycyrrhizauralensisand other Glycyrrhiza species[J].Microbiol Immunol,2014,58(3):180-187.
[38] Kusano A,Nikaido T,Kuge T,et al.Inhibition of adenosine 3c,5c-cylicmonophosphate phosphodiesterase by flavonoids from licorice roots and 4-arylcoumarins[J].Chem Pharm Bull,1991,39(4):930-936.
[39] Wang W,Hu X,Zhao Z,et al.Antidepressant-like effects of liquiritin and isoliquiritin fromGlycyrrhizauralensisinthe forced swimming test and tail suspension test in mice[J].Prog Neuro Psychoph,2008,32(5):1179-1185.
[40] Haraguchi H,Ishikawa H,Mizutani K.Antioxidative and superoxide scavenging activities of retrochalcones in Glycyrrhiza inflata[J].Bioorg Med Chem,1998,6(3):339-347.
[41] Lee J W,Ji Y J,Yu M H,et al.Antimicrobial effect and resistant regulation ofGlycyrrhizauralensison methicillin-resistant Staphylococcus aureus[J].Nat Prod Res,2009,23(2):101-111.
[42] Sitaraghav R G,Hanumaiah T,Ali Keshavarz S.Glepidotin C:A minor antimicrobial bibenzyl fromGlycyrrhizalepidota[J].Phytochemistry,1989,28(12):3556-3557.
[43] Biondi D M,Rocco C,Ruberto G.New dihydrostilbene derivatives from the leaves ofGlycyrrhizaglabraand evaluation of their antioxidant activity[J].J Nat Prod,2003,66(4):477-480.
[44] Fukai T,Cai B S,Maruno K,et al,An isoprenylated flavanone fromglycyrrhizaglabraand rec-asay of licorice phemols[J].Phytochemistry,1998,49(7):2005-2013.
[45] Fu Y,Chen J,Li Y J,et al.Antioxidant and anti-inflammatory activities of six flavonoids separated from licorice[J].Food Chem,2013,141(2):1063-1071.
[46] 高东英,张如意.云南甘草化学成分的研究[J].中草药,1994,25(10):507-508.
[47] 蔡立宁,张如意,王邠,等.刺果甘草化学成分的研究[J].药学学报,1992,27(10):748-751.
[48] Chen J,Zhao X,Ye Y,et al.Estrogen receptor beta-mediated proliferative inhibition and apoptosis in human breast cancer by calycosin and formononetin[J].Cell Physiol Biochem,2013,32(6):1790-1796.
[49] Kim H J,Seo S H,Lee B G,et al.Identification of tyrosinase inhibitors fromGlycyrrhizauralensis[J].Planta Med,2005,71(8):785-787.
[50] Hatano T,Yasuhara T,Fukuda T,et al.Phenolic constituents of licorice.II.Structures of licopyranocoumarin,licoarylcoumarin and glisoflavone,and inhibitory effects of licorice phenolics on xanthine oxidase[J].Chem Pharm Bull,1989,37(11):3005-3009.
[51] 傅乃武,刘朝阳,张如意,等.甘草黄酮类和三萜类化合物抗氧化作用的研究[J].中药药理与临床,1994(5):26-29.
[52] Hatano T,Fukuda T,Miyase T,et al.Phenolic constituents of licorice.III.Structures of glicoricone and licofuranone,and inhibitory effects of licorice constituents on monoamine oxidase[J]. Chem Pharm Bull,1991,39(5):1238-1243.
[53] Hatano T,Shintani Y,Aga Y,et al.Phenolic constituents of licorice.VIII.Structures of glicophenone and glicoisoflavanone,and effects of licorice phenolics on methicillin-resistant Staphylococcus aureus[J].Chem Pharm Bull,2000,48(9):1286-1292.
[54] Yamazaki S,Morita T,Endo H.Isoliquiritigenin suppresses pulmonary metastasis of mouse renal cell carcinoma[J].Cancer Lett,2002,183(1):23-30.
[55] Sato Y,He J X,Nagai H.Isoliquiritigenin,one of the antispasmodic principles ofGlycyrrhizaularensisroots,acts in the lower part of intestine[J].Biol Pharm Bull,2007,30(1):145-149.
[56] Haraguchi H.Mode of antibacterial action of retrochalcones from Glycyrrhiza Inflata[J].Phytochemistry,1998,48(l):125-129.
[57] Kobayashi S,Miyamoto T,Kimura I,et al.Inhibitory effect of isoliquiritin,a compound in licorice root,on angiogenesis in vivo and tube formation in vitro[J].Biol Pharm Bull,1995,18(10):1382-1386.
[58] 王青,苗文娟,向诚,等.乌拉尔甘草化学成分研究[J].中草药,2012,43(10):1886-1890.
[59] Yoon G,Jung Y D,Cheon S H.Cytotoxic allyl retrochalcone from the roots ofGlycyrrhizainflata[J].Chem Pharm Bull,2005,53(6):694-695.
[60] Kim S J,Kim C G,Yun S R,et al.Synthesis of licochalcone analogues with increased anti-inflammatory activity[J].Bioorg Med Chem Lett,2014,24(1):181-185.
[61] Franceschelli S,Pesce M,Vinciguerra I,et al.Licocalchone-C extracted fromGlycyrrhizaglabrainhibits lipopolysaccharide-interferon-γ inflammation by improving antioxidant conditions and regulating inducible nitric oxide synthase expression[J].Molecules,2011,16(7):5720-5734.
[62] 梁鸿,张如意.圆果甘草化学成分的研究[J].北京医科大学学报,1992,24(5):399-400.
[63] 罗丽平,李艳静,张慧,等.HPLC-Q-TOFMS/MS偶联DPPH添加法测定甘草黄酮类成分体外代谢产物的抗氧化活性[J].中国新药杂志,2013,22(21):2547-2552.
[64] Dao T T,Nguyen P H,Lee H S,et al.Chalcones as novel influenza A(H1N1)neuraminidase inhibitors fromGlycyrrhizainflata[J].Bioorg Med Chem Lett,2011,21(1):294-298.
[65] Chin Y W,Jung H A,Liu Y,et al.Anti-oxidant Constituents of the Roots and Stolons of Licorice(Glycyrrhizaglabra)[J].J Agric Food Chem,2007,55(12):4691-4697.
[66] Fu K S,Satoh K,Nomura T.Preliminary evaluation of antinephritis and radical scavenging activities of glabridin fromGlycyrrhizaglabra[J].Fitoterapia,2003,74(7):624-629.
[67] Fukai T.Antinephritis and radical scavenging activity of prenylflavonoids[J].Fitoterapia,2003,74(7):720-724.
[68] Tanabe S,Desjardins J,Bergeron C,et al.Reduction of bacterial volatile sulfur compound production by licoricidin and licorisoflavan A from licorice[J].J Breath Res,2012,6(1):1752-7155.
[69] Kajiyama K,Hiraga Y,Takahashi K,et al.Flavonoids and isoflavonoids of chemotaxonomic significance fromGlycyrrhizapallidiflora(Leguminosae)[J].Biochem Syst Ecol,1993(1):1978-1993.
[70] Tamir S,Eizenberg M,Somjen.Estrogen-like activity of glabrene and other constituents isolated from licorice root[J].Steroid Biochem,2001,78(3):291-298.
[71] Vaya J,Belinky P A,Aviram M.Antioxidant constituents from licorice roots:isolation,structure elucidation and antioxidative capacity toward LDL oxidation[J].Free Radic Biol Med,1997,23(2):302-313.
[72] 王建国,周忠,刘海峰,等.甘草的活性成分及其在化妆品中的应用[J].日用化学工业,2004,34(5):249-251.
[73] Somjen D,Katzburg S,Vaya J.Estrogenic activity of glabridin and glabrene from licorice roots on human osteoblasts and prepubertal rat skeletal tissues[J].J Steroid Biochem Mol Biol,2004,91(4-5):241-251.
[74] Cho H J,Lima S S,Lee Y S,et al.Hexane/ethanol extract ofGlycyrrhizauralensislicorice exerts potent anti-inammatory effects in murine macrophages and in mouse skin[J].Food Chem,2010,121(4):959-966.
[75] Kuroda M,Mimaki Y,Sashida Y.Phenolics with PPAR-Ligand-Binding activity obtained from licorice(GlycyrrhizauralensisRoots)and ameliorative effects of glycyrin on genetically diabetic KK-Ay mice[J].Bioorg Med Chem Lett,2003,13(24):4267-4272.
[76] Wang Q E,Lee F S,Wang X.Isolation and purification of inflacoumarin A and licochalcone A from licorice by high-speed counter-current chromatography[J].J Chromatogr A,2004,1048(1):51-57.
[77] 王彩兰,张如意,韩永生,等.乌拉尔甘草中新香豆素的化学研究[J].药学学报,1991,26(2):147-150.
[78] Lee S,Oh H M,Lim W B,et al.Gene induction by glycyrol to apoptosis through endonuclease G in tumor cells and prediction of oncogene function by microarray analysis[J].Anticancer Drugs, 2008,19(5):503-515.
[79] Eerdunbayaer,Orabi M A,Aoyama H,et al.Structures of two new flavonoids and effects of licorice phenolics on vancomycin-resistant Enterococcus species[J].Molecules,2014,19(4):3883-3897.
[80] Weidner C,de Groot J C,Prasad A,et al.Amorfrutins are potent antidiabetic dietary natural products[J].Proc Natl Acad Sci USA, 2012,109(19):7257-7262.
[81] Wang Y W,Zhang H B,Shi Y R.Inhibition of glycyrrhiza polysaccharide on virus[J].Acta Sci Nat Univ Nankaiensis,2001,34(2):126-128.
[82] Wang Y W,Zhang H B,Lv J.Research on the biological activities of a polysaccharide extracted from reside ofGlycyrrhizaUralensisFisch[J].Acta Sci Nat Univ Nankaiensis,2000,33(4):46-48.
[83] 周蓉,齐莉,王雅芬,等.甘草多糖的分离纯化及高效毛细管电泳分析[J].分析化学,1999,27(2):245-249.
[84] 孙润广,张静.甘草多糖螺旋结构的原子力显微镜研究[J].化学学报,2006,64(24):2467-2470.
[85] 王岳五,张海波,陈水平,等.草残渣中多糖的分离纯化及性质分析[J].南开大学学报(自然科学),1999,33(4):36-38.
[86] 史坤.甘草多糖的结构分析及免疫调节作用研究[D].天津:天津科技大学,2007:58-63.
[87] Shimizu N,Tomoda M,Satoh M,et al.Characterization of a polysaccharide having activity on the reticuloendothelial system from the stolon ofGlycyrrhizaglabravar.glandulifera[J].Chem Pharm Bull,1991,39(8):2082-2086.
[88] 热娜·卡斯木,丛媛媛,屠鹏飞.胀果甘草多糖的分离纯化及其理化性质[J].华西药学杂志,2008,23(4):448-450.
[89] Sato H,Goto W,Yamamura J,et al.Therapeutic basis of glycyrrhizin on chronic hepatitis B[J].Antiviral Research,1996,30(2-3):171-177.
[90] Owada T,Matsubayashi K,Sakata H.Interaction between desialylated hepatitis B virus and asialoglycoprotein receptor on hepatocytes may be indispensable for viral binding and entry[J].J Viral Hepat, 2006,13(1):11-18.
[91] Ryoko S,Maiko O,Hiroko T,et al.Inhibitory effect of glycyrrhizin on the phosphorylation and DNA-binding abilities of high mobility group proteins 1 and 2invitro[J].Biol Pharm Bull,2001,24(8):906-911.
[92] Ohtsuki K,Abe Y,Shimoyama Y.Separation of phospholipase A2 in Habu snake venom by glycyrrhizin(GL)-affinity column chromatography and identification of a GL-sensitive enzyme[J].Biol Pharm Bull,1998,21(6):574-578.
[93] 张明发,沈雅琴.18α-和18β-甘草酸治疗肝病的疗效比较[J].抗感染药学,2011,8(3):163-166.
[94] Harada S.The broad anti-viral agent glycyrrhizin directly modulates the fluidity of plasma membrane and HIV-1 envelope[J].Biochem J,2005,392(1):191-199.
[95] Cinatl J,Morgenstern B,Bauer G,et al.Glycyrrhizin,an active component of liquorice roots,and replication of SARS-associated coronavirus[J].Lancet,2003,361(9374):2045-2046.
[96] Hatano T,Yasuhara T,Miyamoto K,et al.Anti-human immunodeficiency virus phenolics from licorice[J].Chem Pharm Bull,1988,36(6):2286-2288.
[97] 张明发,沈雅琴.甘草酸及其衍生物的抗炎和抗变态反应研究进展[J].现代药物与临床,2011,26(5):359-363.
[98] 张明发,沈雅琴.甘草及其活性成分抗炎与抗炎机制的研究进展[J].现代药物与临床,2011,26(11):261-268.
[99] Moghadamnia A A,Motallebnejad M,Khanian M.The efficacy of the bioadhesive patches containing licorice extract in the management of recurrent aphthous stomatitis[J].Phytother Res,2009,23(2):246-250.
[100] Okada K,Tamura Y,Yamamoto M,et al.Identification of antimicrohial and antioxidant constitutes from licorice of Russia and xinjiang origin[J].Chem Pharm Bull,1989,37(9):2528-2530.
[101] 张明发,沈雅琴.甘草消化系统药理研究进展[J].临床药学,2009,30(6):264-267.
[102] Choi Y J,Lim S S,Jung J Y,et al.Blockade of nitroxidative stress by roasted licorice extracts in high glucose-exposed endothelial cells[J].J Cardiovasc Pharmacol,2008,52(4):344-354.
[103] Visavadiya N P,Narasimhacharya A V.Hypocholesterolaemic and antioxidant effects ofGlycyrrhizaglabra(Linn)in rats[J].Mol Nutr Food Res,2006,50(11):1080-1086.
[104] 胡菩,敖明章,崔永明,等.甘草多糖的抗肿瘤活性及对免疫功能的影响[J].天然产物研究与开发,2008,20(5):911-913.
[105] Nerya O,Vaya J,Musa R,et al.Glabrene and isoliquiritigenin as tyrosinase inhibitors from licorice roots[J].J Agric Food Chem,2003,51(5):1201-1027.
[106] 吉媛媛.利用甘草渣制备羧甲基纤维素[J].山西化工,1997(2):43-44.
[107] 段金廒,吴启南,宿树兰,等.中药资源化学学科的建立与发展[J].中草药,2012,43(9):1665-1671.
ResearchAdvancesinResourceChemistryandUtilizationofGenusGlycyrrhiza
ZHENGYunfeng1,2,WEIJuanhua1,LENGKang1,TAOWeiwei2,FANGShiqi1,PENGGuoping1,2,DUANJin’ao1,2*
(1.SchoolofPharmacy,NanjingUniversityofChineseMedicine,Nanjing210023,China;2.JiangsuCollaborativeInnovationCenterofChineseMedicinalResourcesIndustrialization,Nanjing210023,China)
The plants ofGlycyrrhizaand their products,which were regarded as valuable natural resource,have been widely applied to many areas including biological medicine,food industry,pastoral industry and animal husbandry.In recent years,great successes of researches on resources of the genusGlycyrrhizawere achieved.However,due to the destruction of ecological environment and uncontrolled consumption onGlycyrrhiza,resource scarcity of the plant had become a serious problem.In this paper the authors thoroughly summarized the advances of species,resource distribution,chemical compositions and their bioactive actions,and multi-ways comprehensive utilization etc.based on the thoughts of resources chemistry of Chinese medicinal materials.These data would provide some scientific data and references for the further research on the exploitation and comprehensive utilization of plants resources in genusGlycyrrhiza.
Glycyrrhiza;resource chemistry;bioactive ingredients;pharmacologic actions;comprehensive utilization
2014-11-13)
国家自然科学基金项目(81202881);江苏省自然科学基金(SBK201123752);江苏省高校优势学科建设工程资助项目(YSXK-2010)
*
段金廒,教授,博士生导师,研究方向:中药资源及方药功效物质基础研究,E-mail:dja@ njutcm.edu.cn
10.13313/j.issn.1673-4890.2015.10.024
