超声波与氯胺联用工艺去除水中三氯生的研究
2015-08-30李青松周生辉李国新陈国元马晓雁高乃云厦门理工学院水资源环境研究所福建厦门602福建师范大学环境科学与工程学院福建福州507浙江工业大学建筑工程学院浙江杭州00同济大学污染控制与资源化研究国家重点实验室上海200092
李青松,周生辉,李国新,陈国元,马晓雁,高乃云(.厦门理工学院水资源环境研究所,福建 厦门602;2.福建师范大学环境科学与工程学院,福建 福州 507;.浙江工业大学建筑工程学院,浙江 杭州00;.同济大学污染控制与资源化研究国家重点实验室,上海 200092)
超声波与氯胺联用工艺去除水中三氯生的研究
李青松1*,周生辉1,2,李国新1,陈国元1,马晓雁3,高乃云4(1.厦门理工学院水资源环境研究所,福建 厦门361024;2.福建师范大学环境科学与工程学院,福建 福州 350117;3.浙江工业大学建筑工程学院,浙江 杭州310014;4.同济大学污染控制与资源化研究国家重点实验室,上海 200092)
采用超声与氯胺联用工艺对水中三氯生(TCS)的去除进行了研究,考察了超声功率、氯胺投加量、TCS初始浓度、pH值和自由基捕获剂等因素对TCS去除的影响,鉴定识别了降解产物并探讨联用工艺降解TCS的机理.结果表明,超声和氯胺联用去除TCS具有协同效应,可以有效地去除TCS.超声波功率为600W,TCS浓度为200µg/L,氯胺浓度为5mg/L时,120min后TCS去除率可达90.8%.联用工艺中增加超声功率可以提高TCS的去除,TCS的去除率随氯胺浓度升高呈现出先升高后降低的趋势,随着初始浓度的升高而下降,碱性环境有利于TCS的去除,pH值为10.7时,TCS的去除可达100%,自由基捕获剂叔丁醇TBA对TCS的去除有抑制作用. GC/MS扫描分析表明2,4-二氯苯酚(2,4-DCP)为TCS的降解产物.
三氯生;超声;氯胺;降解产物
三氯生(2,4,4'-三氯-2'-羟基二苯醚,TCS)是药品和个人护理用品(PPCPs)中一种典型的广谱抗菌消毒剂,广泛添加在个人护理用品、药物制剂及纺织品中.环境中低浓度TCS曾被认为对人体和环境是高度安全的,长期以来其环境效应被人们忽视[1-2].研究表明[3-5]TCS能干扰人的内分泌系统,一定条件下可转化为氯酚、2,8-二氯-p-二噁英(2,8-Cl2DD)等毒性更强的持久性污染物.近年来水体中TCS浓度呈上升趋势,严重威胁到水体生物安全及人体健康[6-9].
研究者采用氧化和吸附等技术对TCS的去除进行了研究[10-12].超声波技术在去除水中难降解污染物方面效果显著[13-16],但超声利用率低、能耗大,为强化污染物的去除效果,超声与其他水处理技术联用成为最近关注的热点[17-21].氯胺是一种相对稳定的氧化剂,同时也是一种绿色消毒剂,与自由氯消毒法相比,其消毒过程中较少消毒副产物产生,常用来替代自由氯消毒,然而其氧化性较弱,难以去除内分泌干扰有机物与药品成分有机物[22].为了克服这一缺点,本文将氯胺与超声波技术结合起来,强化消毒效果的同时提高降解水中有机物的能力.
本文利用超声波与氯胺联用工艺去除水中TCS,研究超声波功率、氯胺浓度、pH值、自由基捕获剂及TCS初始浓度对去除的影响.
1 试验部分
1.1试剂与仪器
TCS(德国Dr.Ehrenstorfer公司,纯度>99.5%);乙腈(HPLC级,德国 Merck);叔丁醇(TBA)、NH4Cl、KH2PO4、K2HPO4、NaClO和Na2S2O3等均为化学纯;试验用水采用Milli-Q超纯水(18.2MΩ).
LC-20A高效液相色谱仪(Shimadzu,日本),自动进样器(SIL-20A),检测器(SPD-M20A);UV2550 (Shimadzu,日本);GCMS-QP2010ultra (Shimadzu,日本),GC/MS自动进样器(AOC-5000,日本岛津),色谱柱(Rxi®-5ms:30m×0.32mm× 0.25μm,日本岛津).pH仪 (Eutevch,美国);便携式水质分析仪(Dr2800,哈希);超声波处理器(FS-1200N,上超生析超声波仪器有限公司),工作频率为20kHz.
1.2试验方法
氯胺配制以 KH2PO4与 K2HPO4为缓冲溶液,pH值为7.8~8.0,NaClO与NH4Cl配制而成,其中Cl2:N=4:1.称取10.0mgTCS,配制成100mg/L的标准储备液(用乙腈作为助溶剂),使用时稀释至所需的浓度.
试验在完全混合间歇式条件下运行:TCS溶液置于反应器内,并通过管路5、7和8混合循环,反应器外有冷却套管,反应温度控制在室温,反应器内加入一定浓度的TCS溶液,再加入一定量的氯胺溶液,启动水泵完全混合 2min后,开启超声(探头深入液面 3cm)同时开启循环冷却水,并开始计时,设定反应时间后取样,水样滴加过量的Na2S2O3溶液抑制反应继续进行,样品过0.45 µm玻璃纤维膜后进行水质分析.反应装置见图1.
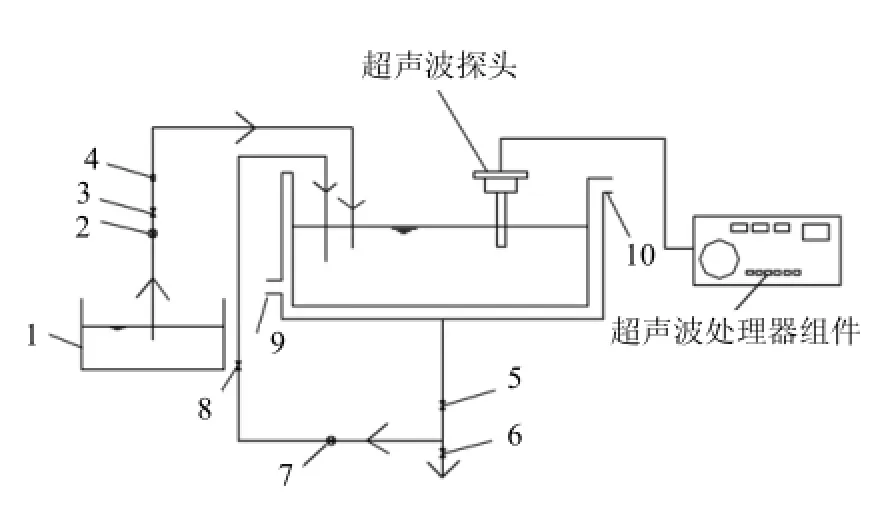
图1 试验工艺流程示意Fig.4 Schematic diagram of the reactor
1.3分析方法
试验中采用HPLC和GC/MS对TCS及其降解产物进行鉴定分析.
HPLC条件:色谱柱为Insertsil C18 (250mm×4.6mm, 5μm),流动相为乙腈/水-70/30 (V:V),流速为0.8mL/min,检测波长λ=230nm,进样体积10µL,S/N大于3.
GC/MS条件:载气为高纯氦气,90kPa;进样量1μL;无分流进样方式;进样口温度为 280℃;炉温控制:初始温度为75℃,保留1min,以10℃/min升温至150℃,持续5min,然后以15℃/min升温至280℃,持续3min;MS离子化温度为250℃;接口温度280℃;采用scan扫描:m/z起始为50,终止为600,扫描时间为4至24min.
2 结果与讨论
2.1氯胺、超声、超声/氯胺联用降解TCS
超声反应条件为超声功率600W,频率20kHz;超声和氯胺反应条件为超声功率 600W,频率20kHz,氯胺投加量为 3mg/L,TCS初始质量浓度为200µg/L,TCS的降解效果见图2.

图2 氯胺、超声及超声/氯胺工艺降解TCS的效果Fig.4 Degradation efficiencies of TCS by chloramine, ultrasound and ultrasound/chloramine
由图2可知,氯胺氧化30min后,TCS的去除率为13.40%,60min后TCS的去除为15.08%,此后去除随时间几乎没有变化,单独氯胺去除 TCS效果不佳.超声作用60min和120min后TCS的去除率分别为 47.07%和 50.02%,超声比氯胺有更好的去除效果.超声/氯胺工艺可以显著提高TCS的去除,TCS去除随反应的进行而逐渐增加,60min时TCS去除率为66.61%,120min时去除率可达83.53%.
氯胺对于有机物的去除主要是氧化去除,但由于较低的氧化电位,单独氯胺无法有效去除 TCS.超声降解有机污染物机理主要为声空化理论,超声作用时水中的微小气泡核经历振荡、生长、收缩、崩溃等一系列动力学过程,产生瞬时的高温高压,同时生成氧化性极强的羟基自由基,使得水中的污染物在高温热解、自由基氧化效应、机械效应和超临界氧化效应的作用下去除[23-24].
超声工艺中,60min和120min时TCS去除率均有增加,试验中超声对TCS的去除要好于氯胺的去除,主要原因可能是超声产生的自由基氧化还原电位更高,可以更有效的去除TCS.投加一定量的氯胺溶液能显著增加TCS的去除,反应时间60,120min时,TCS的去除与二者单独作用相加相比,去除分别增加了 7.17%和 26.14%,超声/氯胺工艺去除TCS具有协同增效效应.
考察了超声作用下氯胺的变化,浓度为3mg/L的氯胺溶液超声 120min后浓度仅降低9.8%,表明超声波作用下氯胺相对稳定.超声/氯胺工艺具有协同效应可能是因为超声作用下空化泡崩溃时除产生羟基自由基外,还有超声产生的射流作用导致分子碰撞加剧,增大了溶液分子接触反应的机率.
2.2超声/氯胺联用降解TCS影响因素
2.2.1超声波功率对TCS去除的影响 TCS浓度为 200μg/L,氯胺投加量设定为 3mg/L,调节超声功率,考察超声功率对 TCS去除的影响,结果见图3.由图3可知,超声波功率为240W时,反应120min后TCS的去除率为55.5%,而当超声波功率分别提高到360,480,600W时,TCS的去除率增加为65.7%、80.2%、83.5%.
试验表明,超声波功率对TCS的去除起促进作用, TCS的去除随着超声功率的增加而升高,提高超声波功率能增加TCS的去除.
由于在超声波作用下,水溶液发生空化效应促使水分子分解成羟基自由基(∙OH)和氢原子(∙H)[25-26],其反应可以表达为式(1).

图3 超声波功率对TCS去除的影响Fig.4 Effect of ultrasonic power on TCS removal

增加超声波功率使溶液中产生更多的空化泡,增强了空化效应,提高了超声波分解水分子的速度,从而增加了溶液中∙OH浓度,并加快了传质过程,提高了TCS的去除率.lnc与反应时间t之间呈线性关系,TCS降解曲线呈现出一级反应的特征,参数见表1.实验范围内,一级反应速率常数由0.104min-1增加到600W时的0.228min-1.

表1 不同功率下联合工艺降解TCS的一级动力学拟合Table 1 First-order kinetics model of TCS degradation in ultrasound/chloramine processes under different powers
2.3氯胺浓度对TCS去除的影响
TCS初始浓度为200μg/L时,超声波功率设定为 600W,氯胺的投加量分别为 0,1.25,3,5,7.5, 10mg/L,考察氯胺浓度对 TCS去除的影响,结果见图4.由图4可知,TCS的去除率随氯胺浓度升高呈现出先升高后降低的趋势.单独超声120min 时TCS去除率仅为50%.当投加1.25mg/L的氯胺溶液后,TCS去除率升高为71%.增加氯胺浓度至5mg/L时,TCS的去除率增加为90.8%.继续增加氯胺浓度至10mg/L, TCS的去除率反而降低为80.4%,TCS的去除率随氯胺浓度升高呈现出先升高后降低的趋势.

图4 氯胺浓度对TCS去除的影响Fig.4 Effect of chloramine concentrations on TCS removal
Wu等[22]研究发现,氯胺相对稳定,难以氧化降解TCS.我们的前期研究也证明氯胺对TCS基本没有去除作用.但是在超声波作用下,氯胺与超声波发生协同作用,显著提高了 TCS的去除.这可能是超声波条件下,不仅可以产生自由基,而且声空化效应的机械作用会增加溶液中的TCS与氯胺的有效碰撞次数,提高了 TCS的去除率.然而继续增加氯胺的浓度时, TCS的去除反而降低,这可能是因为氯胺浓度的增加导致溶液中Cl-离子浓度相应地增加,而Cl-容易捕获∙OH生成氧化性较低的C1,进而降低TCS的去除.
2.4TCS初始浓度对TCS去除的影响
超声功率为600W时,氯胺溶液的浓度设定为3mg/L,改变TCS的初始浓度,考察初始浓度对TCS去除率的影响,结果见图5.由图5可知,TCS初始浓度为 108, 212, 323, 527μg/L时,反应120min后TCS去除率分别为95.4%、83.5%、74.4%和62%.试验表明TCS初始浓度对联用工艺的去除效果影响较大,TCS去除率随着初始浓度的升高而下降.这是因为在超声功率和氯胺浓度一定的情况下,发生空化反应的能力是相同的,浓度越高,

图5 初始浓度对TCS去除的影响Fig.4 Effect of initial concentrations on TCS removal
单位浓度TCS还原的羟基自由基就越少,所以导致TCS去除率随着浓度的增高而降低.不同浓度时TCS降解曲线呈现出一级反应的特征,其一级反应动力学拟合曲线参数见表2.

表2 TCS不同初始浓度下联合工艺降解TCS的一级动力学拟合Table 1 First-order kinetics model of TCS degradation in ultrasound/chloramine processes at different concentrations
2.5pH值对TCS去除的影响
试验中TCS的浓度为200μg/L,超声波功率为600W,投加3mg/L的氯胺溶液,调整溶液pH值,考察溶液 pH值对去除率的影响,结果见图6.由图6可知,实验范围内TCS去除率随pH值升高而升高.pH值为6.7时,TCS去除率为72.0%.pH值为7.2、8.7及9.4时,TCS去除率分别为76.9%、83.5%、92.4%.当pH值为10.7时, TCS的去除最高,此时TCS的浓度已低于检测限.
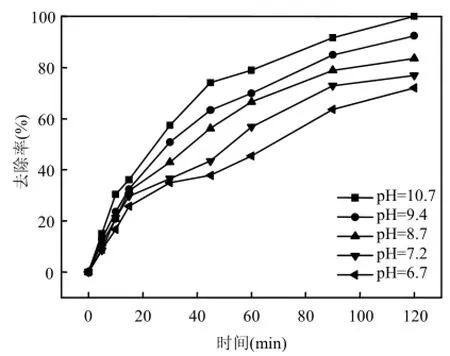
图6 pH值对TCS去除的影响Fig.4 Effect of pH on TCS removal
一方面较高的溶液pH值有利于氯胺的反应持久性,提高其氧化性能[27];另一方面 pH 值可以改变污染物的存在形态和亲疏水性,影响到超声过程中其在空化泡和溶液中的分布和去除途径. TCS为疏水性、弱挥发性物质,当溶液呈弱碱性时,TCS一部分以分子形式存在(TCS的pKa= 7.9)[28],随着酸性的增强,以分子形式存在的 TCS就越多,而分子形式的 TCS疏水性较强,倾向于向空化泡内移动进行热解反应,强碱环境中 TCS以负离子形式存在,倾向于在空化泡气液界面或进入本体溶液中同空化效应产生的∙OH等进行氧化反应[29-30].试验结果表明,TCS发生在空化泡溶液界面和本体溶液中的氧化反应起主导作用,而空化泡内的热解作用较弱.Nilsun等[31]在研究pH对超声去除NP的影响时具有类似的结论.
2.6自由离子捕获剂对去除率的影响
叔丁醇(TBA)通常认为是一种自由基清除剂,常用于确认反应存在自由基反应,如果投加自由基捕获剂而导致去除率下降则表明反应过程包含自由基参与降解[32].试验中取 1L初始浓度为200μg/L的TCS溶液,设置超声波功率为600W,投加3mg/L的氯胺溶液,以TBA模拟自由基捕获剂,考察自由基捕获剂对 TCS去除的影响,结果见图 7.由图 7可知,TCS去除随自由基捕获剂TBA 浓度上升而下降,TBA 投加量为 0.001, 0.01,0.05,0.1mg/L时,TCS的去除率为 70.3%、41.0%、27.8%和20.0%,表明联用工艺降解TCS反应过程中有自由基参与反应.
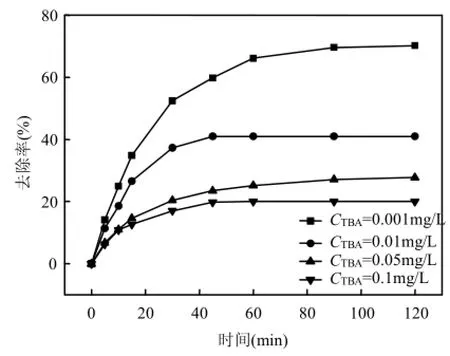
图7 自由基捕获剂对TCS去除的影响Fig.4 Effect of free radicals scavenger on TCS removal
作为自由基捕获剂,TBA可以清除超声空化气泡内的∙OH,阻止∙OH在空化气泡界面处积累和向水相的进一步扩散,使得超声产生的∙OH被TBA捕获,只有少量进入溶液.同时,TBA和它的产物在空化气泡内积累,降低了空化气泡中混合气体的比热容比,进而降低空化气泡崩溃时的相对温度和压力.这2种因素导致TBA的加入有效的抑制了超声对TCS的去除.可推断工艺去除中自由基氧化为TCS的主要降解途径.
2.7TCS降解机制
采用C18小柱,对400mL联用工艺去除TCS溶液进行 SPE富集,再用乙腈洗脱,富集液进行GC/MS扫描分析,结果见图8.

图8 超声波与氯胺联用降解TCS氧化产物的质谱扫描图Fig.4 MS spectra for main oxidized product of TCS in presence of ultrasonic and chloramines
由图 8可见,扫描图上分别在 10.425, 33.775min有2个相对明显的峰.其中, 33.775min时的出峰经鉴定为 TCS,10.425min时的出峰为TCS的氧化产物,该产物特征碎片为 m/z 63,98,126,162,鉴定为2,4-DCP.
Vikesland等[31]实验发现,氯胺与 TCS反应有5,6-Cl2-TCS、4,5-Cl2-TCS和4,5,6-Cl3-TCS的生成.Gao等[34-36]研究发现,在较低的羟基自由基浓度下,TCS的主要降解产物为2,4-DCP和多氯联苯二噁英,在较高羟基自由基浓度下,TCS与其中间产物都会被完全降解矿化.实验中除了2,4-DCP,未鉴定出这 3种物质,这可能是由于羟基自由基率先攻击这3个物质,亦有可能是超声波的其他作用促使该3个物质分解,有待进一步深入分析.
3 结论
3.1超声和氯胺联用去除 TCS具有协同效应,可以有效降解 TCS,降解符合一级反应动力学模型.超声波功率为 600W,氯胺浓度为 5mg/L 时,TCS去除率可达90.8%.
3.2联用工艺中TCS的去除随氯胺浓度升高呈现出先升高后降低的趋势,TCS去除率随TCS初始浓度的升高而下降,碱性环境有利于TCS的去除,TBA对TCS的降解起抑制作用,联用工艺降解TCS反应过程中有自由基参与降解.
3.3GC/MS鉴定表明2,4-DCP为TCS的降解产物.
[1] Singer H, Muller S, Tixier C, et a1. Triclosan: occurrence and fate of a widely used biocidc in the aquatic environment: field measurements in wastewater treatment plants, surface waters, and 1ake sediments [J]. Environ. Sci. Technol., 2002,36(23):4998-5004.
[2] Von der Ohe P C, Schmitt-Jansen M, Slobodnik J, et al. Triclosan -the forgotten priority substance? [J]. Environ. Sci. Pollut. R., 2012,19(2):585-591.
[3] Ingerslev F, Vaclavik E, Halling B. Sørensen. Pharmaceuticals and personal care products: a source of endocrine disruption in the environment?* [J]. Pure Appl. Chem., 2003,75(11/12):1881-1893.
[4] Canosa P, Morales S, Rodríguez I, et a1. Aquatic degradation of triclosan and formation of toxic chlorophenols in presence of low concentrations of free chlorine [J]. Anal. Bioanal. Chem., 2005, 383(7/8):1119-1126.
[5] Lores M, Llompart M, Sanchez-Prado L, et a1. Confirmation of the formation of dichlorodibenzo-p-dioxin in the photodegradation of triclosan by photo-SPME [J]. Anal. Bioanal. Chem., 2005,381(6):1294-1298.
[6] Marshall R, Royer T. Pharmaceutical compounds and ecosystem function: an emerging research challenge for aquatic ecologists [J]. Ecosystems, 2012,15:867-880.
[7] Braoudaki M, Hilton A C. Low level of cross-resistance between triclosan and antibiotics in Escherichia coli K-12and E.coli O55compared to E.coli O157 [J]. Fems Microbiol. Lett., 2004, 235(2):305-309.
[8] Brausch J M, Rand G M. A review of personal care products in the aquatic environment: environmental concentrations and toxicity [J]. Chemosphere, 2011,82(11):1518-1532.
[9] Schultz M M, Bartell S E, Schoenfuss H L. Effects of triclosan and triclocarban, two ubiquitous environmental contaminants,on anatomy, physiology, and behavior of the fathead minnow (pimephales promelas) [J]. Arch. Environ. Con. Tox., 2012,63(1):114-124.
[10] Yu J C, Kwong T. Y, Luo Q, Cai Z W. Photocatalytic oxidation of triclosan [J]. Chemosphere, 2006,65(3):390-399.
[11] Chen X J, Richard J, Liu Y L, et al. Ozonation products oftriclosan in advanced wastewater treatment [J]. Water Res., 2012,46(7):2247-2256.
[12] Behera S K, Oh S Y, Park H S. Sorption of triclosan onto activated carbon, kaolinite and montmorillonite: Effects of pH, ionic strength, and humic acid [J]. J. Hazard. Mater., 2010,179:684-691.
[13] Yao J J, Gao N Y, Li C, et a1. Mechanism and kinetics of parathion degradation under ultrasonic irradiation [J]. J. Hazard. Mater., 2010,175(1-3):138-145.
[14] Mehrdad A, Hashemzadeh R, Ultrasonic degradation of Rhodamine B in the presence of hydrogen peroxide and some metal oxide [J]. Ultrason. Sonochem., 2010,17(1):168-172.
[15] Dükkancl M, Gündüz G. Ultrasonic degradation of oxalic acid in aqueous solutions [J]. Ultrason. Sonochem., 2006,13(6):517-522.
[16] Sathiskumar P S, Madras Giridhar. Ultrasonic degradation of butadiene, styrene and their copolymers [J]. Ultrason. Sonochem., 2012,19(3):503-508.
[17] Chiha M, Hamdaoui O, Baup S, et al. Sonolytic degradation of endocrine disrupting chemical 4-cumylphenol in water [J]. Ultrason. Sonochem., 2011,18(5):943-950.
[18] Rominder P S S, Mohan N, Uthappa D, et al. Ultrasound assisted destruction of estrogen hormones in aqueous solution: Effect of power density, power intensity and reactor configuration [J]. J. Hazard. Mater., 2007,146(3):472-478.
[19] Ji Guodong, Zhang Baolong, Wu Yingchao. Combined ultrasound/ozone degradation of carbazole in APG1214surfactant solution [J]. J.Hazard. Mater., 2012,225-226:1-7.
[20] 魏 红,李 娟,李克斌,等.左氧氟沙星的超声/H2O2联合降解研究 [J]. 中国环境科学, 2013,33(2):257-262.
[21] 周作明,荆国华.超声波/H2O2/CuO协同氧化降解苯酚 [J]. 中国环境科学, 2006,26(3):280-283.
[22] Wu Qihua, Shi Honglan, Adams Craig D, et al. Oxidative removal of selected endocrine-disruptors and pharmaceuticals in drinking water treatment systems, and identification of degradation products of triclosan [J]. Sci. Total. Environ., 2012, 439:18-25.
[23] Song Weihua, O'shea K E. Ultrasonically induced degradation of 2-methylisoborneol and geosmin [J]. Water Res., 2007,41(12):2672-2678.
[24] Ifelebuegu A O, Onubogu J, Joyce E, et al. Sonochemical degradation of endocrine disrupting chemicals 17β-estradiol and 17α-ethinylestradiol in water and wastewater [J]. Int. J. Environ. Sci. Technol., 2014,11(1):1-8.
[25] Adewuyi Y G. Sonochemistry: environmental science and engineering applications [J]. Ind. Eng. Chem. Res., 2001,40(22):4681-4715.
[26] Adewuyi Y G. Sonochemistry in environmental remediation. 1. Combinative and hybrid sonophotochemical oxidation processes for the treatment of pollutants in water [J]. Environ. Sci. Technol., 2005,39(10):3409-3420.
[27] 汪雪娇.氯胺消毒特性及其副产物的生成研究 [D]. 上海:同济大学环境科学与工程学院, 2008:42-47.
[28] Wong-Wah-Chung P, Rafqah S, Voyard G, et al. Photochemical behaviour of triclosan in aqueous solutions: kinetic and analytical studies [J]. J. Photoch. Photobio. A., 2007,191(2/3):201-208.
[29] Pang Y I, Abdullah A Z, Bhatia S. Review on sonochemical methods in the presence of catalysts and chemical additives for treatment of organic pollutants in wastewater [J]. Desalination, 2011,277(1-3):1-14.
[30] Chowdhury P, Viraraghavan T. Sonochemical degradation of chlorinated organic compounds, phenolic compounds and organic dyes-A review [J]. Sci. Total. Environ., 2009.407(8):2476-2492.
[31] Ince N H, Gültekin I, Tezcanli-Güyer G. Sonochemical destruction of nonylphenol: Effects of pH and hydroxyl radical scavengers [J]. J. Hazard. Mater., 2009,172(2/3):739-743.
[32] Song Weihua, Cruz A A, Rein K, et al. Ultrasonically induced degradation of microcystin-LR and -RR: identification of products, effect of pH, formation and destruction of peroxides [J]. Environ. Sci. Technol., 2006,40(12):3941-3946.
[33] Greyshock A E, Vikesland P J. Triclosan reactivity in chloraminated waters [J]. Environ. Sci. Technol., 2006,40(8):2615-2622.
[34] Bester K. Fate of triclosan and triclosan-methyl in sewage treatment plants and surface waters [J]. Arch. Environ. Con. Tox., 2005,49(1):9-17.
[35] Gao Y P, Ji Y M, Li G Y, et al. Mechanism, kinetics and toxicity assessment of OH-initiated transformation of triclosan in aquatic Environments [J]. Water Res., 2014,49:360-370.
[36] Sanchez-Prado L, Barro R, Garcia-Jares C, et al. Sonochemical degradation of triclosan in water and wastewater [J]. Ultrason. Sonochem., 2008,15(5):689-694.
Degradation of triclosan in aqueous solution by using ultrasound combined with chloramine.
LI Qing-song1*, ZHOU Sheng-hui1,2, LI Guo-xin1, CHEN Guo-yuan1, MA Xiao-yan3, GAO Nai-yun4(1.Water Resources and Environmental Institute, Xiamen University of Technology, Xiamen 361005, China;2.College of Environmental Science and Engineering, Fujian Normal University, Fuzhou 350117, China;3.College of Civil Engineering and Architecture, Zhejiang University of Technology, Hangzhou 310014, China;4.National Key Laboratory of Pollution Control and Reuse, Tongji University, Shanghai 200092, China).
China Environmental Science, 2015,35(9):2670~2676
Ultrasound and chloramine combined process was employed in this paper to remove triclosan (TCS) in aqueous solution. The effects of several factors such as ultrasonic power, chloramine dosage, TCS initial concentration, pH and radical scavenger on TCS degradation were studied. Furthermore, the degradation products were identified and the degradation mechanism of TCS by combined process was discussed. The results indicated that the combination of ultrasound and chloramine can remove TCS effectively and possess significant synergetic effect on the degradation. The degradation rate of TCS could reach 90.8% within 120min under the conditions of ultrasonic power 600W, TCS initial concentration of 200μg/L, and chloramine dosage of 5mg/L. TCS degradation efficiency decreased with the raise of initial concentration of TCS, and tended to increase firstly and then decrease with the increase of chloramine concentration. Alkaline environment was conducive to the TCS removal, and the degration efficiency of TCS could reach 100% when pH value was 10.7. The presence of free radical scavenger TBA had an inhibitory effect on TCS degradation. The identification and recognition of degradation products by GC/MS indicated 2,4-dichlorophenol (2,4-DCP) was the main degradation products of TCS during the combined process.
triclosan;ultrasound;chloramine;degradation product
X703.1
A
1000-6923(2015)09-2670-07
2015-02-06
国家自然基金项目(51378446,51208468,51309197);福建自然基金项目(2013J01212);福建高校新世纪优秀人才计划项目(JA14227);厦门市科技局项目(3502Z20131157,3502Z20130039)
*责任作者, 副研究员, leetsingsong@sina.com
李青松(1979-),男,山东东明人,副研究员,博士,主要从事水处理理论与技术研究.发表论文40余篇.
