血塞通分散片指纹图谱研究
2015-08-10段红吉来国防杨光梅
段红吉,张 洪,来国防,杨光梅
(1.云南植物药业有限公司,云南 昆明650109;2.云南省食品药品检验所,云南 昆明650011)
血塞通分散片主要成分是从三七中提取的三七总皂苷和相应量辅料,精制而成(规格:50mg/片)。血塞通分散片主要成分为三七总皂苷(三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd)[1-2]。
血塞通分散片主要用于散瘀止血,消肿定痛;用于咯血,吐血,便血,崩漏,外伤出血,胸腹刺痛,跌扑肿痛,能活血化瘀、止痛。血塞通分散片能抑制由ADP 引起的家兔血小板聚集,扩张脑血管,使脑血流量增加,也具有抗血栓和抗凝血作用[3]。
指纹图谱是评价中药及其制剂质量稳定的有效方法,通过多成分的特征峰及多维的数据角度进行综合分析揭示血塞通分散片的指纹图谱特征[4-6],为血塞通分散片的质量控制提供新的参考方法。
1 材料与方法
1.1 材料与试剂
血塞通分散片(10 批批号分别为:20150501、20150502、20150503、20150601、20150602、20150603、20150605、20150606、20150607、20150608),样品由云南植物药业有限公司提供。
三七总皂苷对照品(含三七皂苷R16.9%、人参皂苷Rg128%、人参皂苷Re 3.8%、人参皂苷Rb129.7%、人参皂苷Rd 7.3%),购自中国食品药品检定研究院,批号:110870-201002。纯化水为屈臣氏纯化水;乙腈(色谱纯),甲醇(色谱纯),其余试剂为分析纯。
1.2 仪器与设备
Agilent1260 液相色谱仪(配有二极管阵列检测器、四元梯度泵、在线脱气装置、自动进样器),Chem-Station 工作站(Agilent 科技有限公司),用十八烷基硅烷键合硅胶为填充剂的色谱柱作为分析柱[7-8]。
1.3 对照品与供试品制备
1.3.1 对照品溶液的制备
取三七总皂苷对照提取物适量,精密称定,加70%甲醇使溶解,并稀释制成每1mL 含2.5mg 的溶液,即得。
1.3.2 供试品溶液的制备
本制剂为三七总皂苷加适量赋形剂制成的片剂。因《中华人民共和国药典》2010 版一部“三七”项药材中皂苷类成分含量测定时选用甲醇为提取溶剂,“三七总皂苷”项提取物指纹图谱时选用70%甲醇为提取溶剂,且本制剂中多数辅料在乙醇中不易溶解,故选择此3 种溶剂进行提取考察。即:取重量差异项下的同一批次样品,研细,称取适量(约相当于三七总皂苷25mg)3 份,各置10mL 量瓶中,分别精密加入甲醇、乙醇、70%甲醇至刻度,称定重量,超声处理(功率250W,频率33kHz)20min,放冷,再称定重量,并用相应溶剂补足减失的重量,作为供试品溶液。同时,考察了3 个不同提取时间对本品指纹图谱的影响。即:取重量差异项下的同一批次样品,研细,称取适量(约相当于三七总皂苷25mg)3 份,各置10mL 量瓶中,加入甲醇至刻度,称定重量,分别超声提取(功率250W,频率33kHz)10,20,30min 后,放冷,再称定重量,并用甲醇补足减失的重量,作为供试品溶液。按1.4 项的色谱条件,分别吸取对照品溶液和供试品溶液各20μL 进样,记录色谱图,测定其相似度,结果见表1。
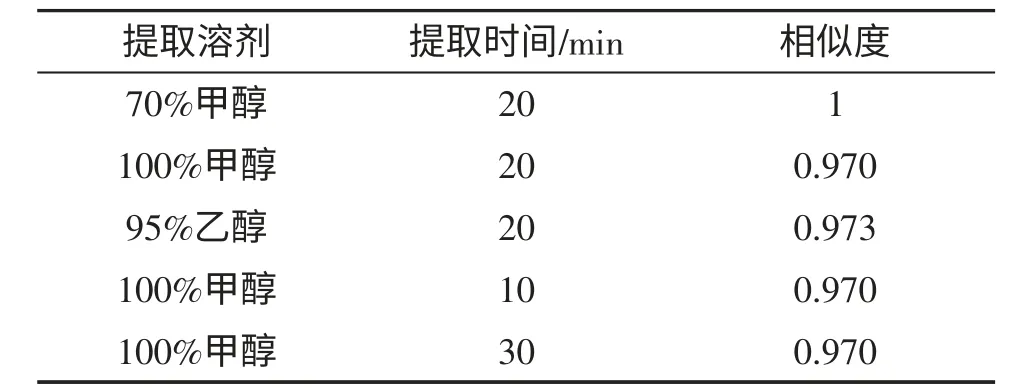
表1 提取因素考察
结果表明3 种提取溶剂及提取时间,对图谱无明显影响。故选择70%甲醇为提取溶剂,超声时间为10min,并将此条件列入正文。
1.3.3 阴性对照溶液的制备
按处方比例及制法,制备缺三七总皂苷对照药品。再按上述所得供试品溶液制备方法制成缺三七总皂苷的阴性对照溶液。
1.4 色谱条件与系统适用性试验
1.4.1 色谱柱、检测波长的选择
参照《中华人民共和国药典》2010 版一部“三七总皂苷”指纹图谱项,选用十八烷基硅烷键合硅胶为填充剂的色谱柱作为分析柱,检测波长为203nm。
1.4.2 流动相比例的选择
照《中华人民共和国药典》2010 版一部“三七总皂苷”指纹图谱项,选择以乙腈为流动相A,以水为流动相B,进行梯度分析。以分离度、峰的对称性、保留时间等为评价指标。结果表明以下表流动相比例较好,见表2。

表2 流动相比例的选择
1.4.3 系统适用性试验
见图1-3,根据供试品的HPLC 图谱,色谱柱的理论塔板数以人参皂苷Rg1峰计均不低于6 000。人参皂苷Rg1、人参皂苷Re 的分离度均大于1.5。
图1 对照品HPLC 图谱
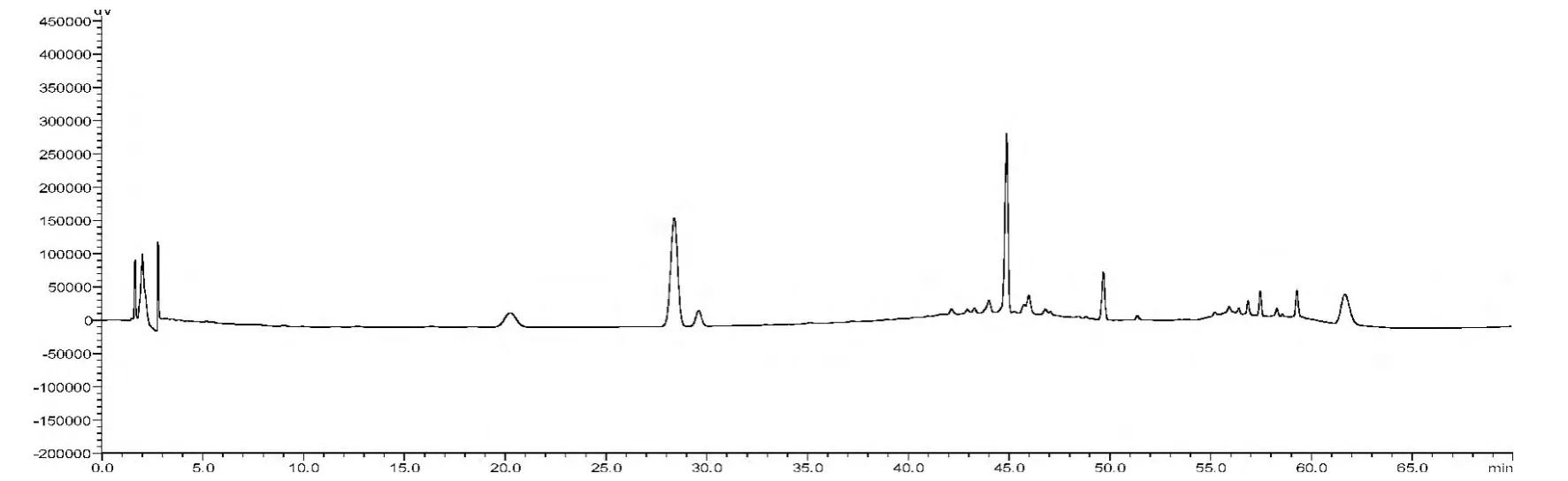
图2 供试品HPLC 图谱
图3 阴性对照药品HPLC 图谱
2 指纹图谱及技术参数
取10 批不同生产批次的血塞通分散片,照2.2所得方法进行处理,并按1.4 项的色谱条件,分别吸取对照品溶液和供试品溶液各20μL 进样,记录色谱图,记为S1-S11,其中S1对照品色谱,S2-S11分别为批号20150501、20150502、20150503、20150601、20150602、20150603、20150605、20150606、20150607、20150608 的血塞通分散片图谱,见图4。利用《中药色谱指纹图谱相似度评价系统2004A 版》软件,采用中位数法,时间窗为0.1,对图谱信息进行相似度评价及共有峰的共有图谱信息拟合,得到血塞通分散片的HPLC 指纹图谱,然后确定共有峰[9]。计算单峰面积占总峰面积的百分比,并以保留时间和峰面积较为平稳的人参皂苷Rg1色谱峰作为参比峰,计算各共有指纹峰的相对保留时间和相对峰面积的值。
2.1 指纹图谱
10 批血塞通分散片供试品生成共有峰32 个。其中,对照品与供试品生成共有峰29 个。选定其中5 个共有峰作为共有指纹峰,指纹峰的选择原则是匹配度为100%,相对峰面积比值RSD≤10%,相对峰面积比值≥0.1[10]。经单峰定位后,确定此5 个峰,按保留时间由小到大,依次分别为三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd,为三七总皂苷中的主要有效成分,见图5-6。
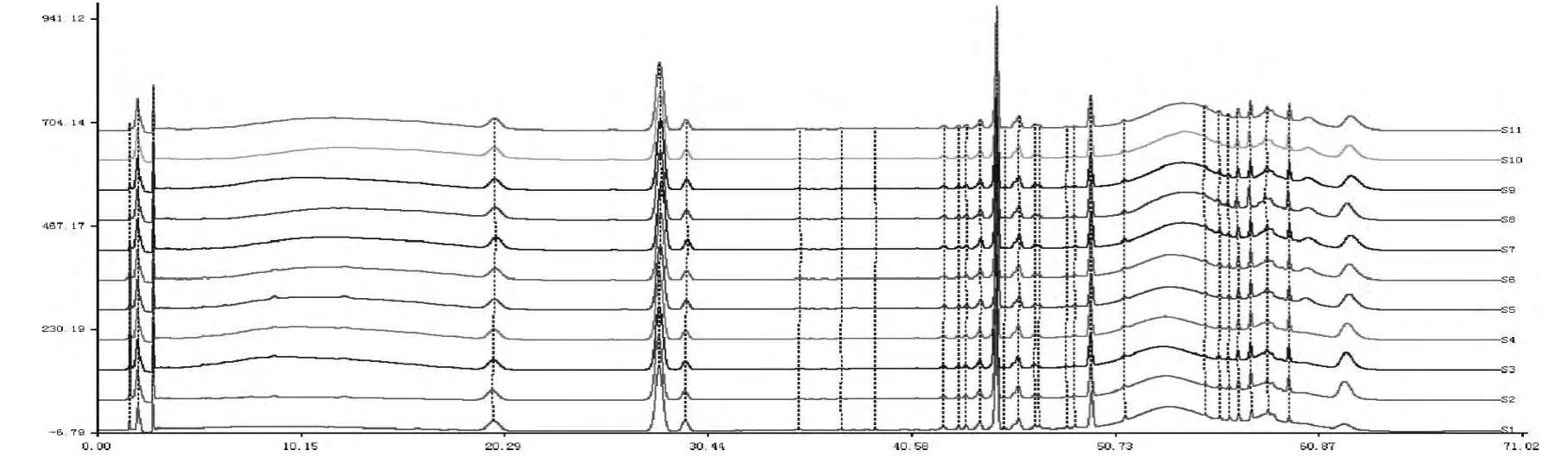
图4 对照品及10 批供试品色谱图
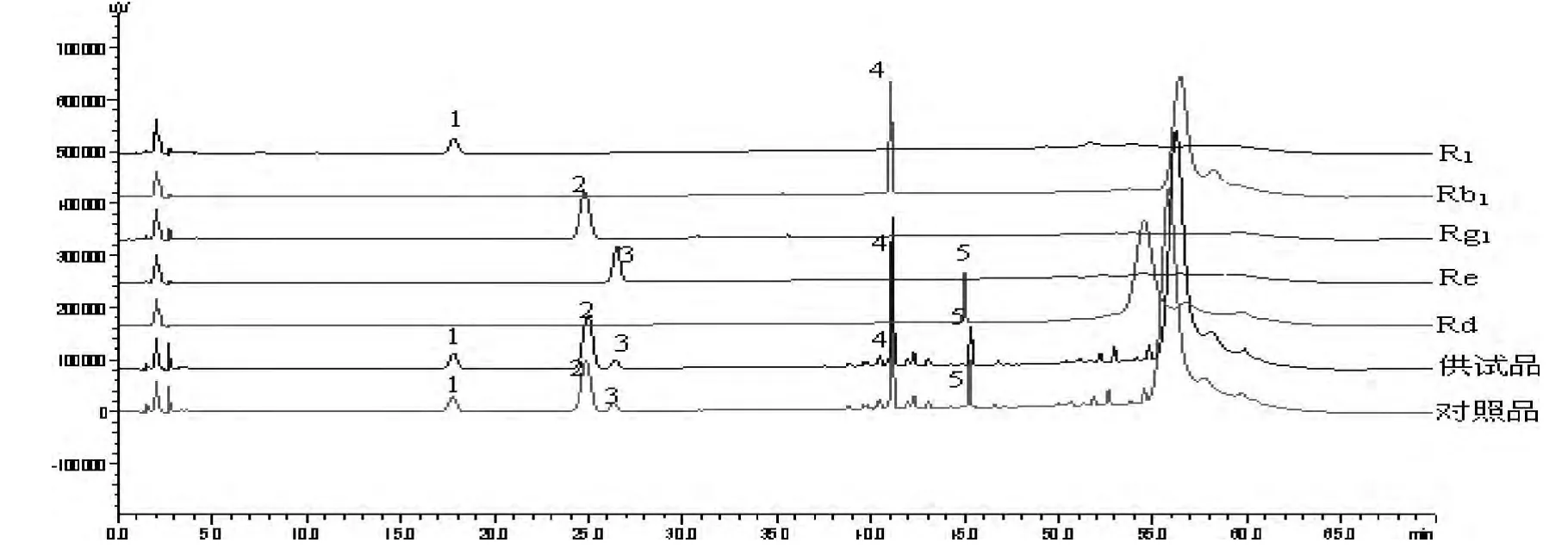
图5 单峰定位结果
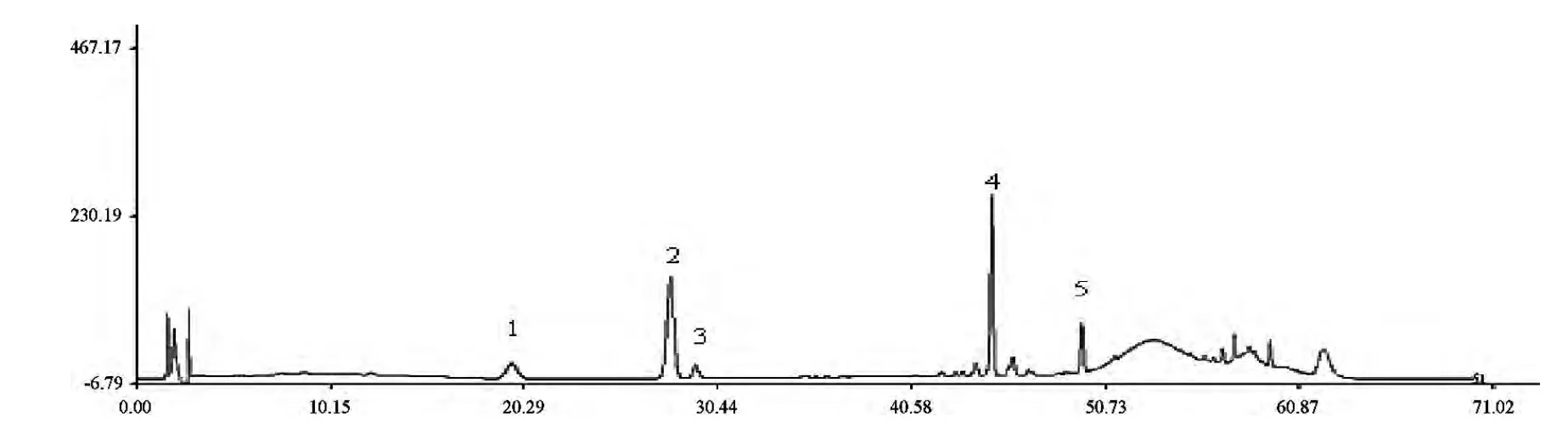
图6 共有指纹峰图谱
2.2 共有峰的峰号及保留时间
1 号峰,保留时间:19.774,为三七皂苷R1
2 号峰,保留时间:28.029,为人参皂苷Rg1
3 号峰,保留时间:29.335,为人参皂苷Re
4 号峰,保留时间:44.810,为人参皂苷Rb1
5 号峰,保留时间:49.503,为人参皂苷Rd以保留时间和峰面积较为平稳的人参皂苷Rg1色谱峰作为参比峰,计算各共有指纹峰峰面积的比值,见表3。
结果表明,5 个峰的相对峰面积比值RSD 小于5%,峰面积比值均在允许范围(准许误差范围是利用《中药色谱指纹图谱相似度评价系统2004A 版》软件所得)内,5 个指纹峰的相对保留时间一致性较好,指纹图谱具有相似度较高的共有峰。
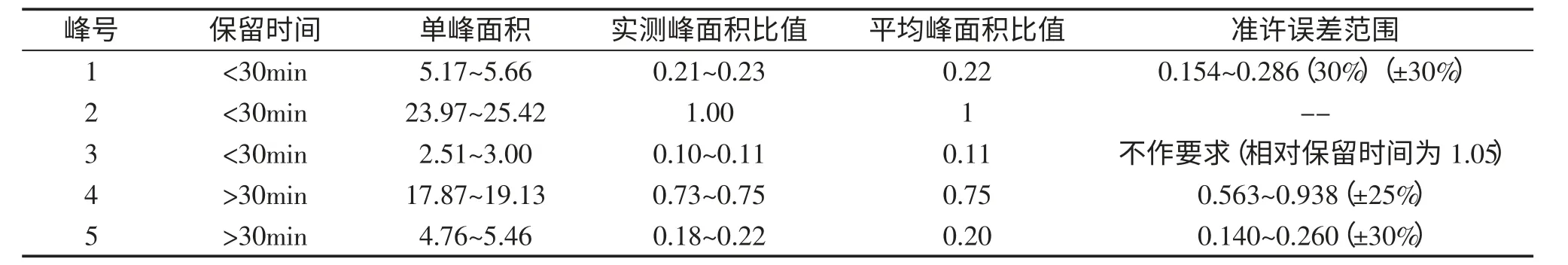
表3 共有指纹峰峰面积的比值
2.3 非共有峰
非共有峰面积占总峰面积10%~15%.
3 方法学考察
3.1 专属性试验
分别精密吸取混合对照品溶液、供试品溶液、阴性对照溶液各20μL,进样,记录色谱图,见图1-3。在该色谱条件下的分离效果较好,对照品图谱与供试品图谱,相似度为0.98。阴性样品在于对照品及供试品出峰相应的保留时间处未见明显色谱峰,表明本品中辅料成分对三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd 的测定无干扰。
3.2 精密度
取同一批次血塞通分散片,研细,称取适量(约相当于三七总皂苷25mg),精密称定,照2.2 所得方法进行处理,并按1.4 项的色谱条件,连续进样5次,每次20μL。记录色谱图,记为S1-S5。利用《中药色谱指纹图谱相似度评价系统2004A 版》软件,对图谱信息进行相似度评价,计算相似度[11]。以人参皂苷Rg1色谱峰作为参比峰,计算各共有指纹峰的相对保留时间和相对峰面积的RSD 值,结果见表4。
3.3 重复性
取重量差异项下本品,研细,称取适量(约相当于三七总皂苷25mg)6 份,照2.2 所得方法进行处理,并按1.4 项的色谱条件,吸取供试品溶液各20μL进样,记录色谱图,记为S1-S6。利用《中药色谱指纹图谱相似度评价系统2004A 版》软件,采用中位数法,时间窗为0.1,对图谱信息进行相似度评价,计算相似度。以保留时间和峰面积较为平稳的人参皂苷Rg1色谱峰作为参比峰,计算各共有指纹峰的相对保留时间和相对峰面积的RSD 值,结果见表5。
3.4 稳定性
取同一批次血塞通分散片,研细,称取适量(约相当于三七总皂苷25mg),精密称定,照2.2 所得方法进行处理,并按1.4 项的色谱条件,分别于0,2,4,8,12,16 h 精密吸取同浓度供试品溶液20μL 进样,记录色谱图,记为S1-S6。利用《中药色谱指纹图谱相似度评价系统2004A 版》软件,采用中位数法,时间窗为0.1,对图谱信息进行相似度评价,计算相似度。以保留时间和峰面积较为平稳的人参皂苷Rg1色谱峰作为参比峰,计算各共有指纹峰的相对保留时间和相对峰面积的RSD 值,结果见表6。

表4 精密度考察
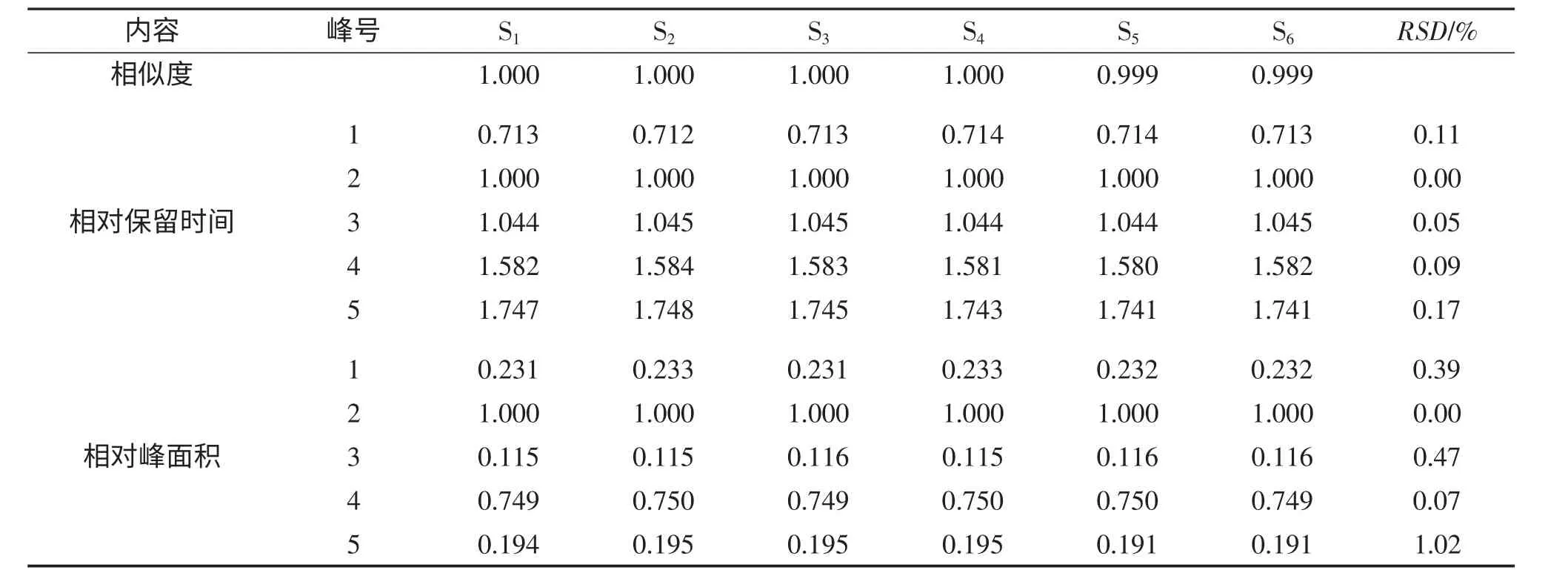
表5 重复性测定结果
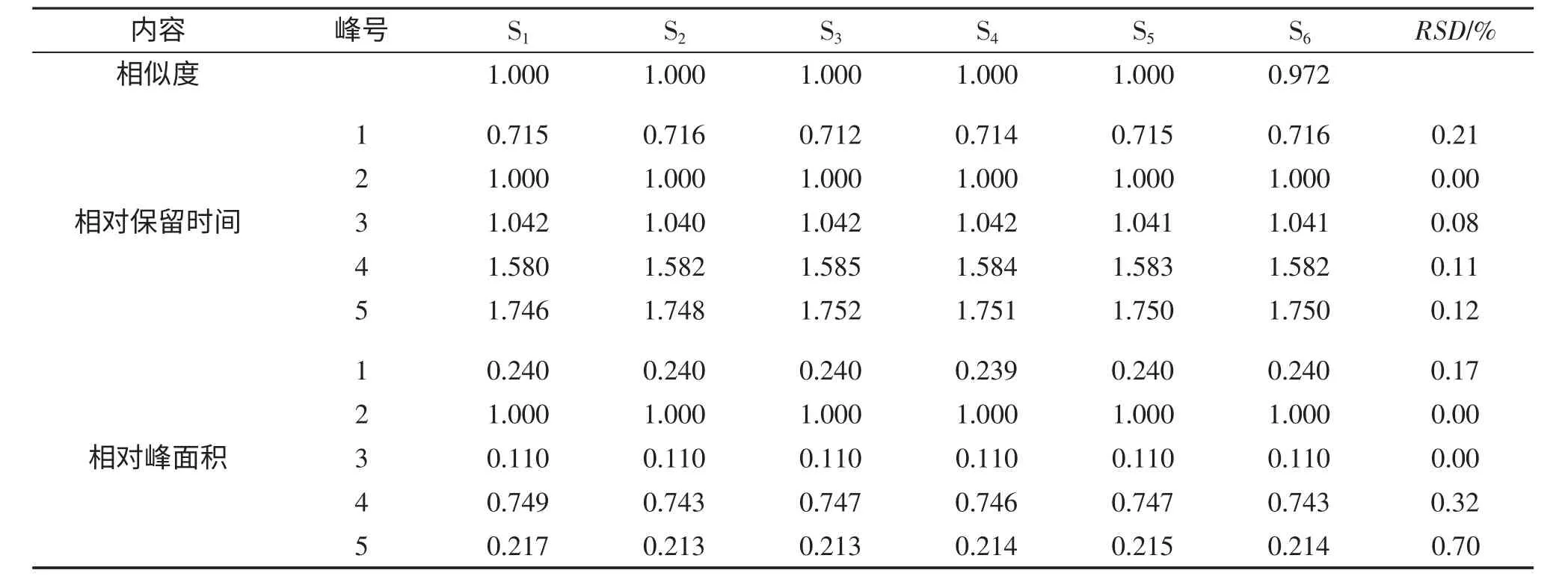
表6 稳定性考察
4 总结
本文以三七皂苷R1、人参皂苷Rg1、Re、Rb1、Rd峰为参照峰,建立了血塞通分散片HPLC 指纹图谱。应用“中药色谱指纹图谱超信息特征评价系统”软件对血塞通分散片HPLC 指纹图谱定性、定量信息进行多维的数据分析。采用双定性相似度(SF 和SF’)和双定量相似度(C 和P)来评价血塞通注射液指纹图谱的化学成分分布比例特征和含量分布特征。评价出10 批血塞通注射液质量完全合格。本实验所建立的血塞通注射液指纹图谱具有良好的精密度和重现性,结合双定性双定量相似度评价法能较好地控制其质量[12-15]。
[1] 国家药典委员会. 中华人民共和国药典(一部)[M]. 北京:化学工业出版社,2005:10.
[2] 丁婷. 血塞通分散片制剂工艺的研究[J]. 长沙医学院学报,2014,12(1):29-36.
[3] 张晓青,张阳根. 血塞通分散片对心脑保护作用的实验研究[J]. 中国现代医学杂志,2005,15(10):1503-1505.
[4] 杨雪梅,刘旭,严轶琛,等. 三七药材指纹图谱的研究[J].第一军医大学学报,2004,24(12):1410 -1411.
[5] 黎琼红,张国刚. 三七药材的指纹图谱[J]. 沈阳药科大学学报,2006,23(4):229 -232.
[6] 刘晓丽,周清,孙国祥. 血塞通注射液HPLC 数字化指纹图谱研究[J]. 辽宁中医杂志,2012,39(11):2238-2241.
[7] 代龙. HPLC 法测定血塞通分散片中三七皂苷R1及人参皂苷Rg1、Rb1的含量[J]. 奇鲁药事,2009,28(6):333-335.
[8] 汪存存. 血塞通分散片的含量测定方法分析[J]. 国际医药卫生导报,2008,14(6):58-63.
[9] 王芳,张贺,葛平,等. 基于高效液相色谱技术的中药制剂指纹图谱构建及应用现状[J]. 中国基层医药,2014,21(16):2548-2550.
[10] 丁红霞,杨静,吴宗耀,等. 中药质量控制中色谱指纹图谱技术探究[J]. 河南中医,2013,33(7):1155-1156.
[11] 许丹萍. 中药色谱指纹图谱相似度的计算[J]. 数学学习与研究,2012(13):119.
[12] 李昕,王月茹,马利,等. 中药色谱指纹图谱在中药质量评价中的应用[J]. 生物医学工程学杂志,2012,29(1):192-196.
[13] 田立权. 中药指纹图谱的主要技术分析手段概论[J]. 民营科技,2011(2):98.
[14] 任非,智丽敏,付颖,等. 中药指纹图谱色谱技术及其在质量控制中的应用与研究[J]. 河北医药,2010,32(21):3075-3078.
[15] 梁逸曾,王兵,曾茂茂,等.色谱指纹图谱与中药质量控制[J].世界科学技术—中医药现代化,2010,12(1):94-98.
