MnO2-CuO-CeO2复合催化剂的制备及处理化工集装罐清洗废水的应用
2015-07-25李桂菊朱丽香孟攀攀
李桂菊,田 明,朱丽香,孟攀攀
(天津市海洋资源与化学重点实验室,天津科技大学海洋科学与工程学院,天津 300457)
MnO2-CuO-CeO2复合催化剂的制备及处理化工集装罐清洗废水的应用
李桂菊,田 明,朱丽香,孟攀攀
(天津市海洋资源与化学重点实验室,天津科技大学海洋科学与工程学院,天津 300457)
针对非均相贵重金属催化剂成本高,非均相过渡金属催化剂性能良好、成本低,但使用寿命短、易流失的特点,研制高效复合MnO2-CuO-CeO2非均相过渡金属催化剂.采用正交实验对催化剂制备过程中的n(Cu)∶n(Mn)、Ce的摩尔分数、焙烧温度、焙烧时间进行探讨,确定最佳制备条件,并对其结构和组成通过扫描电镜分析、X射线衍射分析及热重分析进行表征.用该催化剂催化氧化模拟苯酚废水,对催化剂用量、氧化剂H2O2用量、反应温度、反应时间进行优化,确定最佳反应条件并利用其进行降解化工集装罐清洗废水的应用研究.研究表明催化剂MnO2-CuO-CeO2的最佳制备条件为:n(Cu)∶n(Mn)=4∶6、Ce的摩尔分数为10%、焙烧温度为600,℃、焙烧时间为4,h.催化氧化法处理苯酚废水的最佳工艺参数:催化剂用量0.8,g/L、H2O2用量与COD比值为3、反应温度170,℃、反应时间1,h.化工集装罐清洗废水COD去除效果显著,COD去除率达到95%左右.
MnO2-CuO-CeO2催化剂;制备方法;催化氧化;集装罐清洗废水
随着物流业的迅速发展,越来越多的化工货物利用集装罐装运,装过危险货物或其他化学品的集装罐不同程度地受到所装货物的污染.按国际货物运输的规定,集装罐在具备清洁、干燥、无异味的基本条件后才能再次使用,因此,开展化工集装罐清洗业务势在必行.洗罐中产生的废水种类多、浓度高,难生物降解,容易对环境造成污染.其危害不亚于各种工业废水,对周围环境的污染日益严重[1-3],迫使人们从科学上和技术上重视新的水净化技术的开发[4-7],以保护自然资源和环境.多组分催化剂湿式催化氧化处理(CWO)是一项非常有前景且可行的技术,能有效矿化许多难生物降解污染物、有害或难以用传统生物方法处理的有机底物[8-9].但是,贵金属催化剂需要高温(>473,K)条件下才能进行湿式催化氧化,从经济角度考虑不适合常规应用[10].因此,研制一种有效而价格低廉的湿式催化氧化催化剂迫在眉睫.铁、铜和锰催化剂被认为是非常有效的CWO催化剂[11-14],因此,与贵金属系催化剂相比,多组分过渡金属仍然是更佳的选择.
本研究通过沉淀法制备了MnO2-CuO-CeO2催化剂,确定了制备方法及最佳制备条件,并对催化剂的性能进行了表征.利用该催化剂进行了应用实验,为环境中难降解的有机污染物的去除提供了一个简单、方便、有工业应用前景的新方法.
1 实 验
1.1 实验装置
本实验采用大连通达反应釜厂生产的磁力驱动高压反应釜,主要结构包括热电偶、高压釜体、加热外套、磁力搅拌器、控制仪等,具体结构如图1所示.

图1 湿式催化氧化反应装置简图Fig. 1 Diagram of wet oxidation reactor
1.2 催化剂的制备与表征
1.2.1 催化剂的制备方法
将1,mol/L的硝酸铜溶液、1,mol/L硝酸锰溶液按一定比例混合,分别在每种比例的混合溶液中加入一定量的浓度为1,mol/L的硝酸铈溶液,在恒温磁力搅拌器上利用电节点温度计控温,边搅拌边加热至所需反应温度(50,℃),到达反应温度后待温度稳定,以5,s一滴的速度向混合盐溶液中滴加沉淀剂(氨水)并不断搅拌,直到溶液pH达到8.7后停止沉淀剂的滴入,保持反应温度并继续搅拌陈化3,h,达到陈化时间后,撤走热源继续搅拌至室温,将冷却后的混合物用蒸馏水进行充分滤洗,所得滤饼放入恒温干燥箱内在105,℃的温度下烘干过夜,烘干后用研钵研成粉末,再放入马弗炉中在实验所设定的温度下焙烧一定时间,制得MnO2-CuO-CeO2复合催化剂.
1.2.2 催化剂制备条件的筛选
采用正交实验考察制备因素n(Cu)∶n (Mn)、Ce的摩尔分数、焙烧温度、焙烧时间对催化活性的影响.表1为4因素3水平正交实验的设计.

表1 正交实验的设计Tab. 1 Design of the orthogonal experiment
1.2.3 催化剂的表征
为了观察催化剂表面细致的形貌,了解催化剂表面的微观结构,采用JEOL公司JSM-6380LV型扫描电镜对催化剂进行形貌分析.
采用美国TA公司的Q50TGA型热分析仪进行热重实验,实验中通入流量为60,mL/min的氮气以保持动态气氛,实验终温为900,℃,升温速率为10,℃/min.通过热重分析可以分析催化剂在热处理过程中的失水、分解、结晶等现象.
采用日本Rigaku公司D/max 2500型X射线衍射仪测定催化剂的晶体结构.测试条件:Cu靶(λ= 1.540,6,nm)作为X射线源,扫描速度为8°/min,扫描范围10°~90°.
1.3 工艺条件的确定
利用自制的催化剂,探讨催化剂用量、氧化剂H2O2用量、反应温度、反应时间对模拟苯酚废水的湿式催化氧化降解的影响.实验采用单因素实验法,初始工艺条件为:反应温度170,℃、反应时间1,h、H2O2投加量为原水COD的3倍、催化剂用量为1.0,g/L.改变其中任意一个条件,以处理后COD去除率为评价指标,进行单因素实验,确定适宜的工艺参数.
1.4 应用实验
利用自制的多组分催化剂,对化工集装罐清洗下来的10种清洗废水,在最佳工艺条件下进行催化氧化应用实验,通过COD的去除率,评价其实际应用的前景.
2 结果与讨论
2.1 催化剂制备条件的筛选
根据4因素3水平正交实验,制备9种不同的催化剂,并在相同反应条件下,即:取200,mL苯酚模拟废水(初始COD为1,600,mg/L,pH为5.16)、按照1.0,g/L加入催化剂、过氧化氢加入量为COD的3倍、反应温度为170,℃、反应时间为1,h,通过COD的去除率确定9种催化剂的催化性能,正交实验结果见表2.

表2 正交实验结果Tab. 2 Results of the orthogonal test
由表2可知4个影响因素的显著水平为:n(Cu)∶n(Mn)>焙烧时间>焙烧温度>Ce的摩尔分数.金属Ce对催化剂的性能影响最小,是因为其主要作用是防止催化剂活性组分的流失,提高催化剂的使用寿命[1].由表2可以确定催化剂制备条件最佳组合为A3B2C3D2,即,n(Cu)∶n(Mn)=4∶6、Ce的摩尔分数20%、焙烧温度600,℃、焙烧时间4,h.以最佳组合制备的催化剂处理模拟废水后出水COD为178.63,mg/L,COD的去除率为88.84%.与第7组相比较,最佳组合去除率略低,最终确定铜锰铈系列催化剂最佳制备条件为n(Cu)∶n(Mn)=4∶6、Ce的摩尔分数10%、焙烧温度600,℃、焙烧时间4,h.
2.2 催化剂的表征
2.2.1 扫描电镜分析
图2是最佳条件下制备的催化剂的扫描电镜图.由图2可知:该催化剂颗粒非常细,有晶体结构.研究[15]表明催化剂中的小半径的Cu、Mn取代了CeO2中的大半径的Ce,进入到CeO2晶格中,从而产生很多的表面空位,形成缺陷结构,加快了供氧速度,从而提高了催化剂活性.

图2 催化剂的扫描电镜图Fig. 2 SEM photograph of the catalysts
2.2.2 X射线衍射分析
最佳条件下制备的催化剂的XRD图谱如图3所示.由图3可知:该催化剂的活性成分为CeO2、CuO和MnO2.在600,℃焙烧后,3种金属都处于高价态,因此其活性会较高[16].

图3 催化剂的XRD图谱Fig. 3 XRD pattern of the catalysts
2.2.3 热重分析
对最佳制备方法制备的催化剂进行热重分析.结果如图4所示.图4中TG曲线上在700~830,℃有一个显著失重,可能是由于3种金属氧化物的受热分解造成的.通过各催化剂的TG曲线可以看出,该催化剂热稳定性好.
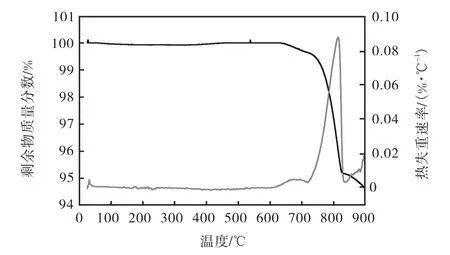
图4 催化剂TG-DTG曲线Fig. 4 TG-DTG curve of the catalysts
2.3 工艺条件的选择
2.3.1 催化剂用量
取质量浓度为0.4,g/L(COD约为1,000,mg/L)的模拟苯酚废水200,mL,加入3,g/L的H2O2作为氧化剂,催化剂用量分别取0.5、0.8、1.0、1.5,g/L,将混合液放入反应釜内,调节反应温度为170,℃,反应时间为1,h,考察其对COD的去除率的影响,确定最佳的催化剂用量,结果如图5所示.
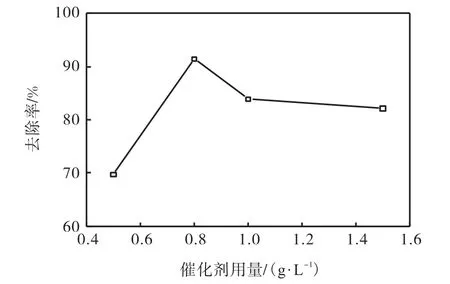
图5 催化剂用量对COD去除率的影响Fig. 5 Effect of the dosage of catalyzer on COD removal rate
由图5可知:催化剂用量由0.5,g/L增加到0.8,g/L,出水COD去除率由69.7%升到91.4%,继续增加催化剂用量,出水COD去除率则开始下降;当催化剂用量为1.5,g/L时,出水COD去除率降到82.1%,所以最佳催化剂用量为0.8,g/L.
分析原因,Mn+的催化氧化反应机理为:Mn+首先与H2O2作用产生M(n-1)+和HO2·,M(n-1)+和HO2·再分别与H2O2反应产生氧化性更强的HO·,HO·进攻有机物RH,引发自由基反应,达到氧化降解有机物的目的.反应机理[12]表示如下:


过量的Mn+抑制反应机理中式(2)的正向进行,因而在相同的反应时间内不仅使产生HO·减少,而且使反应体系中存在大量的M(n-1)+而发生式(4),消耗HO·,导致苯酚去除率稍有所降低.
2.3.2 氧化剂H2O2用量
取质量浓度为0.4,g/L(COD约为1,000,mg/L)的模拟苯酚废水200,mL,加入0.8,g/L催化剂,氧化剂用量为变量,分别控制H2O2用量为2、3、4、5,g/L(即H2O2用量与原水COD的比值分别为2、3、4、5),将混合液放入反应釜内,调节反应温度为170,℃,反应时间为1,h,考察其对COD的去除情况,结果如图6所示.
从图6可以看出:随着H2O2用量的增加,处理后苯酚废水的COD去除率增加,当H2O2用量为3,g/L时,COD去除率达到最高值91.7%;而继续增加H2O2用量处理后苯酚废水的COD去除率反而降低.即,H2O2用量与原水COD的比值为3时,COD去除效果最好.分析原因,当H2O2用量较低时,由式(2)知,产生HO·的数量自然就减少.另外,由于H2O2是HO·的捕捉剂,H2O2用量过高时又会使产生的HO·大大减少.
2.3.3 反应温度
取质量浓度为0.4,g/L(COD约为1,000,mg/L)的模拟苯酚废水200,mL,加入0.8,g/L催化剂,加入3,g/L H2O2,将混合液放入反应釜内,分别在130、150、170、190,℃下反应,反应时间为1,h,考察其对COD的去除情况,结果如图7所示.
由图7可以看出:当温度从130,℃升到170,℃,苯酚废水COD去除率从58.3%明显增加到90.1%,说明反应温度对H2O2发生均裂产生HO·的影响很大,反应温度越高,吸收的能量越高,O—O越容易断裂,产生的HO·越多,对氧化降解苯酚越有利.在170,℃后再提高温度,COD去除率基本不变,而且在170,℃去除率已经达到90.1%,从能耗角度考虑,选择最佳反应温度为170,℃.
2.3.4 反应时间
取质量浓度为0.4,g/L(COD约为1,000,mg/L)的模拟苯酚废水200,mL,加入0.8,g/L催化剂,加入3,g/L H2O2,将混合液放入反应釜内,反应温度为170,℃,将反应时间作为变量,反应0.5、1、1.5、2,h,考察其对COD去除率的影响,结果如图8所示.由图8可知:反应体系的苯酚废水COD去除率随时间的增加先不断上升,当去除率达到91.4%以后略有下降.理论上讲,反应时间越长对降解苯酚越有利,从经济角度考虑,选择最佳反应时间为1,h.

图8 反应时间对COD去除率的影响Fig. 8 Effect of reaction time on COD removal rate
2.4 应用实验
选10种典型的化工集装罐清洗废水,利用自制的催化剂,根据上述实验得出的最佳操作条件(催化剂用量0.8,g/L、氧化剂H2O2用量与COD的比值为3、反应温度170,℃、反应时间1,h)进行催化氧化处理,结果见表3.

表3 清洗废水的水质指标Tab. 3 Water quality index after treatment
从表3可以看出,湿式催化氧化工艺对化工集装罐清洗废水的处理效果非常显著,COD去除率达到95%左右.
3 结 论
(1)通过沉淀法制备复合非均相MnO2-CuO-CeO2催化剂.通过正交实验得出各影响因素对催化剂制备的显著水平为:n(Cu)∶n(Mn)>焙烧时间>焙烧温度>Ce的摩尔分数.催化剂制备的最优条件是:n(Cu)∶n(Mn)=4∶6、Ce的摩尔分数10%、焙烧温度600,℃、焙烧时间4,h.其活性成分为CeO2、CuO和MnO2.
(2)利用该催化剂,在催化剂用量0.8,g/L、氧化剂H2O2用量与COD的比值为3、反应温度170,℃、反应时间1,h的工艺条件下对常见的10种化工集装罐清洗废水进行催化氧化处理,处理效果显著,COD去除率都达到95%左右.处理后的水可以作为化工集装罐清洗水回用,实现节能减排.
[1] Li G J,Lei G X,Zhang J,et al. Catalytic wastewater treatment from chemical container cleansing[J]. Russian Chemical Bulletin,2010,59(8):1523-1527.
[2] 高廷耀,陈洪斌,夏四清,等. 我国水污染控制的思考[J]. 给水排水,2006,32(5):9-13.
[3] 雷岗星,李桂菊,朱丽香. 湿式催化氧化法处理罐式集装箱清洗废水的研究[J]. 水处理技术,2009,35(4):89-92.
[4] Comninellis C,Pulgarin C. Anodic oxidation of phenol for waste water treatment[J]. Journal of Applied Electrochemistry,1991,21(8):703-708.
[5] Alnaizy R,Akgerman A. Advanced oxidation of phenolic compounds[J]. Advances in Environmental Research,2000,4(3):233-244.
[6] 蔡乃才,简翠英,董庆华. TiO2光催化剂表面载铂方法的研究[J]. 催化学报,1989,10(2):137-142.
[7] 钟理,陈建军. 高级氧化处理有机污水技术进展[J].工业水处理,2002,22(1):1-5.
[8] Arena F,Trunfio G,Negro J,et al. Optimization of the MnCeOxsystem for the catalytic wet oxidation of phenol with oxygen(CWAO)[J]. Applied Catalysis B:Environmental,2008,85(1/2):40-47.
[9] Miranda B,Díaz E,Ordóñez S,et al. Oxidation of trichloroethene over metal oxide catalysts:Kinetic studies and correlation with adsorption properties[J]. Chemosphere,2007,66(9):1706-1715.
[10] 董岳刚,严莲荷,赵晓蕾,等. 湿式催化氧化法废水处理中催化剂和实验条件的优选[J]. 精细化工,2002,19(3):149-151.
[11] 张文兵. 均相和非均相高级氧化技术处理水中有机污染物的研究[D]. 广州:中国科学院研究生院(广州地球化学研究所),2003.
[12] 何莼,奚红霞,张娇,等. 沸石和活性炭为载体的Fe3+和Cu2+型催化剂催化氧化苯酚的比较[J]. 离子交换与吸附,2003(4):289-296.
[13] Hočevar S,Krašovec U O,Orel B,et al. CWO of phenol on two differently prepared CuO-CeO2catalysts[J]. Applied Catalysis B:Environmental,2000,28(2):113-125.
[14] Neri G,Pistone A,Milone C,et al. Wet air oxidation of p-coumaric acid over promoted ceria catalysts [J]. Applied Catalysis B:Environmental,2002,38(4):321-329.
[15] Shan W J,Feng Z C,Li Z L,et al. Oxidative steam reforming of methanol on Ce0.9Cu0.1Oycatalysts prepared by deposition-precipitation,coprecipitation,and complexation-combustion methods[J]. Journal of Catalysis,2004,228(1):206-217.
[16] 潘履让. 固体催化剂的设计与制备[M]. 天津:南开大学出版社,1991.
责任编辑:周建军
Preparation of Composite Catalyst MnO2-CuO-CeO2and Treatment of Wastewater from Chemical Container Cleaning
LI Guiju,TIAN Ming,ZHU Lixiang,MENG Panpan
(Tianjin Key Laboratory of Marine Resources and Chemistry,College of Marine Science and Engineering,Tianjin University of Science & Technology,Tianjin 300457,China)
Aiming at the high cost of heterogeneous catalysts of noble metals and theshort service life of heterogeneous transition metal catalysts which are easy to drain,an efficient heterogeneous transition metal catalyst was studied with MnO2-CuO-CeO2as the active component. The effects of the molar ration of Cu-Mn,molar percentage of Ce,calcination temperature and calcination time on the performance of the composite catalyst MnO2-CuO-CeO2were explored. The optimal preparation conditions were determined with orthogonal experiment and the structure and composition of the catalysts were characterized with scanning electron microscopy(SEM),X-ray diffraction(XRD)and thermal analysis(TA). The technical parameters such as the dosages of oxidant(H2O2)and catalyst,reaction time and temperature were studied by treating simulated phenol wastewater. Eventually,practial research on the treatment of the cleaning wastewater of containers was carried out under the optimal technological conditions. The results showed that the optimum preparation conditions were achieved when the molar ratio of Cu-Mn was 4∶6,the molar percentage of Ce was 10%,calcination temperature 600,℃ and calcination time 4,h. The optimum treatment efficiency was achieved when the dosage of catalyst was 0.8,g/L,the molar ratio of H2O2to COD was 3∶1,reaction time 1,h and reaction temperature 170,℃. The COD removal rate of the waste water of ten categories of containers cleaning wastewater was about 95%.
MnO2-CuO-CeO2catalyst;preparation method;catalytic oxidation;wastewater from chemical container cleaning
X703.1 文献标志码:A 文章编号:1672-6510(2015)01-0067-06
10.13364/j.issn.1672-6510.20140078
2014-05-19;
2014-11-01
李桂菊(1969—),女,黑龙江人,教授,liguij@tust.edu.cn.
