刺五加叶亚慢性经口毒性试验研究
2015-07-22张晶莹宋昕恬孙兰孟令仪白雪松吉林省疾病预防控制中心吉林长春30062吉林医药学院营养教研室吉林吉林3203
张晶莹,宋昕恬,孙兰,孟令仪,白雪松(.吉林省疾病预防控制中心,吉林长春30062;2.吉林医药学院营养教研室,吉林吉林3203)
刺五加叶亚慢性经口毒性试验研究
张晶莹1,宋昕恬1,孙兰1,孟令仪1,白雪松2,*
(1.吉林省疾病预防控制中心,吉林长春130062;2.吉林医药学院营养教研室,吉林吉林132013)
摘要:评价刺五加叶的食用安全性。根据《食品安全性毒理学评价程序和检验方法》对刺五加叶进行90 d喂养试验。Wistar大鼠80只,分为4组,雌雄各半,分别给予实验组刺五加叶8.0、6.0、4.0 g/kg BW,对照组给予正常饲料。90 d后各组动物生长发育情况良好,给予刺五加叶对大鼠体重、食物利用率无明显影响,血常规、肝功能、肾功能、脏器系数等指标未见异常。刺五加叶对大鼠血液生化、血液学等指标无明显影响,未引起大鼠肝脏、肾脏等主要器官组织形态学改变。
关键词:刺五加叶;亚慢性经口毒性试验;大鼠
刺五加[Acanthopanax senticocus(Rupr:et Maxim.)Harms]系五加科植物[1],是我国北方地区常用的药材之一,主要入药部位为干燥根及根茎,其茎、叶也具有药理活性[2-3]作用。随着人们对于刺五加研究不断的深入,刺五加叶中的多种有效活性成分不断被开发出来,具有深入研究的价值。为了满足新资源食品评审的要求,根据《食品安全性毒理学评价程序和检验方法》对大鼠进行了90 d喂养试验。
1 材料和方法
1.1试剂与仪器
刺五加叶,粉末状:由五常北秀健康产业有限公司提供;SYSMEX-XT1800i型五分类血球计数仪:日本产;五分类试剂盒:由上海科华东菱诊断用品有限公司提供;TBA-120FR全自动生化分析仪:日本东芝;生化试剂盒:由深圳迈瑞生物医疗电子股份有限公司提供。
1.2实验动物
健康Wistar大鼠,雌雄各40只,体重(70~85)g,由长春市亿斯实验动物技术有限责任公司提供,生产许可证号:SCXK-(吉)2011-0004。本实验动物环境设施合格证,吉动设字10-1005,温度20℃~22℃、湿度55%~65%。
1.3方法
动物购入后饲养3 d,随机分为对照组及3个受试物组,每组雌雄各10只。人体推荐量为每日3.0 g,即3.0 g/60 kg BW,相当于0.05 g/kg BW。最高剂量组以成人日摄入量的160倍计,即8.0 g/kg BW,中剂量组6.0 g/kg BW相当于成人摄入量的120倍,低剂量组4.0 g/kg BW,相当于成人摄入量的80倍。将3个试验组受试物均匀掺入基础饲料中(采用逐渐扩大、充分混匀、反复过筛的方法),含量依次为10.0%、8.0%、6.0%。对照组喂饲正常基础饲料。大鼠饲料摄入量按体重8%计算,由于高、中、低剂量组受试物的比例均大于5%,故饲料中补充酪蛋白(由甘肃省临夏州华安生物制品有限公司生产),具体方法如下:基础饲料蛋白含量为18.94%,高剂量组样品占饲料比例10.0%,超出最大规定量5.0%,则高剂量组饲料按0.947%比例加入酪蛋白。中剂量组样品占饲料比例8.0%,超出最大规定量3.0%,则中剂量组饲料按0.568%比例加入酪蛋白;低剂量组样品占饲料比例6.0%,超出最大规定量1.0%,则低剂量组饲料按0.189%的比例加入酪蛋白。大鼠单笼喂养90 d,自由饮食。
1.4观察指标
1.4.1一般观察指标
每天观察动物的表现、行为活动、中毒状况、死亡情况。每周称一次体重、两次食物摄入量,计算食物周利用率及总利用率。
1.4.2血液学指标及血液生化指标
于试验中期尾静脉采血,进行血液学及血液生化指标检测。血液学指标采用SYSMEX-XT1800i进行检测;血液生化指标采用TBA-120FR全自动生化分析仪进行检测:谷丙转氨酶(ALT)、谷草转氨酶(AST)、尿素(UREA)、肌酐(Cr)、血糖(Glu)、总蛋白(TP)、白蛋白(Alb)、胆固醇(TC)、甘油三脂(TG)。禁食16 h后,于试验第91天称重,用1%戊巴比妥钠生理盐水溶液,按5.0 mL/kg BW腹腔注射麻醉后,下腔静脉采血,进行血液学及血液生化指标检测。
1.4.3病理检查
第91天进行大体解剖,组织病理检查(肝、肾、脾、胃、十二指肠、睾丸或卵巢)。
1.5数据统计
采用单因素方差分析,方差齐时,各组间两两比较用LSD方法,不齐时,各组间两两比较采用Tamhane’s方法。所有数据的统计处理均采用SPSS11.5统计软件进行。
2 实验结果
2.1一般观察情况
整个实验过程中动物无死亡,无异常行为表现。3个剂量组所有试验组动物在实验期内毛发光泽、黏膜红润,活动自如,排泄物无异常,生长发育正常,体重、进食量、食物利用率与对照组相比均无差异(P>0.05)。
2.2血液学指标
90 d喂养试验中期和末期大鼠血常规检验结果表明,各剂量组动物的白细胞(WBC)、淋巴细胞(LY)、单核细胞(MO)和分叶细胞(GR)、红细胞(RBC)、血红蛋白(Hgb)各项指标结果均在正常范围内,与对照组比较无统计学差异(P>0.05)。
2.3生化指标
由表1、2可见,试验末期雄性高剂量组ALb与对照组比较,有统计学差异(P<0.05);雄性中剂量组TG与对照组比较,有统计学差异(P<0.05);雌性中剂量组ALT与对照组比较,有统计学差异(P<0.05),但在本实验室历史正常值范围内,其余各剂量组各项血液生化指标试验中期及末期ALT、AST、BUN、CR、GLU、TP、ALB、CHO、TG与对照组比较,无统计学差异(P>0.05)。

表1 刺五加叶90 d喂养试验中期生化检测结果Table 1 Acanthopanax leaves mid 90 d feeding study biochemical test results
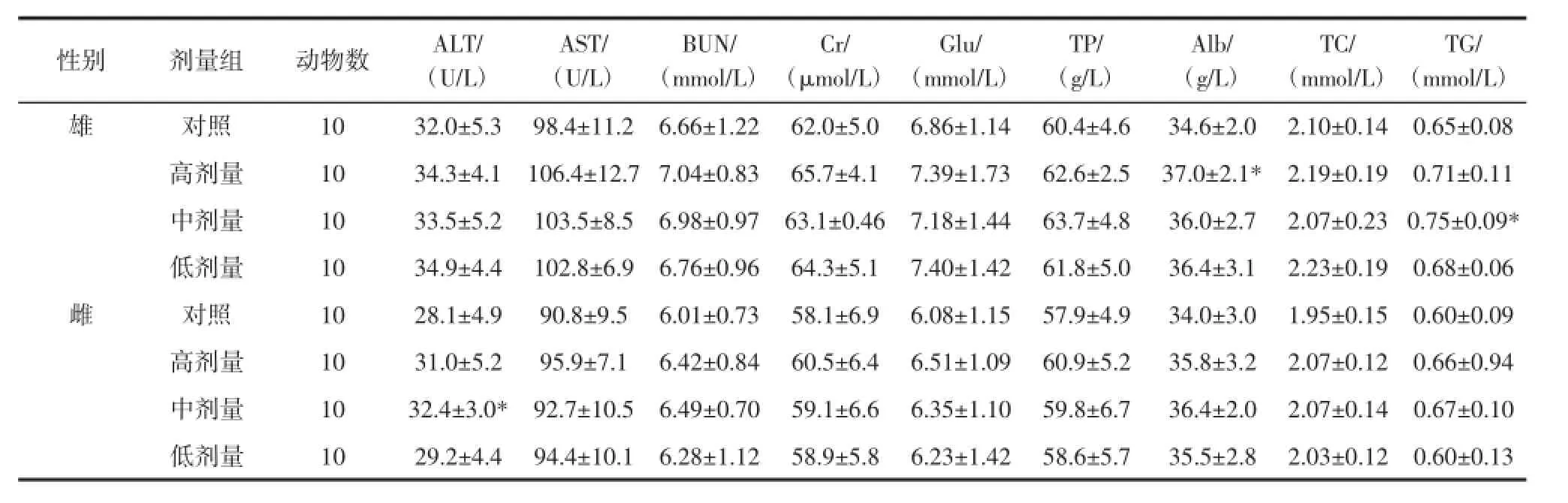
表2 刺五加叶90 d喂养试验末期生化检测结果Table 2 Acanthopanax leaves end 90 d feeding study biochemical test results
2.4病理学检查
刺五加叶90 d喂养试验病理学检查结果见图1。

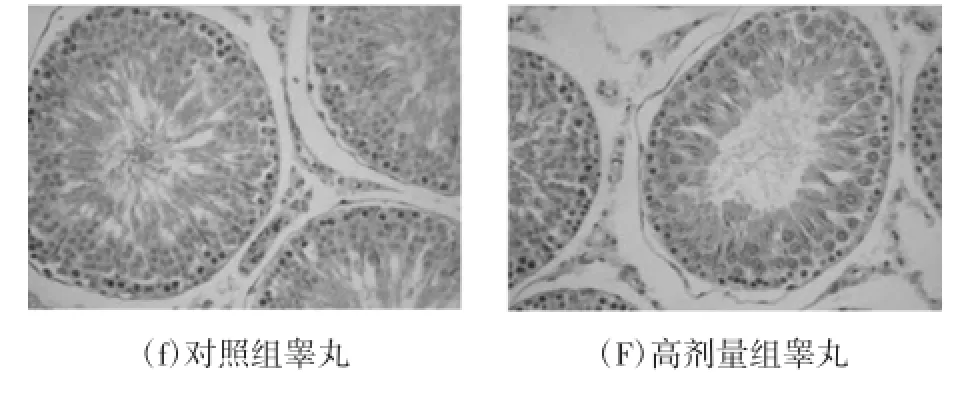
图1 刺五加叶90 d喂养试验病理学检查结果Fig.1 Acanthopanax leaves 90 d feeding study pathology results
切片镜检,肝脏:呈暗红色,质软,表面光滑、平整,未见隆起及包块。镜下所见:对照组雌性2例,雄性1例,高剂量组雌性1例,雄性1例可见肝小叶点状坏死;对照组雌性2例,雄性3例,高剂量组雌性1例,雄性3例可见肝小叶炎细胞浸润;其余被膜完整,无明显异常病理改变。脾:镜下所见:高剂量组脾脏与对照组比较,无明显差异。可清楚看到脾脏实质的红髓、白髓及边缘区三部分,被膜及脾小梁未见纤维结缔组织增生,淋巴滤泡未见反应性增生。肾脏:高剂量组与对照组双侧肾脏等大似豆形,表面光滑平整,未见明显增大与缩小。镜下观察:肾被膜光滑,肾小球在切片上呈圆形,肾皮质区肾小球未见明显增大或萎缩、纤维化、变性等,毛细血管袢未见坏死,肾小球毛细血管未见扩张充血、管壁未见增厚。小管上皮完好,间质无炎细胞浸润,为正常肾脏组织结构。其余动物肾脏一般结构均未发现异常改变。胃:镜下主要观察胃黏膜。对照组雌性1例,雄性2例,高剂量组雌性2例,雄性1例可见胃固有层内少量嗜酸粒细胞浸润;余为正常胃黏膜结构。十二指肠:镜下主要观察黏膜,高剂量组与对照组十二指肠黏膜表面可见大小不一的肠黏膜,呈叶片状,黏膜上皮呈高柱状,可见十二指肠肠腺,各层结构的细胞未见异常,高剂量的十二指肠结构与对照组比较无明显差异。睾丸:镜下观察:高剂量组与对照组睾丸曲细精管结构清晰,各级生精细胞形态正常,精子细胞清晰可见,支持细胞未见异常。睾丸间质未见出血、坏死、钙化或精子肉芽肿形成。曲细精管内可见精原细胞、初级精母细胞、次级精母细胞、精子细胞和精子,为正常睾丸组织结构。卵巢:镜下观察:高剂量组与对照组卵巢表面为扁平或立方细胞,皮质层内可见许多发育不同阶段的卵泡,卵泡间为结缔组织,髓质区由结缔组织组成,含较多血管,高剂量组的卵巢与对照组相似,未见异常。
3 结论与讨论
近年来,随着刺五加叶的相关报道不断增多,对刺五加叶中的化学成分和药理活性具有了较好的研究[4-5],但对其安全性评价方面较少。本次研究,给予不同剂量的刺五加叶进行90 d喂养试验,期间动物的全身情况良好,活动正常,无口鼻出血情况、拒食和其它异常行为,生长发育良好。对体重、食物利用率均未见明显影响。在实验中期、末期对大鼠血液学、肝肾功能等指标进行了检测,均无明显影响。组织病理学检查显示,除有少许常见自发病变,肝、肾、脾、胃、十二指肠、睾丸、卵巢等主要器官无组织形态结构损伤,均未观察到与喂养刺五加叶有关的组织病理学改变。为刺五加叶进入新资源食品提供理论依据和参考品。
参考文献:
[1] 国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2010:192-193
[2]李志峰,杨金义,张武岗,等.刺五加的化学成分研究[J].中草药, 2011,42(5):852-855
[3]梁启明,曲绍春,于晓风,等.刺五加叶皂苷B对急性心肌梗死大鼠的保护作用[J].中草药,2010,41(3):444-447
[4]刘建华,吕宁,李敬芬.刺五加茎叶果实的生药学研究[J].时珍国医国药,2007,18(5):1193-1194
[5]王知斌,郭江涛,姜海,等.刺五加叶的化学成分和药理作用研究[J].中医药信息,2013,30(3)29-31
DOI:10.3969/j.issn.1005-6521.2015.24.011
收稿日期:2014-07-18
作者简介:张晶莹(1978—),女(汉),主管医师,硕士,主要从事食品毒理学研究。
*通信作者:白雪松(1978—),男(满),副教授,硕士,主要从事预防医学。
Study on the Toxicity of Subchronic Oral of Acanthopanax Leaves
ZHANG Jing-ying1,SONG Xin-tian1,SUN Lan1,MENG Ling-yi1,BAI Xue-song2,*
(1.Jilin Provincial Center for Disease Control and Prevention,Changchun 130062,Jilin,China;2.Department of Nutrition,Jilin Medical College,Jilin 132013,Jilin,China)
Abstract:To investigate the toxicity of Acanthopanax leaves on rats,on the basis of Technical Standards for Testing﹠Assessments of Food,a ninety days feeding study of Acanthopanax leaves was conducted,80 rats were randomly divided into 4 groups,and each group consisted of 10 males and 10 females.The experimental group were given Acanthopanax leaves 8.0,6.0,4.0 g/kg BW for 90-days,control group received normal feed. The result showed that,after the challenge of Acanthopanax leaves,for 90-days,we detect no abnormality of animal growth and development,weight,and food efficiency.Also Acanthopanax leaves,there was no adverse effect of liver function,kidney function,and organ coefficients.Acanthopanax leaves at above mentioned doses causes no pathological changed in rats liver and kidney,and no changes in serum biological indexes.
Key words:Acanthopanax leaves;subchronic oral toxicity test;rats
