邻菲啰啉- Fe(Ⅱ)分光光度法测定头孢唑啉钠
2015-04-19刘荣森赵文善
刘荣森,赵文善
(1.河南林业职业学院, 河南 洛阳 471002; 2.河南大学 化学化工学院, 河南 开封 475004)
邻菲啰啉- Fe(Ⅱ)分光光度法测定头孢唑啉钠
刘荣森1,赵文善2*
(1.河南林业职业学院, 河南 洛阳 471002; 2.河南大学 化学化工学院, 河南 开封 475004)
建立了用邻菲啰啉-Fe(Ⅱ)分光光度法测定头孢唑啉钠的方法.头孢唑啉钠在0.10 mol·L-1NaOH溶液中,100 ℃水浴加热降解为含巯基的化合物.巯基化合物把Fe3+还原为Fe2+. 加入邻菲啰啉显色,通过测定生成的橘红色配位化合物的吸光度间接测定头孢唑啉钠的含量.头孢唑啉钠浓度在0.02~40 mg·L-1范围内呈现良好线性关系,线性回归方程A=0.043c(mg·L-1)-0.001,相关系数R=0.998 8,表观摩尔吸光系数ε=2.05×104L·(mol·cm)-1,相对标准偏差RSD=1.27%,检测限(3σ/k)0.065 mg·L-1.在此基础上,测定了市售头孢唑啉钠粉针剂的含量,回收率在99.17%~101.2%之间,结果令人满意.
头孢唑啉钠;邻菲啰啉;Fe(Ⅱ);分光光度法
头孢唑啉钠是一种头孢菌素类抗生素,适用于治疗敏感细菌所致的中耳炎、支气管炎、肺炎等各种炎症.头孢唑啉钠自1971年由日本藤泽药品公司开发上市以来,临床应用已有40余年的历史.测定头孢唑啉钠的含量对控制药品质量及指导临床用药具有重要意义.对于头孢唑啉钠含量测定方法的研究较多的是上世纪末和本世纪初.文献已报道的头孢唑啉钠的测定方法有高效液相色谱法[1-3]、化学发光法[4-7]、紫外分光光度法[8-9]、微分脉冲伏安法[10]等.这些方法有的需要贵重仪器,有的操作繁琐.而本文作者利用邻菲啰啉-Fe(Ⅱ)分光光度法测定头孢唑啉钠,具有线性范围宽、灵敏度高、仪器简单、试剂便宜等优点.其测定的基本原理是:头孢唑啉钠能在碱性溶液中降解为含巯基的化合物[11],该化合物中的巯基能把Fe(Ⅲ)还原成 Fe(Ⅱ),在pH=4的缓冲溶液中,加入适量邻菲啰啉,邻菲啰啉与Fe(Ⅱ)形成橙红色配合物,在511 nm处测定吸光度,从而间接测定头孢唑啉钠含量.
1 试验部分
1.1 仪器和试剂
TU-1900型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);恒温水浴箱(江苏省金坛市环宇科学仪器厂);PHS-3C型精密酸度计(上海大普仪器有限公司).
头孢唑啉钠标准溶液:1.000 0 g·L-1,准确称取头孢唑啉钠对照品0.200 0 g,用水溶解后,转移至200 mL容量瓶中并稀释至刻度,置于4 ℃避光保存.Fe3+溶液:100 mg·L-1,称取FeCl3·6H2O晶体0.242 0 g,适量稀盐酸溶解,转移至500 mL容量瓶中,用水稀释至刻度.邻菲啰啉溶液:0.15%,称取邻菲啰啉0.150 0 g,加入5.0 mL无水乙醇溶解,转移至100 mL容量瓶中,用水稀释至刻度(临用时配制).pH=4缓冲溶液:由0.2 mol·L-1CH3COONa溶液和0.2 mol·L-1的CH3COOH溶液配置而成[12].头孢唑啉钠为标准品,其余试剂均为分析纯,水为二次蒸馏水.
1.2 试验方法
1.2.1 头孢唑啉钠的降解
准确移取10.00 mL 1.000 0 g·L-1头孢唑啉钠标准储备液或样品溶液,加入1.0 mol·L-1NaOH 5 mL和35 mL水,置于100 ℃水浴中降解40 min. 迅速用流水冷却至室温,用1.0 mol·L-1HCl调节pH至7,定容至100 mL.
1.2.2 头孢唑啉钠的测定
准确移取一定量的头孢唑啉钠降解液,放入比色管中,加入含100 mg·L-1Fe3+的溶液2.00 mL,pH=4的NaAc-HAc缓冲溶液3.00 mL,0.15%邻菲啰啉1.20 mL,用水稀释至12.50 mL,30 ℃放置50 min,以待测物空白为参比,在511 nm处测定吸光度.根据测定的吸光度的值计算头孢唑啉钠的含量.
2 结果和讨论
2.1 反应机理推断
据文献[11]报道,头孢唑啉钠在NaOH溶液中易发生降解生成巯基的化合物.头孢唑啉钠的降解反应如下:

所生成的巯基化合物能将Fe(III)还原为Fe(II),Fe(II)与邻菲啰啉生成稳定的橙红色络合物,根据生成的橙红色配合物的吸光度间接测定头孢唑啉钠的含量.

2.2 最大吸收波长的选择
以水为参比溶液,在400~600 nm波长范围内,扫描了试剂空白(邻菲啰啉-Fe(Ⅲ)混合溶液,用NaAc-HAc缓冲溶液调节pH=4)的吸收光谱(图1曲线b),以试剂空白为参比,扫描了头孢唑啉钠降解液与Fe3+及邻菲啰啉反应(用NaAc-HAc缓冲溶液调节pH=4)生成的橘红色配合物的吸收光谱(图1曲线a).头孢唑啉钠降解液与Fe3+及邻菲啰啉反应生成的橘红色配合物混合溶液的最大吸收波长为511 nm.试剂空白在511 nm处有少量吸收.为消除试剂干扰, 以试剂空白为参比进行测定.
2.3 头孢唑啉钠降解条件的优化
在碱性条件下,头孢唑啉钠降解能生成含巯基的化合物[11],巯基化合物中的巯基易被三价铁氧化.故本实验首先把头孢唑啉钠进行降解,考察了不同浓度的NaOH溶液,不同降解温度,不同降解时间对头孢唑啉钠降解的影响.

(a)Fe3++邻菲啰啉+头孢唑啉钠钠降解液;(b)试剂空白.图1 吸收光谱Fig.1 Absorption spectra
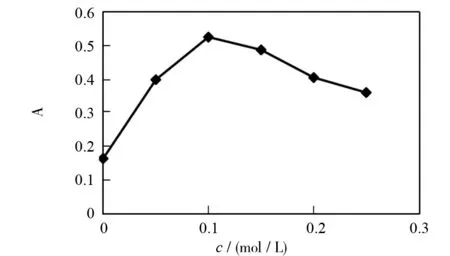
图2 NaOH浓度的影响Fig.2 Effect of concentration of NaOH
图2为NaOH浓度对头孢唑林钠降解的影响.固定降解温度为100 ℃,降解时间为40 min,当NaOH浓度为0.10 mol·L-1时,溶液的吸光度最大,说明在此条件下头孢唑啉钠已降解完全,当NaOH浓度继续增大时,吸光度降低,这可能是因为头孢唑林钠降解产生的巯基化合物进一步分解造成的,因此选择NaOH浓度为0.10 mol·L-1.
图3为温度对降解的影响.固定NaOH浓度为0.10 mol·L-1,降解时间为40 min,随着降解温度的升高,溶液吸光度增大,当降解温度达到100 ℃时,吸光度达到最大,故选择降解温度为100 ℃.
图4为时间对降解的影响.固定NaOH浓度为0.10 mol·L-1,降解温度为100 ℃,当降解时间为40 min时,溶液的吸光度最大,继续延长降解时间,吸光度反而降低,这可能是因为头孢唑林钠降解产生的巯基化合物中的巯基随着时间的延长会进一步降解造成的.

图3 降解温度的影响Fig.3 Effect of temperature

图4 降解时间的影响Fig.4 Effect of time
2.4 FeCl3和邻菲啰啉用量的选择
为使头孢唑林钠降解液反应完全,Fe3+要保持过量.随着FeCl3用量的增加,溶液的吸光度随之增大,当FeCl3用量为2.00 mL时,吸光度达到最大.继续增加FeCl3用量,吸光度几乎保持不变,说明FeCl3已与头孢唑林钠降解液反应完全.故选择含Fe3+100 mg·L-1的FeCl32.00 mL.
考察了邻菲啰啉用量对吸光度的影响.当邻菲啰啉用量为1.20 mL时,吸光度达到最大,继续增加邻菲啰啉用量,吸光度几乎保持不变,说明邻菲啰啉已与还原生成的Fe2+配位完全,故选择0.15%邻菲啰啉用量为1.20 mL.
2.5 Fe(Ⅱ)与邻菲啰啉显色反应的pH及缓冲溶液用量选择
Fe(Ⅱ)与邻菲啰啉生成配位化合物受到溶液酸碱度的影响. 实验表明,当溶液pH=4时,溶液的吸光度最大,故本实验选用pH=4的NaAc-HAc缓冲体系.当缓冲溶液用量大于2.50 mL时,吸光度最大且趋于稳定.为保持溶液的pH,选择缓冲溶液用量为3.0 mL.
2.6 Fe(Ⅱ)与邻菲啰啉反应温度和时间的选择
当反应温度为30 ℃,反应时间为50 min时,溶液吸光度最大.当温度为20 ℃时,反应速度较慢,70 min时吸光度还在增大.当温度为40 ℃时,由于温度过高,造成Fe2+与邻菲啰啉的配合物不稳定,吸光度下降.本实验选定Fe(Ⅱ)与邻菲啰啉反应温度为30 ℃,反应时间为50 min.
2.7 工作曲线
配置一系列浓度的头孢唑啉钠标准溶液,按照1.2的实验方法进行降解和显色,然后测定吸光度,进行线性回归.头孢唑啉钠浓度在0.02~40.0 mg·L-1范围内呈现良好线性关系,线性回归方程A=0.043c(mg·L-1)-0.001,相关系数R=0.998 8,表观摩尔吸光系数ε=2.05×104L·(mol·cm)-1.按照试验方法平行测定11份试样,相对标准偏差RSD=1.27%,检测限(3σ/k)为0.065 mg·L-1.
2.8 样品中头孢唑啉钠的测定及回收率实验
取市售头孢唑啉钠粉针剂适量,精密称定,加水溶解,配制成含头孢唑啉钠1.000 0 g·L-1的溶液,准确移取10.00 mL样品溶液,按照1.2的试验方法进行降解和测定.将测定值带入回归方程计算出头孢唑啉钠的含量(见表1).并进行了回收率实验,回收率在99.17%~101.2%之间,结果令人满意.说明该方法可用于头孢唑啉钠含量的测定.

表1 样品的测定及回收率实验(n=6)
[1] 于和,林宏,林澜. 高效液相色谱法测定注射用头孢替唑钠的含量[J]. 天津药学, 2011, 23(1): 24-25.
[2] 邢蓉, 张大萍. 高效液相色谱法测定不同药厂头孢唑啉钠粉针含量[J]. 安徽医药, 2003, 7(1): 36-37.
[3] 张小华, 葛竹兴, 张龙, 等. 高效液相色谱法测定五星肠安中头孢唑啉钠和恩诺沙星[J]. 分析试验室, 2004, 23(6): 31-34.
[4] SUN H W, SHI S S, WANG J, et al. A novel chemiluiminescence system based on Ag(III) Complex oxidation sensitized by rhodamine 6G and the application for the determination of cefazolin sodium in the injectable powder and human urine [J]. Asian J Chem, 2012, 24(9):3865-3869.
[5] SUN Y Y, TANG Y H, YAO H, et al. Potassium permanganate-glyoxal chemiluminescence system for flow injection analysis of cephalosporin antibiotics:cefalexin, cefadroxil, and cefazolin sodium in pharmaceutical preparations [J]. Talanta, 2004, 64(1): 156-159.
[6] 张德懿, 马永钧, 周敏, 等. 流动注射化学发光法测定针剂中的头孢唑啉钠[J]. 分析试验室, 2006, 25(2): 44-47.
[7] DU Jianxiu, LI Hong. Sensitive chemiluminescence determination of thirteen cephalosporin antibiotics with luminol-copper(II) reaction [J]. App Spectros, 2010, 64(10): 1154-1159.
[8] 邹泽, 刘斌. 紫外分光光度法测定头孢唑啉钠的含量[J]. 现代医药卫生, 2003, 19(11): 1498.
[9] 王宝宇, 张永丰, 姜明晶, 等. 紫外光谱法测定头孢唑啉钠含量[J]. 黑龙江医药, 2000, 13(2): 77-78.
[10] IRENA B, PIOTR M, ANNA G, et al. Determination of selected drugs in human urine by differential pulse voltammetry technique [J]. Bioelectrochemistry, 2008, 73(1): 5-10.
[11] 张玉忠, 赵红, 袁倬斌. 头孢唑啉降解产物在银亚微盘电极上的电化学行为及其测定[J]. 分析化学, 2002, 30(1): 9-12.
[12] 夏玉宇. 化验员实用手册[M]. 北京: 化学工业出版社, 1999: 376-378.
[责任编辑:任铁钢]
Spectrophotometric determination of cefazolin sodium by using 1,10-phenanthroline-Fe(Ⅱ)
LIU Rongsen1, ZHAO Wenshan2*
(1.HenanForestryVocationalCollege,Luoyang471002,Henan,China; 2.CollegeofChemistryandChemicalEngineering,HenanUniversity,Kaifeng475004,Henan,China)
A new spectrophotometric method has been established to determine cefazolin sodium using 1,10-phenanthroline-Fe(Ⅱ). In the 0.10 mol·L-1NaOH solution, cefazolin sodium could be degraded to form the compound containing the sulfhydryl group at 100℃ water-bath heating. It has been demonstrated that the Fe3+could be reduced to form Fe2+by cefazolin sodium. By determining the absorbance of the orange complex after adding 1,10-phenanthroline, the indirect determination of cefazolin sodium can be achieved. The concentration of cefazolin sodium has a good linear relationship in the range of 0.02-40 mg·L-1, and the linear regression equation isA=0.043c(mg·L-1)-0.001 with a correlation coefficient of 0.998 8. What’s more, the apparent molar absorption coefficient is 2.05×104L·(mol·cm)-1, and the relative standard deviation is 1.27% with the detection limit of 0.065 mg·L-1. This method has been applied to determine the cefazolin sodium powder injection in pharmaceuticals with satisfactory results. The recovery rate was in the range of 99.17%-101.2%.
cefazolin sodium; 1,10-phenanthroline; Fe(Ⅱ); spectrophotometry
2014-11-01.
河南省科技厅基金项目(122600345020).
刘荣森(1964-),男,副教授,研究方向为物质成分分析.*
,E-mail:zhaowenshan@henu.edu.cn.
O657.32
A
1008-1011(2015)01-0054-04
