红色长余辉荧光粉Ca2Zn4Ti16O38∶Pr3+的水热辅助合成及发光性质
2015-04-01夏茂谷智强刘琼张吉林周文理廉世勋余丽萍
夏茂 谷智强 刘琼 张吉林,2 周文理,2 廉世勋,2 余丽萍*,,2,
(1湖南师范大学化学化工学院,长沙410081)
(2湖南师范大学资源精细化与先进材料湖南省高校重点实验室,长沙410081)
红色长余辉荧光粉Ca2Zn4Ti16O38∶Pr3+的水热辅助合成及发光性质
夏茂1谷智强1刘琼1张吉林1,2周文理1,2廉世勋1,2余丽萍*,1,2,
(1湖南师范大学化学化工学院,长沙410081)
(2湖南师范大学资源精细化与先进材料湖南省高校重点实验室,长沙410081)
采用水热法辅助合成了纯相Ca2Zn4Ti16O38∶Pr3+荧光粉,初始nCa∶nZn∶nTi=2∶4.1∶15,煅烧条件为1 050℃空气气氛烧结5 h。并以X射线衍射、扫描电镜、紫外可见漫反射光谱和荧光光谱表征了样品的物相组成、微观形貌和光谱性质。合成的荧光粉在高温煅烧后仍较好地保持了球形的微观形态,优化的Pr3+掺杂浓度为0.015。Ca2Zn4Ti16O38∶Pr3+荧光粉在471 nm波长激发下发射红光,发射谱通过高斯分峰拟合得到位于605、620和645 nm的3个发射峰,分别对应于Pr3+的1D2→3H4,3P0→3H6和3P0→3F2跃迁。在471 nm波长激发下,Ca2Zn4Ti16O38∶Pr3+的614 nm红光发射表现出超长余辉特性,表明该荧光粉是一种能被可见光有效激发的红色长余辉荧光粉。
Ca2Zn4Ti16O38∶Pr3+;水热法;红色长余辉荧光粉
0 引言
Pr3+掺杂的碱土钛酸盐红色长余辉荧光粉Ca0.8Zn0.2TiO3∶Pr3+[1-8]由于具有良好的热稳定性和化学稳定性,以及发光亮度高,余辉时间长,色纯度高,价格低廉,环境友好等优点,成为最有潜力作为红色长余辉材料。与CaTiO3∶Pr3+[9-12]相比,Ca0.8Zn0.2TiO3∶Pr3+的发光强度和余辉时间都有明显的改善。但Ca0.8Zn0.2TiO3∶Pr3+只是名义组成,它包含CaTiO3、Zn2TiO4和Ca2Zn4Ti16O383种物相[3,8]。研究发现Zn2TiO4∶Pr3+不具有长余辉特性,因此,Ca2Zn4Ti16O38∶Pr3+对Ca0.8Zn0.2TiO3∶Pr3+的长余辉增强可能起到重要的作用。
Gatehouse等[13]在CaO-ZnO-TiO2三元体系中,1 200℃煅烧90 h获得了Ca2Zn4Ti16O38化合物,但是含有少量的Zn2TiO4和CaTiO3相。文献[14]报道了煅烧温度对Ca2Zn4Ti16O38合成的影响,煅烧温度达到1 050℃时,只有Ca2Zn4Ti16O38,Zn2TiO4和TiO23种物相。我们研究小组采用溶胶凝胶法合成出纯相的Ca2Zn4Ti16O38[15-16],煅烧时间减少到21 h。
因此研究新的制备方法来进一步缩短Ca2Zn4Ti16O38反应时间势在必行。水热法作为近年来兴起的一种制备材料的新方法给我们提供了一个很好的解决途径。水热法合成CaTiO3[12,17-23]和Ca0.8Zn0.2TiO3[8]已有报道,但是尚未有水热合成Ca2Zn4Ti16O38的报道。因此,本论文主要采用水热法辅助制备Ca2Zn4Ti16O38∶Pr3+荧光粉,并优化其光学性质。
1 实验部分
实验所用Ca(Ac)2·H2O、Zn(Ac)2·2H2O、钛酸正丁酯、乙二醇、柠檬酸、尿素、氨水均为分析纯;Pr6O11纯度为99.99%。将Pr6O11溶于浓盐酸后,配成0.005 mol·L-1的PrCl3溶液。将Ca(AC)2·H2O和Zn(AC)2· 2H2O配制成0.6 mol·L-1的溶液。
按照表1给出的nCa∶nZn∶nTi,称取一定量的钛酸正丁酯,在磁力搅拌下逐滴加入适量乙二醇,随后加入柠檬酸,该混合溶液逐渐变为淡黄色(A溶液)。用移液管准确量取Ca(Ac)2、Zn(Ac)2和PrCl3溶液,将其混合均匀(B溶液)。将B溶液逐滴加入到A中,滴完后加入尿素作为矿化剂,随后用氨水调节溶液pH值为7.20。继续搅拌0.5 h后,转入到40 mL聚四氟乙烯内衬的不锈钢反应釜,密闭后放入烘箱中于220℃进行水热处理2 h。随后自然冷却到室温。将所得沉淀用去离子水离心洗涤数次,至溶液澄清无色之后将洗涤后的样品转入瓷坩埚中,于烘箱中90℃干燥,将干燥后的粉末研磨后得前驱体粉末。再于高温箱式炉内,空气气氛中600~1 100℃煅烧5 h,自然冷却到室温,研磨得到所需样品。
采用日本理学D/MAX-2500(18 kW)X射线仪分析晶体物相组成(采用Cu靶,加速电压40 kV,电流250 mA)。用日立F-4500荧光分光光度计测试样品的激发和发射光谱以及余辉衰减曲线(175 W氙灯,R928光电倍增管电压400 V,滤光片为UV 390 nm,激发与发射的狭缝宽度均为5 nm)。紫外可见漫反射光谱由配备有积分球的日立U-3310型分光光度计测试。采用JSM-5600 LV扫描电镜观察样品的微观形貌。
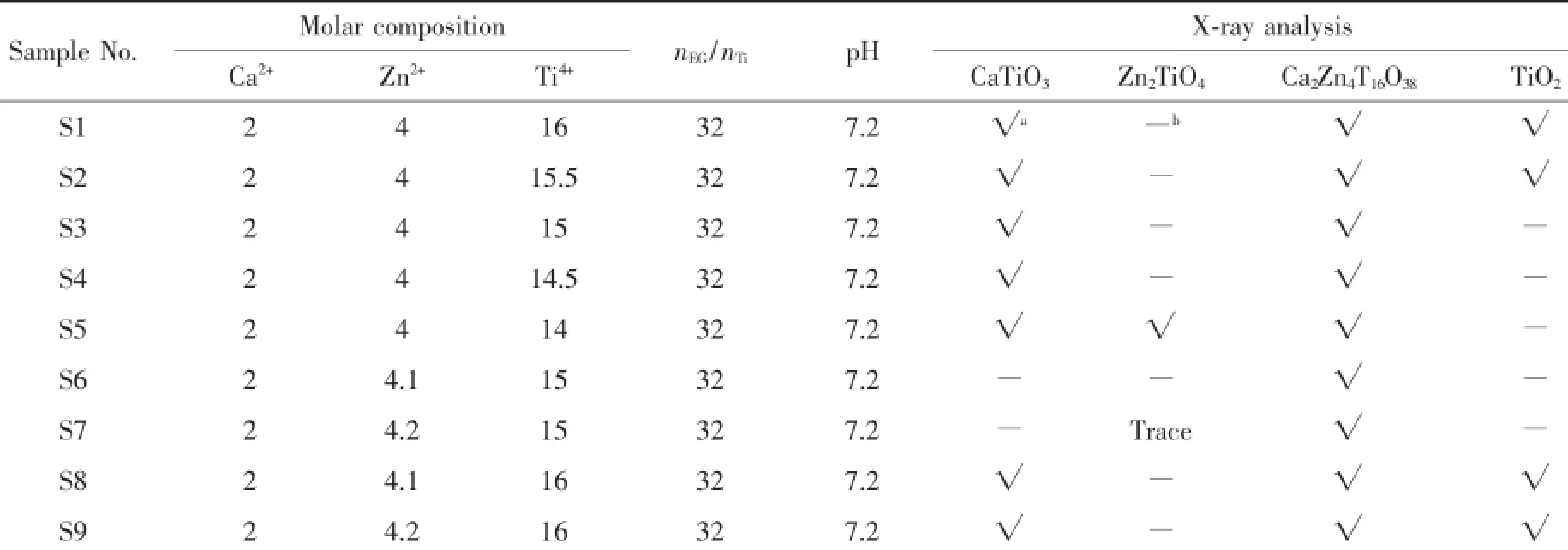
表1 制备条件和物相分析Table 1Preparation condition of samples and XRD analysis
2 结果与讨论
2.1 水热辅助合成Ca2Zn4Ti16O38的反应机理
图1为水热后前驱体的XRD图,从图中可知水热后的沉淀产物主要由CaCO3和TiO2组成,未探测到含Zn的物种,推测可能处于非晶态。尿素在70℃以上开始水解,若是在敞开体系,随着CO2气体的溢出,其最终的水解产物是OH-离子,而在封闭的水热反应釜内,由于水解产生的气体不能释放,最终水解产物是CO32-和OH-离子,而这两种离子都有可能作为沉淀剂,使所需的金属离子以沉淀形式从溶液中析出[24]。因此本论文涉及的反应机理推测为:

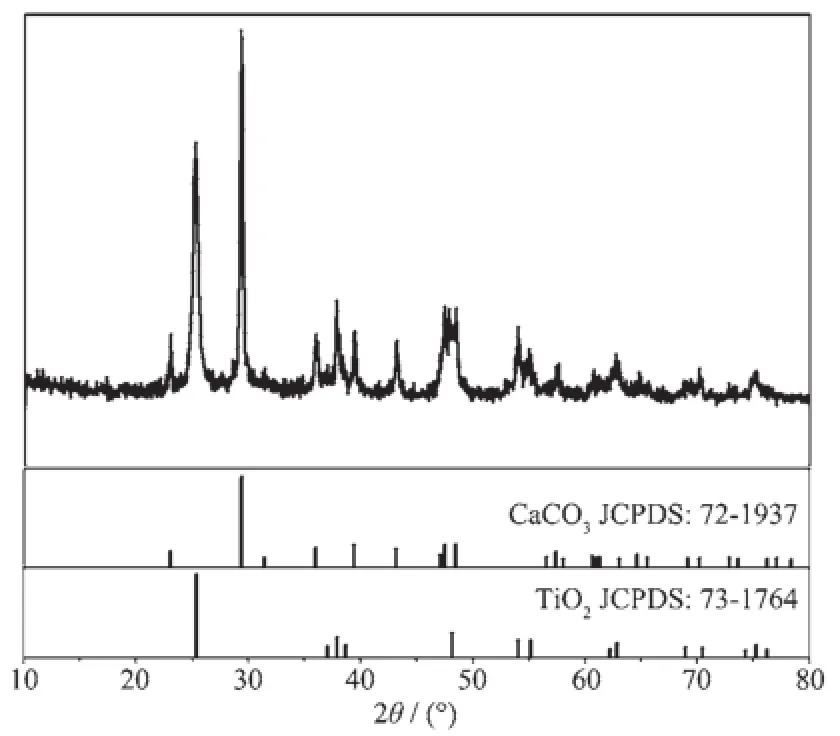
图1 水热后样品的XRD图Fig.1XRD patterns of samples after hydrothermal treatment
2.2 Ca/Zn/Ti物质的量比对荧光粉物相的影响
图2是不同的nCa∶nZn∶nTi所合成产物1 050℃煅烧5 h的XRD图谱。由图可知,每一个试样都含有菱方的Ca2Zn4Ti16O38(JCPDS No:85-1102)相,此外还可探测出少量的TiO2、CaTiO3或Zn2TiO4。通过与标准卡片对照,发现S6为纯相Ca2Zn4Ti16O38。nCa∶nZn∶nTi= 2∶4.2∶15的S7,也能获得目标产物,但是含有痕量的Zn2TiO4相。该实验结果与文献[16]报道的Zn2+略微过量或Ti4+少许不足时获得纯相Ca2Zn4Ti16O38的结论一致。
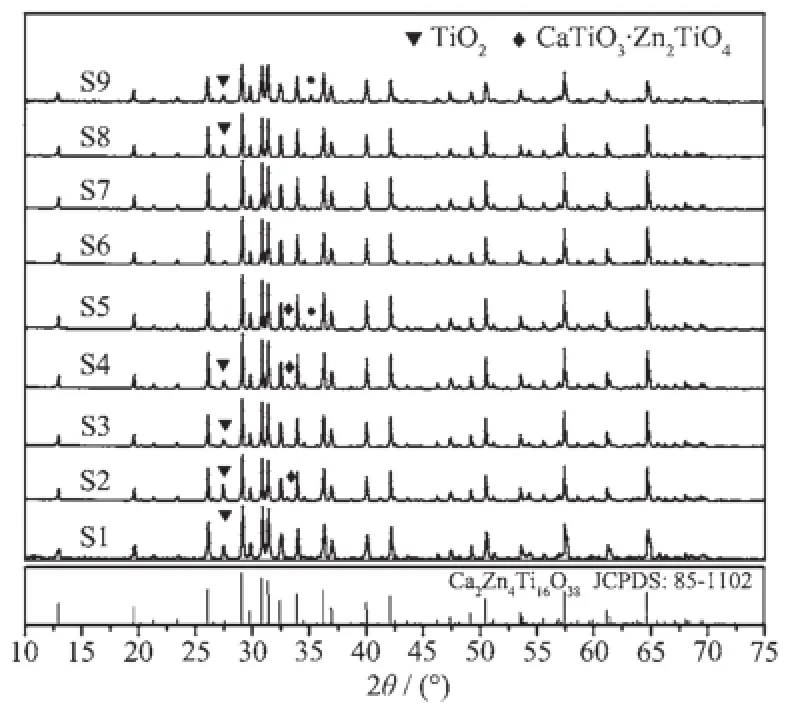
图2 不同nCa∶nZn∶nTi时样品的XRD图谱Fig.2XRD patterns of samples prepared with different mole ratios of nCa∶nZn∶nTi
2.3 水热时间对荧光粉形貌的影响
图3(a)、(b)和(c)为样品S6不同水热时间的SEM照片,从图中可以看出,当水热时间仅为0.5 h时,颗粒的尺寸在0.26~0.8 μm,既有小尺寸的球形颗粒,又有较大尺寸的不规则颗粒;当水热时间延长至1 h,明显看到颗粒的团聚增加,大尺寸颗粒增加,而当水热时间增加到2 h,颗粒呈球形,且尺寸大多分布在0.32~0.45 μm。将水热后2 h的样品经1 050℃煅烧后,颗粒保持了水热后的球形,但颗粒大小增加到1 μm左右(见图3d)。从水热时间与颗粒尺寸的变化可以知道,Ca2+、Zn2+和Ti4+离子的沉淀是一个沉淀溶解的动态过程,时间太短颗粒的均匀性很难达到一致,而水热2 h是获得球形颗粒的最佳时间,低温水热处理再结合高温煅烧基本上能保持颗粒的近似球状。

图3 样品S6水热后及煅烧后的扫描电镜照片Fig.3SEM micrograph of sample S6 hydrothermal treatment for 0.5 h(a),1 h(b),2 h(c)and calcined at 1 050℃for 5 h(d)
水热辅助法与溶胶-凝胶法、固相法制备的Ca2Zn4Ti16O38粉末相比,其微观形态有较大差异,溶胶-凝胶法获得的是团聚的颗粒,且形状不规则[15],而固相法获得颗粒尺寸平均3~6 μm,且为CaTiO3、Ca2Zn4Ti16O38、Zn2TiO4和TiO2的混合相[14]。
2.4 煅烧温度对荧光粉物相及光学性质的影响
图4为nCa∶nZn∶nTi=2∶4.1∶15时,不同温度下煅烧5 h时样品的XRD图。当煅烧温度为600℃时,主相是正交的TiO2(JCPDS No:21-1272)相,没有明显的Ca2Zn4Ti16O38生成。700℃时样品中检测到Ca2Zn4Ti16O38相,除含有正交相的TiO2外,还含有四方的金红石(JCPDS No.73-2224)以及微量的CaTiO3相。当温度升高到800℃,Ca2Zn4Ti16O38物相衍射峰增强,同时正交的TiO2相消失,金红石相及微量CaTiO3相仍然存在。当温度达到1 000℃时,CaTiO3相消失。当温度达到1 050℃,金红石相消失,获得纯Ca2Zn4Ti16O38相。

图4 不同温度煅烧5 h样品的XRD图Fig.4XRD patterns of samples calcined at different temperatures for 5 h
图5 为不同煅烧温度样品的激发与发射光谱图。614 nm监控下的激发光谱主要由位于320 nm的A带、400 nm附近的B带和450~500 nm范围内的C带组成,分别对应于价带到导带(O2-2p→Ti4+3d)之间的电子跃迁,Pr3+向Ti4+离子的价间电荷迁移(IVCT,即Pr3+/Ti4+⇌Pr4+/Ti3+)跃迁[10]和Pr3+的4f→4f (3H4→3P0,1,2+1I6)跃迁。该激发谱与文献[15-16]有明显差别,溶胶-凝胶制备的Pr3+掺杂Ca2Zn4Ti16O38以B带为主激发峰,而水热辅助法获得的纯Ca2Zn4Ti16O38∶Pr3+荧光粉则以C带为主激发峰,推测可能与溶胶-凝胶法引入硼,形成BTi′缺陷有关。
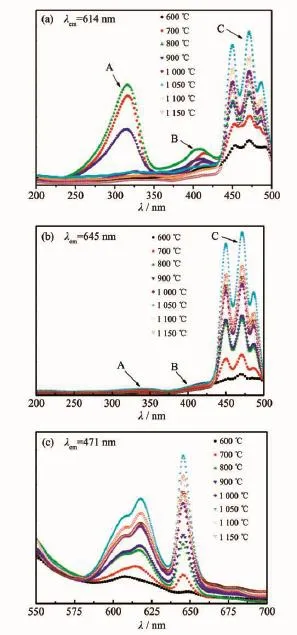
图5 不同煅烧温度下样品的激发光谱(a)(b)和发射光谱(c)Fig.5Excitation(a)(b)and emission(c)spectra of samples calcined at different temperatures
在煅烧温度相对较低时(700~900℃),A带的激发峰较明显,随着煅烧温度的升高,A带的激发峰强度逐渐降低,当温度达到1 000℃时,A带的强度已非常弱。而C带的激发峰强度随煅烧温度的升高逐渐增强,当温度达到1 050℃时,C带的激发峰强度达到最大,温度继续升高,C带的强度下降。B带激发强度随温度的变化不明显。645 nm波长监控下得到的激发光谱中以C带为主,A带和B带的强度非常弱。结合XRD结果可知,A带的激发强度主要由CaTiO3的含量决定,而C带的激发强度主要由Ca2Zn4Ti16O38的含量决定。图5(c)所示是样品在471 nm激发下的发射光谱图。随着煅烧温度的升高,样品的发射强度逐渐增强,在1 050℃达到最大,当温度继续升高,发射强度反而降低。Pr3+离子随温度升高不断进入晶格中,发光中心的浓度增加,从而使发光强度不断增强;而温度继续增加,粉体材料的烧结程度加剧,体积收缩较为严重,晶体结晶度有所下降,有可能使发光粉发生了缺陷组成的变化,从而导致了发光强度降低。在471 nm波长激发下,发射光谱中有2个发射主峰分别是位于614和645 nm处的红光发射,分别归因于Pr3+的1D2→3H4跃迁和3P0→3F2跃迁[15-16]。
2.5 Pr3+离子浓度对样品发光性质的影响
为进一步优化Ca2Zn4Ti16O38∶Pr3+中Pr3+离子的浓度,按照上述优化的合成条件,制备了一系列不同Pr3+离子掺杂浓度的样品,其相应的发射光谱如图6所示。随着Pr3+离子掺杂浓度增加,样品的发光强度逐渐增加;当Pr3+离子浓度达到0.015时,发光强度最强;Pr3+离子浓度继续增大,发光则减弱。这主要是由于Pr3+离子浓度增加,减小了Pr3+离子之间的距离,增大了非辐射跃迁机率,从而使发光减弱。
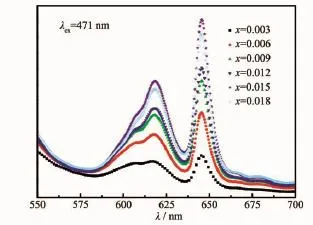
图6 Ca2Zn4Ti16O38∶xPr3+的发射光谱Fig.6Emission spectra of Ca2Zn4Ti16O38∶xPr3+
2.6 样品的衰减曲线
图7是Ca2Zn4Ti16O38∶Pr3+荧光粉归一化之后的余辉衰减曲线。471 nm波长激发产生的614 nm和645 nm的发光都具有长余辉衰减特性。Ca2Zn4Ti16O38∶Pr3+荧光粉的衰减曲线可根据单指数公式(1)进行拟合,

其中,I表示余辉强度,A0和A是常量;t是时间;τ是衰减时间。拟合曲线的相关度接近于1,645和614 nm发射的余辉时间分别为485.97和577.40 ms。结果表明471 nm波长激发,614 nm的发光表现超长余辉性能。
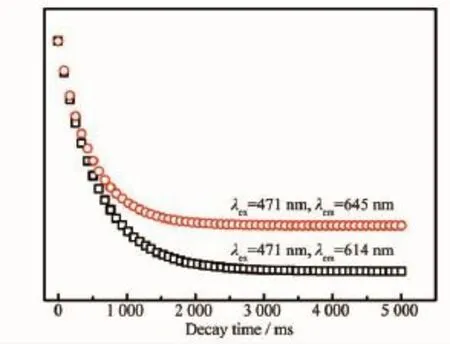
图7 Ca2Zn4Ti16O38∶Pr3+的余辉衰减曲线Fig.7Decay curve of Ca2Zn4Ti16O38∶Pr3+
2.7 样品的漫反射光谱
图8是基质及Pr3+掺杂样品的紫外可见漫反射光谱图。很明显,Pr3+离子的掺入有助于增强基质在近紫外到可见光区的吸收。内插图所示为根据Ca2Zn4Ti16O38的漫反射光谱求带隙能Eg[25]。经过公式(2)~(4)将漫反射光谱转换为(F(R)hν)2对hν的关系图,做基质吸收边带切线与横坐标相交,该点对应的横坐标即为带隙能Eg。


图8 Ca2Zn4Ti16O38和Ca2Zn4Ti16O38∶Pr3+紫外可见漫反射光谱Fig.8UV-visible diffuse reflection spectra of Ca2Zn4Ti16O38and Ca2Zn4Ti16O38∶Pr3+samples
其中h为普朗克常数(6.626 196×10-34J·s),ν为频率,λ为入射光波长,R为反射系数,F(R)为吸收系数,Eg为带隙(能量单位),A为比例常数。n值则根据所对应半导体带隙跃迁性质而定,若为直接允许跃迁,取n=1/2;直接禁阻跃迁,n=3/2;间接允许跃迁,n=2;间接禁阻跃迁,n=3。根据直接带隙材料的n= 1/2,可求得Ca2Zn4Ti16O38∶Pr3+的带隙为3.57 eV。
2.8 Ca2Zn4Ti16O38∶Pr3+发光机理探讨
在Ca2Zn4Ti16O38的晶胞中,Ca2+离子有2种格位,分别是位于顶点的Ca1格位和位于中心的Ca2格位(如图9所示)。Ca1格位处于12个O原子形成的立方八面体的中心,而Ca2格位处于6个O原子形成八面体的中心。晶胞中Zn2+离子也有2种格位,Zn1与4个O原子配位形成正四面体结构,Zn2与6个O原子配位形成八面体结构。Ca2+、Pr3+和Zn2+的离子半径分别为0.099,0.101 3和0.074 nm。根据离子半径匹配原则,Pr3+离子会优先取代Ca1格位或Ca2格位形成PrCa·正电荷缺陷。当然,Pr3+离子也有可能取代Zn1或Zn2格位,形成PrZn·正电荷缺陷,但是由于Zn四面体格位比较稳定,不容易被取代。文献[16]通过密度泛函计算,证实在Ca2Zn4Ti16O38结构中,Pr3+离子分别取代了Ca2+和Zn2+离子的格位,形成2种发光中心PrCa·和PrZn·,且PrZn·的陷阱深度要比PrCa·的深0.222 eV。

图9 Ca2Zn4Ti16O38∶Pr3+的晶胞结构Fig.9Crystal structure of Ca2Zn4Ti16O38∶Pr3+
仔细观察图5(c)和图6所示的发射光谱,发现除位于614 nm和645 nm处的2个发射外,在605 nm附近可观察到1个明显的肩峰。将发射光谱进行高斯分峰拟合可得到605,620和645 nm 3个发射峰,如图10所示。根据文献[9,26-27]的报道,可将这3处发射跃迁分别归因于Pr3+的1D2→3H4跃迁、3P0→3H6跃迁和3P0→3F2跃迁。由此可见,Ca2Zn4Ti16O38∶Pr3+荧光粉是一种能被蓝光有效激发的红色荧光粉,并具有非常缓慢的衰减。
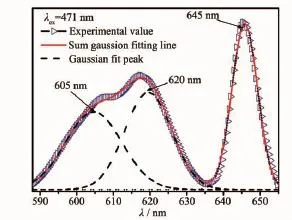
图10 Ca2Zn4Ti16O38∶Pr3+发射光谱的Gaussian分峰拟合Fig.10Fitting of emission spectra into three Gaussian peaks for Ca2Zn4Ti16O38∶Pr3+
其发光机理示意图如图11所示,光生电子首先被激发至导带或3PJ能级,然后通过非辐射弛豫到3P0能级。在此能级上,一部分电子通过辐射跃迁回到3F2和3H6能级,分别发出645和620 nm的红光;另一部分电子通过非辐射跃迁弛豫至1D2能级,然后通过辐射跃迁返回3H4基态发出605 nm的红光。这表明,有2种发光中心存在于Ca2Zn4Ti16O38∶Pr3+荧光粉样品中。一种是Pr3+占据Ca的格位形成PrCa·,对应于605 nm处的红光发射;另一种是Pr3+占据了Zn的格位形成PrZn·,对应于620和645 nm处的红光发射。
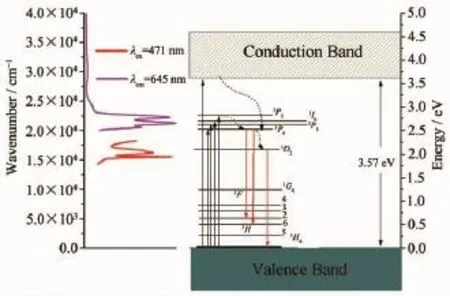
图11 Pr3+在Ca2Zn4Ti16O38中的跃迁示意图Fig.11Schematic transition mechanism of Pr3+in Ca2Zn4Ti16O38
3 结论
通过控制nCa∶nZn∶nTi=2∶4.1∶15,220℃水热2 h,再通过1 050℃煅烧5 h成功制备了纯相Ca2Zn4Ti16O38∶Pr3+荧光粉。水热辅助法有助于球形颗粒的形成,并在高温煅烧后保持了近球形。与高温固相法和溶胶凝胶法相比,大大缩短了煅烧时间,粉末微观均匀性较好。最佳Pr3+离子掺杂浓度为0.015。Ca2Zn4Ti16O38∶Pr3+荧光粉在471 nm波长激发下发射红光,发射峰分别位于605、620和645 nm,归因于Pr3+的1D2→3H4,3P0→3H6和3P0→3F2跃迁。而且在471 nm激发,614 nm处的发光显示了超长的余辉。实验结果表明Ca2Zn4Ti16O38∶Pr3+是一种能被蓝光有效激发的红色长余辉荧光粉,有潜力应用于转光膜、蓝光激发白光LED用红粉。
[1]Royce M R,Matsuda S,Tamaki H.U.S.Patent,5650094. 1997.
[2]Haranath D,Khan A F,Chander H.Appl.Phys.Lett.,2006, 89(9):091903
[3]Lian S X,Zuo C G,Yin D L,et al.J.Rare Earths,2006,24 (1):29-33
[4]Tang W J,Chen D.J.Am.Ceram.Soc.,2007,90(10):3156-3159
[5]Yuan X,Shi X,Shen M,et al.J.Alloys Compd.,2009,485 (1/2):831-836
[6]Chung S.M.,Kang S.Y.,Shin J.H.,et al.J.Cryst.Growth, 2011,326(1):94-97
[7]Kim G.,Lee S.J.,Kim Y.J.Opt.Mater.,2012,34(11):1860-1864
[8]Yu L P,Xia M,Chen X,et al.J.Mater.Res.,2013,28(18): 2590-2597
[9]Diallo P T,Boutinaud P,Mahiou R,et al.Phys.Status Solidi A,1997,160(1):255-263
[10]Boutinaud P,Pinel E,Dubois M,et al.J.Lumin.,2005,111 (1/2):69-80
[11]Kymen T,Sakamoto R,Sakamoto N,et al.Chem.Mater., 2005,17(12):3200-3204
[12]Minami K,Hakuta Y,Ohara M,et al.ECS Trans.,2013,50 (41):19-24
[13]Gatehouse B M,Grey I E.J.Sol.State Chem.,1983,46(2): 151-155
[14]Zhao F,Yue Z,Lin Y,et al.Ceram.Int.,2007,33(6):895-900
[15]ZHOU Wen(周文),YU Li-Ping(余丽萍),LIAN Shi-Xun(廉世勋),et al.Chinese J.Lumin.(发光学报),2010,31(5):712-718
[16]Lian S X,Qi Y,Rong C Y,et al.J.Phys.Chem.C,2010, 114(15):7196-7204
[17]Yang X,Fu J,Jin C,et al.J.Am.Chem.Soc.,2010,132 (40):14279-14287
[18]Dong W,Zhao G,Song B,et al.CrystEngComm,2012,14 (20):6990-6997
[19]Sun Z,Cao G,Zhang Q,et al.Mater.Chem.Phys.,2012, 132(2/3):937-942
[20]Wu B,Zhang Q,Wang H,et al.CrystEngComm,2012,14 (6):2094-2099
[21]Yang J,Geng B,Ye Y,et al.CrystEngComm,2012,14(8): 2959-2965
[22]Lozano-Snchez L M,Lee S W,Sekino T,et al.CrystEngComm, 2013,15(13):2359-2362
[23]Yu D,Zhang J,Wang F,et al.Cryst.Growth Des.,2013,13 (7):3138-3143
[24]XU Guang-Guang(徐金光),TIAN Zhi-Jian(田志坚),WANG Jun-Wei(王军威),et al.Chem.J.Chinese Universities(高等学校化学学报),2004,25(1):90-94
[25]Zhao X K,Fendler J H.J.Phys.Chem.,1991,95(9):3716-3723
[26]Lazarowska A,Mahlik S,Grinberg M,et al.Opt.Mater., 2013,35(11):2001-2005
[27]Xu B,Liu J,Song C,et al.J.Am.Ceram.Soc.,2012,95(1): 250-256
Hydrothermal Assisted Synthesis and Photoluminescence Properties
of Red Persistent Ca2Zn4Ti16O38∶Pr3+Phosphor
XIA Mao1GU Zhi-Qiang1LIU Qiong1ZHANG Ji-Lin1,2ZHOU Wen-Li1,2LIAN Shi-Xun1,2YU Li-Ping*,1,2
(1Collage of Chemistry and Chemical Engineering,Hunan Normal University,Changsha 410081)
(2Key Laboratory of Sustainable Resources Processing and Advanced Materials of Hunan Province,Hunan Normal University,Changsha 410081)
Pure Ca2Zn4Ti16O38∶Pr3+phosphors were synthesized by a hydrothermal assisted method with the molar ratio of nCa∶nZn∶nTibeing 2∶4.1∶15 and then calcined at 1 050℃for 5 h.Crystal phase,microstructure and optical properties were investigated by X-ray diffractometer,scanning electron microscope,UV-Vis spectroscope and luminescence spectrofluorometer.As-synthetic phosphors retain sphere even though firing at 1 050℃for 5 h. The optimum Pr3+concentration was 0.015.Upon excitation with 471 nm,the red emission spectra can be fitting into three peaks using Gaussian method.The three emission peaks located at 605,620 and 645 nm can be ascribed to1D2→3H4,3P0→3H6and3P0→3F2transition of Pr3+,respectively.It is noted that excited at 471 nm,the phosphor displays a super-long afterglow with the emission peak at 614 nm,indicating it being a persistent red long phosphor for visible-light conversion.
Ca2Zn4Ti16O38∶Pr3+;hydrothermal method;red persistent phosphor
O61
A
1001-4861(2015)02-0253-07
10.11862/CJIC.2015.061
2014-07-14。收修改稿日期:2014-12-10。
国家自然科学基金(No.21471055,51402105)、湖南省自然科学基金(No.12JJ2029,2015JJ2100)、湖南省高校创新平台开放基金(No.12K030)和湖南省高校科技创新团队支持计划(湘教通[2012]318号)资助项目。
*通讯联系人。E-mail:seaheart_yu@163.com
