壳聚糖/银-铜复合抗菌剂的制备及在硅橡胶基体上的应用
2015-03-22马森源高向华宋秀龙李闲闲魏丽乔
康 虹,马森源,高向华,宋秀龙,李闲闲,魏丽乔
(太原理工大学 a.新材料界面科学与工程教育部重点实验室,b.材料科学与工程学院,太原 030024)
壳聚糖/银-铜复合抗菌剂的制备及在硅橡胶基体上的应用
康 虹a,马森源a,高向华b,宋秀龙a,李闲闲a,魏丽乔a
(太原理工大学 a.新材料界面科学与工程教育部重点实验室,b.材料科学与工程学院,太原 030024)
采用化学法合成了一种壳聚糖/银-铜(CAC)共混的复合抗菌剂,利用表面官能团链接方式接枝到硅橡胶基体上,制成抗菌硅橡胶高分子材料。通过SEM、TEM、XPS等测试方法对抗菌硅橡胶进行表征分析,采用抑菌环法和震荡烧瓶法表征复合抗菌剂和抗菌材料的抗菌性能。结果表明,CAC复合抗菌剂其细菌存活率对大肠杆菌仅达到18%,对金黄色葡萄球菌为26%,其初始分解温度较CS/Ag溶胶提高了大约70 ℃,具有良好的抗菌性和热稳定性;制备的抗菌硅橡胶高分子材料方法简单,成本低廉,其抗菌功能层厚度约为50~70 μm,且对大肠杆菌和金黄色葡萄球菌的抗菌率均达到96%以上,抗菌性能优良。
壳聚糖/银-铜复合抗菌剂;抗菌硅橡胶;抗菌性能
近些年,随着现代医疗技术的不断发展,医用介入导管被广泛使用。其中导尿管的利用率相对较大,但大部分导尿管会因其长期留置而导致患者相关性尿路感染,直至死亡[1-2]。为此,研制性能优良的抗菌剂,并将其接枝到基体,制备一种抗菌医用高分子材料是当今医疗领域的研究重点之一[3-4]。壳聚糖(CS)是一种在自然界广泛存在且含量较多的多糖[5]。马滢发现,改性后的壳聚糖对细菌的抑菌效果增强了[6],原因是具有生物相容性和活泼的官能基团,易于与其他金属粒子螯合,形成金属配合物[7];而且壳聚糖安全无毒可降解,能被广泛应用在医疗器械和饮用水净化等领域。但是,壳聚糖单独使用时,抗菌性能较差,所以在抗菌性能要求比较高的情况下不能单独作为一种抗菌剂使用。银(Ag)的抗菌广谱性和抗菌效果比其他金属都要高,当降低银的粒径,达到纳米级时,因为纳米材料具有某些特殊的表面性能和表面效应,使得抗菌效果有更大提高。王婧讨论了壳聚糖/纳米银复合抗菌溶胶对大肠杆菌和金黄色葡萄球菌均有显著的抑菌性能[8],安靖探讨了壳聚糖载银纳米微球对大肠杆菌和金黄色葡萄球菌同样有较高的抗菌性[9]。但是,银本身价格比较昂贵,另外,近些年来研究者对其大量使用而带来的毒性研究也越来越多[10-11]。而铜在自然界中广泛存在,且是一种重要的微量元素(存在于大多数生物体中,且环保又相对便宜)[12-13],其抗菌效果仅次于银。朱晓红发现,壳聚糖/铜能增强对某些植物病原菌的抑制作用[14]。
笔者拟采用少量铜来替代一部分银,制备出一种绿色环保、价格低廉、抗菌性能优良的复合抗菌剂,并将其接枝到医用高分子材料硅橡胶的表面,形成抗菌功能涂层。采用JSM-6700F型场发射扫描电子显微镜(FSEM)、PHI 1600 ESCA型X射线能谱仪(XPS)和接触角测试仪等,对抗菌硅橡胶的微观形貌、化学结构和亲疏水性等进行表征分析,利用抑菌环法和震荡烧瓶法对其抗菌性能进行测定。
1 实验
1.1 材料与试剂
壳聚糖(CS),浙江玉环海洋生物化学有限公司生产;大肠杆菌、金黄色葡萄球菌,硝酸银、硝酸铜、PBS、乙醇等其他试剂均为分析纯;硅胶,南晨生硅橡胶股份有限公司生产。
1.2 壳聚糖/银-铜复合抗菌剂(CAC)的制备
将1 mmol/L的 AgNO3和0.5 mmol/L的Cu(NO3)2按设计比例溶于100 mL去离子水中,在一定温度下搅拌2 h;然后加入0.5 g壳聚糖(CS)固体粉末,在一定温度下恒温搅拌0.5 h,得到抗菌剂悬浊液;在常温下进行抽滤、干燥、研磨,最终得到淡蓝色粉末状抗菌剂[15]。
1.3 抗菌硅橡胶的制备
首先将一定尺寸的硅橡胶悬挂,并用丙酮、盐酸等化学试剂进行表面清洗,主要是去除表面的污渍。之后将其置于紫外辐射下进行表面活化,激发硅橡胶表面的活性基团,以备抗菌剂能与之结合。最后将样品在制备好的抗菌剂中进行浸泡,一定时间、温度之后取出干燥[16],最终得到抗菌硅橡胶。
1.4 壳聚糖/银-铜复合抗菌剂(CAC)对细菌的抑菌性能
本文参照日本标准JIS Z2801—2010[17],大肠杆菌和金黄色葡萄球菌作为试验菌,复抗菌剂采用计算细胞存活率和菌环法评定其抗菌性能,抗菌硅橡胶测定采用震荡烧瓶法表征其抗菌活性,并计算抑菌率。
2 结果与讨论
2.1 壳聚糖/银-铜复合抗菌剂的工艺参数优化及其结构表征
2.1.1 工艺参数对CAC复合抗菌剂抗菌性能的影响
图1-a和1-b分别为不同反应温度下大肠杆菌和金黄色葡萄球菌的抑菌环抑菌效果图。从图中可以看出,温度梯度为40→50→60 ℃ 时,大肠杆菌和金黄色葡萄球菌的抑菌环直径分别为11 mm和12 mm,远远大于日本卫生标准的7 mm,说明抑菌效果良好。其原因是梯度的反应温度提供了递增的能量,使得硝酸银分散较好,也易形成小粒径的银单质。比较恒温40 ℃和50 ℃的结果,也可以看出升高温度有利于提高还原反应的速度,增加了反应体系中纳米颗粒的成核率,从而形成更多的纳米颗粒[18]。所以升高一定的反应温度可以使粒径变小,且不会发生团聚现象。当反应温度达到60 ℃时,抗菌剂中的粒子会发生剧烈的碰撞,且壳聚糖发生降解,导致银离子很难与壳聚糖发生螯合。所以选择温度梯度为40→50→60 ℃为制备CAC复合抗茵剂的最佳反应温度。
从图1-c和1-d中可以看出,当硝酸盐摩尔比n(AgNO3)∶n(Cu(NO3)2)=1∶3时,大肠杆菌和金黄色葡萄球菌的抑菌环直径分别为11 mm和9 mm,其抑菌效果良好。其原因是在此比例下,硝酸铜过量会使Ag+更多地与壳聚糖分子中的氨基发生反应,从而获得更多的单质银。

a,c,e-大肠杆菌;b,d,f-金黄色葡萄球菌图1 不同工艺条件的CAC复合抗菌剂的抑菌环效果图Fig.1 Inhibition zones of CAC at different process conditions against(a,c,e-E.coli;b,d,f-S.aureus)
从图1-e和1-f中可以看出,粒径大小会对抗菌剂的抗菌性能产生影响,主要是因为抗菌剂粒径较小,与细菌接触时的比表面积会增大,从而加大杀死细菌的几率。
综上所述,制备CAC复合抗菌剂的最佳工艺条件为:温度梯度为40→50→60 ℃,n(AgNO3)∶n(Cu(NO3)2)=1∶3,粒径较小时,抗菌性能最优。
2.1.2 CAC复合抗菌剂的微观表面形貌
图2-a 显示为优化后的CAC复合抗菌剂的扫描电镜照片。图中可以明显看出其外观结构致密,呈大块片层状,且表面存在均匀的颗粒状物质。通过XPS元素分析可见Ag、Cu、C、N和O等元素(图2-b)的峰值出现,从而可以确定此制备过程发生了还原反应,有单质银或者是铜的颗粒生成。

图2 CAC复合抗菌剂的SEM图(a)和XPS元素谱图(b)Fig.2 SEM image (a) and XPS element pattern (b) of CAC
图3为优化后CAC复合抗菌剂的透射电镜照片。图中可以看到,颗粒状物质均匀分散在基体表层上,形状多为球形或类球形,无团聚现象。其原因是此制备过程并没有改变壳聚糖本身的片层结构,这种结构可以充当稳定剂[19],从而避免颗粒的团聚。

图3 不同放大倍数下的CAC 复合抗菌剂的TEM 图像Fig.3 TEM micrographs of CAC under different magnification
2.1.3 CAC复合抗菌剂的晶体结构分析
图4所示为CAC复合抗菌剂的XRD谱图。CAC复合抗菌剂在2θ=19.6°,44.3°处有吸收峰。19.6°是壳聚糖的吸收峰,44.3°是银的吸收峰。用公式D=Kλ/Bcosθ计算出此晶面间距是0.201 nm,是银的(200)晶面。表明所制得的抗菌剂中有纳米银粒子,且制备过程并没有改变纳米银的晶体结构。
这里的K是谢乐常数,等于0.89;λ等于0.154 056 nm;B是吸收峰的半峰宽,θ是吸收角度。

图4 CAC复合抗菌剂的XRD谱图Fig.4 XRD spectrum of CAC antibacterial agent
2.1.4 CAC复合抗菌剂的热稳定性分析
图5所示是CS/Ag溶胶和CAC复合抗菌剂的热稳定性能的谱图。由图可知,CS/Ag溶胶的初始分解温度为65 ℃,而CAC复合抗菌剂的初始分解温度为135 ℃。很明显,加入铜之后的抗菌剂热稳定性提高了大约70 ℃。其原因是壳聚糖特殊的片层状结构,且加入铜之后的壳聚糖基体表面更致密,使得结构更稳定。这一性能可以应用于耐温抗菌材料的领域,从而扩展了抗菌剂的应用范围,对材料的发展有更重要意义。

图5 CS/Ag溶胶和CAC复合抗菌剂的TGA曲线图Fig.5 TGA curves of CS/Ag colloidal sol and CAC composite antibacterial agent
2.1.5 CAC复合抗菌剂的抗菌性能
图6为使用CAC复合抗菌剂分别对大肠杆菌和金黄色葡萄球菌的细菌存活率。从大肠杆菌的细菌存活率中(6-a)可以看出,其细菌的存活率为18%,抗菌性能优良;从金黄色葡萄球菌的细菌存活率中(6-b)也可以看到细菌存活率较低,仅有26%,说明CAC复合抗菌剂对大肠杆菌和金黄色葡萄球菌有较好的抗菌性。将两图同向对比,可以得知CAC复合抗菌剂对大肠杆菌比金黄色葡萄球菌的抗菌能力要强。
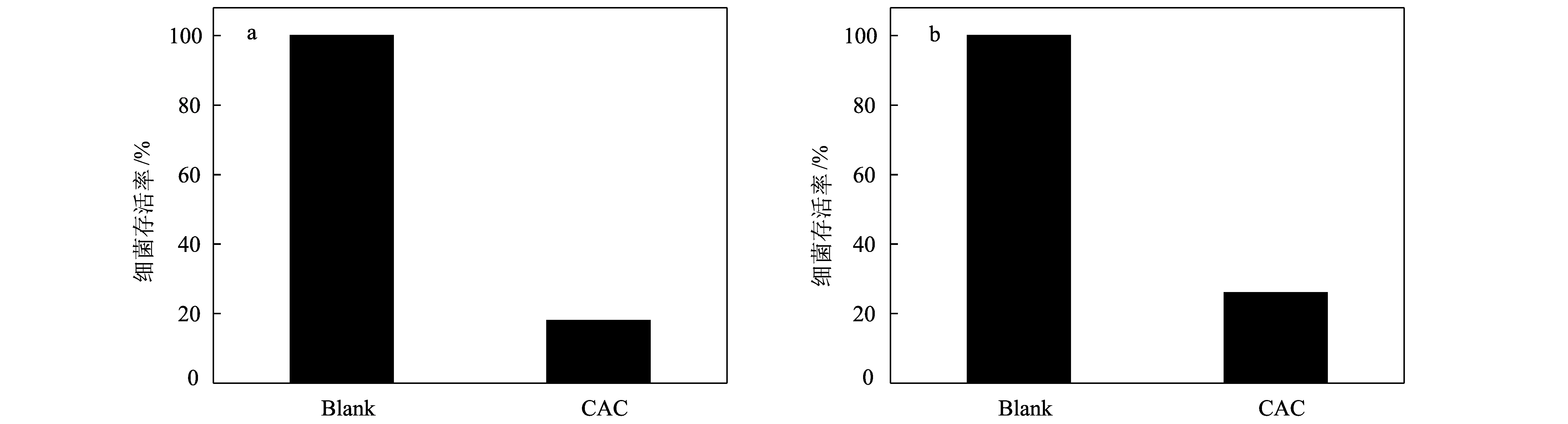
图6 CAC复合抗菌剂对大肠杆菌(a)和金黄色葡萄球菌(b)的细菌存活率Fig.6 Degree of microbial growth (%) for E. coli (a) and S. aureus (b) when using the CAC antibacterial agent
2.2 抗菌硅橡胶的结构及其抗菌性能
2.2.1 抗菌硅橡胶的微观形貌
图7为接枝CAC复合抗菌剂后硅橡胶的表面与断面SEM图像。由图7-a可以看出,基体表面抗菌涂层致密并且平整,可以看到细小的微球状物质堆砌在表面。由图7-b可以明显地看到,厚度大约为50 μm的抗菌涂层与基体结合紧密,且抗菌涂层覆盖了整个基体表面。

图7 抗菌硅橡胶的SEM图像(a-表面;b-断面)Fig.7 SEM images of antibacterial silicone rubber (a) on the surface (b) on the cross-section
2.2.2 抗菌硅橡胶的XPS分析
通过XPS曲线确定元素的种类和价态。由图8-a可以看出,抗菌涂层中的各元素的法向分量表现为峰(Ag 3d) (图8-b),(Cu 2p)(图8-c),(Si 2s)、(Si 2p) (图8-d)。分析单个元素的XPS谱图,由图8-b中得知,(Ag 3d)有明显的两个峰值,归因于(Ag 3d)3/2(372.7 eV) 和(Ag 3d)5/2(368.0 eV)两个轨道,其代表的是Ag+和Ag0两个价态;利用XPS Peak软件将其进行分峰拟合,用分峰后的面积公式计算得到单质银所占比例为70%,因此银主要以单质银存在于基体中[20]。图8-c中可以看到,在结合能为937.7 eV处有一个强特征峰,其代表的是Cu2+的信号,造成键结合能有偏差的原因可能是抗菌剂自身pH值、制备温度和其他金属对其的影响[21],此制备过程没有改变铜的价态,Cu2+主要是充当抗菌有效成分。
将抗菌硅橡胶中各元素的含量计算结果列于表1中,从表中可以看出银和铜的含量(质量分数)分别为0.17%和1.67%,虽然其含量较少,但仍可说明有抗菌成分银和铜结合到硅橡胶基体中[22],这与EDS谱图的分析结果相吻合。

a-抗菌硅橡胶;b-Ag元素;c-Cu元素;d-Si 元素图8 CAC复合抗菌剂接枝硅橡胶后的XPS谱图Fig.8 XPS spectrograms of antibacterial silicone rubber a,element Ag b,element Cu c and element Si d

表1 抗菌硅橡胶的元素分析
2.2.3 抗菌硅橡胶的接触角测试分析
图9所示为硅橡胶和抗菌硅橡胶的接触角测试结果。图9-a所示的硅橡胶接触角为106°,而图9-b的抗菌硅橡胶的接触角为87°,其接触角明显下降,样品表面由疏水性变成了亲水性。其原因是接枝CAC复合抗菌剂后,抗菌剂上的亲水性基团—OH和—NO3对硅橡胶的影响,所以CAC复合抗菌剂改善了硅橡胶的亲水性,从而扩大了硅橡胶在医用制品中的应用范围。

图9 接触角测试的试验结果 (a-硅橡胶;b-抗菌硅橡胶)Fig.9 Contact angle measurements of (a) Silicone rubber (b) antibacterial Silicone rubber
2.2.4 抗菌硅橡胶的抗菌性能震荡烧瓶测试
利用震荡烧瓶实验法测试其抑菌率,所选用的测试菌种是大肠杆菌与金黄色葡萄球菌,测试结果见表2所示。样品对大肠杆菌与金黄色葡萄球菌的抑菌率均大于96%,显示出较高的抑菌水平。
3 结论
1) 本实验制备CAC复合抗菌剂的最佳工艺条件为:温度梯度为40→50→60 ℃,n(AgNO3)∶n(Cu(NO3)2)=1∶3;其细菌存活率对大肠杆菌和金黄色葡萄球菌仅达到18%和26%;初始分解温度较CS/Ag溶胶提高了大约70 ℃,具有良好的抗菌性和热稳定性。
2) 采用该工艺制得的CAC复合抗菌剂中,银主要是以纳米级的单质银存在,起主要抗菌作用。
3) 将CAC复合抗菌剂接枝到硅橡胶表面制成抗菌硅橡胶,其抗菌功能层厚度约为50~70 μm。
4) 由于亲水性基团—OH和—NO3的加入,使得硅橡胶表面由疏水性变为亲水性,且对大肠杆菌和金黄色葡萄球菌的抑菌率均达到96%以上,抗菌性能良好,可用于医疗治疗的橡胶抗菌导管制作,广泛应用于医疗卫生领域。
[1] 张利,刘春,魏丽乔,等.抗菌医用导尿管的抗感染性能测试[J].太原理工大学学报,2013,43(06):655-659.
[2] Patel H R,Arya M.The urinary catheter:‘a-voiding catastrophe’[J].Hospital medicine (London,England:1998),2001,62(3):148-149.
[3] 许并社,魏丽乔,肖传实,等.纳米级壳聚糖与胶乳接枝共聚物的制备工艺:中国,ZL200810055431.2[P].2011-05-25.
[4] 魏丽乔,许并社,卢英兰,等.一种纳米硅酸盐抗菌组合物及其制备方法:中国,ZL02102183.X [P].2007-06-27.
[5] 吉向飞,李玉平.抗菌剂及抗菌材料的发展和应用[J].太原理工大学学报,2003,34(1):11-15.
[6] 马滢,刘鹏涛,刘忠.羧甲基壳聚糖的制备及其在抗菌纸中的应用[J].功能材料,2010(4):648-651.
[7] Božanic' D K,Trandafilovic' L V,Luyt A S,et al.‘Green’synthesis and optical properties of silver-chitosan complexes and nanocomposites[J].Reactive and Functional Polymers,2010,70(11):869-873.
[8] 王婧.壳聚糖/纳米银复合抗菌剂合成及羊毛抗菌层界面形成机理探索[D].太原:太原理工大学,2012.
[9] An J,Ji Z,Wang D,et al.Preparation and characterization of uniform-sized chitosan/silver microspheres with antibacterial activities[J].Materials Science and Engineering:C,2014,36:33-41.
[10] 朱玲英,郭大伟,顾宁.纳米银细胞毒性体外检测方法研究进展[J].科学通报,2014,(22):2145-2152.
[11] 荔霞,刘永明,齐志明,等.纳米铜毒性研究进展[J].动物医学进展,2010,31(8):74-78.
[12] Reicha F M,Sarhan A,Abdel-Hamid M I,et al.Preparation of silver nanoparticles in the presence of chitosan by electrochemical method[J].Carbohydrate polymers,2012,89(1):236-244.
[13] Tan K S,Cheong K Y.Advances of Ag,Cu,and Ag-Cu alloy nanoparticles synthesized via chemical reduction route[J].Journal of nanoparticle research,2013,15(4):1-29.
[14] 朱晓红,桑青,倪付花,等.壳聚糖及壳聚糖铜对6种植物病原真菌的抑菌活性[J].安徽农业科学,2010,(18):9577-9579.
[15] 张利,魏丽乔,康虹,等.一种壳聚糖与银铜共混制备复合抗菌剂的方法:中国,ZL201410379214.4[P].2014-11-19.
[16] 沙晓娟,郭睿劼,赵起,等.表面改性在提高硅胶基体与抗菌涂层结合力中的应用[J].化工进展,2014,33(6):1513-1516.
[17] JIS Z 2801-2010 Antibacterial products:Test for antibacterial act[S].Japanese industrial specifications.Japan:2012.
[18] Zhou N,Liu Y,Li L,et al.A new nanocomposite biomedical material of polymer/Clay-Cts-Ag nanocomposites[J].Current Applied Physics,2007,7:e58-e62.
[19] Donia A M,Atia A A,Elwakeel K Z.Recovery of gold (Ⅲ) and silver (Ⅰ) on a chemically modified chitosan with magnetic properties[J].Hydrometallurgy,2007,87(3):197-206.
[20] 陈晓丽. SiO-2载银复合抗菌剂的色泽改性及其在纺织品中的应用[D].太原:太原理工大学,2013.
[21] Yuan W,Liu X,Li L.Synthesis,characterization and photocatalytic activity of cubic-like CuCr2O4 for dye degradation under visible light irradiation[J].Applied Surface Science,2014,319:350-357.
[22] Fuchs M,Abidin Z,Kübel C,et al.Patterned deposition of allophane nanoparticles on silicon substrates[J].Clays and Clay Minerals,2012,60(5):456-463.
(编辑:庞富祥)
Preparation of Chitosan/silver-copper Composite Antibacterial Agent and Its Application on Silicone Rubber Matrix
KANG Honga,MA Senyuana,GAO Xianghuab,SONG Xiulonga,LI Xianxiana,WEI Liqiaoa
(a.KeyLaboratoryofInterfaceScienceandEngineeringinAdvancedMaterialsof
TaiyuanUniversityofTechnology,MinistryofEducation;b.CollegeofMaterialsScienceandEngineering,TaiyuanUniversityofTechnology,Taiyuan030024,China)
In this paper, Chitosan/Silver/Copper (CAC) antibacterial agent was prepared by chemical reduction, an antibacterial polymer material of silicone rubber was obtained by grafting surface functional groups onto silicone rubber matrix. The sample was characterized by scanning electron microscopy (SEM), transmission electron microscopy (TEM),and X-ray photoelectron spectroscopy (XPS). The antibacterial activity of composite antibacterial agents and antibacterial materials was characterized by inhibition zones and shake flask tests. Finally, the conclusion was:the degree of microbial growth of CAC against E.coli and S.aureus is only 18% and 26% respectively,the initial decomposition temperature of CAC is about 70 ℃ higher than that of CS/Ag colloidal sol, CAC antibacterial agent exhibits high antibacterial activities and thermal stability;The preparation process for the antibacterial silicone rubber is simple and inexpensive,the thickness of antibacterial function layer is about 50-70 μm, the antibacterial ratio is above 96% for E.coli and S. aureus,with excellent antibacterial activities.
antibacterial agent;antibacterial silicone rubber;antibacterial activity
1007-9432(2015)05-0489-06
2015-03-23
山西省科技项目资助:医用纳米抗菌导管材料的开发(800104-02010005)
康虹(1989-),女,内蒙古包头市人,硕士生,主要从事抗菌材料、高分子材料表面改性的研究,(E-mail)18334704725@163.com,(Tel)18334704725
马森源,男,教授,主要从事环保型阻燃、防火材料的研究,(E-mail)senyuanma@hotmail.com,(Tel)13466828636
TB333
A
10.16355/j.cnki.issn1007-9432tyut.2015.05.002
