清蛋白结合型紫杉醇单药三线或以上维持治疗非小细胞肺癌的临床观察
2015-03-16吴异兰赵忠全欧阳学农
王 晗,吴异兰,赵忠全,欧阳学农△
(1.南京军区福州总医院肿瘤科,福州 350025;2.福建中医药大学,福州 350025)
·论 著·
清蛋白结合型紫杉醇单药三线或以上维持治疗非小细胞肺癌的临床观察
王 晗1,吴异兰2,赵忠全1,欧阳学农1△
(1.南京军区福州总医院肿瘤科,福州 350025;2.福建中医药大学,福州 350025)
目的 探讨非小细胞肺癌(NSCLC)患者在三线或多线接受清蛋白结合型紫杉醇单药治疗有效后,继续维持治疗的疗效和不良反应。方法 将19例在三线治疗或以上治疗中使用清蛋白结合型紫杉醇4个周期无进展的患者分为维持治疗组(9例)和对照组(10例),维持治疗组继续使用清蛋白结合型紫杉醇单药维持治疗,直到病情进展或不能耐受为止。结果 维持治疗组患者和对照组患者的无进展生存时间(PFS)分别为4.4个月和5.66个月,不良反应为血液学毒性和神经毒性等。结论 清蛋白结合型紫杉醇单药维持治疗三线或多线化疗的NSCLC患者具有临床疗效,不良反应可耐受。
肺癌; 清蛋白结合型紫杉醇; 化疗; 维持治疗
大多数非小细胞肺癌(NSCLC)确诊时已进入中、晚期,化疗给晚期NSCLC患者带来了一定的生存疗效,但肿瘤最终会对化疗药物产生耐药性而使疾病进展,因此患者需接受多线化疗。因多次治疗失败后患者体力通常评分不高,无法耐受不良反应较大的药物,目前三线治疗尚无标准化疗方案,仅有20%~30%的患者有条件接受,其余则难以从进一步化疗中获益[1]。因此应当选择有效、低不良反应的化疗药物,将三线治疗的机会利用好,延长患者生存期。清蛋白结合型紫杉醇是新型无溶剂型紫杉醇类化疗药物,是紫杉醇和清蛋白结合的纳米微粒,可通过稳定微管抑制肿瘤细胞有丝分裂,其使临床治疗晚期NSCLC患者有了更多选择。本研究探讨清蛋白结合型紫杉醇单药化疗用于三线或以上治疗有效后,继续使用其维持治疗的疗效和不良反应。报道如下。
1 资料与方法
1.1 一般资料 该院NSCLC患者19例,在三线治疗或以上治疗中使用清蛋白结合型紫杉醇4个周期无进展的患者,按照随机数字表法分为维持治疗组(9例)和对照组(10例)。随访时间截止于2014年1月,随访率100%。2组患者的性别、年龄等一般资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:(1)病理证实为NSCLC。(2)ⅢB期和Ⅳ期。(3)三线或以上化疗使用清蛋白结合型紫杉醇单药4个周期病情未进展。(4)预计生存期大于3个月;美国东部肿瘤协作组(ECOG)评分小于2分。(5)骨髓功能、肝肾功能和心电图均正常。(6)全部患者均有可评价病灶;可经CT或MRI检测病灶大小。见表1。
1.2 治疗方法 对照组给予最佳支持治疗,每6周随访行影像学检查,直至疾病进展或病死。维持治疗组继续使用清蛋白结合型紫杉醇单药化疗,直至疾病进展或出现不能耐受的严重不良反应。治疗期间每2个周期(6周)行影像学检查(CT或MRI)以评价化疗疗效,每周期进行相关实验室检测评价化疗安全性。2组患者均可使用免疫支持制剂及中成药,但不使用有抗肿瘤活性的中成药、细胞毒性抗肿瘤或分子靶向药物。清蛋白结合型紫杉醇用法:剂量130 mg/m2,于第1天、第8天滴注,每21 d为1个周期,使用前无需抗过敏预处理,将药物溶解于100 mL生理盐水,30 min内静滴完毕。化疗前给予5-HT3受体拮抗剂预防恶心、呕吐等不良反应,给药期间及给药后1 h内行心电监护。
1.3 疗效及不良反应评价标准 采用RECIST1.1版标准评价疗效,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD)。不良反应评价根据NCI-CTC3.0标准分为0~4级。每周期化疗前后评估监测药物对患者血液、神经、心脏、肝脏、肾脏等多个器官系统的不良反应,出现1~2级不良反应时行对症处理,3~4级时酌情减量或停药。
1.4 统计学处理 所有数据采用SPSS 19.0统计软件进行分析,不同亚组间比较应用χ2检验,生存分析使用Kaplan-Meier法。P<0.05为差异有统计学意义。
2 结 果
2.1 2组患者疗效结果比较 对照组患者PR 1例,SD 9例。维持治疗组患者中,1例患者完成了5个周期化疗后出现进展,4例患者完成6个周期化疗,1例患者完成7个周期化疗,2例完成了8个周期化疗,1例患者接受了10个周期化疗。维持治疗组患者PR 2例,SD 7例。无进展生存时间(PFS)为从化疗开始至疾病进展或病死时间。对照组患者PFS均数为4.4个月(95%CI3.96~4.83个月),中位PFS为4个月。维持治疗组患者PFS均数为5.66个月(95%CI4.86~6.46个月),中位PFS为5个月。2组比较差异有统计学意义(P=0.013)。见图1。
2.2 2组患者不良反应结果比较 维持治疗组患者2例CTC 4级粒细胞减少而降低化疗剂量;1例CTC 4级血小板减少,终止治疗;1例严重下肢感觉麻木而减量。维持治疗组和对照组各有2例患者治疗前心电图正常,但治疗期间出现心电图ST-T改变,但无任何症状。未出现任何过敏反应,呼吸系统、肾功能异常。见表2。
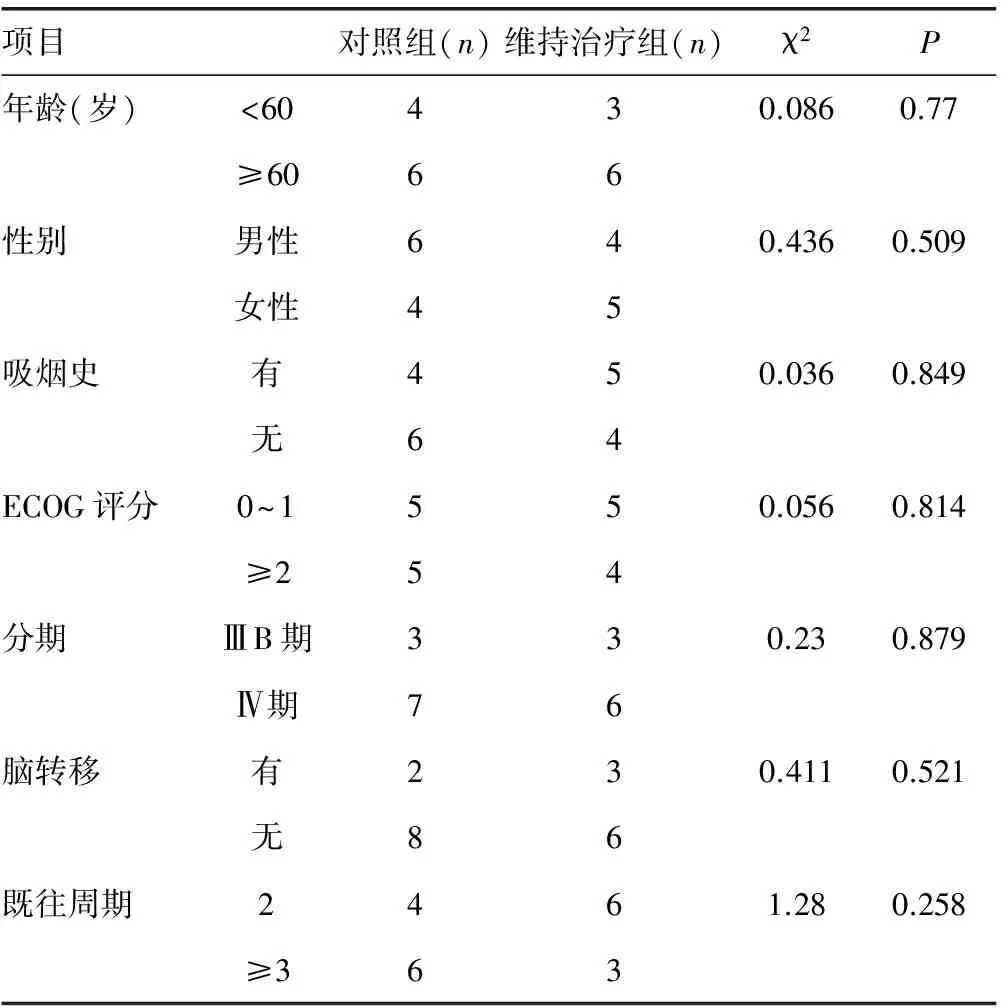
表1 2组患者一般资料结果比较

表2 2组患者接受清蛋白结合型紫杉醇的不良反应结果比较
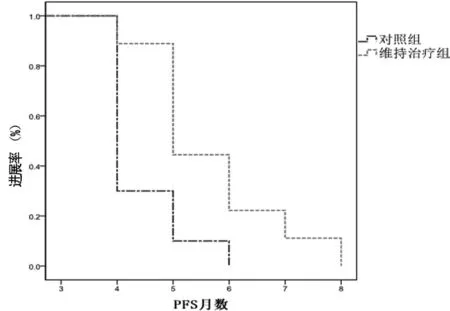
图1 2组患者接受清蛋白结合型紫杉醇的无进展生存期比较
3 讨 论
化疗是晚期NSCLC治疗的常用方案,但经过多种联合化疗后,患者最终仍将出现进展。如何利用化疗机会,在患者能耐受化疗时用维持治疗增加患者临床疗效,是目前研究的重点[2]。维持治疗的目的是患者在接受一定周期的化疗后巩固疗效,使肿瘤达到最大控制效应,以期最大限度地获得肿瘤缓解率及延长生存期。有研究表明经过4 个周期的化疗且疾病未进展的患者,维持化疗是一种可行选择[3]。有学者研究报道,同药维持治疗可延长NSCLC患者总体生存[4]。本研究选择接受过4个周期的清蛋白结合型紫杉醇治疗而未出现进展的患者,继续使用清蛋白结合型紫杉醇进行同药维持治疗。
本研究不良反应结果显示,2组患者的不良反应主要是血液学毒性,神经系统和胃肠道的不良反应,以及各种实验室检查异常。血液学毒性以中性粒细胞减少最为常见,经给予粒细胞集落刺激因子后均能恢复。2组患者贫血时常规补充铁剂,达到CTC 2级时,开始使用促红细胞生成素治疗,未出现CTC 4级贫血。感觉神经病变包括各种神经感觉异常。实验室检测可观察到轻度的丙氨酸氨基转移酶/天门冬氨酸氨基转移酶、碱性磷酸酶、尿酸升高,均无症状,不影响给药。所有患者均出现脱发,并有不同程度的乏力。
有研究文献表明,含铂的两药化疗方案为NSCLC一线化疗的地位,但铂类联合方案会使化疗相关的不良反应增加[5]。因此,在三线及以上化疗过程中单药治疗也是一个重要手段。有关研究结果显示,NSCLC二线治疗中,无论是否有效,培美曲塞单药组与联合组的疗效相当,因此单药治疗方案既可获得较好疗效又可保证其安全性,值得推荐[6]。本研究采用清蛋白结合型紫杉醇单药治疗,未联合使用铂类药物。同时在粒细胞集落刺激因子、促红细胞生成素支持下患者耐受性较好,能从维持治疗中获得PFS的改善。
相关学者在关于维持治疗的研究中发现,吉西他滨、培美曲塞等药物应用于NSCLC维持治疗时的PFS从5.1个月到3.8个月不等,与对照组比较,差异有统计学意义(P<0.05)[7-8]。维持治疗研究中,因所有患者最终都出现进展,有效率不作比较。本研究对照组的PFS均数为4.4个月,维持治疗组为5.6个月,2组比较,差异有统计学意义(P<0.05),和相关研究结果符合。
因为多药耐药的影响,多线化疗治疗失败出现进展后,许多化疗药物的疗效都不如一线治疗。紫杉醇在临床应用中对多种恶性肿瘤有较好疗效,但应用在NSCLC的二线化疗时则可能因多药耐药问题导致效果欠佳。本研究未纳入接受清蛋白结合型紫杉醇化疗满4周期前出现进展的患者,也排除一部分可能对清蛋白结合型紫杉醇耐药的患者,因此本组肿瘤对清蛋白结合型紫杉醇的反应较好,且对照组患者的PFS也大于4个月。有关研究提示,利用纳米技术设计的新型药物对克服多药耐药有帮助[9-10]。清蛋白结合型紫杉醇是新型纳米制剂,是由紫杉醇和人血清蛋白制成的微粒,利用清蛋白能和肿瘤间质中富含半胱氨酸的酸性分泌蛋白(SPARC)结合的特性,给药后药物能在肿瘤间质形成高浓度,从而增强疗效,对正常组织和器官的毒性较小,可以提高药物用量,对紫杉醇治疗失败的患者也有较好的疗效,且无需使用聚氧乙烯蓖麻油作为溶剂,过敏反应发生率低,安全性优于传统紫杉醇[11-13]。本研究维持治疗组患者PFS有延长,可能得益于该剂型。
综上所述,本研究结果表明,对于接受过多线化疗后出现进展的患者,使用清蛋白结合型紫杉醇单药进行维持治疗可使部分患者获益,且不良反应能耐受。但本研究样本量较少,还需更大样本量作进一步的研究。另外,相当一些靶向药物在维持治疗中也体现其价值,如西妥昔单抗、贝伐珠单抗等都被证实有效改善患者的临床疗效[14-15]。化疗药物联合靶向药物的治疗可能可以进一步提高三线以上化疗的效果,值得在将来的研究中深入探索。
[1]Syrigos KN,Saif MW,Karapanagiotou EM,et al.The need for third-line treatment in non-small cell lung cancer:an overview of new options[J].Anticancer Res,2011,31(2):649-659.
[2]Fidias P,Novello S.Strategies for prolonged therapy in patients with advanced non-small-cell lung cancer[J].J Clin Oncol,2010,28(34):5116-5123.
[3]Gerber DE,Schiller JH.Maintenance chemotherapy for advanced non-small-cell lung cancer:new life for an old idea[J].J Clin Oncol,2013,31(8):1009-1020.
[4]Paz-Ares LG,de Marinis F,Dediu M,et al.PARAMOUNT:Final overall survival results of the phase Ⅲ study of maintenance pemetrexed versus placebo immediately after induction treatment with pemetrexed plus cisplatin for advanced nonsquamous non-small-cell lung cancer[J].J Clin Oncol,2013,31(23):2895-2902.
[5]Schiller JH,Harrington D,Belani CP,et al.Comparison of four chemotherapy regimens for advanced non-small-cell lung cancer[J].N Engl J Med,2002,346(2):92-98.
[6]Ardizzoni A,Tiseo M,Boni L,et al.Pemetrexed versus pemetrexed and carboplatin as second-line chemotherapy in advanced non-small-cell lung cancer:results of the GOIRC 02-2006 randomized phase Ⅱ study and pooled analysis with the NVALT7 trial[J].J Clin Oncol,2012,30(36):4501-4507.
[7]Perol M,Chouaid C,Perol D,et al.Randomized,phase Ⅲ study of gemcitabine or erlotinib maintenance therapy versus observation,with predefined second-line treatment,after cisplatin-gemcitabine induction chemotherapy in advanced non-small-cell lung cancer[J].J Clin Oncol,2012,30(28):3516-3524.
[8]Obasaju C,Bowman L,Wang P,et al.Identifying the target NSCLC patient for maintenance therapy:an analysis from a placebo-controlled,phase Ⅲ trial of maintenance pemetrexed (H3E-MC-JMEN)[J].Ann Oncol,2013,24(6):1534-1542.
[9]Iyer AK,Singh A,Ganta S,et al.Role of integrated cancer nanomedicine in overcoming drug resistance[J].Adv Drug Deliv Rev,2013,65(13/14):1784-1802.
[10]Markman JL,Rekechenetskiy A,Holler E,et al.Nanomedicine therapeutic approaches to overcome cancer drug resistance[J].Adv Drug Deliv Rev,2013,65(13/14):1866-1879.
[11]Yardley DA.Nab-paclitaxel mechanisms of action and delivery[J].J Control Release,2013,170(3):365-372.
[12]Hirsh V.Nab-paclitaxel for the management of patients with advanced non-small-cell lung cancer[J].Expert Rev Anticancer Ther,2014,14(2):129-141.
[13]Socinski MA,Langer CJ,Okamoto I,et al.Safety and efficacy of weekly nab(R)-paclitaxel in combination with carboplatin as first-line therapy in elderly patients with advanced non-small-cell lung cancer[J].Ann Oncol,2013,24(2):314-321.
[14]HerbstRS,KellyK,ChanskyK,etal.PhaseⅡselectiondesigntrialofconcurrentchemotherapyandcetuximabversuschemotherapyfollowedbycetuximabinadvanced-stagenon-small-celllungcancer:SouthwestOncologyGroupStudyS0342[J].JClinOncol,2010,28(31):4747-4754.
[15]Barlesi F,Scherpereel A,Rittmeyer A,et al.Randomized phase Ⅲ trial of maintenance bevacizumab with or without pemetrexed after first-line induction with bevacizumab,cisplatin,and pemetrexed in advanced nonsquamous non-small-cell lung cancer:AVAPERL (MO22089)[J].J Clin Oncol,2013,31(24):3004-3011.
Clinic observation of albumin-bound paclitaxel in the maintenance therapy in third or more line treatment in non small cell lung cancer*
WANGHan1,WUYi-lan2,ZHAOZhong-quan1,OUYANGXue-nong1△
(1.DepartmentofOncology,FuzhouGeneralHospitalofNanjingMilitaryRegion,Fuzhou,Fujian350025China;2.FuijianUniversityofTraditionalChineseMedicine,Fuzhou,Fujiang350025,China)
Objective Observe the efficiency in non small cell lung cancer patients who receive maintenance therapy of albumin-bound paclitaxel after a third or more line treatment.Methods 19 patients,who receive maintenance therapy of albumin-bound paclitaxel after a third or more line treatment,were divided into 2 group:control group(10 cases) and maintenance group(9 cases),then maintenance group was treated with albumin-bound paclitaxel until progress disease or intolerable adverse effect.Results The PFS of control group and maintenance group were 4.4 months and 5.66 months,the adverse effect was mainly hematologic toxicity and neurotoxicity.Conclusion The maintenance therapy of albumin-bound paclitaxel is effective and well-tolerated in patients after a third or more line treatment.
lung cancer; albumin-bound paclitaxel; chemotherapy; maintenance therapy
国家自然科学基金项目(81274002);福建省自然科学基金项目(2012J01383);福建省卫生厅青年科研课题项目(2010-1-40)。
王晗,男,硕士,主治医师,主要从事肿瘤化学及生物治疗研究。△
,E-mail:oyxnong@163.com。
10.3969/j.issn.1672-9455.2015.12.003
A
1672-9455(2015)12-1665-03
2014-12-20
2015-02-15)
