注射剂中不溶性微粒的测定及其对微循环功能的影响
2015-03-09梁慧慧陈昕怡钱江辉沙先谊复旦大学药学院药剂教研室智能化递药教育部及全军重点实验室上海
梁慧慧,陈昕怡,钱江辉,沙先谊(复旦大学药学院药剂教研室/智能化递药教育部及全军重点实验室,上海
201203)
近年来注射剂中不溶性微粒可能引发患者严重不良反应等问题越来越引起医药工作者关注,如不溶性微粒造成局部组织缺血、血栓、组织肉芽肿、严重肺功能障碍甚至死亡[1]。然而,目前国内外药典对注射剂的不溶性微粒仅仅设定大于10µm和大于25 µm两个质控点,而对于小于10 µm的粒径,如2.5µm并未严格规定。目前,全球范围内对空气中不溶性微粒的人体危害越来越重视,国内许多一线城市已建立对空气中粒径为2.5µm的不溶性微粒的监测。因此,注射剂中缺乏控制的小粒径不溶性微粒是否会产生临床用药不良反应,也已成为一个重要的研究课题。
本研究选择祛痰药盐酸氨溴索注射剂(AHI)[2-3]为模型药物,考察并比较4个不同生产厂家的盐酸氨溴索注射剂中不溶性微粒的数量和分布;通过复制肢体缺血再灌注(LIR)大鼠小肠肠系膜微循环模型[4-5],考察4个厂家盐酸氨溴索注射剂中不溶性微粒在动物水平上对微循环功能的影响,旨在为进一步提高注射剂的内在质量与临床用药安全性提供参考依据。
1 材料
1.1 仪器
BH-2微循环显微镜(日本Olympus公司);BI-2000图像分析系统(成都泰盟科技有限公司);HANGPING FA-2004电子天平(上海天平仪器厂);MilliQ纯水仪(美国Millipore公司);台式离心机(北京市六一仪器厂);NICOMPTMCW788激光散射粒度仪(美国Nicomp公司);X90-3洁净工作台(上海正值净化科技有限公司,洁净度:100级)。
1.2 药品与试剂
盐酸氨溴索对照品(中国食品药品检定研究院,批号:100599-200502,纯度:>99.6%);盐酸氨溴索注射液[A厂(原研厂),国药准字J20140032,批号:227060(A1)、227086(A2)、128149(A3),规格:15 mg∶2 ml;B厂,国药准字H20041473,批号:20120202(B1)、20120204(B2)、20130132(B3),规格:15 mg∶2 ml];注射用盐酸氨溴索粉末[C厂,国药准字H20031344,批 号:20130327G6(C1)、20130327G10(C2)、20130406T4(C3),规格:每支30 mg;D厂,国药准字H20050243,批号:12100722(D1)、13022726(D2)、13031428(D3),规格:每支15 mg];聚苯乙烯微球标准品(上海启发生物科技有限公司,规格:0.5µm、2.5µm、25µm);甲醇、乙腈(美国TEDIA公司,色谱纯);其余试剂均为分析纯。
1.3 动物
2 方法
2.1 显微镜计数法测定不溶性微粒[6]
按照2010年版《中国药典》(二部)不溶性微粒检查法中显微镜计数法的规定操作,在洁净工作台内进行操作,分别测定A、B、C、D厂共12批盐酸氨溴索注射剂的有效滤过面积上最长粒径大于10 μm和大于25 μm的微粒数。其中,10 μm以上的微粒不得超过3 000粒/支,25 μm以上的微粒不得超过300粒/支。
2.2 光子相关光度(PCS)法测定不溶性微粒[7-9]
采用PCS法,用激光散射粒度仪测定A、B、C、D厂共12批盐酸氨溴索注射剂中不溶性微粒的粒径及分布。测定参数为He-Ne激光;测定角度:90°;温度:23 ℃;黏度:0.933 cPa;折光系数:1.333;波长:632.8 nm。对于注射液,取1支,将其外壁洗净,小心开启,用2ml一次性注射器抽取药液后立即注入检测池中,测定其粒径及分布;对于注射用粉末,先用灭菌注射用水溶解15 min后,再按照注射液的方法测定。
2.3 不溶性微粒对大鼠肠系膜微循环的影响
2.3.1 不溶性微粒混悬液的制备 取盐酸氨溴索注射液1支,用0.2µm孔径滤膜滤过,取滤膜上的残留物用250µl生理盐水重新混悬,即得;取注射用盐酸氨溴索粉末1支,先用生理盐水制备成7.5 mg/ml的溶液,再吸取2 ml用0.2µm孔径滤膜滤过,取滤膜上的残留物用250µl生理盐水重新混悬,即得;取3种粒径的聚苯乙烯微球标准品,用生理盐水稀释成50µg/ml的稀释液,即得。
2.3.2 分组、给药与取样 取大鼠于术前12 h禁食,自由饮水,采用Rosenthal法复制大鼠LIR模型,用橡皮圈环绕结扎大鼠双后肢根部,阻断血流4 h后松解,恢复血流灌注2 h后尾iv单次给药。实验分为模型组与正常组,每组再分为8小组,每小组10只,各组分别尾iv给予生理盐水、4个厂家的盐酸氨溴索注射剂和粒径为0.5、2.5、25 μm的聚苯乙烯微球,给药量为250µl。正常大鼠依次记为CN、CA、CB、CC、CD、CE、CF、CG组,模型大鼠依次记为RN、RA、RB、RC、RD、RE、RF、RG组。给药20 min后观测肠系膜微循环各项指标。
2.3.3 肠系膜微循环指标的观测 实验结束时暴露大鼠距回盲部10 cm处的肠系膜,固定于盛有37 ℃生理盐水的微循环灌流盒中,将微循环显微镜与图像分析系统连接,观察和记录各组大鼠肠系膜微循环变化,测定微静脉血流速度(Blood flow velocity of venule,BFVV)、微静脉管径(Diameter of venule,DV)。①BFVV的测定:采用光点同步扫描法测定BFVV,调节光点使之与血管平行并顺血流方向连续扫描,调节扫描速度使之与血流速度同步并记录;②DV的测量:取血管较直段,与血管纵轴垂直方向测血管直径3次,取平均值。
2.4 统计学处理
3 结果
3.1 不溶性微粒的显微镜计数法测定结果
4个厂家的盐酸氨溴索注射剂中不溶性微粒的数量均符合《中国药典》要求,并且厂家间比较差异无统计学意义(P>0.05)。显微镜计数法测定4个厂家盐酸氨溴索注射剂中不溶性微粒结果见表1。
3.2 不溶性微粒的PCS法测定结果
4个厂家的盐酸氨溴索注射剂在0.5~50 μm的粒子扫描范围内,其不溶性微粒的平均粒径和《中国药典》规定的两个质控粒径差别无统计学意义(P>0.05),但其小粒径(0.5~2.5 μm)的不溶性微粒数量差异具有统计学意义(P<0.05)。其中,盐酸氨溴索注射液的小粒径不溶性微粒数量明显少于注射用盐酸氨溴索粉末复溶15 min后的小粒径不溶性微粒数量。PCS法测定4个厂家盐酸氨溴索注射剂中不溶性微粒结果见表2,粒径分布见图1。
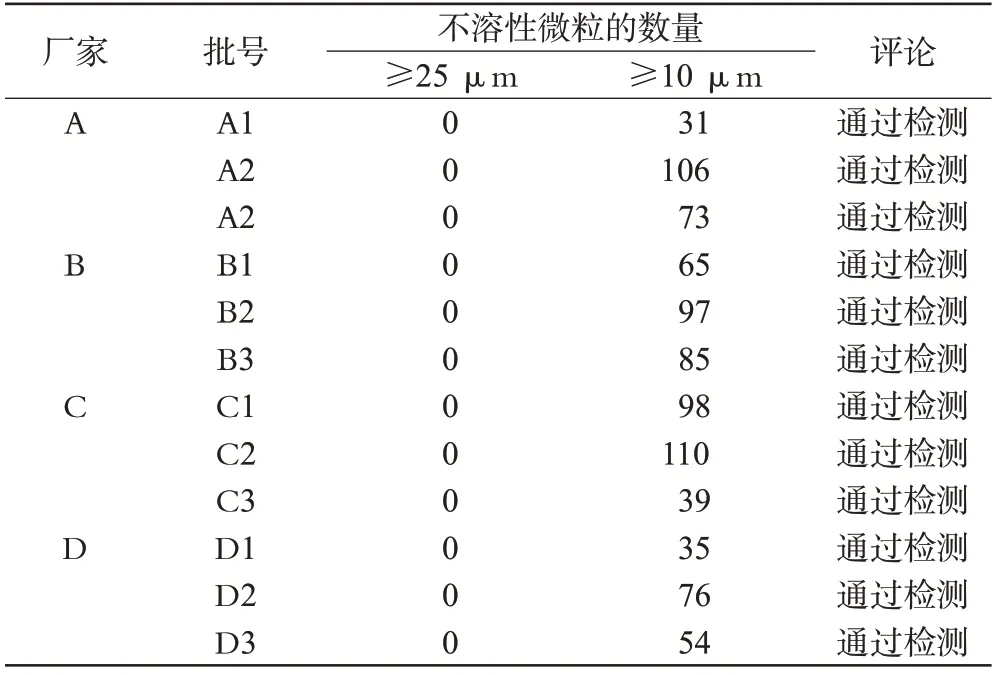
表1 显微镜计数法测定4个厂家盐酸氨溴索注射剂中不溶性微粒结果Tab 1 Results of insoluble particles of AHI from 4 manufacturers testing by microscope counting method
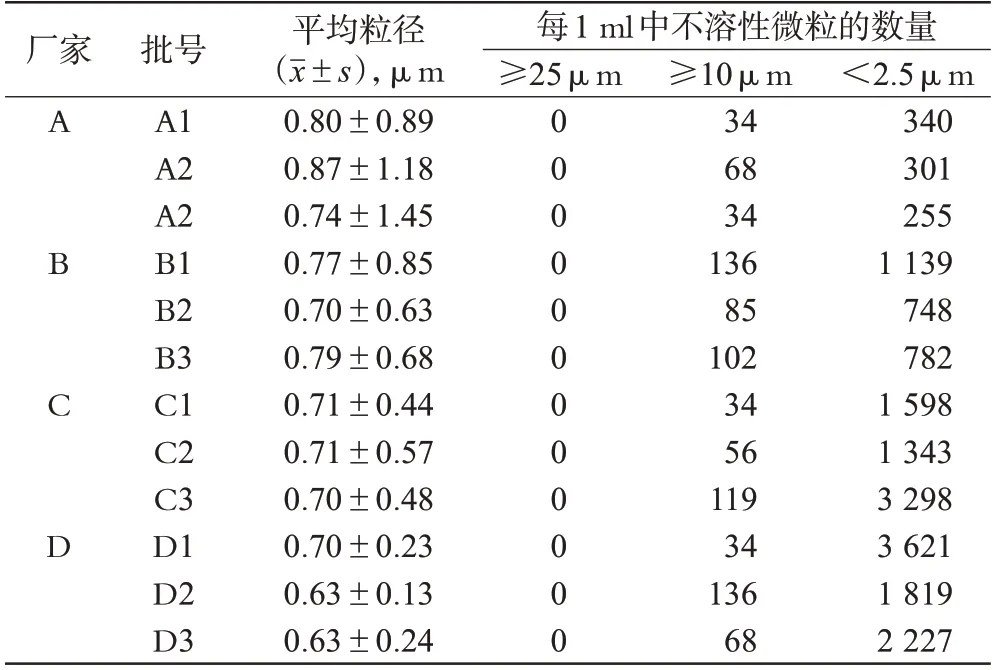
表2 PCS法测定4个厂家盐酸氨溴索注射剂中不溶性微粒结果Tab 2 Results of insoluble particles of AHI from 4 manufacturers testing by PCS
3.3 大鼠的肠系膜微循环情况
在正常状态下,与CN组比较,除CG组外其余各组大鼠BFVV明显减小,CB、CD、CE、CF组大鼠DV明显增加,差异具有统计学意义(P<0.01),其中CE、CF、CG组微循环效果与粒径大小呈负相关。LIR条件下,与RN组比较,其余各组大鼠BFVV明显减小,RB、RD组大鼠DV明显减小,差异具有统计学意义(P<0.01)。这表明在正常状态条件下,CA、CB、CC、CD组大鼠的肠系膜微血管均出现了一定程度的微循环障碍,其中CA组大鼠的微循环状态受影响程度最低,类似于CN组;CE、CF、CG组大鼠的肠系膜受到的微循环影响与粒径呈负相关,即粒径越小影响越严重。而在LIR状态下,RN组大鼠的肠系膜微血管表现出流速减慢的特征,表明成功复制了LIR模型;RA、RB、RC、RD组大鼠的肠系膜微循环均出现明显的一定程度的微循环障碍。正常状态下和LIR状态下各组大鼠的BFVV、DV比较分别见表3、表4。
4 讨论
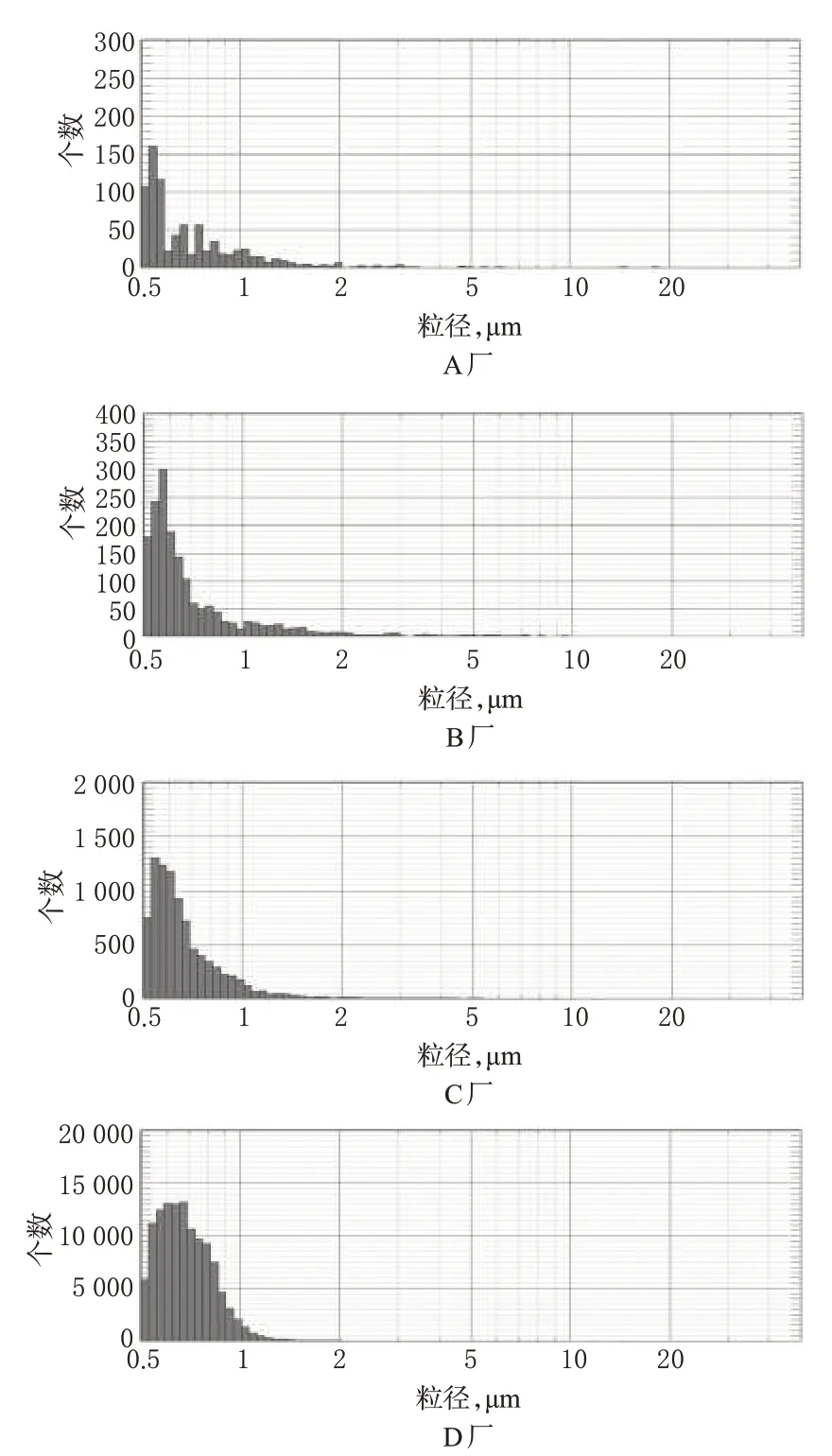
图1 4厂家盐酸氨溴索注射剂中不溶性微粒的粒径分布图Fig 1 Distribution of particle size of AHI from 4 manufacturers
表3 正常状态下各组大鼠的BFVV、DV比较(,n=10)Tab 3 Comparison of BFVV and DV of rats among groups in normal condition(,n=10)

表3 正常状态下各组大鼠的BFVV、DV比较(,n=10)Tab 3 Comparison of BFVV and DV of rats among groups in normal condition(,n=10)
注:与CN组比较,*P<0.01Note:vs.CN group,*P<0.01
本文采用PCS法考察了注射剂中不溶性微粒的粒径及分布。相比于显微镜计数法,PCS法更能直观地分析产品中不溶性微粒的分布。4个厂家的注射剂产品采用PCS法检测不溶性微粒的结果表明,不溶性微粒数量均符合《中国药典》规定;在0.5~50 μm的粒子扫描范围内,其不溶性微粒的平均粒径和《中国药典》规定的两个质控粒径差异无统计学意义(P>0.05),但小粒径的不溶性微粒数量差异具有统计学意义(P<0.05)。其中,原研A厂制剂中的不溶性微粒在此范围内的不溶性微粒数量相对少于其余3个厂家的产品。在考察的制剂中,盐酸氨溴索注射液的小粒径不溶性微粒数量明显少于注射用粉末,分析原因可能是:(1)注射用粉末由于需要加入一定量的甘露醇作为冻干保护剂,可能会引入不溶性微粒;另一方面,由于冻干粉末的溶解具有时间依赖性,未溶解的固体粉末可能也是导致在本研究的复溶时间条件下测定得的小粒径不溶性微粒偏多的重要原因,如延长冻干粉末的复溶时间,可能在一定程度上会降低注射用粉末中小粒径不溶性微粒的数量。(2)注射用粉末中胶塞在复溶过程中也可能导致一定程度的不溶性微粒的产生。(3)制备工艺的差异。
表4 LIR状态下各组大鼠的BFVV、DV比较(,n=10)Tab 4 Comparison of BFVV and DV of rats among groups in LIR condition(,n=10)

表4 LIR状态下各组大鼠的BFVV、DV比较(,n=10)Tab 4 Comparison of BFVV and DV of rats among groups in LIR condition(,n=10)
注:与RN组比较,*P<0.01Note:vs.RN group,*P<0.01
为了进一步评价制剂的内在质量,本文通过建立微循环的动物模型,考察了4个厂家盐酸氨溴索注射剂中不溶性微粒对微循环功能影响的差异性。研究发现,4个厂家的盐酸氨溴索注射剂组大鼠均出现了一定程度的微循环障碍,且影响微循环的程度具有明显的差异性。其中,原研A厂制剂中不溶微粒的数量相对较少,对微循环的影响程度也相对较轻。对于已有微循环损伤的机体(即LIR状态),注射剂中的不溶性微粒对其有更大的损伤。在阳性对照组中,0.5、2.5µm的不溶性微粒在正常状态下对微循环的影响反而高于25µm的不溶性微粒,这可能主要是由于25µm的不溶性微粒经静脉给药后大部分微粒被肺循环滤过后,减少了不溶性微粒在观察部位肠系膜微血管的蓄积,从而在一定程度上降低了不溶性微粒对微循环功能的影响,而小粒径微粒反而更易在微血管部位蓄积。已有文献报道,0.5µm左右的不溶性微粒与心血管系统疾病具有相关性[10],而注射剂中小粒径不溶性微粒数量的差异性是否会引起临床用药过程中患者的不良反应发生的差异性,以及是否具有剂量依赖性,则需要开展进一步的临床评价研究予以确证。
[1]王冰,张梅英.防范静脉输液中不溶性微粒危害的研究进展[J].上海护理,2009,9(1):63.
[2]杨晓蔚.氨溴索临床应用进展[J].中外医学研究,2010,8(12):26.
[3]杨惠娣,徐彬.氨溴索的作用机制及临床应用[J].中国医院药学杂志,2002,22(1):44.
[4]赵霞,孙娜,张连元.大鼠肢体缺血再灌注肠系膜微循环的变化[J].华北煤炭医学院学报,2010,12(1):1.
[5]姚树桐,桑慧,王家富,等.蜂胶水提液预处理对缺血再灌注大鼠小肠肠系膜微循环的改善作用及机制[J].中国病理生理杂志,2010,26(1):23.
[6]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:附录ⅨC.
[7]高玉成,贡立青,曲丹丹,等.基于光阻法原理的智能微粒检测仪[J].仪器仪表学报,2002,23(4):366.
[8]郑学宁,苏林,周金瑞,等.光阻法检查注射液中不溶性微粒[J].中国药学杂志,2002,37(6):458.
[9]沙先谊,马光磊,张娜娜,等.不同厂家依达拉奉注射剂中有关物质及不溶性微粒的比较[J].中国临床药学杂志,2010,19(5):295.
[10]Meng X,Ma Y,Chen R,et al.Size-fractionated particle number concentrations and daily mortality in a Chinese city[J].Environ Health Perspect,2013,121(10):1 174.
