AZ31镁合金表面羟基磷灰石涂层的制备和表征
2015-02-22杜华云安艳丽郭春丽卫英慧侯利锋
范 薇,杜华云,安艳丽,郭春丽,卫英慧,3,侯利锋
(1.太原理工大学 材料科学与工程学院,太原 030024;2.山西医科大学 基础医学院,太原 030001;3.吕梁学院,离石 033000)
AZ31镁合金表面羟基磷灰石涂层的制备和表征
范 薇1,杜华云1,安艳丽2,郭春丽1,卫英慧1,3,侯利锋1
(1.太原理工大学 材料科学与工程学院,太原 030024;2.山西医科大学 基础医学院,太原 030001;3.吕梁学院,离石 033000)
以氢氧化钙和磷酸二氢钙为前驱物,在AZ31镁合金表面通过溶胶凝胶法制备了羟基磷灰石涂层。利用X射线粉末衍射仪(XRD)、扫描电子显微镜(SEM)对涂层的物相组成、表面形貌、截面进行了分析表征,利用电化学工作站测试了该涂层在生理盐水中的动电位极化曲线和电化学阻抗谱,并对涂层在Hank’s模拟体液中的析氢量和浸泡腐蚀形貌进行了表征。结果表明,溶胶凝胶法制备的羟基磷灰石涂层纯度较高,结晶性良好,涂层厚度在8 μm左右;动电位极化曲线结果显示,该涂层的腐蚀电流密度为1.486 4×10-2mA/cm2,与空白镁合金的腐蚀电流密度相比降低了5倍左右。析氢试验及其浸泡腐蚀形貌进一步说明羟基磷灰石涂层能有效地保护镁合金基体。
生物材料;羟基磷灰石涂层;溶胶凝胶法;AZ31镁合金;耐蚀性
生物医用金属材料是用于医学材料的金属或其合金,如钴基合金、钛及钛合金和不锈钢等金属材料,是目前常用于临床医学的材料。由于这些材料的弹性模量与人骨的弹性模量不匹配,长期固定在人体内易引发炎症,需要二次手术取出[1]。AZ31镁合金因其具有密度小,比强度高,弹性模量及屈服强度与人体骨骼较接近等性能,成为最具研究价值的生物医用材料[2-3]。但是,镁合金的耐蚀性差,在生物体内降解速率快[4],不能满足其作为骨植入材料的要求。羟基磷灰石(HAP)耐蚀性高,化学性能好,有良好的生物相容性,是人体骨骼组织的主要成分[5-6],但其较低的抗疲劳强度、脆性,低强度和韧性及较差的抗弯强度又限制了其在人体承重部位的应用[7]。如果将羟基磷灰石覆盖在镁合金表面,不仅可以提高镁合金的耐蚀性能,延缓其降解速率,而且还使羟基磷灰石具有优良的力学性能[8]。因此,在镁合金表面制备羟基磷灰石涂层的研究有着较好的应用前景。
金属基表面制备羟基磷灰石涂层的方法很多,有激光熔覆法[9]、等离子喷涂法[10]、电化学沉积法[11]、仿生溶液法[12]、溶胶凝胶法等[13]。高亚丽[9]等人以65 μm的羟基磷灰石粉末为原料,质量分数为1%的Y2O3和4%聚乙烯醇为添加剂,采用激光熔敷法在铸态AZ91D镁合金表面涂覆了一层羟基磷灰石涂层,但由于激光功率过高,使部分羟基磷灰石发生分解或挥发,使表面涂层的形成变得不连续,同时会使部分镁合金基体熔融。Gu[10]等人在氩气气氛下,通过等离子喷涂技术在钛合金表面制备出羟基磷灰石/Ti-6Al-4V复合涂层,同样由于温度过高,表面的羟基磷灰石发生分解,表面涂层变得不连续。王燕[13]等人以硝酸钙和五氧化二磷为前躯体,通过溶胶凝胶法在纯镁表面制备了羟基磷灰石涂层。与其他方法相比,溶胶凝胶法操作简单,成本低廉,制备的涂层结晶性较好。但用Ca(OH)2和Ca(H2PO4)2·H2O制备羟基磷灰石涂层的研究还未见报道。
本实验首次以Ca(OH)2和Ca(H2PO4)2·H2O为前驱物,通过溶胶凝胶法在AZ31镁合金表面制备了厚度约8 μm的羟基磷灰石涂层,并对涂层的成分、截面形貌及其耐蚀性能进行了分析表征。
1 实验材料与方法
1.1 基体预处理
实验选用尺寸为20 mm×20 mm×1 mm的AZ31镁合金轧板为基体,经过600号、1 000号的砂纸打磨,去除表面的氧化物,用无水乙醇和去离子水超声清洗,之后再用4%稀磷酸溶液活化10 s,最后分别用去离子水、无水乙醇、去离子水超声清洗10 min。
1.2 羟基磷灰石涂层的制备
将配置好的Ca(OH)2过饱和溶液放入70 ℃水浴中加热,然后向其缓慢滴加适量的Ca(H2PO4)2·H2O溶液至钙磷摩尔比为1.67,强力搅拌1 h,静置;对其在80 ℃去水处理,使其成为凝胶。之后将经过预处理的镁合金放入上述凝胶中浸泡2 min,之后以0.1 mm/s的速度进行提拉,接着放在80 ℃干燥箱中干燥15 min,最后放入400 ℃电阻炉中热处理30 min。重复上述步骤5次,制得一定厚度的HAP涂层。
1.3 检测方法
使用X射线衍射仪(XRD,辽宁丹东TD-3500),采用Cu靶(λ=0.154 178 nm)和石墨单色器,步长为0.05°,角度范围为20°~60°,分析涂层的物相组成;日本理学JSM-6700F型扫描电子显微镜(SEM),在5 kV的高压下分析涂层的表面和截面形貌;武汉科斯特CS-350型电化学工作站,以铂电极为辅助电极,饱和甘汞电极为参比电极,生理盐水为腐蚀介质,扫描速率为1 mV/s,进行涂层的耐蚀性检测;利用Hank’s模拟体液测试了涂层的析氢腐蚀情况,并对其浸泡48 h的腐蚀形貌进行了SEM检测,其中Hank’s模拟体液的成分见表1[14]所示。
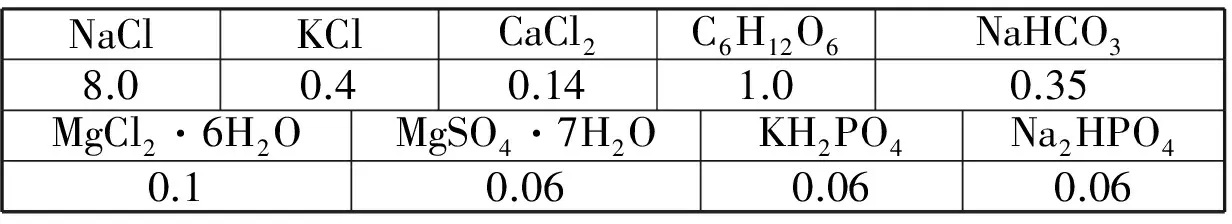
表1 Hank’s模拟体液的成分为 g/L
2 实验结果及讨论
2.1 XRD检测
由于溶胶凝胶法制备的羟基磷灰石涂层很薄,X射线会穿透膜层进入基体,而且羟基磷灰石的特征峰强度较低,会被镁的衍射峰掩盖。为了更好地确定涂层的成分,对从镁合金表面刮下来的粉体进行了XRD检测,得到如图1所示为溶胶凝胶法制备的羟基磷灰石粉体的XRD图。从图中可以看到,在25.88°,28.96°,31.77°,32.20°,32.90°,39.82°,46.71°,49.47°,能明显地看到HAP的特征衍射峰,这些峰与图中羟基磷灰石粉末标准衍射图谱(JCPDS#09-0432)基本一致,而且没有检测到其他杂质的衍射峰存在,说明利用该方法制备的羟基磷灰石纯度较高,其结晶性较好。
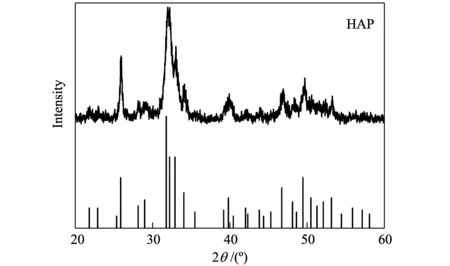
图1 从镁合金表面刮下来的羟基磷灰石粉体的XRDFig.1 X-ray diffraction patterns of HAP scraped from AZ31
2.2 SEM检测

图2 羟基磷灰石涂层的SEM图Fig.2 SEM micrographs of HAP coating
为了观察HAP涂层的形貌,对其进行了SEM检测。图2为制备的羟基磷灰石涂层表面形貌的SEM图。图2-a为羟基磷灰石涂层表面的微观形貌,可以看出,涂层表面有很多气孔形成,呈现出孔状结构,气孔的产生主要是由于凝胶在热处理过程中失去水分子所致;图2-b为HAP涂层表面的宏观形貌图,可以看到膜层表面均匀性较好,但有裂纹产生,裂纹的产生是因为HAP涂层与镁合金基体的膨胀系数及化学键型差别较大[15],在对其进行热处理及冷却过程中二者收缩不同导致涂层开裂,这是溶胶凝胶法不可避免的现象;图2-c为羟基磷灰石涂层的截面形貌,可以看到涂层厚度均匀,约为8 μm左右。
2.3 电化学测试
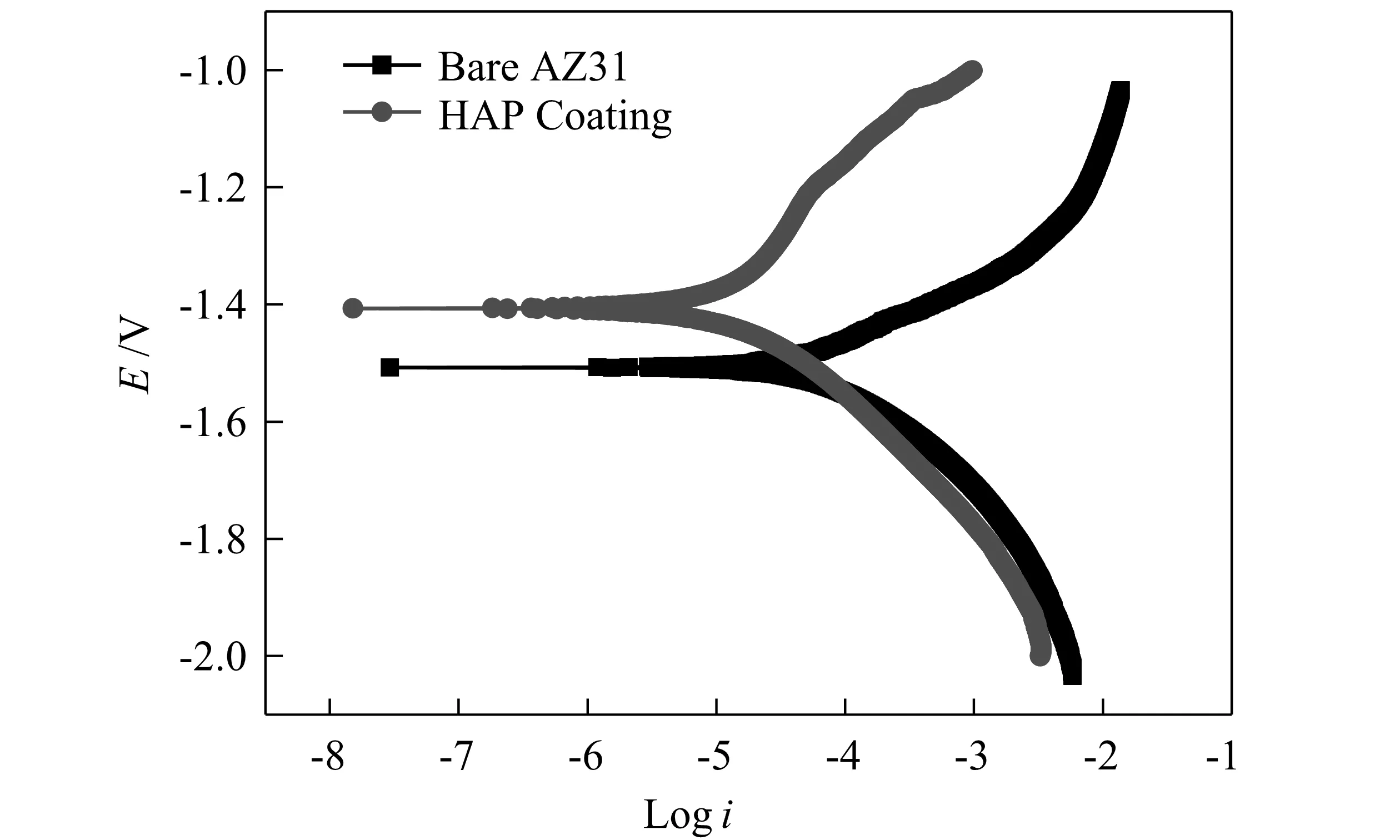
图3 基体处理前后在0.9%的氯化钠溶液中的极化曲线Fig.3 Polarization curves of bare AZ31 and HAP coating
医用植入材料在体内的腐蚀属于电化学腐蚀。图3为处理前后的AZ31镁合金在质量分数为0.9%的生理盐水中的动电位极化曲线。由图可以看出,处理前后二者阴极极化曲线斜率基本相似,基体表面处理后其自腐蚀电位升高,而且曲线整体左移了,说明其腐蚀电流密度减小,耐蚀性变好了。表2为通过CorShow软件拟合得到的腐蚀参数,可以看出,空白AZ31的自腐蚀电位为-1.507 9 V,而添加HAP涂层后基体的自腐蚀电位升高到-1.406 8 V,说明其耐蚀性有提高的趋势;空白样的腐蚀电流密度为7.3505×10-2mA/cm2,处理后试样的腐蚀电流密度为1.486 4×10-2mA/cm2,与空白镁合金相比降低了近5倍左右,进一步说明HAP涂层能减缓AZ31镁合金在体内发生腐蚀降解的速率,对基体起到保护作用。
电化学阻抗谱经常被用于研究电极材料、固体电解质及腐蚀防护等机理。图4为处理前后的试样在生理盐水中的电化学阻抗谱及其等效电路图。由阻抗图可以看到,处理前后试样的容抗弧直径大小不同,空白镁合金的阻抗曲线为一个小直径的高频区容抗弧和低频区容抗弧,涂层处理后试样的曲线由直径相对较大的高频区容抗弧和低频区容抗弧构成。因为容抗弧的半径越大,涂层电阻越大[16],腐蚀液就越难穿透涂层进入基体界面,因此HAP涂层可以保护镁合金基体,提高其耐蚀性,延缓腐蚀降解速率。
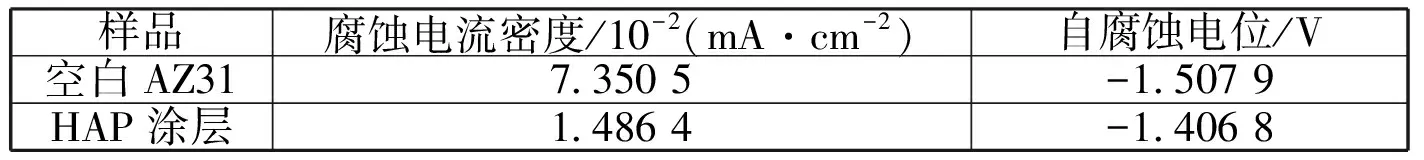
表2 CorShow软件拟合得到的腐蚀参数
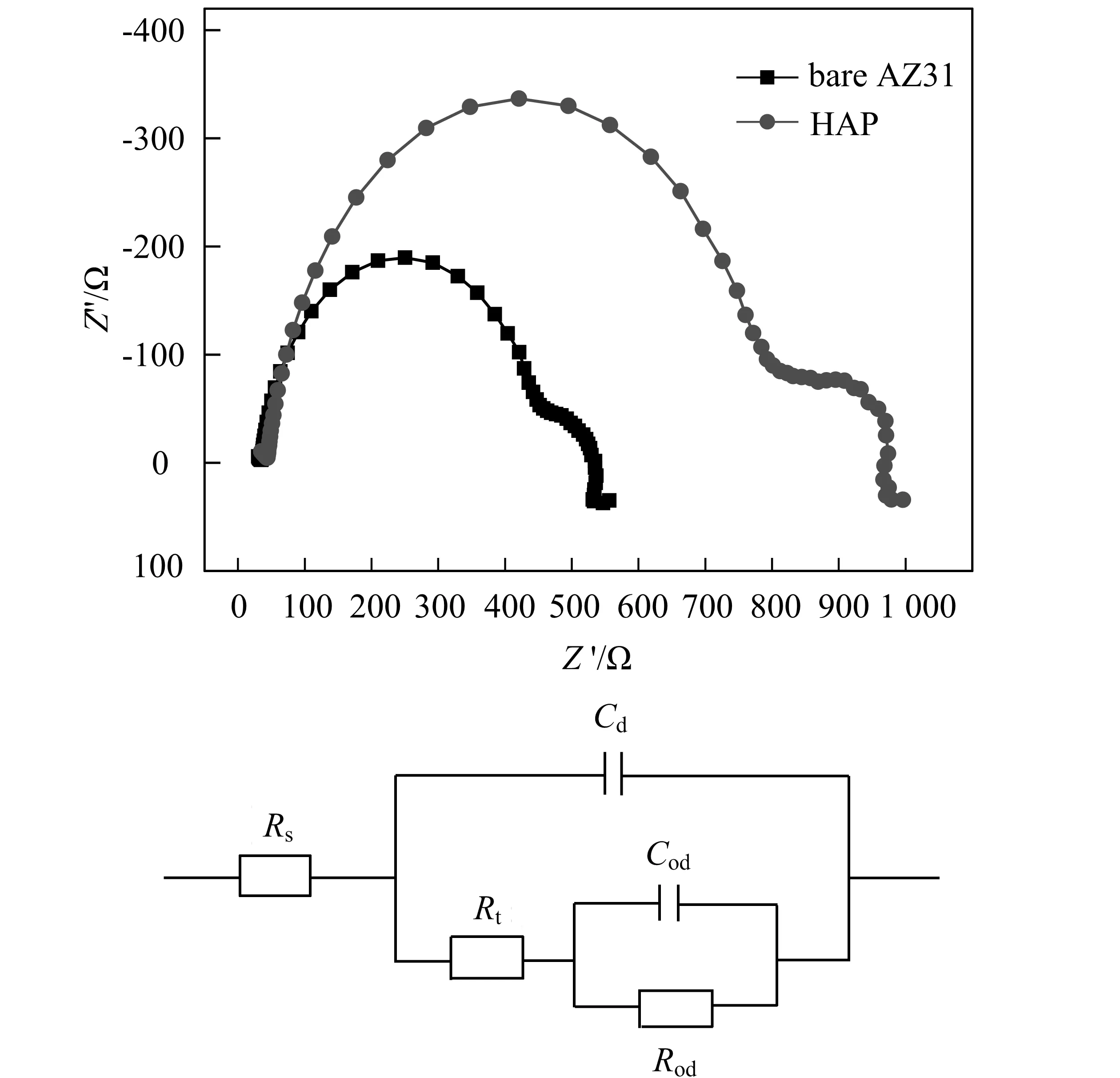
图4 涂层处理前后在0.9%的氯化钠溶液中的电化学阻抗谱及其等效电路Fig.4 Electrochemical impedance spectroscopy of different samples and equivalentcircuit
Zhang[17]等人在研究AZ91D镁合金表面涂层的电化学阻抗时,提出了等效电路的概念。其中高频区的阻抗特征和溶液界面的双电阻层有关,而低频区的阻抗特征与涂层的电阻相关。曹楚南[18]在研究金属表面涂层的破坏过程时得出,液体中水分和腐蚀介质渗透到涂层与基体界面,并和金属基体产生电化学反应,但涂层会阻碍腐蚀介质和水分的渗透,在相对较短的时间段,腐蚀介质和水分不能通过涂层到达涂层与金属基体的界面,在该界面还未发生微电化学反应。在该等效电路中,溶液电阻Rs表示溶液中的离子迁移时遇到的阻力,它一般只与腐蚀液的性质、温度及电解槽的形状大小有关,而与工作电极的关系不大;高频区半圆弧的最高点可以确定双电层电容Cd,电路中Rt为传递电阻,由大容抗弧的直径表示;小容抗弧由Rod和Cod所反映,它的形成是由于吸附型的HAP涂层在电极表面成膜后,本身就有一定的容性阻抗,小容抗弧的直径表示了电路中Rod的大小[19]。表3列出了电化学阻抗谱的拟合参数,可以看出,处理后试样的传递电阻Rt显著增加。Rt越大试样发生电化学反应时的电流就越小,而试样的腐蚀速率与该电流的大小相对应。即传递电阻Rt越大,腐蚀速率越慢。HAP涂层的腐蚀速度较慢,对基体的保护作用增强。

表3 涂层处理前后在0.9%的氯化钠溶液中的电化学阻抗拟合参数
2.4 浸泡腐蚀实验
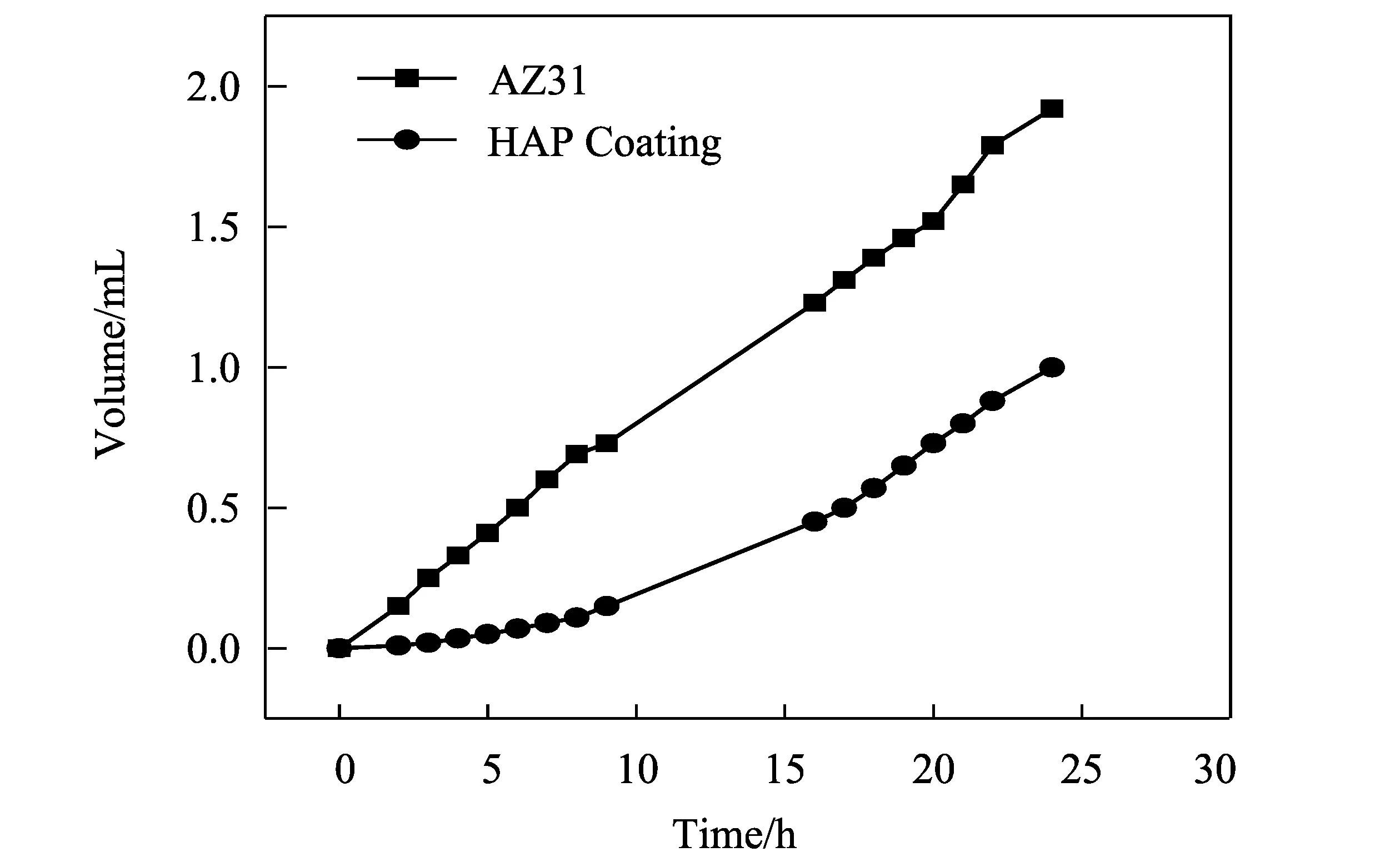
图5 两种基体在Hank’s模拟体液中的析氢腐蚀曲线Fig.5 Hydrogen evolution rates of different samples immersed in Hank’s solution
电化学测试能较为准确地测试AZ31镁合金表面HAP涂层腐蚀速率的大小[20],但该涂层在Hank’s模拟体液中的析氢试验能更好地描述其植入体内后的腐蚀降解情况,因此,对其在模拟体液中的析氢腐蚀进行了测试。图5为处理前后的AZ31镁合金在Hank’s模拟体液中腐蚀析出氢气的体积随时间变化的曲线图。由图可以看出,原始AZ31在模拟体液中产生氢气的速度较快,其体积随时间的变化几乎成正比,说明空白AZ31在模拟体液中保持着基本相同的溶解速度;涂覆羟基磷灰石涂层后,在较短时间内产生的氢气量较少,随后产生的氢气量逐渐增多,最后也几乎呈现出线性变化。这是因为在较短时间内,HAP涂层对镁合金基体保护作用较强,延缓了腐蚀液进入基体表面,当腐蚀液透过涂层缓慢进入基体并逐渐破坏涂层后,其对基体的保护作用慢慢减弱,最后呈现出与空白AZ31类似的线性变化趋势。
电化学测试描述的涂层耐蚀性是在较短时间内测量的,而材料植入人体后需要具备较长时间的耐蚀性。因此,对在Hank’s模拟体液中浸泡48 h后试样的腐蚀形貌进行了SEM检测,进一步描述HAP涂层对AZ31镁合金基体耐蚀性的影响。图6所示为处理前后试样在Hank’s模拟体液中浸泡48 h后的腐蚀形貌图。由图6-a可以看出,浸泡48 h后,空白镁合金的表面遭到严重破坏,产生了很多杂质,说明空白AZ31表面被模拟体液的腐蚀较为严重;图6-b可以看出,处理后的试样表面只出现了一些点蚀,涂层依然保持了其完整性,说明HAP涂层的存在可以延缓腐蚀液穿透涂层进入基体的速度,腐蚀液只能从涂层的裂纹和孔洞进入基体发生点蚀,进一步证实HAP涂层能有效保护镁合金基体,延缓其腐蚀降解速率。
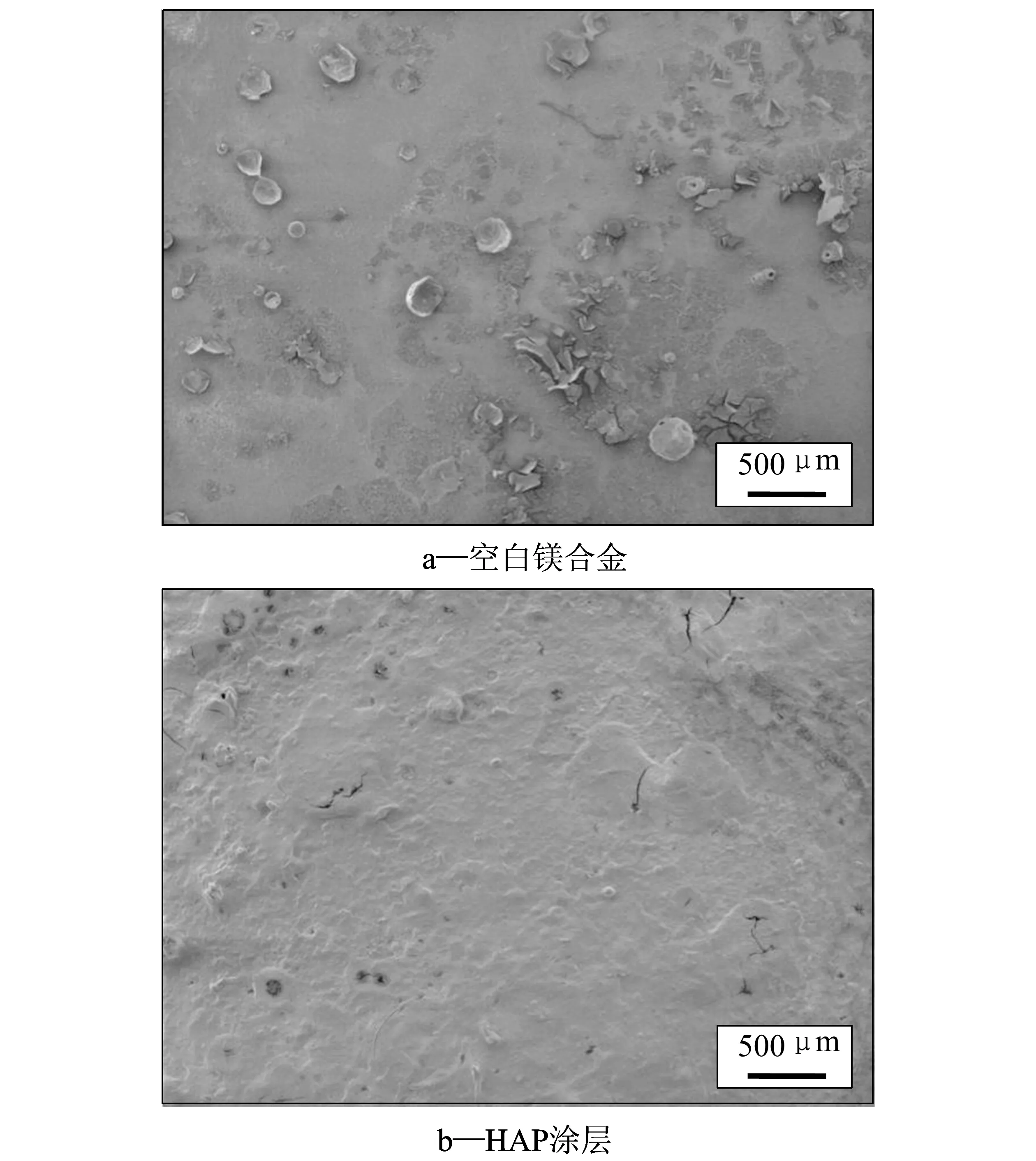
图6 处理前后的试样在Hank’s模拟体液中浸泡48 h的腐蚀形貌Fig.6 Corrosion morphologies of the samples immersed in Hank’s solution for 48 h
3 结论
通过溶胶凝胶法在AZ31镁合金表面制备出了纯度较高、结晶性较好的HAP涂层,涂层表面为多孔结构,且有裂纹产生,涂层厚度约为8 μm。HAP涂层的自腐蚀电位正移,而腐蚀电流密度降低了近5倍,即HAP涂层提高了AZ31的耐蚀性;Hank’s模拟体液中的浸泡析氢试验及其腐蚀形貌进一步证实了这一结果。
[1] Reclaru L,Lerf R,Eschler P Y,et al.Corrosion behavior of a welded stainless-steel orthopedic implant[J].Biomaterials,2001,22(3):269-279.
[2] Hermawan H,Dube D,Mantovani D.Developments in metallic biodegradable stents[J].Acta Biomaterialia,2010,6(5):1693-1697.
[3] 郑玉峰,刘彬,顾雪楠.可生物降解性医用金属材料研究进展[J].材料导报,2009,23(1):1-4.
[4] Rojaee R,Fathi M,Raeissi K.Controlling the degradation rate of AZ91 magnesium alloy via sol-gel derived nanostructured hydroxyapatite coating[J].Materials Science and Engineering:C,2013,33(7):3817-3825.
[5] Choudhury P,Agrawal D C.Sol-gel derived hydroxyapatite coatings on titanium substrates[J].Surface & Coatings Technology,2011,206:360-365.
[6] Yang C,Guo Y K,Zhang M L.Thermal decomposition and mechanical properties of hydroxyapatite ceramic[J].Transactions of Nonferrous Metals Society of China,2010,20(2):254-258.
[7] Singh G,Singh H,Sidhu B S.Corrosion behavior of plasma sprayed hydroxyapatite and hydroxyapatite-silicon oxide coatings on AISI 304 for biomedical application[J].Applied Surface Science,2013,284:811-818.
[8] 张雅静,张丹,习小慧,等.AZ31仿生沉积羟基磷灰石涂层的研究[J].东北大学学报:自然科学版,2011,32(11):1611-1614.
[9] 高亚丽,熊党生,王存山,等.医用镁合金激光熔敷羟基磷灰石涂层初探[J].特种铸造及有色金属,2009,29(4):305-307.
[10] Gu Y W,Khor K A,Cheang P.In vitro studies of plasma-sprayed hydroxyapatite/Ti-6Al-4V composite coatings in simulated body fluid (SBF)[J].Biomaterials,2003,24(9):1603-1611.
[11] Song Y W,Shan D Y,Han E H.Electrodeposition of hydroxyapatite coating on AZ91D magnesium alloy for biomaterial application[J].Materials letters,2008,62(17-18):3276-3279.
[12] 张雅静,张丹,习小慧,等.AZ31仿生沉积羟基磷灰石涂层的研究[J].东北大学学报:自然科学版,2011,32(11):1611-1614.
[13] 王燕,林金辉,李辉,等.镁表面制备羟基磷灰石涂层方法研究[J].科学技术与工程,2013,13(9):2470-2473.
[14] Tan L L,Wang Q,Geng F,et al.Preparation and characterization of Ca-P coating on AZ31 magnesium alloy[J].Transactions of Nonferrous Metals Society of China,2010,20:648-654.
[15] 古一,王志法,夏长清.涂层与基底的热膨胀系数差对垂直界面的微裂纹的影响[J].湖南有色金属,2007,23(3):33-36.
[16] 唐 辉.AZ31镁合金表面含羟基磷灰石涂层的制备及腐蚀行为研究[D].哈尔滨: 哈尔滨工业大学,2013.
[17] Zhang L J,Fan J J,Zhang Z,et al.Study on the anodic film formation process of AZ91D magnesium alloy[J].Electrochimica Acta,2007,52(17):5325-5333.
[18] 曹楚南.电化学阻抗谱导论[M].北京:科学出版社,2002:87-113.
[19] 王保成.材料腐蚀与防护[M].北京:北京大学出版社,2012:230-240.
[20] 刘欢,郭春丽,卫英慧,等.AZ31镁合金表面通过Na2EDTA诱导羟基磷灰石膜层的形成及腐蚀行为[J].太原理工大学学报,2013,44(3):312-316.Formation and Characterization of Hydroxyapatite Coating on the Surface of AZ31
(编辑:庞富祥)
FAN Wei1,DU Huayun1,AN Yanli2,GUO Chunli1,WEI Yinghui1,3,HOU Lifeng1
(1.CollegeofMaterialsScienceandEngineering,TaiyuanUniversityofTechnology,Taiyuan030024,China;2.CollegeofPreclinicalMedical,ShanxiMedicalUniversity,Taiyuan030001,China;3.LüliangUniversity,Lishi033000,China)
In this paper, Ca(OH)2and Ca(H2PO4)2·H2O were used as raw materials to prepare a hydroxyapatite coating on the surface of AZ31 magnesium alloy using a sol-gel technique.Phase analysis,surface morphology study, and cross-section and microstructure characterization of the hydroxyapatite coating were conducted.Potentiodynamic polarization curves and electrochemical impedance spectra were obtainod using electrochemical workstation. Hydrogen evolution rates and corrosion morphologies of the coating immersed in Hank’s solution were also presented. The results indicate that the thickness of hydroxyapatite coating is approximately 8 μm and the corrosion current density of hydroxyapatite coating is 1.486 4×10-2mA/cm2, which is 5 times lower than that of bare AZ31 magnesium alloy. Hydrogen evolution tests and immersion corrosion morphologies further illustrate that hydroxyapatite coating can slow down the rate of biodegradation of AZ31 magnesium alloy effectively.
biomaterials;hydroxyapatite coating;sol-gel;AZ31 magnesium alloy; corrosion resistance
1007-9432(2015)04-0375-05
2015-03-04
国家自然科学基金资助项目:金属材料表面合金层原位形成过程中同步扩散行为的研究(51001079);高等学校博士点专项科研基金资助项目(20091402110010);教育部中国博士后科学基金资助项目(20100471586);山西医科大学青年基金资助项目(2012-057546)
范薇(1988-),男,山西祁县人,硕士生,主要从事镁合金的表面改性研究,(E-mail)fw880801@126.com,(Tel)15135113870
杜华云,男,副教授,主要从事镁合金表面改性研究,(E-mail)dragondu2002@163.com
TG174.4
A
10.16355/j.cnki.issn1007-9432tyut.2015.04.002
