槲皮素包合物微孔渗透泵片制备工艺
2015-01-16吴先闯郝海军宋晓勇张永州刘瑜新张红芹
吴先闯, 郝海军, 宋晓勇*, 张永州, 刘瑜新, 张红芹
(1.河南大学淮河医院药学部,河南开封475000;2.上海医药工业研究院,上海200437;3.国家中药制药工程技术研究中心,上海201203)
[制剂]
槲皮素包合物微孔渗透泵片制备工艺
吴先闯1, 郝海军2, 宋晓勇1*, 张永州1, 刘瑜新1, 张红芹3
(1.河南大学淮河医院药学部,河南开封475000;2.上海医药工业研究院,上海200437;3.国家中药制药工程技术研究中心,上海201203)
目的制备槲皮素环糊精包合物单层渗透泵片。方法以体外累积释放度作为评价指标,采用单因素考察确定最优处方。结果渗透泵片片芯处方中乳糖用量、NaCl用量和PEO用量以及包衣膜处方中包衣增重和致孔剂PEG 4000用量对释药行为有较大影响,优化后的槲皮素渗透泵片在12 h内呈现良好的零级释放 (r=0.995 7),药物累积释放比较完全 (>90%)。结论以环糊精包合物为中间体,可以制备成12 h内零级释药特征明显的单层渗透泵片。
:槲皮素;包合物;微孔渗透泵片
槲皮素(quercetin)是一种类黄酮化合物,广泛存在于蔬菜、水果、干果、谷物及中草药中,对人体心血管系统起着重要的保护作用,包括扩血管、降压、抑制心肌肥厚和保护内皮功能等,无明显的毒副作用,因而成为近年来的研究热点[1-2]。但槲皮素溶解度较差[3],半衰期仅为2~4 h,需要多次给药才能维持有效的血药浓度,往往容易造成血药浓度波动较大,从而损伤人体心脏、肾脏等重要器官[4]。心血管系统的药物一般以防治为主,需要长期、反复用药,容易导致患者的顺应性较差。渗透泵型控释制剂作为缓控释制剂的典型代表,以零级特征释放药物,而且释药几乎不受胃肠道内容物、pH等可变因素的影响,是口服缓控释制剂中最为理想的一种。其中,单层渗透泵制备工艺相对简单,更适合工业化生产,但只适用于水溶性药物。本实验以槲皮素为模型药,采用环糊精包合技术提高其溶解度[5],为进一步制备成单层渗透泵奠定基础,以期为难溶性药物单层渗透泵片的研究提供一定的参考。
1 仪器与试药
1.1 仪器 UV-2401 PC型紫外分光光度仪(日本岛津公司);TDP型单冲压片机 (上海第一制药机械厂);BY300A型小型包衣锅 (上海黄海药检仪器厂);ZRS-8型智能溶出试验仪 (天津大学无线电厂);BDY-100B型恒温摇床 (上海百典仪器有限公司);BP 210D型电子天平 (赛多利斯科学仪器有限公司);HWS-12型智能水浴锅 (上海一恒科技有限公司);DZF型真空干燥箱 (北京中科环试仪器有限公司)。
1.2 试剂 槲皮素 (实验室自制,纯度93.16%);槲皮素对照品 (中国药品生物检定所,批号 100081-201209);聚乙二醇 4000(PEG 4000)、磷酸二氢钾 (国药集团化学试剂有限公司);羟丙基-β-环糊精(HP-β-CD,西安德立生物化工有限公司);乳糖 (80目,德国美剂乐公司);氯化钠 (河北华晨药业有限公司);甘露醇(青岛明月海藻集团有限公司);聚氧乙烯PEO、WSR N-750(美国Dow公司);醋酸纤维素 (CA,结合酸54.5%~56.0%,国药集团化学试剂有限公司);硬脂酸镁 (辽宁奥达制药有限公司);乙腈、甲醇为色谱纯 (美国Merck公司);其余试剂均为分析纯 (国药集团化学试剂有限公司)。
2 方法与结果
2.1 槲皮素包合物制备方法 取HP-β-CD 20 g加水溶解,置于磁力搅拌器上,60℃水浴恒温。另取槲皮素3.8 g,以适量95%乙醇热熔后,缓慢滴加到HP-β-CD中,继续搅拌10 h,减压回收有机溶剂,静置12 h后过滤,旋转蒸发浓缩滤液,60℃真空干燥,研磨后即得槲皮素包合物 (摩尔比为1∶1)。
2.2 槲皮素包合物渗透泵片的制备
2.2.1 片芯制备 将槲皮素包合物、填充剂、渗透活性剂、助悬剂等辅料按处方量以等量递增法混匀,填充于直径8 mm浅冲模内压制片芯,片芯硬度为45~70 N。
2.2.2 包衣液制备 将处方量的醋酸纤维素溶于丙酮中,配制一定浓度的醋酸纤维素丙酮溶液,加入一定量的致孔剂,混匀即得。
2.2.3 渗透泵片制备 将片芯置于包衣锅内,在温度为35℃、包衣液体积流量6 mL/min、转速30 r/min条件下包衣,达到预定增重后,在40℃下固化24 h,即得槲皮素包合物渗透泵片。
2.3 体外释放度试验
2.3.1 槲皮素测定方法 精密称取槲皮素对照品约10mg置于50mL量瓶中,加40mL 95%乙醇溶解后,定容至刻度线作为贮备液。分别量取0.1、0.2、0.4、0.6、0.8、1.0 mL贮备液于10 mL量瓶中,加水定容,在374 nm波长处测定吸收度A,将吸收度A对质量浓度C进行线性回归,得标准曲线方程:C=18.18A+0.081 3(r=0.999 8)。高、中、低质量浓度的平均回收率为100.1%,RSD为 1.0%;日内精密度 RSD为 1.1%、0.79%,1.5%;日间精密度 RSD为 1.3%、1.6%、1.9%。
2.3.2 释放度测定方法 取渗透泵片,依照 《中国药典》2010年版二部附录XD第一法,以900 mL水为溶出介质,转速75 r/min,温度 (37± 0.5)℃,于1、2、4、6、8、10、12 h取5 m L,并同时补充同温度、同体积的溶出介质,样品经0.45μm微孔滤膜过滤,取续滤液,在374 nm波长处测定吸收度并计算渗透泵片在不同时间的累积释放量。
2.4 不同因素对槲皮素渗透泵片释药的影响 槲皮素包合物渗透泵片片芯处方主要考察乳糖用量、NaCl用量和PEO用量(见表1);包衣膜处方主要考察包衣增重和致孔剂PEG 4000用量对释药行为的影响 (见表2)。

表1 渗透泵片片芯处方Tab.1 Com position of core for osmotic pum p tablets
2.4.1 填充剂种类对释放行为的影响 保持片芯处方各组分的用量不变,包衣处方为F12,分别采用等量淀粉、乳糖和甘露醇作为填充剂,考察不同填充剂对槲皮素包合物释药行为的影响。结果见图1,表明不同填充剂种类对药物释放有较大影响。虽然淀粉作为填充剂时药物的累积释放度相对较高,但释药曲线线性不好;而乳糖和甘露醇释药曲线线性优于淀粉,且乳糖的累积释放度高于甘露醇,因此选定乳糖作为填充剂。

表2 渗透泵片包衣膜处方Tab.2 Composition of coating for osmotic pump tablets

图1 不同填充剂种类对释药曲线的影响 (n=3)Fig.1 Different additive's influence to the drug release(n=3)
2.4.2 填充剂用量对释药行为的影响 按照片芯处方F1、F2、F3和F4制备片芯,包衣处方为F12,考察不同填充剂用量对渗透泵释药行为的影响,结果见图2。不同用量的乳糖对释药行为较大的影响,随着用量的增加,释药速率及累计释放度都相应提高,这是由于乳糖作为填充剂的同时提供一定的渗透压,从而促进了槲皮素从释药孔的释放,选择乳糖的用量为110 mg。

图2 乳糖用量对释药曲线的影响 (n=3)Fig.2 Different amounts of lactose consumption on the drug release(n=3)
2.4.3 渗透活性物质用量对释药行为的影响 按照处方F4、F5、F6、F7制备渗透泵片芯,包衣处方为F12,考察渗透活性物质用量对释药行为的影响,结果见图3。当NaCl用量较高时,前期释药相对较快,但累积释放度却并不高;用量较低时,渗透泵的释药速率较慢,累积释放度也较低。NaCl的用量为40 mg时,释药行为较为理想,因此选择渗透活性物质用量为40 mg。

图3 渗透活性物质用量对释药曲线的影响 (n=3)Fig.3 Different amounts of osmotic agent consumption on the drug release(n=3)
2.4.4 助悬剂用量对释药行为的影响 在渗透泵片片芯中加入一定量的助悬剂,有助于增加片芯环境的黏度,提高混悬液的稳定性,最终有助于提高药物的累积释放度[5]。按照处方F7、F8、F9和F10制备渗透泵片芯,包衣处方为F12,考察不同PEO 350用量对药物释放行为的影响,结果见图4。结果表明,PEO 350用量为30 mg时,释药速率适中,药物累积释放度较高,因此最终将片芯处方F8确定为片芯的处方。

图4 助悬剂用量对释药曲线的影响 (n=3)Fig.4 Different amounts of suspending agent consumption on the drug release(n=3)
2.4.5 包衣增重对释药行为的影响 以处方F8作为片芯处方,按照包衣膜处方F11、F12和F13分别制备渗透泵片,考察包衣增重对释药行为的影响,结果见图5。包衣增重较小时,释药速率过快;包衣增重较大时,释药速率又相对较低。当包衣增重为6%时,释药行为较为理想。

图5 包衣增重对释药曲线的影响 (n=3)Fig.5 Differen t coating weight on the d rug release(n=3)
2.4.6 致孔剂用量对释药行为的影响 以处方F8作为片芯处方,按照包衣处方F12、F14、F15制备渗透泵片,考察致孔剂用量对释药行为的影响,结果见图6,致孔剂用量对药物的释放行为有一定的影响。PEG 4000是半透膜常用的致孔剂,不仅具有增塑剂作用,增加包衣膜柔韧性,还兼有调节药物释放速率作用。随着致孔剂用量的增加,释放速率也相应提高,当用量为25%时渗透泵释药行为较为理想,因此处方F14确定为包衣膜处方。
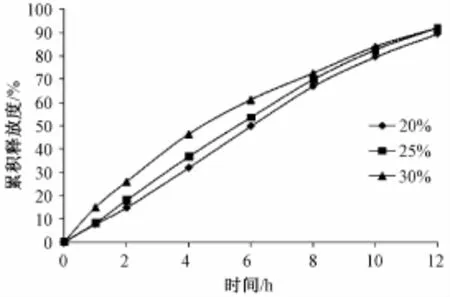
图6 致孔剂用量对释药曲线的影响 (n=3)Fig.6 Different amounts of pore-foam ing agen t consum ption on the drug release(n=3)
2.5 槲皮素包合物渗透泵片处方的确定 结合单因素考察结果,F8和F14最终确定为渗透泵片芯及包衣膜的处方即:槲皮素包合物225 mg,乳糖110 mg,NaCl为40 mg,PEO为30 mg,硬脂酸镁为片芯质量的1%,包衣增重6%,PEG 4000用量为25%。按照优化后的处方制备槲皮素包合物渗透泵片3批,体外释放曲线见图7。

图7 3批渗透泵片释药曲线(n=3)Fig.7 Drug release profile for th ree batches of osmotic pum p(n=3)
2.6 释药曲线的拟合 将优化后处方的释药曲线,以各取样时间点的实测数据,用常用的释药模型以累积释放度对时间进行拟合,求出符合该释药曲线的方程,并用r判断拟合程度,r越接近1,则表示拟合程度愈高,结果见表3。拟合结果显示,药物释放最接近零级释放,然后依次是一级释放模型和Higuchi释放模型。

表3 渗透泵片释药曲线的数学拟合Tab.3 Fitting of drug dissolution curve
2.7 槲皮素渗透泵片与包合物渗透泵片的比较
将槲皮素按照 “2.2”项下方法制备渗透泵片,并按“2.3.2”项下方法进行释放度考察,结果见图8。

图8 槲皮素渗透泵片与包合物渗透泵片体外释药的比较(n=3)Fig.8 Comparison on drug release between inclusion com p lex osmotic pum p and quercetin osmotic pum p(n=3)
结果显示,槲皮素渗透泵片在12 h内累积释放度仅22.91%,而采用包合技术后不但释药速率大大提高,符合零级释药模型,而且在同样时间内累积释放度达到90%以上。说明将槲皮素制备成单层渗透泵,采用包合技术是非常必要的。
3 讨论
槲皮素水溶性较差 (34.08μg/mL,25℃),不能提供足够的渗透压,因此要制备成单层渗透泵片,通过制剂技术提高其溶解度显得较为必要。采用包合技术制备成槲皮素包合物后,尽管其溶解度显著性地提高到22.17 mg/mL,但仍未达到单层渗透泵对药物溶解度的要求 (50~300 mg/mL),因此需要加入一定量的渗透活性物质。口服渗透泵制剂多选用氯化钠作为促渗透剂,这是由于氯化钠的分子质量较小,在相同用量的情况下,氯化钠的摩尔数最大。另外,乳糖作为填充剂的同时也兼作为渗透活性物质[6]。
本研究的渗透泵控释片是以NaCl为渗透活性物质,PEO 350作为助悬剂,但两者的所用比例对释药行为有重要影响[7-14]。这是因为两者是协同关系,同时也相互牵制:NaCl可增加片芯的渗透压,提供释药动力,而PEO遇水膨胀后不仅提供溶胀压,同时也起到助悬作用,因而共同促进了药物释放。在片质量一定的情况下,NaCl比例过高则减少了PEO的用量,使片芯混悬液的稳定性下降,药物沉积于片芯内最终导致累积释放度减小;而PEO比例较高时,由于形成的混悬液黏度较大,导致释药速率下降,达不到理想的释药效果,因而两者又是相互牵制的关系。所以需要通过实验研究,以最终确定PEO与NaCl的合适比例。
本研究在单因素考察的基础上最终确定了制备处方,并按确定的处方制备了三批渗透泵片,结果显示3批渗透泵片重复性较好,且12 h的累积释放度达到90%以上,符合零级释药模型。尽管体外释放达到设计要求,该处方是否合理还需结合体内的释药行为来最终确定。
[1]刘 敏,肖 颖,左爱仁,等.槲皮素、根皮素、水飞蓟宾清除自由基和抑制脂质过氧化活性研究[J].中成药,2012,34(4):753-756.
[2]孙 涓,余世春.槲皮素的研究进展[J].现代中药研究与实践,2011,25(3):85-88.
[3]刘 芸,赵 鹏,张丽华,等.槲皮素亚微乳的制备及特性表征研究[J].中成药,2014,36(5):1077-1080.
[4]冯 中,李晓燕,吴燕红,等.心血管药物缓释制剂的研究进展[J].时珍国医国药,2008,19(11):2664-2666.
[5]邵 伟,谢清春,王春香,等.槲皮素-羟丙基-β环糊精包合物的研究[J].中药材,2002,25(2):121-123.
[6]连潇嫣,任晓文,李洪起,等.吲达帕胺微孔渗透泵片的设计与制备[J].现代药物与临床,2011,26(5):397-402.
[7]Chen H H,Jiang G Q,Ding F X.Monolithic osmotic tablet containing solid dispersion of 10-hydroxycamptothecin[J]. Drug Dev Ind Pharm,2009,35(2):131-137.
[8]Liu X H,Wang S,Chai L Q,et al.A two-step strategy to design high bioavailable controlled-release nimodipine tablets:the push-pull osmotic pump in combination with the micronization/ solid dispersion techniques[J].Int J Pharm,2014,461(1-2):529-539.
[9]钟 玲,臧志和.三七总皂苷微孔渗透泵控释片体外释放度研究[J].中成药,2007,29(6):821-824.
[10]胡鹏翼,陈青阳,郑 琴,等.三七总皂苷微孔渗透泵控释片包衣对体外释药的影响[J].时珍国医国药,2010,21(6):1346-1348.
[11]辛 伟,张志宏,白 敏,等.盐酸青藤碱单室单层渗透泵型控释片的制备及释放考察[J].中国药学杂志,2011,46(19):1500-1505.
[12]Preethi N,Sujatha S.Development and evaluation of swellable elementary osmotic pump tablet ofglipizide[J].Int JPharm Sci Drug Res,2013,5(4):146-151.
[13]Laila H E,Nesrin F T,Rania M B,et al.Development of an osmotic pump system for controlled delivery of diclofenac sodium[J].Drug Discov Ther,2012,6(5):269-277.
[14]陈存香,李三鸣,李红菊,等.法莫替丁单室单层渗透泵片的制备[J].中国新药杂志,2007,16(13):1035-1038.
Preparation of m icro-porosity osmotic pum p tablets containing quercetin-inclusion com p lex
WU Xian-chuang1, HAO Hai-jun2, SONG Xiao-yong1*, ZHANG Yong-zhou1, LIU Yu-xin1,ZHANG Hong-qin3
(1.Department of Pharmacy,Huaihe Hospital of Henan University,Kaifeng 475000,China;2.Shanghai Institute of Pharmaceutical Industry,Shanghai200437,China;3.National Engineering Research Center for Traditional Chinese Medicine,Shanghai201203,China)
AIMTo prepare monolithic osmotic pump tablets containing quercetin-inclusion complex.METHODSThe cumulative percentage release was taken as the standard for evaluation for the in vitro drug release profile,single factor testswere for the determination of the optimal formulation.RESULTSThe composition of core tablet(the amount of lactose,NaCl and polyethylene oxide(PEO))and coating(coating level and the amount of PEG 4000)affected significantly the drug release.More than 90%of quercetin was released from the optimized osmotic pump tablets in 12 hrs,and the optimized formulation achieved the desired zero-order release profile(r=0.995 7).CONCLUSIONMonolithic osmotic pump tablets containing quercetin-inclusion complex as intermediate can deliver drug continually for 12 hrs.
quercetin;inclusion complex;micro-porosity osmotic pump tablets
R944
:A
:1001-1528(2015)06-1205-05
10.3969/j.issn.1001-1528.2015.06.011
2014-07-09
河南省科技发展计划项目 (144300510019);开封市科技发展计划项目 (1403024)
吴先闯 (1985—),男,硕士,主管药师,从事临床药学研究。Tel:(0371)23906849,E-mail:wuxc128@163.com
*通信作者:宋晓勇 (1972—),男,硕士,教授,主任药师,从事临床药学研究。Tel:(0371)23906970,E-mail:sxyyjk@sina.com
