聚乙二醇对Triton X-100胶束特性的影响
2015-01-09张杨龙李夏云刘杨
张杨龙,李夏云,刘杨
(汕头大学理学院生物系,广东汕头515063)
聚乙二醇对Triton X-100胶束特性的影响
张杨龙,李夏云,刘杨
(汕头大学理学院生物系,广东汕头515063)
为深入探索PEG/Triton X-100双水相体系中PEG分子对非离子型表面活性剂Triton X-100胶束特性的影响,利用粘度法对非离子型表面活性剂Triton X-100水溶液的胶束化行为进行表征,研究了PEG分子对Triton X-100水溶液胶束特性粘数[η]和水化程度的影响.结果表明,在含有PEG分子的Triton X-100胶束稀溶液中,PEG的分子量和浓度变化对胶束的特性粘数影响并不显著;但随着PEG分子量的增加,Triton X-100胶束的水化程度增加,胶束外壳与水溶液的相互作用增大.进一步以苯甲酰基乙酰苯胺(BZAA)作为探针,研究PEG分子对胶束内核极性的影响.结果显示PEG分子对Triton X-100胶束内核极性具有显著的影响:PEG浓度越大,BZAA在胶束内烯醇式结构减少,表明胶束内核极性增加;同时随着PEG分子量的增加,对内核极性的影响程度降低.
Triton X-100;胶束;特性粘度;水化程度;内核极性;聚乙二醇
Triton X-100(辛基苯基聚氧乙烯醚)是一种非离子型表面活性剂,分子结构由聚氧乙烯链的亲水性头基和烷烃链的疏水性尾基组成.当其水溶液浓度超过其临界胶束浓度(CMC=0.138×10-3~0.15×10-3g·ml-1)时,Triton X-100分子能够聚集在一起形成胶束,其疏水性尾部聚合形成疏水性内核,对疏水性分子有良好的增溶作用,可应用于强疏水性内在膜蛋白研究[1-2].由非离子型表面活性剂形成的双水相体系是一种分离和纯化膜蛋白的有效手段[3-4],尤其是非离子型表面活性剂与亲水性聚合物形成的双水相体系,可使疏水性膜蛋白富集于表面活性剂相,亲水性蛋白富集于聚合物相,从而实现对疏水性膜蛋白的富集分离.然而,非离子型表面活性剂水溶液中的胶束化行为比较复杂,溶液环境的变化会导致表面活性剂胶束性质的改变[5-7].研究学者结合动态光散射、粘度法、核磁共振等检测方法对非离子型表面活性剂胶束的结构和性质进行一系列的研究,报道了胶束的分子量、大小和形状等性质参数特征[8-9].而对于由PEG(聚乙二醇)与Triton X-100形成的双水相体系[10],尚缺乏对Triton X-100富集相胶束化行为的系统研究,探索Triton X-100胶束化行为受成相组分PEG分子的影响规律,有助于深入探索PEG/Triton X-100双水相体系相平衡特性及疏水性膜蛋白的分配机理.因此,本文基于PEG/Triton X-100双水相体系相平衡中两种成相组分浓度的比例关系,研究PEG分子对Triton X-100胶束化行为的影响,首先通过粘度法[11]研究了PEG分子对Triton X-100胶束特性粘数[η]以及水化作用等基本性质的影响,然后利用苯甲酰基乙酰苯胺(BZAA)作为探针,对Triton X-100胶束溶液的内核极性进行表征,考察PEG分子对胶束内核极性的影响.
1 材料与方法
1.1 实验材料:
Triton X-100、PEG 20 000、PEG 8 000、PEG 4 000均购买于AMERCO公司.苯甲酰基乙酰苯胺(BZAA)来自于Tokyo化工公司;其它试剂均为国产分析纯.
1.2 实验方法:
1.2.1 胶束溶液的制备将Triton X-100用0.01 mol/L磷酸盐缓冲液(PBS,pH=7)溶解,配制成一系列浓度梯度的胶束溶液(0~0.04 g·ml-1),分别测量其粘度.在保证Triton X-100终浓度不变的条件下,与不同分子量的PEG(20 000,8 000和4 000)混合,使PEG的终浓度分别为0.001 g·ml-1、0.005 g·ml-1和0.01 g·ml-1,在同样条件下测量溶液粘度. 1.2.2溶液粘度的测定根据GB/T 1632-93中的方法[12],25℃条件下,利用乌氏粘度计测量Triton X-100胶束水溶液的粘度.分别测量溶液流过毛细管的流出时间t以及对应溶剂流过毛细管的时间t0,溶液粘度与留出时间和体积密度之积成正比,稀溶液和纯溶剂具有相似的密度,故溶液的相对粘度为:

1.2.3 胶束的内核极性的测量根据Shoji et.al所用的方法[13],配制10 mg·L-1的BZAA溶液,以此作为溶剂,按表1分别配制含有不同浓度PEG的(混合)胶束溶液,恒温25℃振荡12 h混匀,在220~350 nm范围内进行光谱扫描.

表1 含有不同浓度PEG的Triton X-100胶束溶液
2 结果与讨论
2.1 Triton X-100胶束外壳的水化
非离子型表面活性剂在CMC以上才会形成胶束,因此以CMC时胶束溶液的粘度为参照,即测定C>CMC时胶束溶液的相对粘度ηr=η/ηcmc,由于Triton X-100的CMC极低,ηcmc与纯溶剂的粘度相似,因此Huggins方程[14]可以改写为:
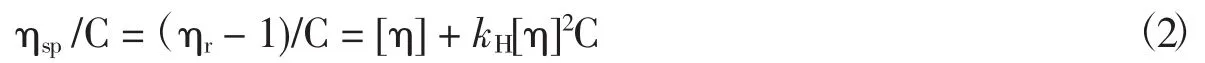
其中,ηsp表示稀溶液的增浓粘度,C代表胶束溶液的浓度,单位是g·mL-1,[η]表示溶液的特性粘数.分别测量不同浓度的Triton X-100胶束水溶液(0-0.03 g·ml-1)的相对粘度ηr,通过ηsp/C~C作图,由直线的截距和斜率可以得到胶束溶液特性粘数[η]和Huggins系数kΗ.特性粘数[η]反映单个Triton X-100胶束对粘度的贡献,Huggins系数kΗ描述胶束与溶液环境之间的相互作用,其数值越大表明相互作用越弱[15].将不同浓度和不同分子量的PEG与Triton X-100水溶液混合后,根据方程(2)得到胶束的特性粘数[η]均在6.0 ml·g-1左右(图1和表2).此研究结果表明低浓度的PEG分子对Triton X-100胶束与水的相互作用没有显著影响.

表2 Trtion X-100/PEG混合胶束外壳的水化
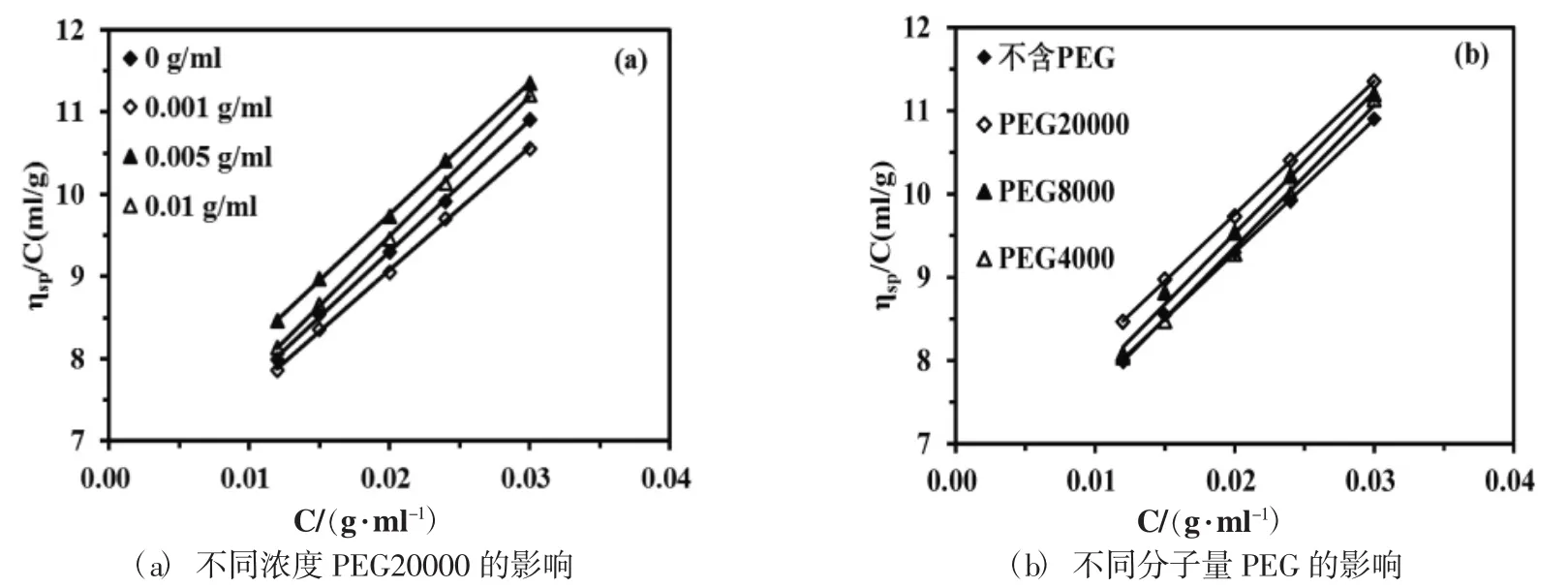
图1 PEG对Triton X-100胶束溶液特性粘数[η]和Huggins系数kΗ的影响
Huggins常数kΗ的数值还可用于表征表面活性剂胶束的形状,Bahadur等人[16]研究嵌段共聚物Pluronic P94水溶液的性质,在一定温度范围内,kΗ约为2左右,可认为Pluronic P94胶束是球形的.而在Triton X-100与PEG的混合水溶液中,kΗ数值为3.7~ 4.0左右,说明Triton X-100胶束并不呈球形.
大多数非离子型表面活性剂在低浓度条件下(接近于CMC),胶束都是呈球型的[9],然而,Wright[17]通过瞬态电双折射技术证实Triton X-100胶束并不呈球形,Dennis等人[18]在此基础上通过粘度法证实Triton X-100胶束形状约为椭球形.因此根据Oncley方程[16]:

其中vm和vs表示表面活性剂胶束和溶剂的偏比容体积(1/ρ),δ表示胶束的水化度(溶解每克溶质所需溶剂的量),用于表征胶束与水的相互作用.ν表示与胶束形状有关的因子.对于稳定的球形分子来说,ν=2.5,而根据Dennis的研究结果,可计算出Triton X-100的ν约为2.8左右.本实验通过方程(3)可以得出Triton X-100胶束表面的水化数δ在1.2(g·g-1)左右(表1),这与H.Paradies等[8]的研究结果(δ=1.21 g·g-1)一致.研究结果表明低浓度PEG分子对Triton X-100胶束没有明显的影响,但随着PEG分子量的增加,Triton X-100胶束的水化数增加,即胶束与水的相互作用增加,不利于Triton X-100胶束的形成.
最后,根据Guth和Simhas方程[19]

可以得到胶束的形状和体积的相关参数:其中,ø表示胶束所占的体积分数,C表示表面活性剂的浓度,V表示水化胶束的有效比容体积.当以V对C作图,所得的V值保持恒定,即近似水平的直线时,可证实Triton X-100胶束尺寸是单分散性的[20].从图2可以看出在PEG和表面活性剂的混合水溶液中,有效比容体积V没有呈现规律性的变化,但是基本保持恒定,证明Triton X-100胶束是单分散性的.

图2 PEG对Triton X-100水溶液有效比容体积V的影响
2.2 Triton X-100胶束的内核极性
Triton X-100溶液在浓度大于CMC后,会自我组装形成胶束聚集体,形成具有疏水性的内核.对于表面活性剂来说,溶液环境的变化会导致胶束内核极性发生变化[19].本实验利用BZAA作为探针,表征溶液环境变化对Triton X-100胶束溶液的影响.BZAA会以烯醇式结构存在于非极性环境中,在310 nm左右有最大吸收峰.而当BZAA在极性环境中以酮式结构存在时,在240 nm处有最大吸收峰[13].

图3 BZAA溶解在不同溶剂中的吸收光谱
2.2.1 BZAA在不同溶剂中的溶解性质首先对溶解在不同溶剂中的BZAA溶液进行光谱扫描,以描述BZAA分子在不同极性溶液中的分子结构变化情况.图3是乙醇、正十二烷以及PBS作为溶剂的BZAA溶液的光谱吸收图.从图中可以看出BZAA极易溶于乙醇,分别在240 nm和310 nm处的最大吸收峰较高;而在十二烷中的溶解性比乙醇低,导致其吸收峰也相对较低;在PBS缓冲液中,310 nm左右处没有最大吸收峰,说明BZAA分子在水溶液中没有烯醇式结构存在.
2.2.2 PEG对Triton X-100胶束内核极性的影响研究表明,Triton X-100分子和PEG分子混合后会发生一定的相互作用,导致Triton X-100胶束的溶剂化作用发生变化[21],从而可引起胶束内核极性的改变.根据BZAA在不同极性溶液环境中的溶解性质,选择10 mg·L-1的BZAA溶液作为母液,分别以此母液配制不同浓度Triton X-100溶液.当Triton X-100溶液的浓度低于临界胶束浓度时(C<CMC),310 nm处几乎没有光谱吸收(如图4中的曲线a和b),而当Triton X-100溶液的浓度高于临界胶束浓度时(C>CMC),310 nm处的具有光谱吸收,随着Triton X-100浓度的增加,光谱吸收值增加(如图4中的c-h曲线).光谱扫描结果表明随着Triton X-100浓度的增加,胶束内核的疏水性逐渐增大.此实验结果与N.Shoji等人的研究结果相似,对于大多数非离子型表面活性剂来说,随着胶束内核疏水性增加,310nm处光谱吸收值增加,240nm处的光谱吸收值减小[13],但是由于TritonX-100本身在280nm处有光谱吸收,会影响BZAA在240nm处的光谱吸收.
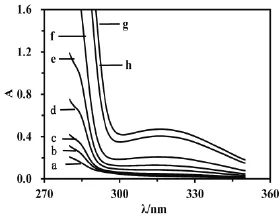
图4 不同浓度的Triton X-100胶束溶液含有10 mg·L-1BZAA的吸收光谱
根据上述扫描结果,最终选择0.005 g·ml-1和0.01 g·ml-1的Triton X-100胶束溶液,进一步研究PEG分子对胶束内核极性的影响.首先将PEG 20 000与Triton X-100溶液按一定比例混合,配制成含有不同浓度PEG 20 000与Triton X-100的二元混合体系,其中Triton X-100的终浓度为0.01 g·ml-1或0.005 g·ml-1.光谱扫描结果如图5所示,图(a)和(b)分别是含有不同浓度PEG 20 000在0.01 g·ml-1和0.005 g·ml-1Triton X-100胶束溶液中对吸收光谱的影响.添加PEG分子后,Triton X-100在310 nm处的光谱吸收值总体呈下降趋势,即在胶束结构中BZAA的烯醇式结构减少,Triton X-100胶束内核的极性增加.PEG浓度越大,对胶束的内核极性影响程度越大,尤其在较高Triton X-100浓度时趋势更加明显.对0.005 g·ml-1Triton X-100溶液的影响也表现出相似的结果,但是由于Triton X-100溶液浓度低,影响程度较低.
为进一步考察不同分子量PEG对Triton X-100胶束内核极性的影响,将浓度为0.01 g·ml-1不同分子量的PEG(20 000,8 000和4 000)与Triton X-100胶束溶液混合,其中Triton X-100的终浓度为0.01 g·ml-1.光谱扫描结果如图6所示,结果表明随着PEG分子量的增大,310 nm处光谱吸收的降低程度减小,即PEG分子量越大,在胶束结构中BZAA烯醇式结构减少,内核极性增加.这可能是由于随着PEG分子量的增大,PEG分子的烷烃链增加,相对疏水性增大,反而对TritonX-100胶束内核极性的影响程度降低.

图6 不同分子量的PEG分别对Triton X-100胶束溶液吸收光谱的影响
3 结论
通过研究在PEG/Triton X-100双水相体系中溶液环境变化对Triton X-100胶束溶液性质影响,表明了PEG分子与Triton X-100分子混合后,会影响Triton X-100胶束的特性粘数[η]、外壳水化数δ、有效比容体积V以及内核极性.
(1)粘度法研究结果表明:添加不同浓度(0~0.01g/ml)和不同分子量的PEG后,Triton X-100胶束的特性粘数[η]、Huggins系数kH没有明显的变化,但是随着PEG分子量的增加,胶束外壳水化数δ逐渐增加.这就说明在Triton X-100胶束稀溶液中,低浓度PEG分子对Triton X-100胶束与水的相互作用影响不大;高分子量的PEG会导致胶束与水的相互作用增加,不利于胶束的形成.
(2)Triton X-100胶束内核极性研究结果表明:PEG会影响Triton X-100胶束内部的结构.在Triton X-100胶束水溶液中添加PEG分子后,BZAA在胶束中的烯醇式结构减少,Triton X-100胶束内核极性增加,PEG浓度越大,Triton X-100胶束内核极性越强.然而,在高分子量PEG与Triton X-100胶束溶液混合后,对胶束内核极性的影响程度反而降低.
[1]Richard R B,Murray P D.Methods in enzymology[J].New York:Academic Press.2009:603-617.
[2]Garavito R M,Miller S F.Detergents as tools in membrane biochemistry[J].Journal of Biological Chemistry,2001,276(35):32403-32406.
[3]Bordier C.Phase separation of integral membrane proteins in Triton X-114 solution[J].Journal of Biological Chemistry,1981,256(4):1604-1607.
[4]Sivars U,Tjerneld F.Mechanisms of phase behaviour and protein partitioning in detergent/polymer aqueous two-phase systems for purification of integral membrane proteins[J].Biochim Biophys Acta,2000,1474(2):133-146.
[5]Mandal A B,Ray S,Biswas A M,et al.Physicochemical studies on thecharacterizationofTriton X-100 micelles in an aqueous environment and in the presence of additives[J].The Journal of Physical Chemistry,1980,84(8):856-859.
[6]Koshy L,Saiyad A H,Rakshit A K.The effects of various foreign substances on the cloud point of Triton X-100 and Triton X-114[J].Colloid&Polymer Science,1996,274(6):582-587.
[7]Schott H.Effect of inorganic additives on solutions of nonionic surfactants:micellar properties[J]. Journal of Colloid and Interface Science,1995,173(2):265-277.
[8]Paradies H H.Shape and size of a nonionic surfactant micelle.Triton X-100 in aqueous solution [J].The Journal of Physical Chemistry,1980,84(6):599-607.
[9]Tanford C,Nozaki Y,Rohde M F.Size and shape of globular micelles formed in aqueous solution by n-alkyl polyoxyethylene ethers[J].The Journal of Physical Chemistry,1977,81(16):1555-1560.
[10]Liu Y,Wu Z Y,Dai J H.Phase equilibrium and protein partitioning in aqueous micellar two-phase system composed of surfactant and polymer[J].Fluid Phase Equilibria,2012,320:60-64.
[11]赵剑曦.表面活性剂胶团水溶液性质的粘度研究方法[J].日用化学工业,2003,33(4):234-236.
[12]GB 1632-93.Determination of viscosity number and limiting viscosity number of polymers in dilute solution[S].
[13]Shoji N,Ueno M,Meguro K.Determination of critical micelle concentrations of some nonionic surfactants by Keto-Enol tautomerism of benzoylacetoanilide[J].Journal of the American Oil Chemists’Society,1978,55(2):297-299.
[14]周祖康,吴佩强,肖峥.粘度法研究胶团的球-棒转变[J].物理化学学报,1985,1(4):340-348.
[15]赵剑曦,陈晓东,江琳沁.二元Pluronic嵌段共聚物相互作用[J].物理化学学报,2000,16(12):1093-1102.
[16]Wright A K.Shape studies on macromolecules in aqueous and detergent solvents by transient electric birefringence[J].Journal of Colloid and Interface Science,1976,55(1):109-115.
[17]Wright A K.Shape studies on macromolecules in aqueous and detergent solvents by transient electric birefringence[J].Journal of Colloid and Interface Science,1976,55(1):109-115.
[18]Robson R J,Dennis E A.The size,shape,and hydration of nonionic surfactant micelles.Triton X-100[J].The Journal of Physical Chemistry,1977,81(11):1075-1078.
[19]Saito Y,Sato T.Effects of polyoxyethylene chain length on micellar structure[J].The Journal of Physical Chemistry,1985,89(10):2110-2112.
[20]El Eini D I D,Barry B W,Rhodes C T.Micellar size,shape,and hydration of long-chain polyoxyethylene nonionic surfactants[J].Journal of Colloid and Interface Science,1976,54(3):348-351.
[21]Qiao L,Eastea A J.The interaction between triton X series surfactants and poly(ethylene glycol)in aqueous solutions[J].Colloid&Polymer Science,1998,276(4):313-320.
Effect of Polyethylene Glycol on Triton X-100 Micellar Properties
ZHANG Yanglong,LI Xiayun,LIU Yang
(Department of Biology,College of Science,Shantou University,Shantou 515063,Guangdong,China)
The effect of polyethylene glycol on Triton X-100 micellar structure and micellar inner polarity is investigated.The shape and hydration of Triton X-100 micelles containing polyethylene glycol are performed based on viscosity method.The results indicate that the intrinsic viscosity of micellar has no significant changes when PEG exists,while the hydration increases with higher molecule weight of PEG.Moreover,the micellar inner polarity measurement is made by a comparison of keto-enol tautomerism usingbenzoylacetaanilide(BZAA).Adecreaseintheenolicabsorptionoccursas polyethylene glycol with different concentration and molecule weight are added to the micellar solutions.The trend is decreased when PEG of higher molecule weight exists in micellar solution of Triton X-100.
Triton X-100;micelles;intrinsicviscosity;hydration;innerpolarity;polyethylene glycol
Q 5
A
1001-4217(2015)01-0040-08
2014-10-08
张杨龙(1988-),男,研究生,硕士,主要研究方向:生物分离技术.E-mail:11ylzhang1@stu.edu.cn
刘杨(1978-),女,教授,博士,主要研究方向:生物分离技术.E-mail:liuyanglft@stu.edu.cn
广东省高等学校优秀青年教师培养计划(Yq2013076),广东省科技计划项目(2012B060400006),广东省高等学校学科与专业建设专项资金项目(2012KJCX0052)
