亚硝酸分配比测定及其初步模拟计算
2014-12-25朱礼洋陈延鑫唐洪彬
朱礼洋,陈延鑫,唐洪彬,何 辉
中国原子能科学研究院 放射化学研究所,北京 102413
Purex流程是复杂的多级逆流萃取流程,对其进行改进或优化需耗费大量的人力物力。采用计算机模拟有助于流程的分析和设计工作,对找出最佳工艺路线和工艺条件具有重要意义[1]。中国原子能科学研究院长期进行Purex流程计算机模拟研究,目前已建立涉及铀、钚、锝和锆等工艺段的动态仿真模型[2-3],但是HNO2对流程的影响仍需进行模拟研究。
在Purex流程中总是存在着HNO2。除了人为向系统加入HNO2或NaNO2外,用浓HNO3溶解乏燃料芯、HNO3的辐照分解以及化学反应等均会产生数量可观的。HNO2在酸性溶液中对不同价态的钚和镎等元素兼有氧化性和还原性,对这些元素的价态控制和走向有重要影响[5]。有机相中TBP对HNO2的萃取率往往很高,这对萃入有机相的核素也有影响。为了在计算机模拟时更准确的反映有HNO2存在时的真实情况,需要建立HNO2在TBP中的分配比模型。Uchiyama等[6]发现镎的萃取行为高度依赖于HNO2和HNO3的浓度,为了预测对镎的萃取,研究了HNO2在TBP/正十二烷与HNO3溶液中的分配情况。但是要建立HNO2的分配比模型,需要同时获得HNO3和HNO2的分配比数据。为此本工作拟同时测定HNO3和HNO2分配比数据,建立HNO2分配比模型,作为重要模块以补充完善Purex流程计算机模拟程序。
1 实验部分
1.1 实验试剂和仪器
NaNO2,基准试剂,天津市科密欧化学试剂有限公司;磷酸三丁酯(TBP)、无水碳酸钠、4-氨基苯磺酸和三水合醋酸钠均为分析纯,国药集团化学试剂有限公司;α-萘胺,优级纯,东京化成工业株式会社;HNO3,分析纯,北京化工厂;高锰酸钾,化学纯,北京化工厂;煤油为加氢煤油,锦西炼油厂。所用TBP和煤油使用前经过洗涤。TBP分别用2.5%(质量分数,下同)Na2CO3和0.1mol/L HNO3各洗3次后用去离子水洗至中性备用。煤油分别经0.1%高 锰 酸 钾、2.5%Na2CO3和0.1mol/L HNO3各洗3次后用去离子水洗至中性备用。
不同浓度TBP/煤油:将洗后的TBP与煤油按一定比例混合均匀,配制一系列不同TBP浓度的TBP/煤油溶液。TBP的含量采用酸饱和法测定[7]。
对氨基苯磺酸溶液:称取0.6g对氨基苯磺酸,加入70mL去离子水。水浴加热溶解完全后,冷却至室温后再加20mL浓HCl,最后稀释至100mL备用。
α-萘胺溶液:称取0.6gα-萘胺,用水浸润后加入1mL浓HCl和50mL去离子水,水浴加热溶解后冷却稀释至100mL备用。
醋酸钠溶液:称取136.1g三水合醋酸钠溶于去离子水后,稀释至500mL备用。
G20Compact Titrator自动滴定仪,美国Mettler Toledo公司;Lambda 950UV/Vis/NIR分光光度计,美国Perkin Elmer公司;GL-88B旋涡混合器,江苏海门其林贝尔仪器制造有限公司;800-1台式电动离心机,金坛市荣华仪器制造有限公司;AUX320电子天平,感量为0.000 1g,日本Shimadzu公司。
1.2 实验方法
配制含有一定浓度的HNO3和NaNO2溶液,配制完成后立即使用。将一定浓度的TBP/煤油与上述溶液等体积混合,在振荡器上充分振荡一定时间后离心分相。有机相和水相的酸度在G20自动滴定仪中用0.1mol/L NaOH滴定获得,其中有机相中HNO3是先反萃到大量水溶液中后滴定得到。
HNO2的分析方法很多,重氮偶联比色法具有灵敏度高等特点[8-9],是本研究采用的方法。其原理是亚硝酸盐与对氨基苯磺酸作用,生成不稳定的化合物,该化合物随即与α-萘胺反应生成红色偶氮化合物。此偶氮化合物的最大吸收波长为525nm。有机相中HNO2需先用对氨基苯磺酸溶液反萃到水相,等体积混合振荡5min后可反萃完全,反萃第二次得到的水相测其吸光度值为本底。取适量萃取平衡水相和反萃有机相得到的溶液,分别加对氨基苯磺酸溶液、醋酸钠溶液和α-萘胺溶液各200μL,稀释到10mL后混匀。在避光处显色。为了掌握合适的显色时间,以Lambda 950监测显色反应开始后525nm处吸光值,结果示于图1。从图1可以看到,吸光度A在10min后不再增加,基本保持不变。但是经过30min后,A值都有缓慢下降的趋势,这是因为生成的偶氮化合物在空气中不稳定,被部分氧化褪色。因此,实验中避光显色15min后应迅速测完所有样品。采用Lambda 950以试剂空白为参比,在525nm处测吸光值,通过标准曲线求得有机相和水相中HNO2的浓度。标准曲线y=37 621x,r2=0.999 5。
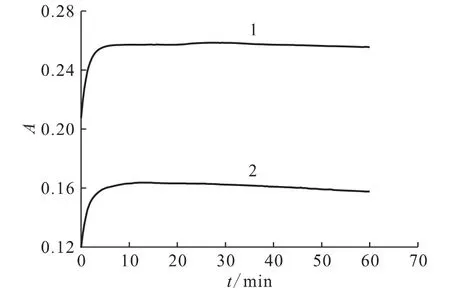
图1 不同浓度HNO2溶液显色时间Fig.1 Chromogenic time of nitrous acid with different concentrations
测得有机相和水相中HNO3和HNO2浓度后,HNO3的分配比D(HNO3)通过有机相和水相中HNO3浓度比值获得,同理得到HNO2的分配比D(HNO2)。

图2 HNO3-HNO2体系萃取前后稳定性Fig.2 Stability of HNO2 in aqueous phase and organic phase
2 结果与讨论
2.1 萃取体系稳定性
考察了含HNO2样品的稳定性。将3mol/L HNO3-0.01mol/L HNO2的水相与30%TBP/煤油有机相以体积比1∶1混合5min后离心分相,分别测平衡水相和平衡有机相在371nm处的吸光度值,结果示于图2。其中水相样品以去离子水为参比,有机相样品以30%(体积分数)TBP/煤油为参比。从图2中可以看到,萃取前水相样品吸光度下降很快,经过4h后吸光度下降到一半以下。萃取后的平衡有机相,其HNO2浓度也较高,且随时间而略有下降,但是下降的速率明显低于萃取前的水相。平衡水相的吸光度比平衡有机相低一个数量级,且平衡水相的吸光度几乎不随时间而变化。这是因为平衡水相的浓度和酸度均下降,特别是HNO2含量很低,且水相上层覆盖了有机相,一定程度上阻止了HNO2的分解。在测试时,离心分离后水相应立即进行重氮化,有机相中HNO2反萃进入水相后,也立即进行重氮化。对一系列HNO3和HNO2浓度下测得数据进行衡算,HNO2的衡算结果为93.83%~111.27%,HNO3的衡算结果为97.65%~104.08%,衡算结果较好。
2.2 平衡时间的影响
在TBP浓度为1.07mol/L、水相中HNO3和HNO2的浓度分别为3.0mol/L和0.02mol/L时,考察不同平衡时间下的分配比,结果示于图3。从图3可见,平衡时间从0.5min到5min,HNO3和HNO2的分配比没有明显变化,HNO3的分配比为0.227±0.006,HNO2的分配比为10.32±0.58。说明HNO3和HNO2可以很快达到萃取平衡。后续实验中混合搅拌的时间定为5min。

图3 不同平衡时间下HNO3与HNO2的分配比Fig.3 Distribution ratio of HNO3and HNO2under different equilibrium time
2.3 TBP 浓度的影响
保持水相中HNO3和HNO2的浓度分别为3.04mol/L和0.01mol/L,有机相中TBP的浓度从0.17mol/L逐渐增加到1.34mol/L,分配比与TBP浓度的关系示于图4。从图4可以看出,HNO3和HNO2的分配比随TBP浓度的增大而线性增加。HNO3的分配比从0.03增加到0.28,而HNO2的分配比从1.29增加到12.49。以lg D对lg cfree(TBP)作图,斜率接近1。因此自由TBP的含量可近似按下式计算。

其中与HNO3和HNO2结合部分的TBP浓度可通过测有机相中HNO3和HNO2浓度获得。ct(TBP)为TBP总浓度。下标o和a分别代表有机相和水相。

图4 分配比与自由TBP浓度的关系Fig.4 Effect of free TBP concentration on the distribution ratio of HNO3and HNO2

图5 分配比与原始水相HNO2浓度关系Fig.5 Effect of HNO2concentration on the distribution ratio of HNO2and HNO3
2.4 HNO2浓度的影响
保持有机相中TBP浓度为1.07mol/L、水相HNO3浓度为2.94mol/L,而HNO2浓度从2mmol/L增 加 到40mmol/L,获得分配比与HNO2浓度的关系示于图5。由图5可以看到,HNO2的分配比基本维持在11左右,随着HNO2浓度上升有略微下降的趋势,从11.8下降到11.0,下降了约15%。而HNO2浓度对HNO3的分配比影响很小,基本维持在0.2左右,测量最高值与最低值之间相差4.5%。这是因为HNO2浓度通常不高,HNO3浓度远大于HNO2浓度,对自由TBP浓度的影响不显著。HNO2浓度从2mmol/L升高到40mmol/L,萃取平衡时自由TBP的浓度仅从0.55mol/L降到0.51mol/L。
2.5 HNO3浓度的影响
在TBP浓度为1.07mol/L、HNO2浓度为10mmol/L下考察HNO3浓度对分配比的影响,结果示于图6、7。由图6可知:HNO3浓度对HNO2分配比影响很大,HNO3浓度越高HNO2分配比越低;当HNO3浓度为0.05mol/L时,测得HNO2分配比约为32,而当HNO3浓度增大到5mol/L时,HNO2的分配比降到5左右。这是因为HNO3的含量增大,会显著降低自由TBP浓度,使其从1.05mol/L降到了0.25mol/L。
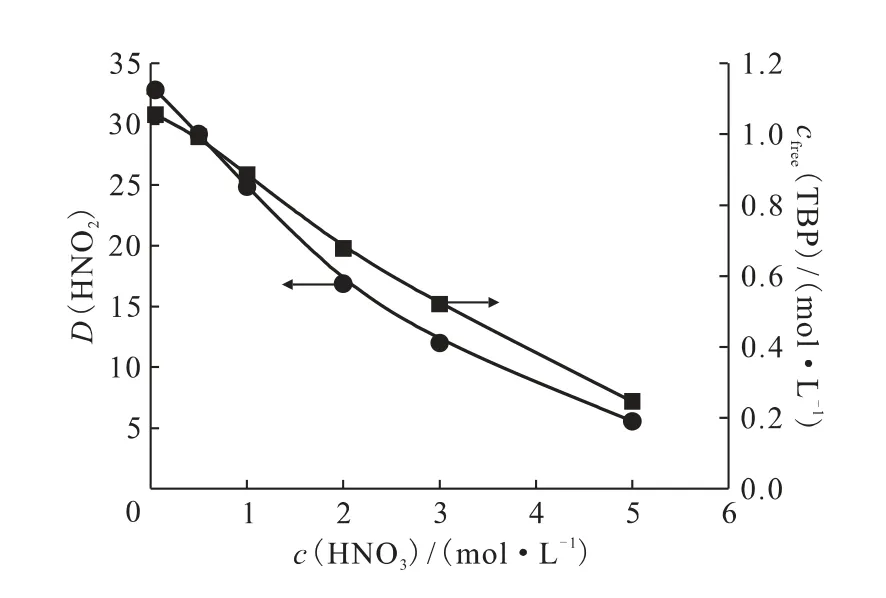
图6 自由TBP浓度和HNO2分配比随原始HNO3浓度的变化Fig.6 Dependence of free TBP concentration and the distribution ratio of HNO2 on initial nitric acid concentration

图7 HNO3浓度对HNO3分配比的影响Fig.7 Effect of nitric acid concentration on the distribution ratio of nitric acid
由图7可见,HNO3分配比先随HNO3浓度的增大而增大,在c(HNO3)>2mol/L时,又随酸度的增大而降低。当有大量的HNO3与TBP络合后,自由TBP的浓度下降效应显著,HNO3分配比开始下降。
2.6 HNO2分配比模型
建立HNO2的分配比模型有助于完善Purex流程计算机模拟程序。HNO2与TBP反应式如下。

表观平衡常数计算如下:

从上式可以看到,HNO2的分配比可以用表观平衡常数与自由TBP的浓度cfree(TBP)进行关联。对于表观平衡常数,从实验结果可以分析其影响因素。如表1所示,在实验范围内HNO2的表观平衡常数受HNO2和TBP的浓度变化影响较小,但是受HNO3浓度的变化影响较大。在TBP浓度为1.07mol/L、HNO2浓度0.01mol/L时,当HNO3浓度从0.5mol/L增大到5mol/L时,HNO2的表观平衡常数则从29.4减小到22.6。这是因为HNO3浓度改变会较大地改变溶液的离子活度。因此表观平衡常数可以简化成平衡水相HNO3浓度ca(HNO3)的函数。对于自由TBP浓度cfree(TBP),在后处理流程中往往含有的大量铀及其他核素会影响自由TBP的含量,而HNO2含量相对较小,对自由TBP的影响不大。同时这些重要核素又有相关的测定方法,从而可以确定出cfree(TBP)。这样就可以通过表观平衡常数与自由TBP浓度估算出HNO2的分配比。参考文献[10]的公式并修正系数得到:

表1 不同条件下HNO2的表观平衡常数以及分配比的实验和计算值Table 1 Apparent equilibrium constants and distribution ratio of HNO2under different conditions

将HNO3浓度值和自由TBP浓度值代入上式计算出D(HNO2)值,并与实验值比较可以看到,误差较小。此处给出的HNO2初步的分配比模型具有实际应用价值,后续可进一步完善。
3 结 论
同时测定了HNO3和HNO2的分配比。在实验研究范围内,水相HNO2浓度2mmol/L~0.04mol/L内,对于HNO3和HNO2的分配比没有显著影响。TBP的浓度升高,HNO2和HNO3的分配比都增加。HNO3浓度升高,HNO3的分配比先升高后下降,而HNO2的分配比下降。HNO2的分配比可以用水相HNO3浓度和有机相自由TBP浓度进行关联,计算结果与实验值较吻合。
[1]陈延鑫,何辉,唐洪彬,等.后处理工艺Purex流程计算机模拟研究现状及展望[J].核化学与放射化学,2012,34(4):194-200.
[2]何辉,胡景炘,张先业,等.基于拟Newton算法的Purex流程计算机模拟程序[J].原子能科学技术,2001,35(3):217-222.
[3]陈延鑫,何辉,张春龙,等.后处理Purex流程洗锝工艺的计算模拟I:计算机模拟及工艺参数分析[J].核化学与放射化学,2013,35(1):19-23.
[4]张志东.二氧化铀中微量硝酸根及乏燃料后处理PUREX流程料液中亚硝酸根的测定方法研究[D].甘肃:兰州大学,2007.
[5]李高亮,何辉.N,N-二甲基羟胺与HNO2的反应动力学[J].应用化学,2012,27(8):916-923.
[6]Uchiyama G,Hotoku S,Fujine S.Distribution of nitrous acid between tri-n-butyl phosphate/n-dodecane and nitric acid[J].Solvent Extr Ion Exch,1998,16(5):1177-1190.
[7]姜圣阶,任凤仪.核燃料后处理工学[M].北京:原子能出版社,1995.
[8]周本军,谢福会,才立辉.采用固体格氏试剂快速测定水中的亚硝酸盐氮[J].煤炭技术,2002,21(5):49-50.
[9]冯尚彩,张克忠,刘玉玲.亚硝酸根催化光度法的研究进展[J].理化检验-化学分册,1998,34(1):37-39.
[10]Tsuhata Y,Asakura T,Morita Y.Development of a computer code,PARC,for simulation of liquidliquid extraction process in reprocessing:JAEAData/Code-2008-010[R].Japan:Atomic Energy Agency,2008.
