双水相合成法制备聚丙烯酰胺的研究
2014-12-23张晓松李梦耀郭印丽李扬张海龙
张晓松,李梦耀,郭印丽,李扬,张海龙
(1.长安大学 环境科学与工程学院,陕西 西安 710054;2.旱区地下水文与生态效应教育部重点实验室(长安大学),陕西 西安 710054)
聚丙烯酰胺是水溶性的高分子聚合物。具有增稠、絮凝、助沉和稳定胶体等功能。目前,制备丙烯酰胺及其衍生物的方法主要有本体聚合、固态聚合、水溶液聚合、反相乳液聚合、反相微乳液聚合、反相悬浮聚合、沉淀聚合、分散聚合、双水相合成等[1-7]。双水相合成反应是将一种水溶性单体、引发剂及分散介质(另一种水溶性聚合物)溶解在水中,形成均相水溶液,一定条件下进行聚合反应,由于聚合物之间的相互作用,会发生相分离,在不同的相中聚集着各自的聚合物,形成互不相容的水溶性聚合物分散液。双水相聚合反应克服了普通水溶液聚合粘度高、搅拌和传热困难等缺陷,且聚合和使用过程中没有有机溶剂污染,后处理简单,是制备水溶性聚合物的新方法。本文以丙烯酰胺(AM)为单体,PAMPEG-H2O 双水相体系,自由基聚合法制备聚丙烯酰胺,考察了引发剂浓度、反应时间、单体浓度、pH、聚乙二醇用量等对产物特性黏度(相对分子质量)及转化率的影响,获得双水相聚合法制备较高分子量聚丙烯酰胺的最佳工艺条件。
1 实验部分
1.1 材料与仪器
丙烯酰胺(AM)、过硫酸铵、亚硫酸氢钠、聚乙二醇(PEG)、盐酸、氢氧化钠、溴酸钾、溴化钾、碘化钾、氯化钠、硫代硫酸钠均为分析纯;无水乙醇,工业级;高岭土,化学纯。
DK-98-1 型电热恒温水浴锅;78HW-1 型恒温磁力搅拌器;AL204 单盘分析天平;101-2AB 型电热鼓风干燥箱;DELTA320 型pH 计;KDM 型调温电热套;CN60M/1835 型乌氏粘度计;HI93703 型浊度测量仪。
1.2 聚丙烯酰胺的合成
广口瓶中加入一定量的丙烯酰胺单体、聚乙二醇和蒸馏水,稍稍加热,完全溶解后,用氢氧化钠调节pH 值6 后,补加蒸馏水,摇动广口瓶,使物料混合均匀,AM 浓度4%,PEG 7%,封口,放入水浴锅中加热,滴加引发剂2 mL,引发反应。控制反应温度65 ℃和时间80 min,得到分相明显的双水相粘稠液,上层主要为聚乙二醇相,下层为聚丙烯酰胺相。用溴量法分别测定聚乙二醇相和聚丙烯酰胺相丙烯酰胺的浓度,计算丙烯酰胺的剩余量和转化率。小心倾倒出上层聚乙二醇水溶液,下层加入工业酒精,并用玻璃棒先慢后快地搅拌,聚丙烯酰胺会以絮状形式析出,及时倒出含水较多的酒精。反复操作,少量多次,得含水较少的白色絮状物,烘干,得到粉状聚丙烯酰胺聚合物。
1.3 相对分子质量的测定[8]
在25 ℃下,以蒸馏水作溶剂,用乌氏粘度计测得PAM 的特性粘度[η],按式(1)计算共聚物的相对分子质量。

式中 Mn——共聚物相对分子质量;
[η]——特性粘度;
802 和1.25——经验常数。
1.4 去浊率实验
选用100 mg/L 皂土浊液作为模拟水样,浊度为30.18 mg/L。250 mL 烧杯中加入200 mL 浊液,加入一定量的聚丙烯酰胺溶液,快速搅拌1 min,缓慢搅拌10 min,静置15 min。取上清液测定剩余浊度,计算去浊率。

式中 S——去浊率,%;
B0——模拟水样的初始浊度,mg/L;
B——模拟水样的剩余浊度,mg/L。
2 结果与讨论
2.1 聚丙烯酰胺的合成
2.1.1 pH 的影响 AM 总量4%,PEG 含量7%,反应总时间80 min,引发剂用量2 mL,反应温度65 ℃,考察pH 对聚合物相对分子质量和转化率的影响,结果见图1。
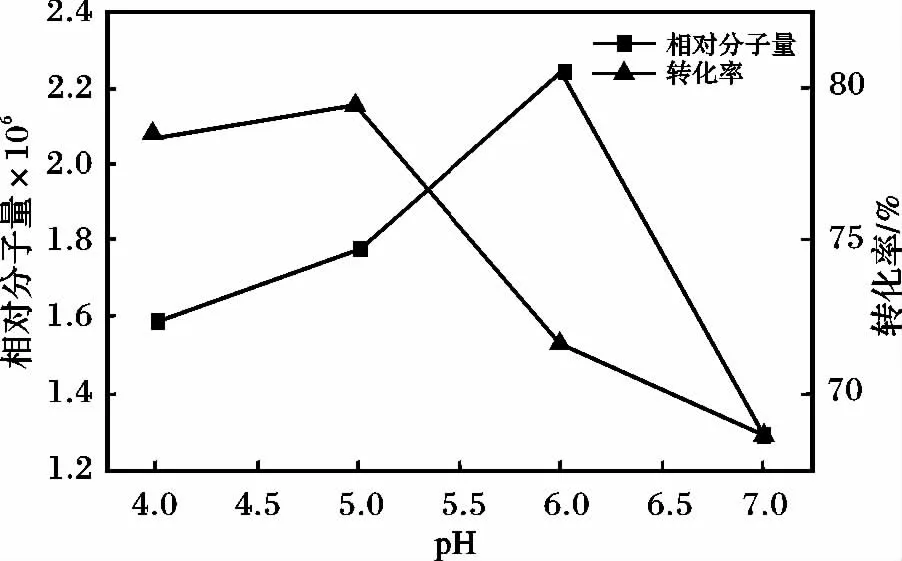
图1 pH 值对相对分子质量和转化率的影响Fig.1 Effect of pH on the relative molecular weight and conversion ratio
由图1 可知,在聚合过程中,随着pH 值的增大,相对分子质量和转化率先增大后减小,可能是由于体系中pH 值的变化对过硫酸盐的分解速率常数有显著的影响。在高pH 条件下,溶液中丙烯酰胺会发生副反应,生成链转移剂氮三丙烯酰胺,抑制聚合物分子量的增长,难以获得高分子量PAM。pH 6.0左右为宜。
2.1.2 单体用量的影响 PEG 含量7%,反应时间80 min,反应pH 值为6,引发剂用量2 mL,反应温度65 ℃,单体浓度对聚合物的相对分子质量和转化率的影响见图2。
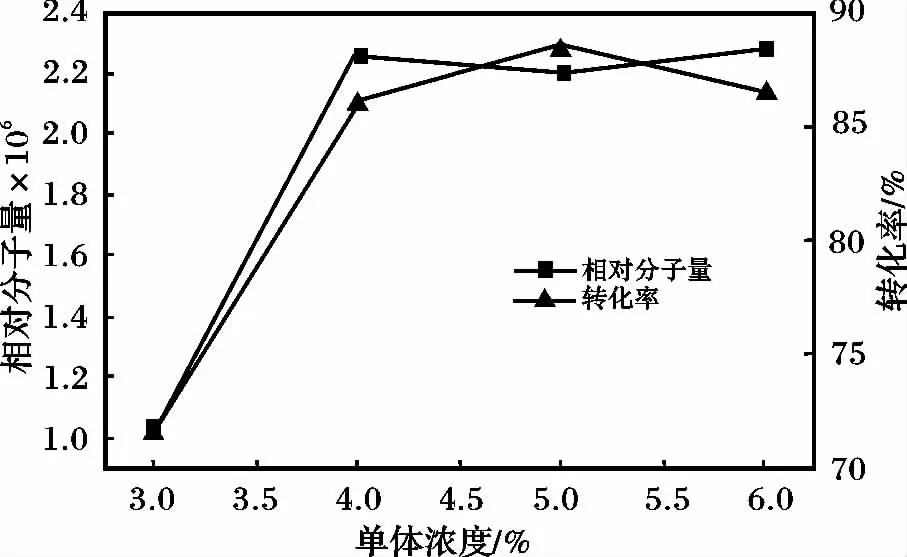
图2 单体总量对相对分子质量和转化率的影响Fig.2 Effect of monomer dosage on the relative molecular weight and conversion ratio
由图2 可知,随着单体浓度的提高,单体转化率、相对分子量呈现先增大后减小趋势。单体量少,单体分子之间的有效碰撞几率比较低,不利于反应进行以及分子链的增长,聚合物相对分子量变小。单体量过多,反应速率过快,使得反应难以控制,易出现交联而降低产物溶解性能,从而使产物的相对分子质量变小。单体浓度4.0% ~6.0%为宜。
2.1.3 PEG 用量的影响 单体总量4%,反应时间80 min,反应pH 值为6,引发剂用量2 mL,反应温度65 ℃,PEG 用量对聚合物相对分子质量和转化率的影响见图3。

图3 PEG 对相对分子量和转化率的影响Fig.3 Effect of PEG on the relative molecular weight and conversion ratio
由图3 可知,随着PEG 用量的增加,聚合物相对分子质量先增大后减小,PEG=7%时相对分子量最大;聚合物转化率随着PEG 用量的增加而增加。PEG 用量7%为宜。
2.1.4 引发剂用量的影响 单体总量4%,PEG 含量7%,反应总时间80 min,反应pH =6,反应温度65 ℃,引发剂用量对聚丙烯酰胺分子量和丙烯酰胺单体转化率的影响见图4。

图4 引发剂对相对分子量和转化率影响Fig.4 Effect of initiator dosage on the relative molecular weight and conversion ratio
由图4 可知,引发剂量小,活性中心少,单体聚合中心就少,相应的聚合反应产物相对分子质量高;引发剂量大,活性中心多,相应的聚合反应产物的相对分子质量低。但是,引发剂用量较少时,难以进行链引发反应,甚至会出现笼蔽效应,降低转化率;引发剂用量过大,自由基数目过多,反应过快,容易发生“爆聚”现象,不利于获得高相对分子质量的聚合物,而且会增大聚合物发生交联的几率。所以,引发剂的用量在2 mL 时,相对分子质量较大;转化率在引发剂用量为1.5 mL 时最高。
2.1.5 反应时间的影响 单体总量4%,PEG 含量7%,反应pH 值为6,引发剂用量2 mL,反应温度65 ℃,不同反应时间下聚合物的相对分子质量和转化率见图5。
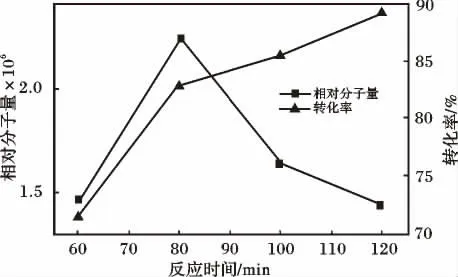
图5 反应时间对相对分子量和转化率的影响Fig.5 Effect of time on the relative molecular weight and conversion ratio
由图5 可知,随着时间的增长,聚合物相对分子量先增大后减小,80 min 时达到最大值,这是因为随着反应时间的增加,聚合反应进行得更加完全,聚合物分子链不断加长,从而使聚合物相对分子质量增加;然而当反应时间过长时,体系粘度增加,不利于单体的聚合,同时副反应增多,不利于合成聚丙烯酰胺。随着时间的增长,聚合物反应越长,转化率提高。
2.1.6 正交实验 控制单体总量4%和反应温度65 ℃,将反应时间、引发剂用量、pH 和PEG 用量按4 因素3 水平做正交实验,以聚合物的相对分子质量为评价指标,结果见表1。

表1 L9(34)的实验结果分析Table 1 Experimental result analysis of L9(34)
由表1 可知,最佳工艺条件为A1B1C3D3,即pH值7,PEG = 9%,反应时间60 min,引发剂用量1.5 mL。最佳反应条件下,做一组聚丙烯酰胺的合成实验。结果聚丙烯酰胺的相对分子量为2 836 821,AM 转化率为88.49%。
2.2 去浊实验
分别用质量分数为1%的聚丙烯酰胺来处理高岭土和PVSK(聚乙烯硫酸钾,胶体为阴离子型)胶体,结果见图6。
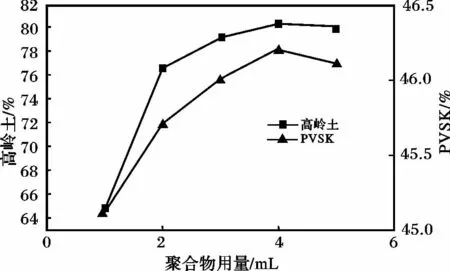
图6 聚丙烯酰胺的去浊实验Fig.6 Removing cloud experimental of polyacrylamide
由图6 可知:①聚丙烯酰胺对高岭土和PVSK的去浊率先随着聚合物用量的增多而增强,后降低。这是因为在聚合物用量较小的时候,聚合物用量越多,其去浊的粒子越多,效果越好,但用量太多,聚合物本身也会增加溶液的浊度;②聚合物对阴离子型胶体的去浊效果不如对高岭土的去浊效果,但是对阴离子型胶体的去浊效果明显。
3 结论
(1)以过硫酸铵和亚硫酸氢钠组成的氧化还原引发体系,在单体总量为4%和反应温度65 ℃条件下,合成聚丙烯酰胺的最佳条件为:pH 值7,反应时间60 min,引发剂用量1.5 mL,PEG =9%。此时合成出聚合物相对分子质量为2 836 821。
(2)质量分数1%的AM 聚合物用量小于4 mL时,去浊能力随着用量增加而增加,当超过4 mL 后,去浊能力下降。
[1] 胡瑞.阳离子型聚丙烯酰胺絮凝剂的合成与应用[D].武汉:华中师范大学,2007.
[2] 王光华,李文兵,王光辉,等. 高相对分子质量聚丙烯酰胺的制备及应用[J]. 精细化工,2004,21(10):50-52.
[3] 张育新,康勇.絮凝剂的研究现状及发展趋势[J]. 化工进展,2002,21(11):799-804.
[4] 单国荣,曹志海,黄志明,等.聚丙烯酰胺-聚乙二醇-水体系相图及丙烯酰胺单体在两相中的分配[J]. 高等学校化学学报,2005,26(7):1348-1351.
[5] 单国荣,曹志海,黄志明,等. 丙烯酰胺在聚乙二醇水溶液中的聚合动力学[J].高分子学报,2003(6):784-788.
[6] Shan G R,Cao Z H.A new polymerization method and kinetics for acrylamide:Aqueous two-phase polymerization[J].Appl Polym Sci,2009,111(3):1409-1416.
[7] Song B K,Cho M S,Yoon K J,et al.Dispersion polymerization of acrylamide with quaternary ammonium cationic comonomer in aqueous solution[J]. J Appl Polym Sci,2003,87:1101-1108.
[8] 王玉峰,胡慧仁,刘国,等. 离子型聚丙烯酰胺离子度的测定[J].中南大学学报:自然科学版,2006,37(3):516-520.
