化学发光免疫分析法检测肝纤维化血清标志物的性能评价
2014-10-11张运洪黄建军江津区中心医院检验科重庆402260
张运洪,何 玲,黄建军(江津区中心医院检验科,重庆 402260)
肝纤维化甚至早期肝硬化如能及时发现并进行抗纤维化治疗,均是可以逆转的。肝纤维化血清学指标检测的临床应用极为广泛,能够为疾病诊断和患者预后判断提供重要信息[1-2]。通常所说的肝纤维化四项(以下简称肝纤四项)指标即最为常用的肝纤维化血清学指标,包括透明质酸(HA)、层粘连蛋白(LN)、Ⅲ型前胶原 N端肽(PⅢP N-P)及Ⅳ型胶原(C-Ⅳ)。目前,化学发光免疫分析技术在上述指标临床检测中的应用已较为广泛。本院2012年年底引进了国产化学发光免疫分析仪用于血清HA、LN、PⅢP N-P及C-Ⅳ检测。根据美国病理家协会(CAP)和ISO15189文件对医学实验室的质量和能力的要求[3-4],本实验室参照美国临床和实验室标准化协会(CLSI)的相关文件,结合通用的评价模式,对上述四个项目的检测精密度、加样针携带污染率、准确度、线性范围、参考区间进行了验证和评价,现将结果报道如下。
1 材料与方法
1.1 仪器与试剂 深圳市新产业生物医学工程股份有限公司生产的MAGLUMI 2000Plus型全自动化学发光免疫分析仪及配套检测试剂(试剂批号:HA为051120714,LN为049120904,PⅢP N-P为052120908,C-Ⅳ为050120907)和标准品。可溯源至美国Sigma公司标准的LN、HA、C-Ⅳ质控品及可溯源至美国Biodesign公司的PⅢP N-P质控品,按使用量分装,-20℃保存。
1.2 临床标本 临床标本为来源于本院的新鲜血清标本,按使用量分装,-20℃保存。
1.3 方法
1.3.1 精密度分析 参照 CLSI EP5-A2文件[5],选取高低两种浓度临床标本连续重复测定20次,计算批内精密度,以批内变异系数(CV批内)表示,最大允许CV为厂家标识CV批内的1/2。选取高低两种浓度临床标本连续测定20d,每天1次,计算批间精密度,以CV批间表示,最大允许CV批间为厂家标识CV批间的1/2。
1.3.2 加样针携带污染率分析 将高浓度标本连续测量3次,测量值分别为H1、H2、H3;再将低浓度标本连续测量3次,测量值分别人为 L1、L2、L3。携带污染率(%)=(L1-L3)/(H3-L3)×100%。
1.3.3 准确度分析 参照 CLSI EP15-A 文件[6],对可溯源的质控品进行检测,检测结果与已知靶值进行比对,计算相对偏差。
1.3.4 线性范围分析 参照 CLSI EP6-A 文件[7],选取浓度达到给定的上、下限值标准的低值标本(L)和高值标本(H),按照5L+0H、4L+1H、3L+2H、2L+3H、1L+4H、0L+5H 的体积比例混合制备6个标本,每个标本重复测定3次后计算均值。将实测值与理论值进行比较。以实测值为Y,理论值为X,计算回归方程:Y=aX+b,要求相关系数(r)>0.975或r2>0.95,斜率a范围为0.97~1.03,截距b与最高浓度比较接近0。
1.3.5 参考区间分析 参照CLSI C28-A2文件[8],选取20例体检健康者(男、女各10例)临床标本,检测各指标水平后建立参考区间,要求男、女健康者中,最多各允许有1例检测结果超出推荐的参考区间。
2 结 果
2.1 精密度 (1)批内精密度:批内精密度分析结果见表1。结果表明肝纤四项的CV批内均未超过5%,也未超过厂家允许最大CV批内的1/2。(2)批间精密度:批间精密度分析结果见表2。结果表明肝纤四项的CV批间均未超过7.5%,也未超过厂家允许最大CV批间的1/2。

表1 肝纤四项检测的批内精密度评价试验结果
2.2 准确度 可溯源的肝纤四项质控品检测及计算结果见表3。相对偏差均未超过±2%,优于厂家允许相对偏差(±10.00%)。
2.3 加样针携带污染率 肝纤四项高浓度标本对低浓度标本造成的携带污染率都小于厂家允许的最大携带污染率(1.00‰),见表4。
2.4 线性范围 肝纤四项线性范围评价试验结果见表5,对应的线性散点图见图1~4。回归方程各参数(r2、a、b)如图所示,都未超过1.3.4中要求的水平。计算获得肝纤四项的线性范围如下:HA 为12.84~1 897.76ng/mL,LN 为20.98~960.59ng/mL,PⅢP N-P为10.72~1 923.48ng/mL,C-Ⅳ为11.85~1 964.49ng/mL。
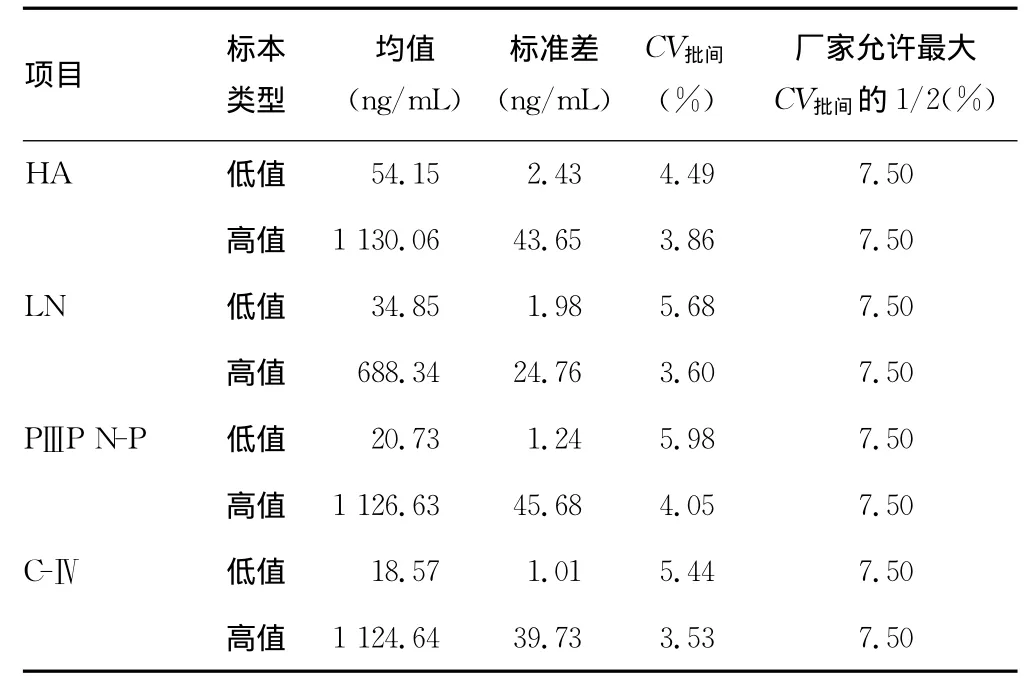
表2 肝纤四项检测的批间精密度评价试验结果
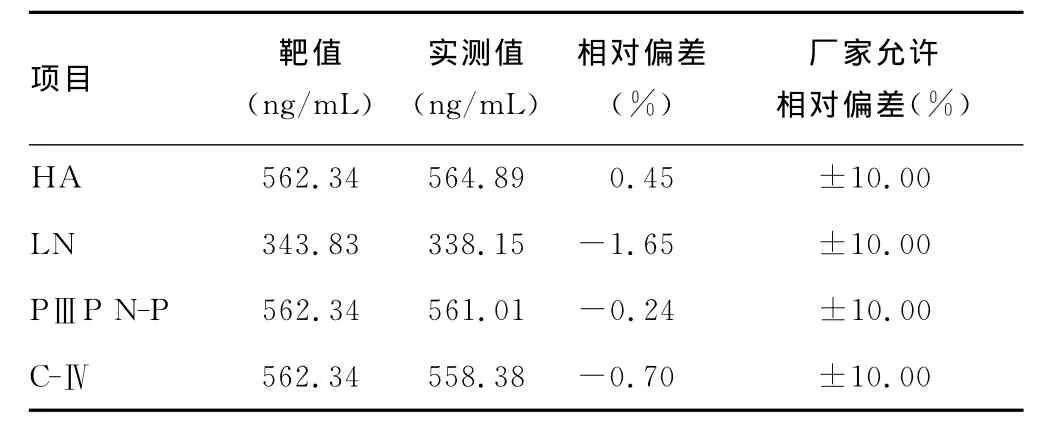
表3 肝纤四项检测的准确度评价试验结果

表4 肝纤四项检测的加样针携带污染率评价试验结果

表5 肝纤四项检测的线性范围评价试验结果(ng/mL)
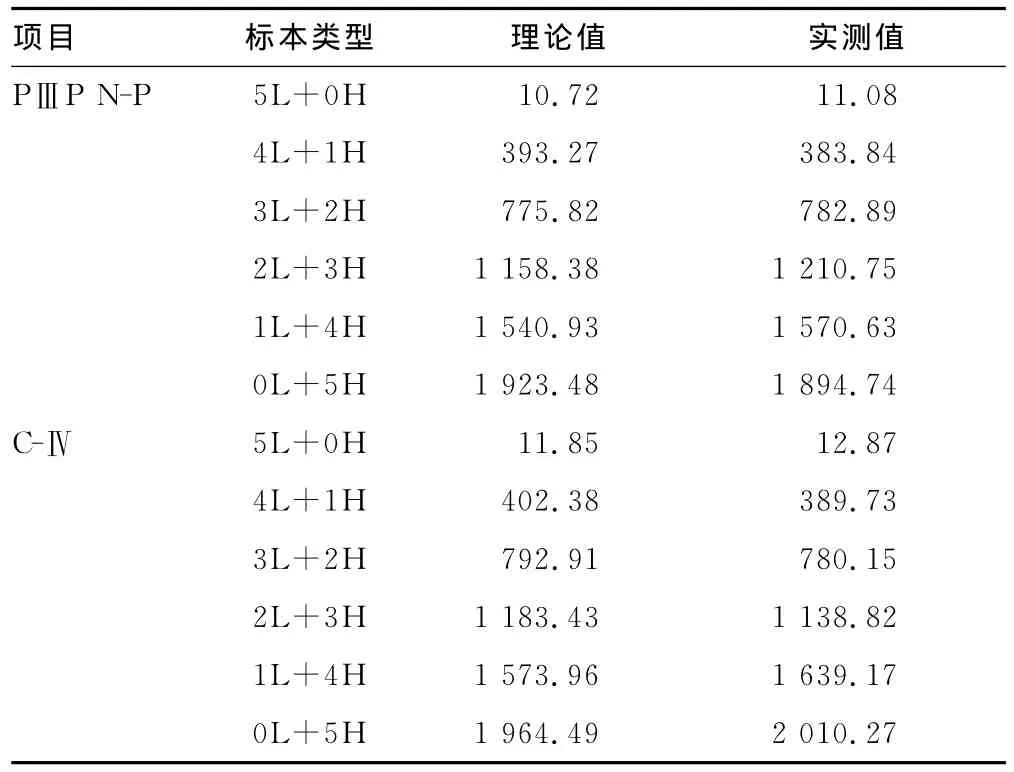
续表5 肝纤四项检测的线性范围评价试验结果(ng/mL)
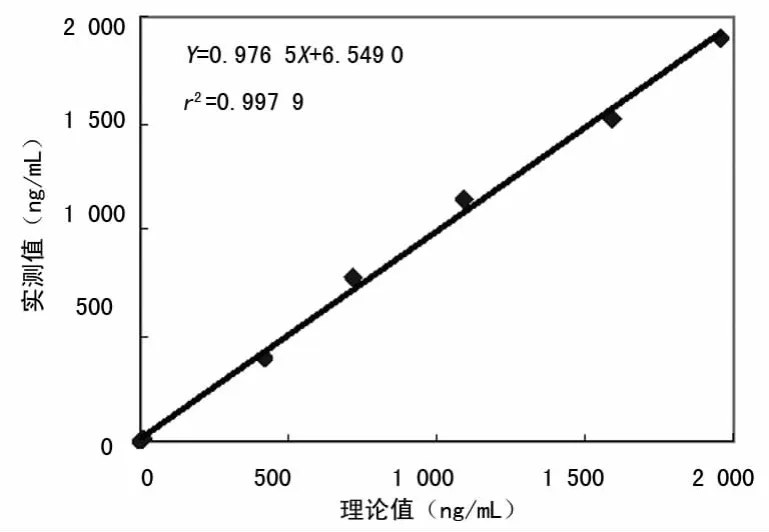
图1 HA线性散点图
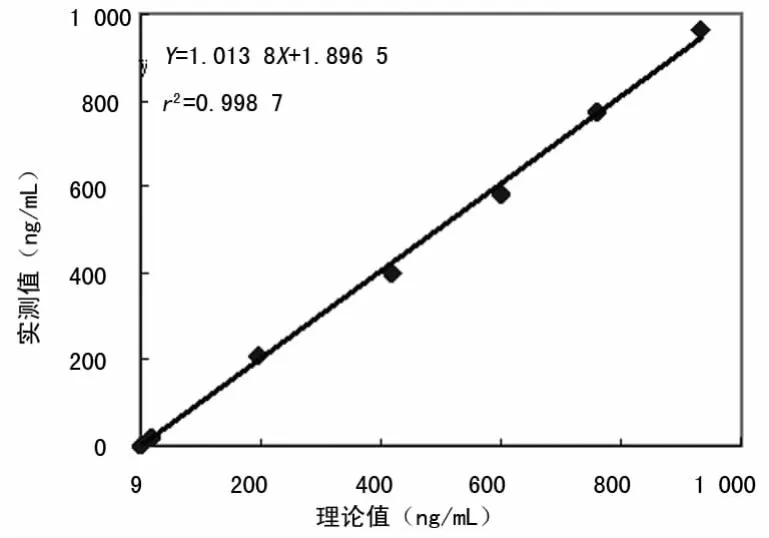
图2 LN线性散点图
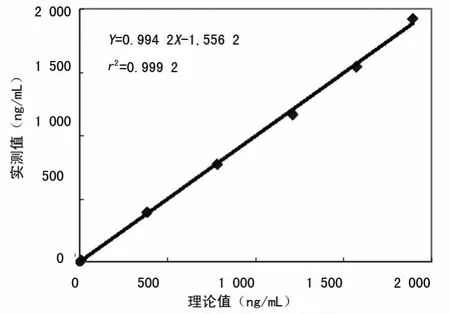
图3 PⅢP N-P线性散点图
2.5 参考区间 厂家提供的肝纤四项参考区间如下:HA<100ng/mL,LN<50ng/mL,PⅢP N-P<30ng/mL,C-Ⅳ<30 ng/mL。本研究纳入的男、女性各10例体检健康者血清标本检测结果均未出现1例或1例以上超过上述参考区间的现象,故可以直接使用厂家提供的参考区间。
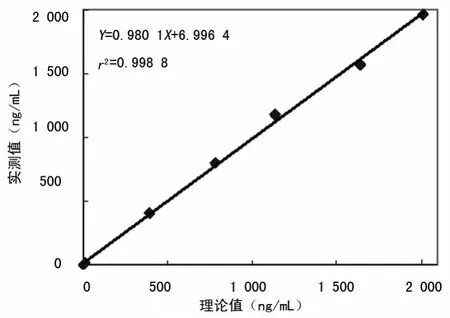
图4 C-Ⅳ线性散点图
3 讨 论
医学实验室将某种检测方法应用临床实际工作之前,必须掌握检测方法的性能指标。一般情况下,仪器或试剂生产已能够提供常用性能指标的评价结果。但是在正式检测临床标本、发出检测报告前,医学实验室仍需对厂商提供的主要方法学性能评价结果予以验证和确认[9]。因此,医学实验室必须结合实际,合理选择方法学验证试验、系统设计方法学验证方案[10]。
检测系统具有良好的重复性和无携带污染是方法学评价的前提和基本保障。本研究中,肝纤四项高低浓度标本检测结果的CV批内和CV批间均小于厂家允许最大变异系数的1/2。因此,可以认为本研究中使用的化学发光免疫分析仪检测肝纤四项的精密度是符合要求的。此外,本研究中的加样针携带污染率分析结果也表明该分析仪的加样针携带污染对标本检测结果的影响是可以忽略的。
准确度可以采用与已有检测系统比较、与室间质评结果比较、与质控品或外部标准品“靶值”比较、与参比实验室比较、计算配制溶液标本的回收率等5种形式来评估。由于肝纤四项无国际标准品,故本研究选择可溯源的质控品进行检测,相对偏差计算结果显示,各项指标的相对偏差均在可接受范围内,说明该分析仪检测肝纤四项的准确性是符合要求的。
可报告范围应和线性范围一致或在线性范围内。本研究结果显示该分析仪检测肝纤四项的线性范围是符合要求的。临床标本检测结果若超过线性范围时,需对其进行进一步验证后方可发出报告。超过下限时,检测结果对目前的诊疗缺乏指导意义。超过上限时,则应在稀释标本后进行在此检测,但可稀释的水平尚需验证。
医学实验室如果采用厂家提供的参考区间,则必须验证该参考区间是否适用于实验室所服务的人群。本研究随机选择了20例体检健康者的标本进行验证,95%以上的检测结果均在厂家提供的参考区间内,因此,可以认为厂家提供的参考区间基本适用于本实验室。
本研究结果显示,MAGLUMI 2000Plus型全自动化学发光免疫分析仪检测肝纤四项的精密度、加样针携带污染率、准确度、线性范围均符合预期要求,厂家提供的参考区间可以接受,可用于临床标本的肝纤四项检测。
[1]Chang TT,Liaw YF,Wu SS,et al.Long-term entecavir therapy results in the reversal of fibrosis/cirrhosis and continued histological improvement in patients with chronic hepatitis B[J].Hepatology,2010,52(3):886-893.
[2]中华肝脏病学会肝纤维化组.肝纤维化诊断及疗效评估共识[J].中华肝脏病杂志,2010,10(5):327-328.
[3]College of American Pathologists.Clinical Immunology Checklist[S].IL,USA:College of American Pathologists,2006.
[4]中国合格评定国家认可委员会.ISO15189医学实验室质量和能力认可准则[S].北京:中国合格评定国家认可委员会,2008:1-36.
[5]Clinical and Laboratory Standard Institute.Evaluation of precision performance of quantitative measurement methods.EP5-A2,Approved guideline-second edition[S].Wayne,PA,USA:CLSI,2004.
[6]Clinical and Laboratory Standard Institute.User demonstration of performance for precision and accuracy.EP15-A,Approved guideline[S].Wayne,PA,USA:CLSI,2001.
[7]Clinical and Laboratory Standard Institute.Evaluation of the Linearity of Quantitative Measurement Procedures.EP6-A,Statistical approved guideline[S].Wayne,PA,USA:CLSI,2003.
[8]Clinical and Laboratory Standard Institute.How to define and determine reference intervals in the clinical laboratory.C28-A2,Approved guideline-second edition [S].Wayne,PA,USA:CLSI,2000.
[9]Centers for Medicare&Medicaid Services.Clinical laboratory improvement amendments of 1988:final rule[Z].Bal,USA:Centers for Medicare&Medicaid Services,2003.
[10]毕波,吕元.定量检测方法学性能验证的系统设计[J].中华检验医学杂志,2007,30(2):143-145.
