丙酮肟水解可逆反应的进程分析和过程工艺
2014-07-24严生虎林春昕沈介发刘建武张跃
严生虎,林春昕,沈介发,刘建武,张跃
(1 常州大学设计研究院,江苏 常州213164;2 常州大学石油化工学院,江苏 常州213164)
酮肟是指酮的羰基氧原子被羟氨基(=NOH)取代的一类化合物。酮肟在酸性条件下可发生水解反应,生成相应的酮和羟胺盐,该反应是可逆反应[1-2]。然而,长期以来化学家和工程师们关注的是酮肟水解反应的逆过程,即由酮和羟胺盐缩合生成酮肟的反应[3]。由环己酮和硫酸羟胺缩合生成环己酮肟的反应过程被发现后,由帝斯曼(DSM)等公司发展成为工业化技术,用于规模化生产己内酰胺,进而用于生产聚酰胺类聚合物尼龙-6 等[4-5],在合成材料工业中产生了深远的影响。
随着近年来液相氨肟化技术的发展,以TS-1为催化剂的丙酮氨肟化反应[6-7]研究逐渐见诸报道。该反应原料价廉易得,丙酮转化率和丙酮肟选择性最高分别达到99%和94%[7],极大地降低了丙酮肟的制备成本,有望替代传统的羟胺盐法工艺。同时,羟胺及其盐作为一类重要的化工中间体,用途日益广泛[8],传统路线生产的羟胺盐产品已不能满足下游日益增长的市场需要。利用酮肟的水解反应合成羟胺盐产品日益成为经济可行的新路线[9]。
近年来,对酮肟水解制备羟胺盐的可逆反应已有一些研究报道。陈林和吕俊英[9-10]研究了由丁酮肟和盐酸反应合成盐酸羟胺的工艺过程,羟胺盐收率达70%以上;由于缺乏及时准确的反应进程分析方法,研究中采用最终产物称重法进行定量测定,产物收率较低。成凤桂、Kobayashi 等[11-12]提出了对酮肟水解反应产物进行定量分析的氧化-还原滴定法,但单一滴定分析方法无法区分羟胺浓度和酮肟浓度;Li 等[6]采用带紫外检测的液相色谱法(HPLC)研究了丙酮在TS-1 催化下的氨肟化反应,但该法不能检测无紫外响应的盐酸羟胺产物。现有方法难以准确把握酮肟水解反应进程,制约了对该反应的深入研究。作者采用自制的丙酮肟为原料,在酸性条件下进行水解反应,研究了反应进程的分析方法,创建了用于对反应体系中丙酮肟浓度、盐酸羟胺浓度同时定量跟踪分析的HPLC-氧化还原滴定组合测试技术。与已有报道的方法相比,本工作分析方法解决了产物称重法无法及时跟踪分析、误差大的问题,解决了单一滴定法无法区分盐酸羟胺浓度及丙酮肟浓度的问题,实现了对反应及时、准确的跟踪分析。在此基础上,建立了反应-蒸馏耦合工艺装置[10],研究了丙酮肟水解可逆平衡反应[2,13]的过程工艺技术,考察了加热温度、蒸发速率、摩尔配比等工艺条件对盐酸羟胺合成的影响,获得了由丙酮肟水解制备盐酸羟胺的优选工艺条件,为该技术的后续研究和应用奠定了基础。
1 实验部分
1.1 材料和装备
丙酮肟,丙酮氨肟化法自制,GC 含量≥99.0%;38%盐酸、硫酸高铁铵,AR,国药集团化学试剂公司;甲醇,色谱级,国药集团化学试剂公司;盐酸羟胺、硫酸羟胺,metals basis 99.99%,阿拉丁试剂公司。
反应-蒸馏耦合实验装置;SPD-15C 型HPLC仪,日本SHIMADZU 公司;LVS-201T 型真空泵,德国ILMVAC 公司;RCT 型磁力搅拌器,IKA 仪器公司。
1.2 实验操作方法
丙酮肟水解制备盐酸羟胺的可逆反应方程式如式(1)。
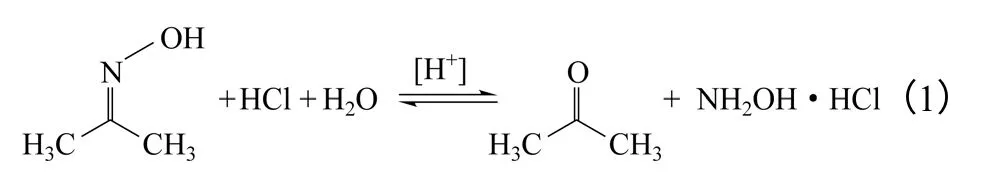
先称量空反应瓶的质量,然后搭建反应-蒸馏耦合装置(带加热器、搅拌器的反应瓶,通过气相管路连接蒸馏管路、冷凝器及收集瓶)。在反应瓶中加入一定量的丙酮肟(记为A,mol)、一定量的盐酸、水,加热开始反应;生成的丙酮被及时蒸出反应体系,与蒸出的水形成混合溶液,生成的盐酸羟胺溶解在反应区残留液中;反应平衡向右移动,盐酸羟胺不断生成。反应结束后,拆卸反应装置,称量反应瓶及其中残留液的质量,计算反应区残留液质量,记为M(g);从中准确称取出一定量样品,记为m(g),加入容量瓶中,加入80mL 蒸馏水稀释,再以数滴氨水中和至pH=7.0 以淬灭反应,定容至100mL,放入冰箱冷藏,用于HPLC 分析和氧化还原滴定分析,由分析结果计算反应的原料转化率和产物收率。至反应平衡不再移动,产物组成不变后结束,产物去精制获得盐酸羟胺产品。
1.3 分析方法
采用本文自建的HPLC-氧化还原滴定组合分析方法对丙酮肟水解反应体系进行分析。其中,HPLC 用于测定样品中的丙酮肟浓度Coxime(HPLC)(mol/L),外标法,分析条件为:Diamonsil C18(5μm,4.6mm×250 mm)色谱柱,流动相为甲醇︰水=7∶3(体积比,下同)的溶液,流动相流速=1mL/min,检测波长为210nm 和265nm,进样量为20μL。氧化还原滴定用于测定样品中的丙酮肟和盐酸羟胺的总浓度CTitration(mol/L),方法为:取10mL 处理后的样品于锥形瓶中,加入5mL 25%H2SO4和10mL 250g/L 的硫酸铁胺溶液,加热煮沸2min 后,加入100mL 1%H3PO4水溶液,趁热以0.01mol/L 的高锰酸钾溶液将黄绿色溶液滴定至粉色,平行3 次,算得样品中CTitration。
按照式(2)、式(3)计算丙酮肟水解反应的原料转化率和产品(盐酸羟胺)收率,盐酸羟胺产物选择性由收率除以转化率计算。
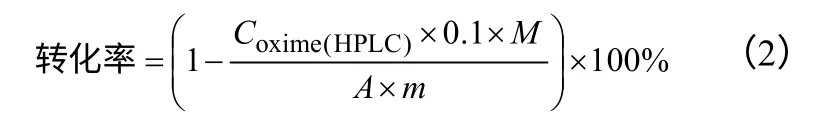
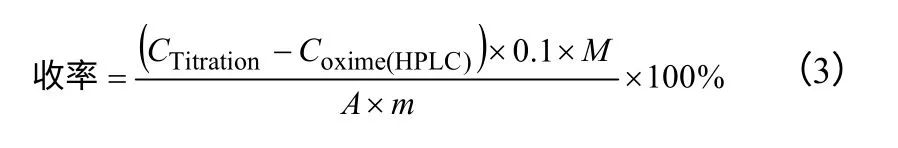
2 结果与讨论
2.1 HPLC-氧化还原滴定组合测试技术
使用紫外检测器的HPLC 可以准确测定混合样品中的丙酮肟含量[6],但无法测出不具备紫外活性的盐酸羟胺。盐酸羟胺和丙酮肟均具有强还原性,可将三价铁离子还原为二价铁离子;同时盐酸羟胺和丙酮肟在强酸的催化作用下均可以等摩尔转化为NH3OH+,NH3OH+通过氧化还原滴定即可确定其含量[11,14]。丙酮肟水解反应结束后的残留液中,存有未反应的丙酮肟和反应生成的盐酸羟胺,单一滴定分析方法无法区分羟胺浓度和酮肟浓度。
先以氨水淬灭平衡反应,致使反应平衡不再移动,再利用HPLC 直接测定残留液中丙酮肟的含量,避免蒸发重结晶等操作引起反应平衡继续移动造成的误差;然后以过量硫酸处理残留液,将丙酮肟和盐酸羟胺等摩尔转化为NH3OH+,最后以氧化还原滴定测出丙酮肟和盐酸羟胺的总量,从而计算得出盐酸羟胺的浓度,分析方法的原理如图1。
在上述HPLC 和氧化还原滴定的条件下,测定6 组不同浓度的丙酮肟溶液(记为Ⅰ),浓度分别为0.008mol/L、0.016mol/L、0.024mol/L、0.032mol/L、0.040mol/L、0.050mol/L;并以组合分析方法测定6组丙酮肟和盐酸羟胺混合溶液(记为Ⅱ),浓度分别为0.34mol/L+0.06mol/L、0.28mol/L+0.12mol/L、0.22mol/L+0.18mol/L 、 0.16mol/L+0.24mol/L 、0.10mol/L+0.30mol/L、0.04mol/L+0.36mol/L,结果如表1。其中丙酮肟和盐酸羟胺混合溶液(Ⅱ)中加入0.02mol/L 的盐酸,以此模拟丙酮肟水解反应液中原料和产品的组成。
由表1 可见,利用本文所建立的HPLC-氧化还原滴定组合测试技术测定不同浓度丙酮肟溶液时,测定结果的平均回收率达100.69%,RSD≤1.23%(n=6),与文献[11]以Ce4+滴定法测定单纯丙酮肟样品的回收率、RSD 水平相当。表1 中也列出了以该组合测试方法测定的混合溶液中丙酮肟浓度和盐酸羟胺浓度,其平均回收率为99.64%,RSD≤2.04(n=6)。可见,本工作所建立的HPLC-氧化还原滴定组合测试方法具有良好的准确性和稳定性。因此,可以该分析方法为基础,对丙酮肟水解反应的反应-蒸馏耦合工艺进行较深入的研究。
2.2 反应-蒸馏过程工艺条件的优化
2.2.1 加热温度对羟胺盐合成的影响
取丙酮肟︰HCl 摩尔比为1∶2,磁力搅拌器转速为1000r/min,反应-蒸馏时间为3h,在反应-蒸馏耦合装置中进行丙酮肟水解反应实验,考察了过程中不同的加热温度对水解反应的影响,结果如图2。
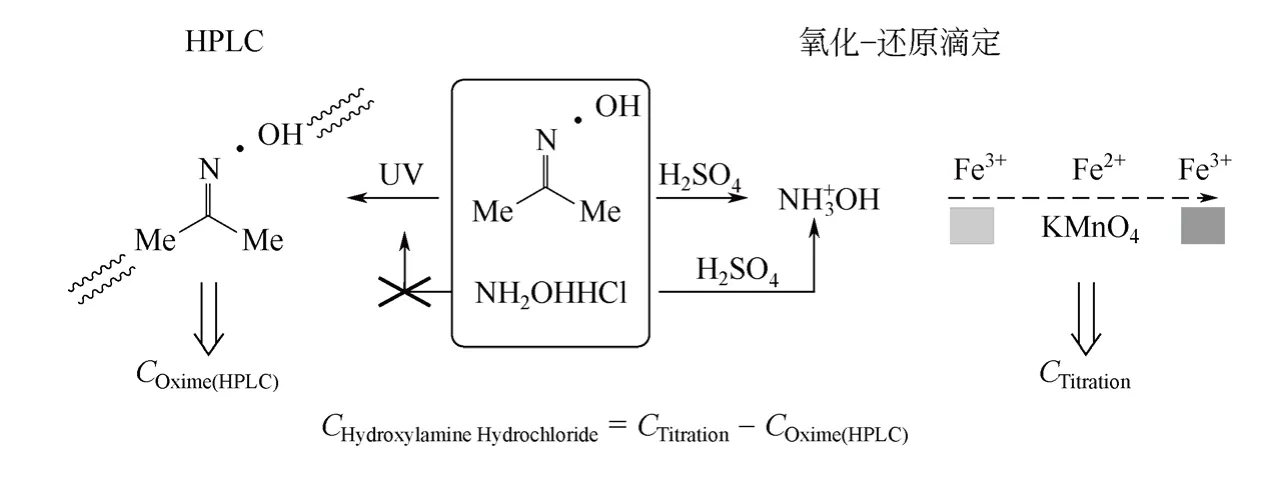
图1 丙酮肟和盐酸羟胺定量测定原理
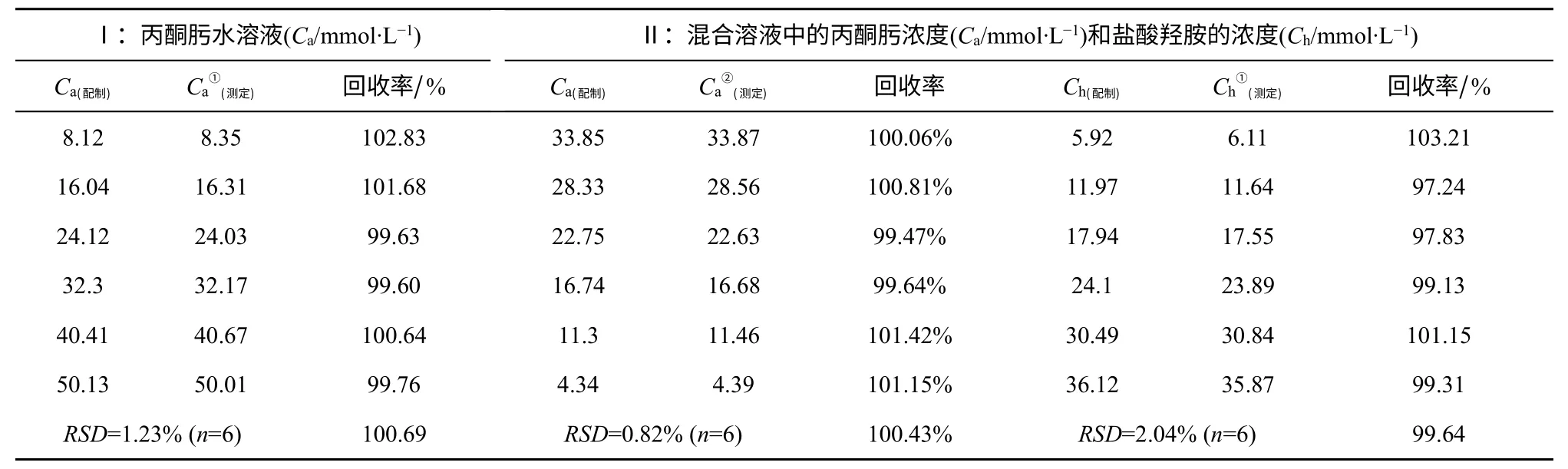
表1 丙酮肟浓度测定和混合溶液中盐酸羟胺浓度测定结果及其回收率
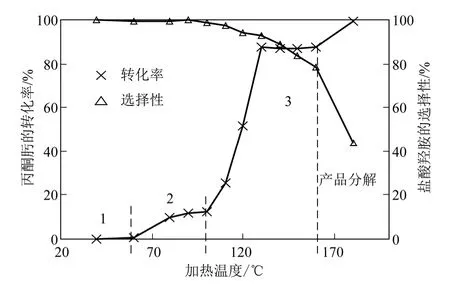
图2 加热温度对丙酮肟水解反应的影响
由图2 可见,随着加热温度的上升,原料转化率呈阶梯上升趋势,产物选择性由缓慢降低逐渐转为快速下降。丙酮肟的水解反应是可逆反应,1000r/min 的搅拌速率、3h 的反应-蒸馏时间足以使反应达到平衡点,反应结果表现为可逆反应的动力学平衡控制,而非传质因素或反应时间因素限制。加热温度对丙酮肟水解可逆反应的原料转化率呈现阶梯式影响,包括三个阶梯:阶梯一(加热温度为40~60℃),该阶段丙酮肟转化率接近0,原因为该阶段加热温度过低(低于丙酮的沸点),产物丙酮难以蒸发脱离反应液,致使反应平衡难以向右移动。之后,在加热温度60~80℃,丙酮肟转化率通过一个明显上升趋势进入第二个阶梯。阶梯二(加热温度为80~100℃),该阶段丙酮肟的转化率在10%左右,且随着加热温度的升高有微微上升趋势,原因为该阶段加热温度超过丙酮的沸点,反应-蒸馏耦合水解过程可使部分丙酮蒸发脱离反应液,实现反应平衡的移动,产物收率达到10.0%~12.4%。在阶梯二的加热温度范围内,水和丙酮的互溶性良好,反应-蒸馏分离出的丙酮量较少;加之反应-蒸馏同时蒸出了产物丙酮及反应物水、HCl,对正、逆反应的影响作用相当,使水解平衡未发生明显的移动。其后,在加热温度100~130℃,由于超过了水的沸点,破坏了水和丙酮互溶体系,产物丙酮被大量蒸出,丙酮肟转化率进入一个迅速上升阶段,直至进入第三个阶梯。文献[10]报道在100℃加热温度下可获得40%的盐酸羟胺收率,这是因为其测算产品收率时,采用真空脱除液相组分以获取盐酸羟胺产物,由于过程中没有淬灭反应,反应平衡会随着分离过程不断向右移动,从而出现较大的偏差,导致产物收率偏大。阶梯三(加热温度为130~160℃),该阶段丙酮肟的转化率在89%左右,盐酸羟胺产物收率在84%左右,原因为该阶段丙酮肟转化率已经较高,丙酮肟浓度已降低至很低的水平,可逆反应的正反应速度显著降低,逆反应速度加快,产物丙酮一经生成即被逆反应又转化为丙酮肟,反应-蒸馏无法再分离出更多的丙酮产物,动力学平衡点稳定不变。与以渗透汽化膜技术[15]进行酮肟水解平衡反应的工艺相比,本工作通过采用较高的加热温度,使产品收率提高了24%,同时避免了使用昂贵的渗透汽化膜,有利于工业化应用。考虑到过高的加热温度(大于160℃)易引起产品盐酸羟胺的分解,因此选择130℃为优选的加热温度。
2.2.2 蒸发速率对羟胺盐合成的影响
取丙酮肟︰HCl 摩尔比为1∶2,磁力搅拌器转速为1000r/min、加热温度为130℃,在反应-蒸馏耦合装置中进行丙酮肟水解反应实验,考察了0.1h、0.2h、0.5h、1h、1.5h、2h、3h、5h 对应的反应液质量变化及原料转化率、产物选择性的变化,并由反应液质量变化计算了不同时间段的平均蒸发速率(某时间段的平均蒸发速率为该时间段起点时刻及终点时刻的反应液质量之差除以该时间段的时长,g/min),结果如图3。
由图3 可见,在反应-蒸馏耦合工艺制备盐酸羟胺刚开始的0.5h 内,蒸发速率较高,对应的丙酮肟转化率随时间的延长呈直线式快速增加趋势,产物选择性从接近100%降低至95%以上;随着时间的延长,蒸发速率下降,丙酮肟转化率的增速逐渐放缓,产物选择性稳定在93%以上;当时间至2h 后,丙酮肟转化率不再增加。蒸发过程是经典的传热过程,其速率取决于传热面积、传热温差和料液的沸点。反应-蒸馏操作中料液温度与加热温度接近,单位质量物料拥有的换热面积也变化不大,因而主要影响因素是加热温度与沸点之差ΔT。ΔT 越大,传热越快,蒸发速率越快。反应刚开始的30min 内,生成的盐酸羟胺量较少,对反应液的沸点影响较小,ΔT 保持相对恒定,反应液蒸发速率稳定在较高水平,此时反应平衡快速向右移动,产品盐酸羟胺的不断积累。当反应产物积累到一定程度以后,反应液沸点逐渐上升,ΔT 变小,蒸发速率下降,反应平衡的移动速度减缓,最终趋于稳定不变,达到最大的丙酮肟转化率和盐酸羟胺收率。由图3 可见,丙酮肟水解反应达到最大的原料转化率所需时间至少为2h。
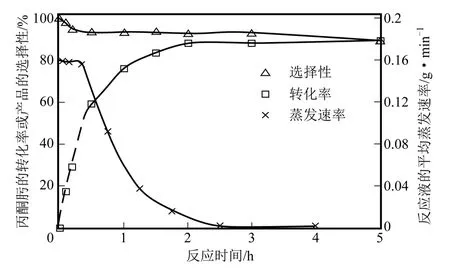
图3 不同时间段的蒸发速率和丙酮肟水解反应结果的对应关系
2.2.3 摩尔配比对羟胺盐合成的影响
在上述优选的工艺条件下,取磁力搅拌器转速为1000r/min、加热温度为130℃、反应-蒸馏时间为3h,在反应-蒸馏耦合装置中进行丙酮肟水解反应实验,考察了不同丙酮肟︰HCl 摩尔比对水解反应的影响,结果如表2。
由表2 可见,随着HCl 投料量的增加,丙酮肟转化率和盐酸羟胺选择性均不断上升,当丙酮肟︰HCl 达到1∶2 后,丙酮肟转化率稳定在最大值89%左右,产物选择性在92%~95%;在丙酮肟︰HCl摩尔比固定的情况下,改变盐酸浓度对丙酮肟转化率和产物选择性没有影响。这是因为盐酸易挥发,在反应-蒸馏的过程中易被部分蒸发而脱离反应体系,使平衡反应难以继续向右移动。增加盐酸用量使反应体系中保留的HCl 组分浓度增大,使丙酮肟转化率增大并趋于最大值,同时使丙酮肟发生其他不良反应的概率降低,产物选择性增加。丙酮肟︰HCl 达到1∶2 后,丙酮肟转化率已处于较高水平,丙酮肟浓度大幅降低,正反应速度显著降低,逆反应速度加快,正逆反应处于动力学速度平衡状态,丙酮肟转化率和盐酸羟胺选择性趋于稳定不变。在此情况下,改变盐酸浓度等价于改变体系中的水量,对上述动力学平衡影响微弱,对丙酮肟转化率和产物选择性影响很小。考虑到采用低浓度的盐酸会产生较多酸性废水,选择最高可能的盐酸浓度(质量分数38%)作为优选浓度。
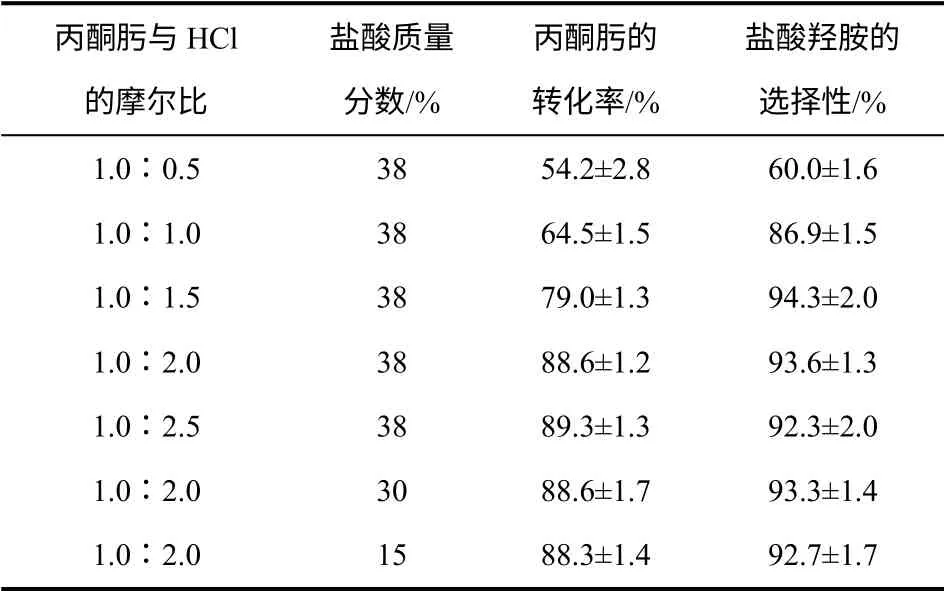
表2 丙酮肟与盐酸的摩尔比对丙酮肟水解反应的影响
3 结 论
(1)建立了对丙酮肟水解可逆反应进程作定量分析检测的HPLC-氧化还原滴定组合分析方法,分析结果的平均回收率达99.64%,相对标准偏差≤2.04%(n=6)。
(2)研究和优化了丙酮肟水解反应制备盐酸羟胺的反应-蒸馏过程工艺条件,具体为:丙酮肟与盐酸的摩尔比为1∶2,盐酸的质量分数为38%,加热温度为130℃,反应时间为3h。在该过程工艺条件下,丙酮肟转化率达到89%左右,盐酸羟胺收率达到84%左右。
[1] Semon W L. The preparation of hydroxylamine hydrochloride and acetone oxime[J].Journal of the American Chemical Society,1923,45(1):188-190.
[2] Smith M B. March’s advanced organic chemistry :Reactions,mechanisms,and structure[M].US:Wiley,2013:1286-1287.
[3] Agne R J. Process for the production of hydroxylammonium acid sulfate:US,3066011[P].1962-11-27.
[4] Bull W C,Marhofer E G,Strickler P D,et al. Preparation of hydroxylamine:US,2827362.A[P].1953-03-18.
[5] Roffia P,Padovan M,Leofanti G,et al. Catalytic process for the manufacture of oxime:US,4794198.A[P].1988-06-08.
[6] Li Zhaohui,Chen Rizhi,Xing Weihong,et al.Continuous acetone ammoximation over TS-1 in a tubular membrane reactor[J].Industrial & Engineering Chemistry Research,2010,49(14):6309-6316.
[7] Liang X,Mi Z,Wang Y,et al.Synthesis of acetone oxime through acetone ammoximation over TS-1[J]. Reaction Kinetics and Catalysis Letters,2004,82(2):333-337.
[8] 高丽雅,檀学军,张东升,等. 羟胺(盐)的合成及其应用研究进展[J]. 化工进展,2012,31(9):2043-2048.
[9] 陈林. 酮肟水解制备羟胺盐工艺[D]. 湘潭:湘潭大学,2009.
[10] 吕俊英. 固体硫酸羟胺和盐酸羟胺的制备[D]. 杭州:浙江大学,2004.
[11] 成凤桂,雷海. 水解-氧化还原滴定法测定锅炉钝化液中的丙酮肟[J]. 分析试验室,2000,19(2):21-23.
[12] Kobayashi Y. Spectrophotometric determination of cyclohexanone oxime in sulfuric acid solution of Epsilon-Caprolactam[J]. Analytical Chemistry,1966,38(7):917-919.
[13] Jencks W P. Studies on the mechanism of oxime and semicarbazone formation1[J]. Journal of the American Chemical Society,1959,81(2):475-481.
[14] 国家质量监督检验检疫总局.GB/T 6685—2007,化学试剂氯化羟胺(盐酸羟胺)[S]. 北京:中国标准出版社,2007:2-3.
[15] 张敏.PDMS/PTFE 用于渗透汽化膜反应器的研究[D]. 北京:北京化工大学,2009.
