地下水污染与防治——电化学技术去除地下水中三氯乙烯
2014-07-20罗晔
罗 晔
(安徽理工大学 安徽淮南 232001)
1 我国地下水污染现状
相对于地下水较强程度的开发利用,地下水资源保护就显得薄弱。地下水资源的环境问题主要指地下水环境质量,也就是地下水污染问题。据《科学通报》13期报道:人类活动导致塔克拉玛干沙漠水体地下水轻度污染。卫生部最新的统计显示,2006年恶性肿瘤成为我国城乡居民的首要死因。而太湖、巢湖等地癌症村的陆续出现,引起了人们对水污染这种环境因素与癌症发病率之间关系的广泛关注。我国地下水污染面积在不断扩大,在我国平原地区,目前要找出一块未被污染的地下水区域竟成了一件很不容易的事情。在水资源相对短缺的北方地区,污染状况更加令人触目惊心,“有河皆枯,有水皆污”并非虚言。
2 地下水污染的防治
2.1 合理开发和利用地下水资源
从可持续发展的角度出发,有计划地开发和利用这些有限的地下水资源。保护地下水资源,制止过量开采地下水,减少地下水位下降幅度,防止地面沉降等,以减少污水的下渗。在开发利用过程中做到采补平衡,严格控制地下水开采量的同时,还应采取多种措施加大对地下水的回灌补给。
2.2 提高公众环境意识并加强地下水保护宣传力度
严格贯彻执行我国的《水污染防治法》《水法》等法规,本着“谁污染,谁治理”的原则,加强执法力度,使每个人都能准确地理解我们的行为给地下水质造成了什么影响。建设必要的污水处理设施;抓好重点污染源的综合治理,对毒性大的污染物,必须在厂内处理,对于毒性小的污染物汇入城市污水处理厂进行集中处理。统筹规划、合理布局。
2.3 建立水质监测网并重点做好水质监测工作
加强基础设施建设,建立水质监测站网,迅速补充和完善地下监测井网,逐步建立和完善水环境监测体系。设立地下水观测专用井,建立地下水动态监测与分析预测服务系统。对重点污染地区(段)进行重点监测,系统掌握区域地表水、地下水水质的污染发展变化及动态特征,为开发利用和管理保护提供及时、科学的依据。
2.4 开展地下水环境脆弱性调查评价及编制评价图册
欧洲、北美和澳大利亚等地区,在地下水污染防治工作中,已经从以污染治理为重点转变为以防止污染为重点,其中采取的一个重要措施即是进行地下水环境脆弱性评价,并编制评价图册。这种方法值得我国借鉴。
3 电化学技术去除地下水中TCE
3.1 实验原理
相关文献报道TCE可以通过催化加氢脱氯生成乙烷[1,2,3],存在H2和O2,Pd催化剂的体系中会生成H2O2[4,5],但是这一发现并没有在相关的调查中提到。而H2O2具有氧化TCE的潜力,并且在Pd催化剂存在的条件下能活化H2O2生成具有强氧化性的·OH(氧化还原电位:2.8V/SHE)[5,6]。基于·OH的强氧化性,溶液中生成的·OH也可以进一步氧化TCE并生成CO2。Pd存在的条件下,催化剂表面能形成·OH[7,8]。但是,在Pd,H2和O2共同存在的条件下H2O2和·OH对TCE降解的贡献从来没有被探索过。本文根据这一思路展开实验,并且验证了不同实验条件下TCE降解的主导方式。

当溶液中不存在Fe(II)时,溶液中发生如下反应:阴极产生H2(2)溶解在溶液中----溶解的H2扩散到Pd催化剂的表面——H2吸附在Pd催化剂表面并且活化成两个活性[H]原子(7)——在不存在Fe(II)的情况下,TCE通过加氢脱氯,形成顺式DCE,乙烯,最终生成乙烷。同时溶解在溶液中的O2扩散并吸附到Pd催化剂的表面,首先氧氧双键被拉长[9](4),接着进一步结合Pd表面的活性[H]生成H2O2,然后H2O2在Pd表面被分解为·OH。因此,在不存在Fe(II)的情况下,仍有少部分的TCE被氧化。整个反应过程以加氢脱氯还原为主导反应途径。
当溶液中存在Fe(II)时,溶液中发生如下反应:溶液中首先发生(1)(2)两个反应——生成的H2和O2吸附到Pd催化剂的表面并结合生成H2O2——由于溶液中存在Fe(II)离子,H2O2与Fe(II)离子结合大量生成强氧化性的·OH(9)——·OH氧化溶液中的TCE,生成有机酸,并进一步氧化成CO2(8)。因此,存在Fe(II)的情况下,大部分的TCE被氧化。整个反应过程以TCE氧化为主导反应途径。
3.2 实验设计
TCE的降解在如图所示的装置中进行,环境温度为(25±1℃)。
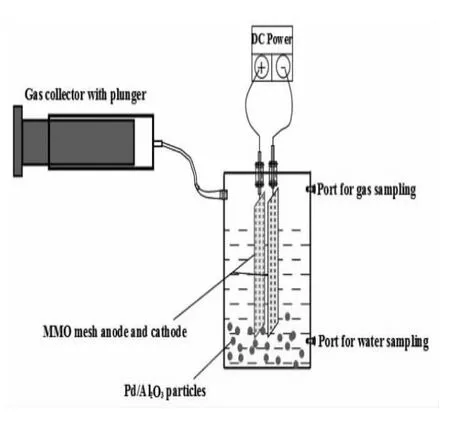
150mL带活塞的注射器连接反应装置,电解过程中气体的膨胀。两块混合金属氧化物(MMO)电极被用作阴极和阳极,电极尺寸为85×15×1.8 mm(长×宽×厚),两块电极相隔42 mm平行放置。每一组实验,加入400mLNa-SO4溶液,1 g/LPd/Al2O3,13.6mg/LFe(II)。Pd/Al2O3催化剂和 Fe(II)的剂量根据实验结果来制定。10mLTCE饱和溶液加入电解质水溶液中形成初始浓度为198 uM(26.1mg/L)的TCE溶液。立即密封实验装置,并用磁力搅拌器搅拌10min帮助TCE在溶液中混合均匀。通过一个聚四氟乙烯的小磁子维持溶液的搅拌速度在600 rpm。施加7 V电压在电解系统上以获得恒定的100mA电流(10mA/cm2)。取水样进行 TCE,顺式 DCE,Cl-,有机酸,pH,氧化还原电位(ORP),Fe(II),H2O2浓度检测。取气体进行气相的顶空测试。为检测反应的降解效率,在加入电解质溶液前通入N2几分钟以赶走溶液中存在的CO2。1mM NaSO4和0.5mM CaSO4加入溶液中模拟地下水化学环境。通过加入20mLTCE饱和水溶液使初始TCE浓度增加一倍到396 uM。所有实验一式两份。
3.2.1 存在和缺乏Fe(II)离子时,TCE的降解
实验条件:环境温度为25±1℃,电极为MMO电极,磁力搅拌器转速为600 rpm,电流为100mA,催化剂量为1 g/LPd/Al2O3,初始pH为4.0,电解质溶液为1mM NaSO4和0.5mM CaSO4,初始TCE浓度为396 uM。一组反应中加入13.6mg/LFe(II),一组不加Fe(II),通过加入和不加Fe(II)离子的两种情况,验证Fe(II)离子对实验反应的影响,从而得出不同情况下TCE降解的主导途径。

实验结果为:TCE不在MMO电极上发生氧化或还原反应,Pd催化剂不吸附溶液中的TCE。这两组实验证实,TCE的降解要在电极和Pd催化剂下共同作用。不存在Fe(II)离子,反应80min,溶液中TCE的浓度从396 uM降低到160 uM。而存在Fe(II)离子,反应80min,溶液中TCE的浓度从396 uM降低到20.2 uM。并且,存在Fe(II)离子时,主要的反应产物是CO2,这说明当存在Fe(II)离子时,溶液中的TCE主要发生氧化反应,在这样的条件下氧化为TCE的主导反应。
3.2.2 Fe(II)离子浓度对TCE降解的影响
实验条件:环境温度为25±1℃,电极为MMO电极,磁力搅拌器转速为600 rpm,电流为100mA,催化剂量为1 g/LPd/Al2O3,初始pH为4.0,电解质溶液为1mM NaSO4和0.5mM CaSO4,初始TCE浓度为396 uM。分别设置5组不同Fe(II)离子浓度来判断Fe(II)离子浓度对TCE降解反应的影响。浓度分别设置为0mg/L、1.4mg/L、6.8mg/L、13.7mg/L、27.3mg/L。

实验结果:Fe(II)离子浓度越高,TCE的降解效果越好。H2O2的积累量随着Fe(II)离子浓度的升高而降低,这是由于Fe(II)离子能促进H2O2的分解。Fe(II)离子浓度越高,·OH浓度越高。Fe(II)离子浓度在0—13.6mg/L的范围时,随着Fe(II)离子浓度浓度的升高,TCE的降解效果越好,·OH的产生量越高。其中·OH的量和TCE的降解效果的相关系数为0.85,说明·OH是TCE降解的主要活性物种。
3.2.3 pH和Pd/Al2O3剂量对TCE降解的影响
实验条件:环境温度为25±1℃,电极为MMO电极,磁力搅拌器转速为600 rpm,电流为100mA,催化剂量为1 g/LPd/Al2O3,初始pH为4.0,电解质溶液为1mM NaSO4和0.5mM CaSO4,初始TCE浓度为396 uM。分别设置不同的初始pH值和Pd催化剂量观察pH、Pd催化剂量对TCE降解效果的影响。pH分别设置为3.0、4.0、5.5、7.0、8.5;Pd催化剂量设置为 0 g/L、0.2 g/L、0.5 g/L、1.0 g

实验结果:pH8.5时,TCE的降解受到抑制,随着pH的降低TCE的降解效果显著增加。在较高的pH时,·OH的产生受到限制,并且溶液中存在的Fe(II)离子以氢氧化物的沉淀形式存在。pH的降低有利于有利于·OH的形成,因此TCE的降解效果更好。催化剂量越大,TCE的降解效果更好。催化剂量越大,能促进吸附更多的H2形成更多的[H],同时也能吸附更多的O2。因此,就能形成更多的H2O2,在有Fe(II)离子存在的条件下,就能生成更多的·OH。所以,TCE的降解效果更好。
3.2.4 地下水化学组成对TCE降解的影响
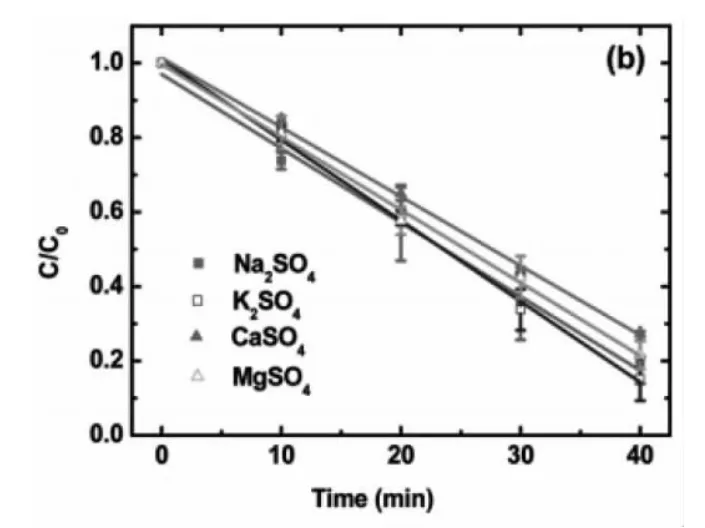
实验条件:环境温度为 25±1℃,电极为MMO电极,磁力搅拌器转速为600 rpm,电流为 100 mA,催化剂量为1 g/L Pd/Al2O3,初始 pH为4.0,电解质溶液为1 mM NaSO4和0.5mM CaSO4,初始TCE浓度为396 uM。设置4组实验,分别加入10mM NaSO4、K2SO4、CaSO4、MgSO4。
实验结果:10mM NaSO4、K2SO4、CaSO4、MgSO4对 TCE的降解效果的影响是相同的,它们只是作为电解质,并不能影响改变TCE的降解途径。
4 结论
在体系缺乏和存在Fe(II)的不同情况下,通过利用金属钯和电解产生的H2和O2来降解模拟地下水中的三氯乙烯(TCE)。在体系中缺乏Fe(II)的情况下,加氢脱氯主导TCE的降解,其中H2O2含量累积达到了17mg/L。在弱酸性条件下,由于H2O2的分解,检测到了低浓度的氧化性羟基自由基,它对TCE的氧化降解略有贡献。
体系中存在Fe(II)时,TCE的降解效率在369μM时80分钟内提高到94.9%。产物的分布情况证明了降解路径转换,即从体系缺乏Fe(II)时79%TCE加氢脱氯到存在Fe(II)时84%的TCE被羟基自由基氧化。在体系中溶液PH=4,初始Fe(II)的浓度从0增加到27.3mg/L时,反应速率常数从2.0增加到4.6 uM/min,TCE的降解遵循零级动力学方程。
TCE的降解速率常数和羟基自由基生成速率常数之间的相关性证明了,羟基自由基是TCE氧化的主要反应活性剂。
体系中存在 10mM的 Na2SO4,K2SO4,CaSO4,和 MgSO4并不会显著影响TCE的降解。一种新型的Pd电极电化学过程提出了治理地下水的方案。
[1]Mcnab,JR.W.W.;Ruiz,R.Palladium-catalyzed reductive dehalogenation of dissolved chlorinated aliphatics using electrolytically-generated hydrogen.Chemosphere1998,37,925-936.
[2]Lowry,G.V;Reinhard,M.Pd-catalyzed TCE dechlorination in water:Effectsof[H2](aq)and H2-utilizing competitive soluteson the TCE dechlorination rate and product distribution.Environ.Sci.Technol.2001,35,696-702.
[3]Lowry,G.V;Reinhard,M.Pd-catalyzed TCE dechlorination in groundwater:Solute effects,biological control,and oxidative catalyst regeneration.Environ.Sci.Technol.2000,34,3217-3223.
[4]Edwards,J.K.;Solsona,B.;Ntainjua,N.E.;Carley,A.F.;Herzing,A.A.;Kiely,C.J.;Hutchings,G.J.Switchingoffhydrogen peroxidehydrogenation in thedirectsynthesisprocess.Science2009,323,1037 1041.[5]Choudhary,V.R.;Samanta,C.;Jana,P.Decomposition and/or hydrogenation of hydrogen peroxide over Pd/Al2O3catalyst in aqueous medium:Factors affecting the rate of H2O2destruction in the presence ofhydrogen.Appl.Catal.A2007,332,70-78.
[6]Yuan,S.H.;Fan,Y.;Zhang,Y.C.;Tong,M.;Liao,P.Pd-catalytic in situ generation ofH2O2from H2and O2produced bywaterelectrolysis for the efficient electro-Fenton degradation of rhodamine B.Environ.Sci.Technol.2011,45,8514-8520.
[7]Hildebrand,H.;Mackenzie,K.;Kopinke,F.D.Highly active Pd-on-magnetite nanocatalysts for aqueous phase hydrodechlorination reactions.Environ.Sci.Technol.2009,43,3254-3259.
[8]Schueth,C.;Kummer,N.A.;Weidenthaler,C.;Schad,H.Field application of a tailored catalyst for hydrodechlorinating chlorinated hydrocarbon contaminants in groundwater.Appl.Catal.B2004,52,197 203.
[9]Staykov,A.;Kamachi,T.;Ishihara,T.;Yoshizawa,K.Theoretical study of the directsynthesisofH2O2on Pd and Pd/Au surfaces.J.Phys.Chem.C2008,112,19501-19505.
