超细碳酸钙粉体的制备
2014-05-14任丽英张群李倩倩
任丽英,张群,李倩倩
(1.安庆医药高等专科学校药学系,安徽安庆 241052;2.安庆师范学院化学化工学院功能配合物安徽省重点实验室,安徽安庆 246003;3.安庆飞凯高分子材料有限公司,安徽安庆 246005)
生物体内存在各种各样的生物矿化材料。从骨骼、牙齿、贝壳、蛋壳到细菌中的磁性体,生物体中包含了一种新型化学,它将软组织与硬组织,有机与无机材料组合在一起。这种在生物体内形成这些矿组织的过程即为生物矿化[1]。碳酸钙是生物矿化的最主要的矿物之一,一直以来是材料学家、矿物学家、生物学家、医学家所关注的研究对象[2-5]。超细碳酸钙粉体功能好坏主要取决于碳酸钙粒子的晶型和粒度分布,不同的使用领域对碳酸钙晶型的要求不一,因此,通过各种方法控制其晶型与粒度的研究越来越多[4]。黄建花等[6]在二甲苯溶液中加入DBS和辅助乳剂正戊醇,然后分别加入碳酸钠、氯化钙水溶液,制得片状碳酸钙。Lei等[7]研究了以PAA-b-PAAL模板,制得盘状聚集体、多核球状、椭圆形、单分散球形和六面体形貌的CaCO3粒子。谢英惠等[8]以SrCl2为晶型控制剂,利用Ca(OH)2悬浮液碳化方法制得针状超细碳酸钙。沈强等[9]以聚乙烯吡咯烷酮(PVP)/小分子表面活性剂(SDS)为模板,制得花状、空心球状和页岩状方解石的碳酸钙晶体。以上碳酸钙晶体的制备方法及合成步骤较为复杂,对反应条件的控制较为严格,不同的条件对碳酸钙微晶的形貌都有不可忽视的影响,除晶形控制剂因素外,溶液的过饱和度、pH值、温度等也都有重要影响。
本文主要是研究不同浓度柠檬酸钠体系对CaCO3的成核及晶体生长产生的影响,并在生物矿化机理的基础上提出CaCO3的结晶机理。
1 实验部分
1.1 试剂与仪器
氯化钙、柠檬酸钠、碳酸铵、盐酸、乙醇、丙酮、硝酸、30%双氧水均为分析纯;实验用水为蒸馏水。
DZF-6020真空干燥箱;D/max-2200PC射线衍射仪;Sirion-200发射扫描电子显微镜。
1.2 实验方法
所有玻璃衬底(玻璃片)及其它玻璃用品放入乙醇中超声30 min,用二次蒸馏水清洗干净,用HNO3/H2O2/H2O(V∶V∶V=1∶1∶1)溶液浸泡12 h。用去离子水清洗干净,最后用丙酮淋洗后自然干燥待用。
称取一定量的无水氯化钙配成一定浓度的溶液,取适量的溶液于小烧杯中,添加少量的柠檬酸钠作为晶形控制剂,用盐酸调节pH至4.0左右,充分搅拌,在烧杯底部斜靠一盖玻片,在另一烧杯中装上碳酸铵固体。各个烧杯均用保鲜膜密封,并在膜上戳3~5个小孔,放入干燥器,以使挥发分解的碳酸铵气体缓慢地进入CaCl2溶液中反应。在设定的反应时间后,取出盖玻片,经洗涤、干燥后,得到测试样品。
2 结果与讨论
2.1 FESEM 分析
柠檬酸钠浓度对产物形貌的影响见图1。

图1 不同浓度柠檬酸钠溶液中形成CaCO3晶体的FESEM照片Fig.1 FESEM images of CaCO3particles obtained in the presence of different concentration
由图1可知,柠檬酸钠浓度为0.5 mmol/L形成的碳酸钙微晶的表面粗糙,呈菱面体向球形过渡形貌,直径大小在2~3 μm,一些微球两两开始融合为一体;柠檬酸钠的浓度为5 mmol/L时,得到的微球相互间进一步融合,菱面体彻底转变为球形,表面光滑且多孔。长度在 5~6 μm;柠檬酸浓度为10 mmol/L时碳酸钙微晶呈现的球形融合体完全过渡转变为两头粗中间细,类似于花生的形状,粒径均匀,在700 nm左右,且粒子分散性良好。由以上可知,柠檬酸钠对晶体的微观形貌有着十分明显的影响。
2.2 XRD 分析
CaCO3晶体X射线粉末衍射分析结果见图2。
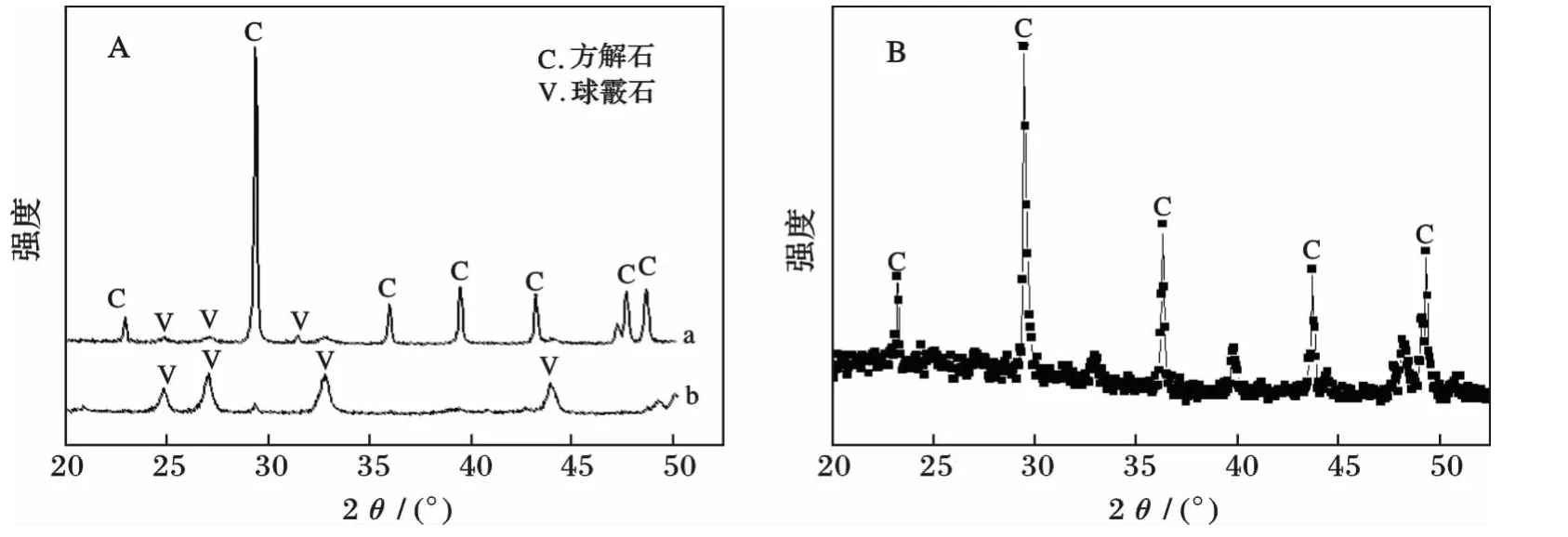
图2 不同浓度柠檬酸钠溶液中形成的CaCO3晶体的X射线粉末衍射A与B图Fig.2 XRD(A and B)of CaCO3particles obtained in the presence of different concentration
由图2可知,在不同浓度柠檬酸钠溶液中所得CaCO3晶体的衍射图谱存在很大差异,以2θ=29.398°的(104)晶面代表方解石,以 2θ=43.804°的(110)晶面代表球霰石,在图2A(a)中,方解石的峰特别尖锐,其强度最大,表明样品的主要晶型为方解石;在图2A(b)中,球霰石的峰变得很强,而方解石的峰消失,此时产物的晶型为球霰石。B图与方解石的标准谱图基本一致,说明在柠檬酸钠浓度为10 mmol/L时,得到的CaCO3晶型只有方解石。Ca-CO3晶体有方解石、球霰石和文石3种稳定构型。晶格中心阳离子Ca2+的配位数不同是区分方解石和球霰石的关键,配位数为6的是能量较低的方解石,配位数为12的是能量较高的球霰石[10-11]。影响配位数高低的主要因素有2个:一是中心阳离子与配位体所带电荷的匹配,二是中心阳离子与配位体空间尺寸的匹配[11]。在酸性条件下,柠檬酸钠分子间存在氢键,氢键之间强烈的相互作用,促成了二聚体或三聚体的形成。当形成的线性二聚体/三聚体使得正负离子的半径比接近0.5时,CaCO3晶体配位数为6[12],说明得到的花生状CaCO3晶型是方解石。
2.3 在不同浓度柠檬酸钠溶液中CaCO3晶体的形成机理
在矿化过程中,碳酸铵分解产生的CO2缓慢扩散,进入柠檬酸钠-氯化钙溶液中形成 CO32-,与Ca2+在柠檬酸钠相面结合,形成有机分子膜包裹的碳酸钙晶种粒子。其中,柠檬酸钠作为一种螯合剂,表面带有的3个羧基在溶液中易电离成负电荷离子,吸附Ca2+形成活性成核中心[R—COO—Ca]yx,然后通过CO32-亲核取代反应逐步形成微小的碳酸钙微晶。微晶的晶型转变很大程度上取决于羧基之间相互距离、大小等因素[13],大量的柠檬酸钠可与Ca2+形成稳定的络合物,在溶液中存在着络合与电离的动态平衡。因此,当CO2缓慢扩散进入柠檬酸钠-氯化钙溶液时,由于柠檬酸钠与Ca2+之间的络合作用使得反应速度减慢,进而延长并扩展了粒子生长的时间和空间,碳酸钙晶体的生长习性也因此有着朝向径向生长的趋势,进而影响晶体产物的形貌。控制剂浓度较低时,柠檬酸钠分子之间的相互作用力(如氢键、静电引力等)很小,粒子通过相互碰撞团聚形成菱面体向球形过渡的形貌(图1a);增大柠檬酸钠浓度,相互作用力加强,柠檬酸钠分子相互之间的距离相互接近,形貌变成微球的融合体;继续增大溶液中柠檬钠的浓度到10 mmol/L,此时,柠檬酸钠在酸性条件下存在强烈的氢键,容易形成二聚体或三聚体,从而形成花生状碳酸钙微晶。综上所述,方解石晶体表面的不同位点对柠檬酸钠的吸附力不同,造成柠檬酸钠对方解石不同位点的生长抑制程度存在差异,这种差异导致了方解石晶体的形貌发生改变[14]。
3 结论
以柠檬酸钠作为晶形控制剂,研究了其对碳酸钙晶体形貌的影响,得出结论如下:
(1)合成花生状碳酸钙晶体最佳条件:柠檬酸钠浓度为 10mmol/L,CaCO3粒子的浓度为20 mmol/L及溶液的pH值为4.0。
(2)花生状碳酸钙的形成是晶形控制剂通过影响晶体生长来实现的,其方式主要是选择性吸附在一定的晶面上,达到改变晶面对介质的表面能。
(3)柠檬酸钠和CaCO3晶体之间存在着无机-有机相之间的界面分子识别。这种界面分子识别的存在,是生物矿化过程中形成各种生物矿物的主要原因,也使得仿生合成新型矿物成为可能。
[1]Naka K,Chujo Y.Control of crystal nucleation and growth of calcium carbonate by synthesis substrates[J].J Chem Mater,2001,13:3245-3259.
[2]Yang J,Liu Y H,Wen T,et al.Controlled mineralization of calcium carbonate on the surface of nonpolar organic fibers[J].Cryst Growth Des,2012,12(1):29-32.
[3]Mann S.Molecular tectonics in biomineralization ard biomimetic materials chemistry[J].Nature,1993,365(7):499-505.
[4]张群,孙新园,陈敏,等.阳离子聚合物聚乙烯亚胺诱导的碳酸钙仿生矿化研究[J].人工晶体学报,2012,41(3):803-808.
[5]Stupp S I,Braun P V.Molecular manipulmion of microstructures:Biomaterials ceranics and sellliconduclo[J].Science,1997,277:1242-1248.
[6]黄建花,童九如.乳液法制备片状 CaCO3[J].现代化工,1994(5):27-30.
[7]Lei M,Tang W H.Effect of a new functional double-hydrophilic block copolymer PAAL oil the morphology of calcium carbonate particles[J].Materials Research Bulletin,2005,40:656-664.
[8]谢英惠,何豫基,任宝山,等.多形状超细碳酸钙的研究[J].河北工业大学学报,2006,29(6):60-63.
[9]Wei H,Shen Q.The effect of carboxymethyl chitosan on the precipitation of calcium carbonate[J].J Crystal Growth,2004,261(4):571-576.
[10]Kresge C T,Leonowicz M E,Roth W J,et al.Ordered mesoporous molecular sieves synthesized by a liquid-crystal template mechanism[J].Nature,1992,359:710-712.
[11]俞伯军,诸晓英,水淼,等.气相扩散法制备的碳酸钙的形貌控制和机理[J].化学通报,2009(10):927-931.
[12]王静梅,姚松年.胆固醇/卵磷脂/壳聚糖体系中碳酸钙模拟生物矿化的研究[J].无机化学学报,2002,18(3):249-254.
[13]Tong H,Ma W T,Wang L L,et al.Control over the crystal phase,shape,size and aggregation of calcium carbonate via a L-aspartic acid inducing process[J].Biomaterials,2004,25:3923-3929.
[14]Clfen H,Qi L M.Systematic examination of the morphogenesis of calcium carbonate in the presence of a doublehydrophilic block copolymer[J].Chem Eur J,2007,7(1):106-116.
