以PHAs为固体碳源的城镇二级出水深度脱氮研究
2014-04-26左剑恶李再兴清华大学环境学院环境模拟与污染控制国家重点联合实验室北京00084河北科技大学环境科学与工程学院河北省石家庄05008浦华环保有限公司北京0000
李 彭,唐 蕾,左剑恶*,袁 琳,李再兴(.清华大学环境学院,环境模拟与污染控制国家重点联合实验室,北京 00084;.河北科技大学环境科学与工程学院,河北省 石家庄 05008;.浦华环保有限公司,北京 0000)
以PHAs为固体碳源的城镇二级出水深度脱氮研究
李 彭1,唐 蕾2,左剑恶1*,袁 琳3,李再兴2(1.清华大学环境学院,环境模拟与污染控制国家重点联合实验室,北京 100084;2.河北科技大学环境科学与工程学院,河北省 石家庄 050018;3.浦华环保有限公司,北京 100020)
利用从连续运行的缓释碳源滤料滤池中取出的聚羟基脂肪酸酯(PHAs)颗粒,研究了微生物和硝酸盐对其的总有机碳(TOC)释放速率的影响,并研究了温度、pH值、硝态氮浓度对其反硝化速率的影响.结果表明:原有的和附着有微生物的PHAs颗粒在去离子水中TOC释放速率分别为0.030,0.053mg/(g·d),远低于水中有硝酸盐时的TOC释放速率[进水NO3--N为30mg/L时,TOC释放速率为0.533mg/(g·d)].温度和pH值对反硝化速率影响较大, pH值为7.5时,在15~35℃范围内, 30℃下的反硝化速率最大,为0.067mg/(g·h);温度为30℃时,pH值在6.0~9.0范围内,pH值为7.8时的反硝化速率最大,达到0.061mg/(g·h).反硝化速率与NO3--N浓度之间的关系符合Monod方程,最大反应速率和半饱和常数分别为4.74mgNO3--N/(gSS·h)和56.6mg/L.
:缓释碳源;固相反硝化;可生物降解聚合物;聚羟基脂肪酸酯;城镇二级出水
城镇污水厂常用深度脱氮技术多为反硝化生物滤池[1-2],但二级出水中有机物含量较少,无法满足生物脱氮的要求.因此,反硝化生物滤池中往往要投加碳源物质,应用较多的是甲醇、乙酸钠、乙醇和葡萄糖等[1-4]液体碳源.由于城镇污水厂的进水水质和水量变化频繁,液体碳源投加量的控制很难响应进水波动,投加过量会导致出水有机碳超标[5-6],投加不足则导致出水亚硝酸盐积累[7];有研究采用玉米芯、稻草、稻壳、麦秆[8-9]等农业废物进行脱氮试验,但这些天然有机材料的碳释放速率不稳定,且含有其他非碳成分,可能需要增加后处理.
近年来一些可生物降解聚合物作为反硝化碳源的可行性受到关注[10-12].1991年国外就有学者提出用 PHB(聚-β-羟基丁酸酯)作为反硝化碳源的设想[13].目前报道较多的有 PCL,PBS和淀粉基共混物等为固体碳源,对地下水和饮用水进行脱氮处理[5,14-15].但对固体碳源有机物的释放规律缺乏报道,本研究采用聚羟基脂肪酸酯(Polyhydroxyalkanoates,PHAs)作为碳源和微生物载体,对固体碳源的有机物释放机制进行研究,同时考察了温度,pH值等环境因素对反硝化速率的影响,以期为固体碳源反硝化工艺的工程应用与实际运行提供技术依据与参考.
1 材料与方法
1.1 试验材料
试验中采用的固体碳源为市售 PHBV(3-羟基丁酸酯和 3-羟基戊酸酯共聚物,(C9H18O6)n)颗粒(意可通,深圳),材料外观为黄色圆柱颗粒,截面直径(3.30±0.11)mm,长度为(4.35±0.87)mm.试验中所用的附着有成熟生物膜的 PHAs颗粒取自位于北京肖家河污水处理厂的缓释碳源滤料滤池试验装置.该滤池装置填料层容积 9.42L,连续运行7个月,进水采用污水厂二级出水,取样期间运行稳定,进出水水质情况如表1所示,进水温度为15℃,过滤速度0.8m/h.

表1 PHAs材料取样期间反应器的进出水水质Table 1 Water quality of influent and effluent of the bioreactor while taking samples of PHAs
1.2 试验装置与用水
试验采用500mL三角瓶作为反应器,瓶口用橡胶塞密封,胶塞上装有排气管排出氮气,并保持反应器内缺氧环境.试验用水由去离子水中加入KNO3和磷酸盐配制,根据试验内容配成不同NO3
--N浓度和pH值的模拟污水.
1.3 试验方法
1.3.1 微生物对PHAs的TOC释放的影响 在250mL三角瓶中分别加入 10.0g(干重)新鲜PHAs颗粒和10.0g(湿重)附着有生物膜的PHAs颗粒,均加入 100mL去离子水.瓶口用橡胶塞密封,置于 30℃恒温振荡箱.其中装有新鲜颗粒的三角瓶,每5d取样测定TOC,并更换去离子水,连续试验50d.装有附有生物膜的PHAs颗粒的三角瓶,每天取样测定TOC,连续试验10d,接下来在超声振荡器中剥离生物膜,PHAs颗粒在 50℃下干燥 24h后称重,用于计算有微生物存在时 PHAs在去离子水中的TOC释放速率.
1.3.2 PHAs颗粒的挂膜性能 将取自现场缓释碳源滤料滤池的附着有生物膜的 PHAs颗粒置于超声振荡器内,使其表面生物膜完全剥离,将PHAs颗粒于50℃下干燥24h后称重,剥离后的生物膜置于105℃下烘干24h后称重.
1.3.3 温度、pH值和NO3--N浓度对反硝化速率的影响 采用序批试验研究温度、pH值和NO3
--N浓度对反硝化效果的影响,在锥形瓶中加入 10g(湿重)附着有生物膜的 PHAs颗粒和300mL的模拟污水,通过恒温振荡箱控制反应温度.研究温度的影响时,将5个上述三角瓶分别置于15,20,25,30,35℃下进行反硝化试验,模拟污水初始NO3
--N浓度为50mg/L,并通过磷酸盐缓冲体系调节pH值为7.5;研究pH值的影响时,利用磷酸盐缓冲溶液将 4个上述三角瓶内模拟污水pH值调整为6.0、6.6、7.2、7.8,利用硼酸-硼砂缓冲溶液将2个三角瓶内模拟污水pH值调整为8.4、9.0,初始NO3--N浓度为50mg/L,温度为30℃;研究进水NO3--N浓度的影响时,初始NO3
--N浓度为15,20,30,50,75mg/L,同时维持pH值为7.5,温度30℃.
1.4 分析方法
水样经 0.45μm 滤膜过滤后进行水质分析, NO3
--N、NO2--N和NH3-N测定分别采用紫外分光光度法、N-(1-萘基)-乙二胺光度法、水杨酸-次氯酸盐光度法(Hach,DR5000);TOC采用燃烧氧化非分散红外吸收法(岛津,TOC-VCPH)测定.使用pH计(Mettler, DELTA320)测定pH值.使用溶解氧测定仪(Hach,HQ30d)测定溶解氧. PHAs颗粒表面观察使用电子扫描显微镜(FEI, QUANTA200).
2 结果与讨论
2.1 微生物和硝酸盐对PHAs的TOC释放的影响
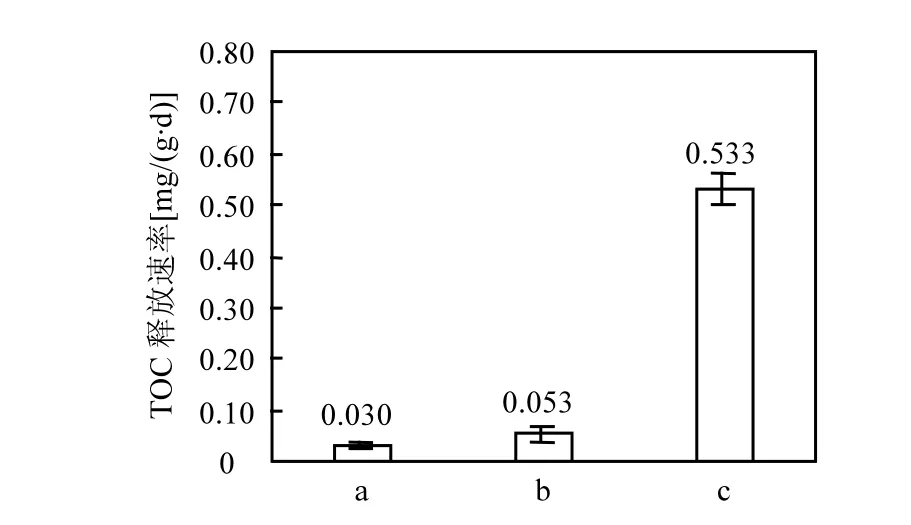
图1 PHAs在不同条件下的TOC释放速率的对比Fig.1 The organic carbon release rates of PHAs under various conditions(a)去离子水中PHAs表面无微生物;(b)去离子水中PHAs表面有生物膜;(c)缓释碳源滤料滤池处理城镇二级出水(进水NO3--N为30mg/L,15℃)
固体碳源材料的有机碳释放包括物理溶解和微生物作用下的水解两种作用.将新鲜的和附着有生物膜的 PHAs颗粒置于去离子水中,通过水中的TOC浓度变化测定TOC释放速率,结果见图1.PHAs在去离子水中的TOC释放速率为0.030mg/(g·d).据报道玉米芯、稻草和稻壳的TOC平均释放率分别为 7.9,2.2,1.6mg/(g·d)[8],可见 PHAs的有机碳释放速率远小于以上天然有机质.当进水中缺乏硝酸盐时,PHAs物理溶出的TOC量极低,不会对出水COD造成影响.附着有生物膜的PHAs在去离子水中的TOC释放速率在前4d为0.068mg/(g·d),接下来6d的TOC释放速率保持稳定,为0.038mg/(g·d),平均释放速率为0.053mg/(g·d).有生物膜附着的 PHAs颗粒在试验前期出现较高的TOC释放速率可能是由于在缺少硝酸盐和O2的情况下,生物膜中的好氧微生物衰亡后产生的溶解性微生物产物(SMP)导致.从以上结果可以看出,即使有微生物存在时, PHAs也不会因水解而释放过多的 TOC.根据现场缓释碳源滤料滤池的运行条件和表 1所示水质数据,按照有机碳质量平衡的方法[16]计算出PHAs的TOC释放速率约为0.533mg/(g·d).结果说明在进水中缺乏硝酸盐的情况下,微生物对PHAs水解作用微弱;只在有硝酸盐存在的情况下,反硝化菌才会分解利用 PHAs作为自身反硝化的碳源.微生物对有机物的水解过程可以响应水中硝态氮浓度的的变化,因此TOC不会因进水波动而过度释放,降低了出水COD超标风险.
2.2 PHAs颗粒的挂膜效果
材料表面所负载的微生物由两部分组成:附着材料生长的微生物和材料间隙生长的微生物.采用重量法测定稳定挂膜的 PHAs表面生物膜量为 0.020g生物膜/gPHAs(干重),又测得 PHAs堆积密度为0.7kg/L,因此以PHAs为填料的反硝化滤池中床层内的污泥浓度可达 14000mg/L.这说明以 PHAs不仅可以作为固体碳源,而且作为反硝化载体,有利于微生物的附着,能够在反应器内实现较高的污泥浓度,从而使得固相反硝化工艺具有较高的反硝化速率.
利用电子扫描显微镜(SEM)观察初始 PHAs颗粒,剥离生物膜后的 PHAs颗粒以及材料表面生物膜,结果如图2所示.由图2(a)可见初始PHAs表面光滑、均匀、无孔隙.图 2(c)显示在微生物的作用下,颗粒表面被腐蚀形成大量的细小孔洞,这些孔洞会增大反硝化菌的附着面积,使得微生物更容易附着.这也说明 PHAs能够作为碳源被微生物利用,而且适宜作为反硝化生物的生物膜载体.图 2(b)中可以看出,PHA表面形成致密,结构良好的生物膜,微生物以杆菌和球菌为主,但具体菌种需要进一步鉴定.相比较范振兴等[11]以聚乳酸(PLA)作为固体碳源的研究中所观察到的以球菌为主的生物膜则有所不同.
2.3 温度对PHAs反硝化效果的影响
通过序批试验研究 15~35℃温度范围内PHAs颗粒的反硝化效果,结果如图3所示.由图3可以看出,温度对反硝化速率的影响较明显,15~30℃之间反硝化速率随温度的升高而增加,在30℃时反硝化速率最大,为0.067mg/(g·h),高于文献报道的淀粉基共混物[14,17],PCL[15,18], PLA[11]等材料的反硝化速率.而35℃时反硝化速率相对30℃时有所下降.15℃时反硝化速率仅为30℃时的20.3%.说明以 PHAs作为反硝化碳源,低温对反硝化速率的影响较大,反硝化菌在低温情况下的代谢受到明显抑制.

图2 PHAs颗粒被微生物利用前后及生物膜表面形态Fig.2 Surface morphology of original, reacted PHAs pellets and biofilm covered

图3 不同温度下的反硝化效果Fig.3 Denitrification rates at various temperatures
2.4 pH值对PHAs反硝化效果的影响

图4 不同pH值条件下的反硝化速率Fig.4 Denitrification rates at various pHs
不同 pH值条件下的反硝化速率如图 4所示.pH值介于6.0~9.0之间时,反硝化速率在pH值为7.8时达到最大,为0.061mg/(g·h).pH值小于7.8时,pH值越高,NO3--N的反硝化速率越大;pH值大于7.8时,反硝化速率随pH值的增大而迅速下降.周海红等[19]以 PBS为碳源及 Jang等[20]以葡萄糖为碳源进行固相反硝化的研究,均发现pH值大于8.0之后,反硝化速率急剧下降.
以PHBV为固体碳源的反硝化方程式为:
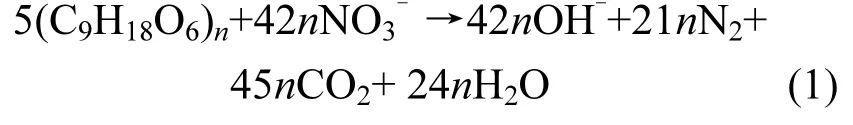
由式(1)可知,反硝化过程产生的碱可使 pH值增高.pH值在6.6~7.2之间时,反硝化速率变化不大,但pH值小于6.6时,pH值波动范围超过了反硝化菌的承受能力,导致反硝化速率明显下降.
一般来说,活性污泥反硝化系统的最佳 pH值通常在7.5左右,pH值为6.5以及9.0时反硝化速率将为最佳值的70%左右[21].而以PHAs作为碳源的反硝化过程,pH值为6.6和9.0时的反硝化速率分别为最佳值(pH=7.8时)的 52.5%和13.1%,说明相对于酸性环境来说,碱性环境对反硝化菌代谢的影响更大.
2.5 NO3
--N浓度对PHAs的反硝化速率的影响测量初始NO3--N浓度为15,20,30,50,75mg/L的三角瓶内浓度变化,同时测量各瓶中颗粒上附着的生物膜质量,得到相应
浓度下反硝化速率分别为 0.991,1.228,1.692,2.213,
在以固体缓释碳源材料的碳源的反硝化过程中,反硝化速率应同时受浓度和释放出的碳源物质的浓度的影响.因此,可以建立试验中三角瓶内反硝化过程的双基质反应动力学方程如下:
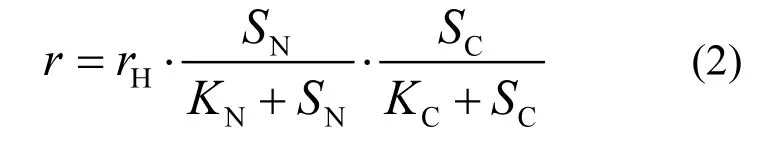
式中: r和rH分别为的反应速率和最大反应速率,和 SC分别为和 COD浓度,mg/L;KN和 KC分别为和溶解性COD的半饱和系数,mg/L.根据ASM1模型推荐,KN为0.5mg/L[21],该值远小于试验中浓度,因此反硝化动力学方程中第二项的值约为1.即式(2)可以近似简化成式(3):

由于试验中所采用的 PHAs颗粒同时兼做缓释碳源材料和反硝化生物膜的载体,其所释放的溶解性COD会快速被附着于其表层的反硝化细菌所利用,而难于直接测量.宋慧敏等[23]报道了在反硝化菌形成的生物膜内的传递规律,对于薄生物膜,膜内与液相中的浓度差别不大.因此如果认为微生物对 PHAs水解释放 COD浓度与液相中浓度成正比,即则固相反硝化动力学方程可以写成式(4):
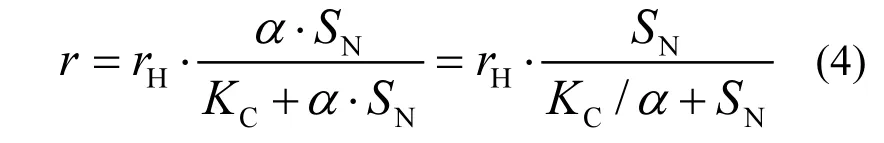
根据ASM1模型推荐,KC为20mg/L[21],则α的值约为 2.83,该值与彻底反硝化所需的COD比例系数2.86也极为相近.有研究者对反硝化动力学进行研究,发现的半饱合系数很低,约为 0.5mg/L[22].在本研究的浓度下,其对反硝化速率应无明显影响,呈零级反应.本研究发现反硝化速率与浓度呈现很好的相关性.其实质是反硝化速率与溶解性COD浓度相关,在缓释碳源反应系统中,有机物的释放浓度受到污水中的浓度的响应控制,即,因此最终表观的现象是反硝化速率与浓度相关.
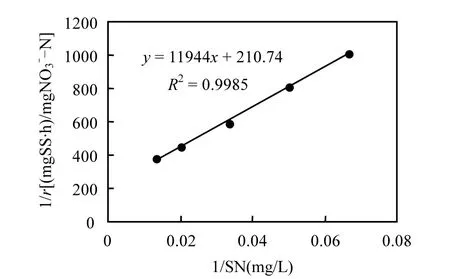
图5 不同进水硝氮浓度下的反硝化速率Fig.5 Denitrification rates with various influent nitrate concentrations
3 结论
3.1 新鲜PAHs颗粒和附着成熟生物膜的PAHs颗粒在去离子水中的 TOC释放速率分别为0.030,0.053mg/(g·d),在PHAs进行城镇二级出水的深度反硝化时 TOC释放速率可达 0.533mg/ (g·d).说明进水中无硝酸盐时,即使有微生物存在,PHAs的TOC碳释放速率也极低.
3.2 PHAs可被微生物利用,并能作为载体在其表面形成以杆菌和球菌为主的生物膜.稳定挂膜的 PHAs表面生物膜量为 0.020g生物膜/ gPHAs(干重),以PHAs为填料的反硝化滤池中床层内的污泥浓度可达14000mg/L.
3.3 PHAs可作为反硝化碳源去除城镇污水二级出水中的硝酸盐,在 15~35℃范围内,初始硝态氮浓度 50mg/L的条件下,30℃时反硝化速率最大,为 0.067mg/(g·h);低温对反硝化速率影响较大,15℃时的反硝化速率仅为30℃时的20.3%. 3.4 pH对反硝化速率影响较大,pH值为7.8时反硝化速率最大,达0.061mg/(g·h); pH值大于7.8时,反硝化速率急剧下降.
3.5 以 PHAs为固体碳源的反硝化速率与NO3
--N浓度之间满足Monod方程,最大反应速率和半饱和常数分别为 4.74mgNO3--N/(gSS·h)和56.6mg/L.
[1] 鲍立新.深床滤池在无锡市芦村污水处理厂的运行效果 [J].给水排水, 2012,28(6):41-43.
[2] Koch G., Siegrist H. Denitrification with methanol in tertiary filtration at wastewater treatment plant Zürich-Werdhölzli [J]. Water Science and Technology, 1997,36(1):165-172.
[3] 王静萱,李 军,张振家,等.固定化包埋颗粒对二级出水深度脱氮特性研究 [J]. 环境科学学报, 2013,33(2):389-394.
[4] Srinandan C S, D`souza G, Srivastava N, et al. Carbon sources influence the nitrate removal activity, community structure and biofilm architecture [J]. Bioresource Technology, 2012,117:292-299.
[5] Boley A, Müller W R. Denitrification with polycaprolactone as solid substrate in a laboratory-scale recirculated aquaculture system [J]. Water Science and Technology, 2005,52(10/11):495-502.
[6] 葛士建,王淑莹,杨岸明,等.反硝化过程中亚硝酸盐积累特性分析 [J]. 土木建筑与环境工程, 2011,33(1):140-146.
[7] Her J J, Huang J S. Influences of carbon source and C/N ratio on nitrate/nitrite denitrification and carbon breakthrough [J]. Bioresource Technology, 1995,54:45-51.
[8] 邵 留,徐祖信,金 伟,等.农业废物反硝化固体碳源的优选[J]. 中国环境科学, 2011,31(5):748-754.
[9] 刘江霞,罗泽娇,靳孟贵,等.以麦秆作为好氧反硝化碳源的研究[J]. 环境工程, 2008,26(2):94-96.
[10] Takahashi M, Yamada T, Tanno M, et al. Nitrate removal efficiency and bacterial community dynamics in denitrification processes using Poly (L-lactic acid) as the solid substrate. Microbes and Environments, 2011,26(3):212-219.
[11] 范振兴,王建龙.利用聚乳酸作为反硝化固体碳源的研究 [J].环境科学, 2009,30(8):2315-2319.
[12] 王旭明,从二丁,罗文龙,等.固体碳源用于异养反硝化去除地下水中的硝酸盐 [J]. 中国科学B辑:化学, 2008,38(9):824-828.
[13] Muller W R, Heinemann A, Schafer C, et al. Aspects of PHA as an H-donor for denitrification in water treatment processes. Water Supply, 1992,10:79-90.
[14] 闫 续,许 柯,耿金菊,等.两种释碳材料的制备及其性能研究[J]. 中国环境科学, 2012,32(11):1984-1990.
[15] 封羽涛,吴为中.可降解聚合物 PCL,PBS在低有机污染水中固相反硝化脱氮效果比较 [J]. 生态环境学报, 2011,20(6/7): 1127-1132.
[16] 唐 蕾,李 彭,左剑恶,等.缓释碳源滤料滤池用于二级出水的深度脱氮 [J]. 环境科学, 2013,34(9):3526-3531.
[17] Li P, Zuo J, Xing W, et al. Starch/PVA blended materials used as solid carbon source for tertiary denitrification of the secondary effluent [J]. Journal of Environmental Sciences - China, 2013,25(10):DOI:10.1016/S1001-0742(12)60259-9.
[18] Zhou H H, Zhao X, Wang J L. Poly (ε-caprolactone) as substrate for water denitrification [J]. International Journal of Environment and Pollution, 2009,38(3):349-359.
[19] 周海红,王建龙,赵 璇.pH对以PBS为反硝化碳源和生物膜载体去除饮用水源水中硝酸盐的影响 [J]. 环境科学, 2006,27(2): 290-293.
[20] Jang A, Ahn H, Kim I S. Monitoring the impact of dissolved oxygen and nitrite on anoxic biofilm in continuous denitrification process [J]. Environment Monitoring and Assessment, 2003,87(2): 133-144.
[21] 徐亚同.pH 值、温度对反硝化的影响 [J]. 中国环境科学, 1994,14(4):308-313.
[22] 国际水协废水生物处理设计与运行数学模型课题组.活性污泥数学模型 [M]. 张亚雷,李咏梅译,上海:同济大学出版社, 2002:24-25.
[23] 宋慧敏,周小红,张永明,等.基于微电极技术的反硝化滤池生物膜特性分析 [J]. 中国环境科学, 2012,32(5):850-854.
Tertiary nitrogen removal of the municipal secondary effluent using PHAs as solid carbon sources.
LI Peng1, TANG
Lei2, ZUO Jian-e1*, YUAN Lin3, LI Zai-xing2(1.State Key Joint Laboratory of Environmental Simulation and Pollution Control, School of Environment, Tsinghua University, Beijing 100084, China;2.School of Environmental Science and Engineering, Hebei University of Science and Technology, Shijiazhuang 050018, China;3.THUNIP Holdings Limited Company, Beijing 100020, China). China Environmental Science, 2014,34(2):331~336
Polyhydroxyalkanoates (PHAs) pellets, which were taken from a denitrification biofilter with sustained-release carbon source materials, were used to investigate the effects of microbes and nitrate on the organic carbon release rate of PHAs and the effects of temperature, pH and NO3--N concentration on the denitrification rates. The results indicated that the total organic carbon (TOC) release rates of original PHAs and those with biofilm attached were determined to be 0.030 and 0.053mg/(g·d) in the deionized water, respectively, which were much lower than that of 0.533mg/(g·d) in simultaneous presence of microbes and nitrate (30mg/L of NO3--N concentration). The effects of temperature and pH on denitrification rates were significant. When influent NO3--N concentration was 50mg/L, the maximum denitrification rates achieved to 0.067mg/(g·h) at 30℃ in the temperature range of 15 to 35℃, and to 0.061mg/(g·h) at pH7.8 in the pH range of 6.0 to 9.0. The relationship between denitrification rates and NO3--N concentrations appeared to be in good agreement with Monod Equation, and the maximum denitrification rate and the saturation constant were 4.74mgNO3--N/(gSS·h) and 56.6mg/L, respectively.
sustained-release carbon source;solid-phase denitrification;biodegradable polymers;polyhydroxyalkanoates (PHAs);municipal secondary effluent
李 彭(1982-),男,辽宁葫芦岛人,清华大学环境学院博士研究生,主要研究方向为污水生物处理和资源化.发表论文5篇.
2013-05-07
国家“863”项目(2009AA063805)
* 责任作者, 教授, jiane.zuo@tsinghua.edu.cn
:X703.5
:A
:1000-6923(2014)02-0331-06
