用化学基本观念引领元素化合物的复习——以“氯气”复习为例
2013-12-28王保强
王保强 袁 林
(1 新沂市第一中学 江苏 新沂 221400;2 新沂市教研室 江苏 新沂 221400)
高中化学课程标准(实验)中明确指出高中教学要使“学生了解化学科学发展的主要线索,理解基本的化学概念和原理,理解化学变化的基本规律,形成有关化学科学的基本观念[1]。 ”形成化学基本观念是高中化学的课程学习的基本目标。目前高中的化学复习往往是利用高三整整一年的时间,在复习过程中,特别是元素化合物的复习过程中,面对学生已经学习过的知识,如何提高复习质量?这是在教学实践中必须回答的问题。 笔者以为,用化学基本观念来引领元素化合物的复习将会使高三复习突破效率不高的瓶颈,取得高质量的复习效果。
一、元素化合物复习中存在的问题
元素化合物知识是指围绕单质及化合物有关的物理性质、化学性质、制法、用途等方面的知识,它是中学化学理论、概念、定律等知识的基础。 化学以与人类社会物质生活紧密相关的化学物质为主要研究对象[2],“世界由物质而丰富,物质由元素而精彩”。 元素化合物中涉及的物质种类繁多,中学化学常见的元素化合物分为非金属元素和金属元素,非金属元素包括卤素、氧族、氮族和碳族,金属元素包括碱金属、碱土金属、铝、铁、银和铜。在学习元素化合物知识时,很多需要在新课学习时通过分组实验进行验证理解。 由于在新课学习时就没有采用实验的方式进行学习,因此在复习时仍然需要通过记忆来强化知识点,无疑给复习增加了很大的难度。 由于化学学科在我省属于选修科目, 不纳入高考总分计算,尽管化学教师能够坚守自己的课堂阵地,但学生普遍不太重视,每周的课时相对较少,课后没有化学自习时间。 在教学实践中,在第一学期寒假质量检测前基本上一轮复习结束,复习时间紧迫,很多教师把元素化合物知识的学习时间段认为是化学复习的提速阶段,导致学生在学习时疲于应付。 新课程改革已经近10 年,但是由于高考模式没有改变,高三化学一线教师目前仍然受到应试教育的影响,教师与学生往往沉溺于习题的训练中,教师忙于找题,学生忙于做题,导致学生的提升的空间很小。
二、化学基本观念的内容
化学基本观念, 不是具体的化学知识和技能, 也不是化学知识和技能的简单组合,它是学生通过化学学习在头脑中保留的,在遇到周围的化学问题时所具有的基本的观念性的东西, 也可以认为是学生所获得的对化学的总观性的认识[3],形象地说是知识挥发留下来的印迹。尽管化学基本观念是一种对事物深层的本质认识,但在教学实践中,根据对基本观念的理解分解为常见的可以操作的教学目标, 仍然可以通过课堂教学得到强化的。具体反映在课堂上可围绕化学的核心概念、 基本技能,如元素、守恒、绿色化学等观念开展教学。 结合新课程标准中的三维目标,笔者认为化学基本观念的网络关系如图(图1)。

图1 中学化学基本观念体系
三、基本观念指引下的元素化合物复习
在复习教学中,基本观念引导下的复习应该是对整个中学化学复习而言,并不仅仅一节课、一个单元的学习,它应该不露痕迹地贯穿复习教学的始终。 化学基本观念的建立若缺少师生持续的心智努力和情感付出,缺乏对相关事实、概念的深入理解,任何复习都是浅层次的认知重复行为[4]。在课堂教学目标设计时,化学基本观念一般不单独列出作为教学目标或教学重点,即并不是让学生以背诵记忆的方式来实现, 但是通过一节课、一个单元的学习之后,学生明显可以感觉到化学基本观念层面上的提升。
在一节复习课上对所有的知识点向排地雷一样全都梳理一遍,这显然是不合适的。 教师在备课时需要根据学生已有的经验和教学内容确定复习课预期所达到的基本观念,这个基本观念是对课程标准和考试说明解读后得到的。 教师要把这个观念转化为上位目标,并根据上位目标,设计出更加具体和更具有操作性的教学目标,这是因为教学目标是围绕筛选出的重点知识并整合核心概念而设计的。 如果教学中没有围绕基本观念的深入理解并进行设计,那么元素化合物的复习课将会停留在较低的认知水平,学生就会倾向对基本的知识、基本事实进行死记硬背,教师也就会拿出唯一的杀手锏——“默写化学方程式和离子方程式”。 教学中的这种目标设计不仅整合了具体知识的学习,关键是它能把学生的思维聚焦并引导到更深的基本理解上。
复习案例——以氯气复习为例
[知识目标]
(1)能够画出氯气及含氯化合物之间的网络图。
(2)能正确书写氯气及含氯化合物有关的化学方程式。
(3)了解氯水的消毒和漂白作用。
(4)知道实验室制取氯气的反应原理。
[能力目标]
(1)能从化学反应基本类型和氧化还原反应的角度分析氯气与常见物质的反应,并能写出相关的离子方程式。
(2)能用化学平衡的原理分析氯水中成分的变化。
(3)通过氯气及其化合物的性质、制法和用途等知识的复习,理解化学基本观念中的分类观、微粒观、元素观和变化观。
[设计目的]结合考试说明和课程标准的内容,确定本节复习的重点应该是从氧化还原反应的角度理解与氯气及含氯化合物的化学反应方程式。 具体引领复习的观念有分类观、微粒观、元素观和变化观。 教学目标中没有将情感态度价值观目标列出, 不是说可以忽略此目标,而是将此目标融入知识目标和能力形成的过程中。
[教学过程]
[思考]1.将Cl2、HClO、Ca(ClO)2、HCl 、NaCl 的互变关系整理成知识网络。
[学生活动]学生尝试连线整理,并相互讨论给出网络图(如图2)。
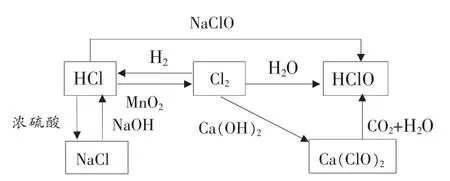
图2 氯气及其化合物关系网络图
[设计目的]通过含氯的单质及化合物关系网络图,提醒学生尽管它们是5 种不同的物质,但是都含有氯元素。 它们之间的区别在于它们的组成和化合价,在物质转化时要注意化合价的变化。 这道思考题主要渗透元素观和变化观。
[思考]2.可以从不同的角度对物质进行分类,如氯及其化合物分类标准一:
单质:Cl2; 氧化物:ClO2;酸:HCl、HClO、HClO4;盐:氯化物、次氯酸盐、氯酸盐。
请你整理出两种对常见氯及其化合物的分类方法。[学生讨论并尝试分类]
(1)分类标准二:按化合价高低分类
-1 价:HCl、氯化物;0 价:Cl2;+1 价:HClO、次氯酸盐;+3 价:不常见; +5 价:氯酸钾; +7 价:HClO4
(2)分类标准三:按物质性质分类
氧化性:Cl2、ClO2、HClO、 次氯酸盐、 氯酸盐、HCl(H+)、HClO4(H+)
还原性:HCl(Cl-)、Cl2
溶液呈酸性:Cl2、HCl、HClO、HClO4
溶液呈碱性:次氯酸盐
[设计目的]学生利用分类观的知识,依据不同的分类标准,进行分类练习,培养学生动手能力和创新能力。学生练习的目的是强化分类观的形成。
[教师引导] 我们还可以按物质参与的化学反应类型分:(3)分类标准四:按反应类型分类(如图3)

图3 氯气、次氯酸、次氯酸盐按照反应分类图
[设计目的]通过教师给出示例,学生根据化学反应类型进行练习。 教师的示范所给出的是物质分类知识,分类的依据是物质的组成结构。
[学生练习] 学生按照反应类型分别书写对应的化学方程式。
比如与氯气有关的反应有:
化合反应:Cl2+H2→、Cl2+金属单质→、Cl2+FeCl2→
置换反应:Cl2+NaBr→、Cl2+NaI→
氧化还原反应:有单质(Cl2)参与的化合、置换反应都属于氧化还原反应;Cl2+H2O→、Cl2+碱→, 另:SO2、SO32-、S2-也能被Cl2氧化。
可逆反应:Cl2+H2O⇌HCl+HClO
取代反应;Cl2+CH4→
加成反应:Cl2+C2H4→
水解反应(可逆反应):NaClO+H2O⇌NaOH+HClO
[设计目的]通过书写Cl2、HClO、次氯酸盐三类物质所能发生的化学反应,落实方程式书写技能,培养学生的元素观和变化观。
[提出问题]4.氯水中的化学平衡(条件对化学平衡的影响)
[投影]氯水的制备:往蒸馏水中通入氯气至溶液呈浅黄绿色。 (如图4)
[提问思考] 氯水中存在哪些物质发生变化的过程?含有哪些成分? 氯水应如何保存?
利用上述问题,可以讨论:
(1)溶解平衡:Cl2在水中的溶解性小,1 体积水约能溶解2体积的Cl2,氯水呈浅黄绿色,具有挥发性,Cl2的挥发和溶解构成了溶解平衡。
(2)化学平衡:溶于水中的氯气部分与水发生如下反应并达到化学平衡:Cl2+H2O⇌HCl+HClO。 HClO 在光照条件下会分解:

图4 氯水的制备
(3) 电离平衡:HClO 在溶液中存在电离平衡:HClO
通过上面三种平衡的分析,可知新制氯水中含有的分子、离子微粒有哪些并了解其相对浓度大小。
[设计目的]以氯水为例,通过对氯水中存在的三种平衡关系分析,引导学生从氯水中的微观粒子之间的关系进行思考,培养学生的微粒观和平衡观。
[典例分析]
[例1] 下列四种物质在空气长时间放置会变质,在变质过程中,既发生氧化还原反应,又发生非氧化还原反应的是( )
A.食盐 B.漂白粉 C.氯水 D.硫酸亚铁溶液
[思路分析]食盐在空气中不变质;漂白粉在空气中发生如下反应:Ca (ClO)2+CO2+H2O=2HClO+CaCO3↓,;氯水中只是硫酸亚铁溶液中只是Fe2+被氧化为Fe3+。
[答案]B
[设计目的] 掌握含氯化合物的化学性质及反应中元素的价态变化。
[例2] 已知氯水中有如下平衡:Cl2+H2O⇌HCl+HClO。 常温下,在一个体积为50mL 的针筒里吸入40mL氯气后,再吸进10mL 水。写出针筒中可能观察到的现象_______。 若将此针筒长时间放置, 又可能看到何种变化_______;试用平衡观点加以解释_______。
[思路分析] Cl2在H2O 中能溶解, 气体体积缩小,Cl2在H2O 中的溶解度小,Cl2大都是以分子形式存在,溶液呈浅黄绿色。 若此针筒长时间放置,气体体积进一步缩小,气体和溶液均变成无色;原因是氯水存在着平衡
Cl2+H2O⇌HCl +HClO, 由 于HClO 逐 渐 分 解而不断地向右移动,最终Cl2耗尽全部转化为O2,导致气体体积缩小和黄绿色褪去。
[答案]气体体积缩小,溶液呈浅黄绿色。 气体体积继续减小, 气体和溶液均变成无色; 氯水中的平衡Cl2+H2O⇌HCl+HClO,又由于,HClO不断分解,平衡右移,最终Cl2耗尽全部转化成O2。 由总反应式2Cl2+2H2O=4HCl+O2,可知,气体体积减少。
[设计目的]氯水中含有多种微粒,这些微粒在一定条件下会发生变化,通过化学平衡的分析,强化学生的微粒观和平衡观的意识。
[例3 ] 某同学在实验过程中发现存放氯水的试剂瓶中是一种无色澄清的溶液,请你分析可能的原因是①_______②_______③_______④_______。
[学生讨论后讲解] 氯水中因为存在可逆反应Cl2+H2O⇌HCl+HClO, 使其成分复杂且随着条件的改变,平衡发生移动,使成分发生动态的变化。 如放置时间过长氯水最终转变为盐酸。 当外加不同的反应物时,要正确判断是何种成分参与了反应。 氯水中的HClO 能使有色物质被氧化而褪色。 反之,也有许多物质能使氯水褪色,发生的变化可属物理变化(如萃取),也可属化学变化,如歧化法(加碱液)、还原法(如Mg、SO2等)、加成法(加不饱和的有机物)等。
[答案]长时间放置氯水后转化为稀盐酸;溶液中加入了碱溶液;溶液中通入了二氧化硫气体;溶液中通入了乙烯气体。
[设计目的]通过氯水由浅黄绿色变为无色,结合氯水中的微粒变化,可能存在多种可能性,渗透化学的分类观。
四、教学反思
传统的化学教学强调对陈述性知识的记忆,无法激发学生对化学知识的学习兴趣和深层理解,针对化学复习中以“事实文本”的教学弊端,美国课程专家艾里克森认为:教学内容应该围绕核心概念进行选择,以便挖掘和评价更深层次的理解力。 高三复习的重点应该从单纯地对元素及化合物知识的罗列和重复转移到物质的实际运用中,同时在分类应用中提高理解和转化知识的能力;提高高考复习更多的是思维能力的提升,而不是掌握更多的事实材料;学习重心应该从记忆事实转移到理解可迁移的核心观念和对更为根本的知识结构进行深层理解[5]。 作为氯气一节内容,一般是作为高三进行复习时首先要学习的内容。 氯气的复习对于高三化学复习有导向作用,特别是对元素化合物的复习,本节课所采用的方法以及蕴含的理念建构都影响着高三化学复习的质量。 氯气一节的知识很多,直接让学生书写化学方程式,或将有关氯气及其化合物内容印制成导学案让学生填写,这些复习方式太单调,学生的积极性不高。 如何设计有效的问题,引导学生思考并且落实化学的基础知识和基本技能呢? 高中化学课程标准将“形成有关化学学科的基本观念”作为一个显性的目标明确提出,既是对新授课教学的要求,同时对高三化学复习也有指导意义。 本节从知识上分析主要有:氯气的化学性质、氯水的性质。 笔者通过化学基本观念来引领问题的设计,以氯及其化合物的方程式为载体,围绕化学基本观念中的分类观、元素观、平衡观和微粒观展开学习,学生普遍感到有提升,收获很大。
高中元素化合物知识的复习是渗透化学基本观念的最佳阶段。 教师要在复习中善于抓住时机,用基本观念引领学生走出元素化合物的多而杂的无序局面,使学生通过复习元素化合物,不仅对知识掌握得牢固,而且掌握住复习的方法和策略,提升复习的自信心,形成持久的化学基本观念。
[1] 中华人民共和国教育部. 普通高中化学课程标准 (实验)[S].北京:人民教育出版社,2003:7
[2] 宋心琦.化学实验改革建议之四——金属的物理性质和某些化学性质[J].化学教学,2012,(9):3
[3] 曾国琼,吴平.通过元素化合物知识复习培养学生的化学基本观念[J].中学化学教学参考,2011,(9):13
[4] 毕华林,辛本春.促进“观念建构”的化学教学策略[J].中学化学教学参考,2011,(7):3
[5] 莘赞梅.应用系统思考整体把握“微粒观”的建构和发展[J].中学化学教学参考,2012,(7):21
