多胺功能化介孔氧化硅对布洛芬的吸附与pH控释
2013-10-23王海霞刘焕蓉杨恒权
王海霞,刘焕蓉,杨恒权
(山西大学 化学化工学院,山西 太原 030006)
自2001年介孔氧化硅材料首次应用在药物缓释以来,掀起了科学家们对该领域的研究热潮[1].Horcajada发现介孔材料MCM-41的表面功能化基团对布洛芬吸附和缓释有显著影响[2].Tang进一步发现羧基功能化的介孔材料MSU不仅能增大对药物法莫替丁的吸附量,同时也有缓释作用[3].Vallet-Regi使用后嫁接法对MCM-41进行氨基修饰,发现氨基化的MCM-41对布洛芬有明显的缓释作用[4].
布洛芬是一种良好的解热镇痛消炎药,市场需求量较大.但布洛芬在体内溶解度较低,对胃肠道黏膜刺激作用较大.药物控释制剂可实现药物靶向释放,减缓对胃肠道黏膜的刺激作用,提高药效,因此开发布洛芬控释载体具有重要的意义.人体不同部位pH值不同,在发炎、感染、恶性肿瘤等病变部位的pH值也有别于正常部位[6],因此pH响应性介孔氧化硅药物控释系统日益受到研究者们的重视.例如,Yang等通过嫁接法对介孔材料SBA-15的孔道进行了羧基化修饰,实现了对古霉素的pH控释[7].Deng Feng等通过嫁接法,制备了三胺功能化的介孔氧化硅材料,研究表明该材料对布洛芬具有中等吸附量,并且在不同pH下对布洛芬有控释作用[8].然而,嫁接法引入有机基团,通常导致基团分布不均,难以实现对介孔材料的区域选择性修饰,并且有机基团的负载量难以控制,从而影响介孔材料对药物释放的有效调控.
针对上述问题,我们通过采用分步共缩聚法,结合进一步化学修饰,合成了在壳层分布有五胺功能化基团的介孔氧化硅纳米球,通过XRD、N2物理吸附、TEM、IR和元素分析等对材料的结构和组成进行表征,并研究了该材料对布洛芬的吸附性能和pH响应性控制释放行为.
1 实验部分
1.1 试剂
布洛芬(IBU,中国安耐吉试剂公司,分析纯),正硅酸甲酯(TMOS)、四乙烯五胺(TEPA)、磷酸二氢钠、磷酸氢二钠均购于aladdin试剂公司,分析纯,溴乙基三乙氧基硅烷(自制,1H NMR鉴定),十六烷基三甲基溴化铵(CTAC,南京旋光科技有限公司,分析纯),甲醇、正己烷、甲苯购于国药集团化学试剂有限公司(分析纯).
1.2 材料的合成
1.2.1 MCM-41的合成
取十六烷基三甲基氯化铵(3.52g,11mmol)、无水甲醇(505mL)、蒸馏水(400mL)、NaOH(1mol/L,2.2mL),置于1000mL的烧瓶中,25℃下搅拌30min后,滴加 TMOS(1.58g,10.44mmol),继续搅拌11.5h.静置后抽滤,用去离子水洗涤2次,再用乙醇回流萃取3次,每次12h,抽滤,真空干燥24h.惰性气体保护下,在管式炉中220℃煅烧5h.
1.2.2 MCM-41@Br的合成
按照1.2.1取十六烷基三甲基氯化铵、无水甲醇、蒸馏水、NaOH溶液,置于1000mL烧瓶中,25℃下搅拌30min后,滴加 TMOS(1.32g,8.7mmol),继续搅拌1.5h,再加入 TMOS(0.22g,1.45mmol)和溴乙基三乙氧基硅烷(0.078g,0.29mmol)的混合液,继续搅拌10h.按1.2.1的方法进行后处理.
1.2.3 MCM-41@TEPA的合成
称取1.0g MCM-41@Br,置于50mL圆底烧瓶中,120℃下抽真空3h,然后加入0.4g TEPA和15 mL甲苯,在惰性气体保护下回流24h.冷却至室温后,离心,分离沉淀物,用甲苯洗涤2次,再用乙醇洗涤5次,将得到的粉末真空干燥.
1.3 药物吸附
称取 MCM-41、MCM-41@Br和 MCM-41@TEPA各0.6g,分别置于三个50mL圆底烧瓶中,加入浓度为30mg/mL的布洛芬正己烷溶液,密封,室温搅拌24h.静置,离心后分离上清液,稀释后采用紫外分光光度法在263nm处测定溶液中剩余布洛芬的浓度.将剩余的固体沉淀物分别用正己烷快速冲洗,再经室温风干,得到的吸附有布洛芬的材料分别称为IBU/MCM-41,IBU/MCM-41@Br,IBU/MCM-41@TEPA.样品对布洛芬的吸附量由以下公式计算:
吸附量=(c0-c1)V1/m0
其中,c0为溶液中布洛芬的初始浓度,c1为溶液中残余布洛芬的浓度,V1为加入布洛芬溶液的体积,m0为加入介孔材料的质量.
1.4 药物释放
称取0.1g IBU/MCM-41、IBU/MCM-41@Br和IBU/MCM-41@TEPA各两份,分别加入到含有100 mL pH值为2.0和7.4的缓冲液的圆底烧瓶中,在37℃条件下搅拌,定时取样3.0mL,离心,取上清液,用紫外分光光度计扫描其吸收强度.
1.5 表征条件
采用日本理学D/max-rA型粉末衍射仪(XRD)进行物相和结构分析,Cu Kα为射线源,管电压为40 kV,管电流为100mA,扫描角度分辨率为0.02°,扫描速率为5°/min;美国ASAP2020系列全自动比表面及孔隙度分析仪表征材料比表面积,在液氮温度(77K)下,以N2为吸附质,采用BET计算材料比表面积;TEM照片在日本JEM-2000EX 120kV透射电子显微镜下获得,加速电压为120kV;IR分析采用美国Thermo Nicolet NEXUS470型红外吸收光谱仪;元素分析采用德国Vario EL元素分析仪;布洛芬浓度的测定采用北京普析通用仪器TU-1900紫外可见分光光度仪.
2 结果与讨论
2.1 材料合成
在合成介孔材料的过程中采用分步加入硅烷的方法,实现对介孔氧化硅纳米球的区域选择性功能化[9].材料制备过程及结构如图1(P241)所示,CTAC在溶液中组装形成胶束,第一步加入的TMOS,在碱性的合成体系中与胶束相互作用,经水解得到介孔氧化硅内核;第二步加入溴乙基三乙氧基硅烷和TMOS,水解后在介孔氧化硅内核的表面缩聚形成壳层;这样就选择性地将含有溴的有机基团修饰在介孔氧化硅纳米球的外壳层,并且分布均匀,溴有机基团的负载量可以通过加入的含溴硅烷量进行控制.然后,再通过与TEPA发生N-烷基化反应将五胺基团引入到介孔氧化硅纳米球的壳层.
2.2 结构表征
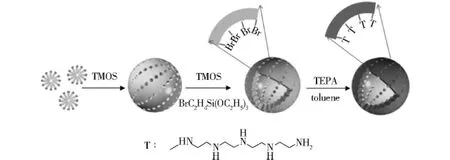
图1 材料合成过程和结构示意图Fig.1 Schematic illustration for the material synthesis process and structure
图2(P241)为 MCM-41@Br和 MCM-41@TEPA的小角XRD谱图.MCM-41@Br在2θ≈2.5°处出现一个明显的介孔材料特征衍射峰,归属于(100)晶面,且峰强度较高,表明材料内部具有一定的有序性介孔结构.引入TEPA长链后,2θ≈2.5°处的衍射峰得以保留,表明引入TEPA长链后介孔结构得以基本保持,但峰强明显降低,这是由于引入有机基团后改变了孔墙和孔道的对比度所引起的.MCM-41@TEPA N2物理吸附/脱附等温曲线如图3所示,其曲线为典型的Ⅳ型曲线,在相对压力为0.4到0.8之间出现了明显的毛细管凝聚现象,表明所合成材料具有丰富的介孔孔道.孔道大小在3.6nm左右,比表面积为443m2/g,孔体积为0.35cm3/g,较大的孔径与高的比表面有利于布洛芬的吸附.

图2 MCM-41@Br和MCM-41@TEPA XRD图谱Fig.2 XRD patterns of MCM-41@Br and MCM-41@TEPA2000

图3 MCM-41@TEPA和IBU/MCM-41@TEPA N2吸附/脱附等温曲线Fig.3 N2adsorption/desorption isotherms of MCM-41@TEPA and IBU/MCM-41@TEPA
图4为MCM-41@TEPA的透射电镜(TEM)照片.从a图中可以看到样品成规则的球形且尺寸大小均一,直径在400nm左右.进一步放大后(图b),可以看到小球上有丰富的孔道,且孔道排列规则,呈放射状,大小均匀,大约在3~4nm,与N2吸附测定结果基本一致.

图4 MCM-41@TEPA透射电镜照片:(a)低倍放大;(b)进一步放大Fig.4 TEM images of MCM-41@TEPA:(a)low magnified;(b)more magnified
2.3 组成分析
MCM-41@TEPA红外图谱见图5(P242).在1080~1200cm-1处出现了比较宽的特征峰,为氧化硅材料Si-O-Si骨架振动吸收峰;2750~3000cm-1处出现的吸收峰为C-H键伸缩振动峰,表明有机基团被成功地引入到材料上;3400~3750cm-1处的宽峰,可以归属于材料表面的硅羟基的特征峰,表明材料有机功能化后仍然保留了丰富的硅羟基,有利于药物吸附.同时对MCM-41@TEPA各元素进行定量分析,C、N含量(质量分数)分别为12.97%、1.1%,C/N为11.63,高于理论值,可能的原因是由于一部分溴乙基被包埋在介孔材料的孔墙中,不易和TEPA充分反应;此外孔道中还有少量的模板剂没有去除干净,也会引起C比例的增高.N的含量高达1.1%,表明TEPA被成功引入到材料上.

图5 MCM-41@TEPA和IBU/MCM-41@TEPA FT-IR谱图Fig.5 FI-IR spectra of MCM-41@TEPA and IBU/MCM-41@TEPA
2.4 吸附性能
在相同条件下,不同样品对布洛芬的吸附量如图6所示.MCM-41@TEPA对布洛芬表现出较高的吸附能力,吸附量可达220mg/g,而 MCM-41、MCM-41@Br的吸附量分别为140mg/g、120mg/g.MCM-41和MCM-41@Br可以吸附布洛芬是由于孔道表面的硅羟基和布洛芬分子的-COOH之间发生氢键作用,而MCM-41@TEPA不仅存在氢键作用,并且其壳层分布的胺链能与布洛芬分子的-COOH之间形成较强的相互作用,因而MCM-41@TEPA可以吸附更多的药物分子.以上结果表明材料表面功能化对药物的装载起着关键作用.MCM-41@TEPA的吸附量略高于文献中三胺功能化的介孔氧化硅球[8],可能是由于所引入的TEPA链为五胺基团所引起的.

图6 不同样品对布洛芬的吸附量Fig.6 Amount of IBU adsorption on different samples
为进一步了解布洛芬在材料上的吸附状态,对IBU/MCM-41@TEPA进行了红外表征,见图5.与未吸附布洛芬的 MCM-41@TEPA 相比,在1730cm-1、1562 cm-1和1455cm-1处出现了新的吸收峰.1730cm-1出现的弱峰,归为布洛芬分子中C=O键伸缩振动峰;1562 cm-1出现的吸收峰归属于-COO-的非对称伸缩振动峰,表明布洛芬分子中羧基上的质子转移到了胺链的-NH-单元上,两者之间发生较强的相互作用;1455 cm-1处出现的峰归属为C-H键弯曲振动峰.以上结果表明布洛芬分子吸附在了介孔材料上.
IBU/MCM-41-TEPA N2吸附/脱附等温曲线见图3.与未吸附布洛芬的MCM-41@TEPA相比,吸附曲线发生明显变化,曲线类型由Ⅳ型变为Ⅱ型,0.4-0.8之间的毛细凝聚现象基本消失,表面积和孔体积显著下降,分别为83m2/g和0.17cm3/g,进一步表明布洛芬分子吸附在了介孔材料的孔道内.
2.5 控制释放
由于人体正常体液pH大约为7.4,胃液pH大约为1.5~2.0,因此我们选用pH=7.4和pH=2.0条件下进行释放实验.图7(P243)是IBU/MCM-41、IBU/MCM-41@Br和IBU/MCM-41@TEPA分别在pH=7.4和pH=2.0条件下的药物释放曲线.图7(a)IBU/MCM-41@TEPA的释放曲线表明,pH较高条件下体系在5min、20min、50min时,释放率分别达到44%、58%、73%;pH 较低条件下,5min、20min、50min时,释放率分别为19%、21%、23%,20min后,释放率基本保持不变,维持在24%左右.IBU/MCM-41@TE-PA在pH=2时表现出与pH=7.4时不同的释放行为,具有pH敏感性,达到了pH控释的目的.
为进一步探索IBU/MCM-41@TEPA表现pH控释的原因,我们对IBU/MCM-41和IBU/MCM-41@Br的释放行为也进行了研究.如图7(b)所示,IBU/MCM-41体系在pH=7.4时,布洛芬释放速率较快,在5min,20min,50min时,释放率分别达到了48%,69%,79%,在2h时基本释放完全;pH=2.0时,释放速度有所减缓,5min,20min,50min的释放率分别为25%,40%,53%,但随着时间的变化,慢慢接近于pH=7.4条件下的释放率,最终和pH=7.4时的释放率相当,均接近于100%.IBU/MCM-41@Br体系在pH=7.4时,布洛芬释放速率也较快,5min,20min,50min,释放率分别达到57%,70%,83%,2h时基本释放完全;pH=2时,5 min,20min,50min的释放率分别为27%,35%,62%,比在pH=7.4时释放速率有所减缓,但最终的释放率与较高pH条件下相当,详见图7(c).
以上结果表明,IBU/MCM-41与IBU/MCM-41@Br的释放规律相类似,均不具有控释作用,而IBU/MCM-41@TEPA 具有pH 控释作用.IBU/MCM-41@TEPA具有控释作用可能的释放机理如图8所示,MCM-41@TEPA壳层分布有多胺长链,在pH=7.4时胺链非质子化,材料的孔道处于开放状态,药物可以自由地通过孔道释放出来,因此其释放率较高;但在pH=2时,由于氨基结合质子,使胺链质子化带有正电荷,同种电荷排斥,胺链伸展与周围胺链相互交叉,使材料的孔道闭合,药物分子被保留于孔道内部不能释放出来,从而实现了控释目的.需要指出的是,由于材料表面会不可避免地吸附部分布洛芬,从而导致酸性条件下的释放率并不为零.IBU/MCM-41与IBU/MCM-41@Br均不具有控释作用,这是由于无论硅-OH还是-CH2CH2Br均不具有pH响应性,且与布洛芬分子之间的相互作用力较弱,因此对药物的释放速率无显著影响.
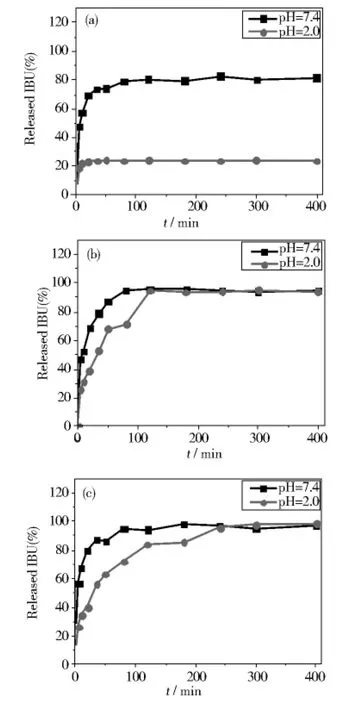
图7 在不同pH下布洛芬的释放曲线:(a)IBU/MCM-41@TEPA,(b)IBU/MCM-41,(c)IBU/MCM-41@BrFig.7 Release curve of IBU at different pHs:(a)IBU/MCM-41@TEPA,(b)IBU/MCM-4and,(c)IBU/MCM-41@Br
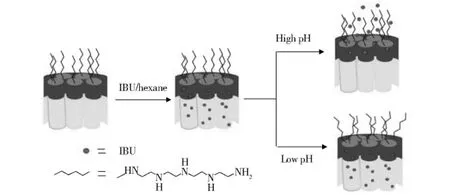
图8 pH响应控制释放原理示意图Fig.8 Schematic illustration for the principle of pH-responsive controlled release
3 结论
本文采用了分步共缩聚法并结合化学修饰,合成得到了仅在壳层分布有pH敏感性基团的介孔氧化硅药物控释材料,该材料具有较大的比表面积和孔容,高度有序的孔道结构.MCM-41@TEPA对布洛芬表现了良好的吸附性能,吸附量高达220mg/g,略高于文献值.在pH=7.4时,布洛芬可以快速释放,释放量可达80%以上;而在pH=2时,仅有24%的布洛芬被释放出来,绝大多数的药物被保留在材料的孔道当中.这种释放率的差异归因于壳层多胺基团在不同pH条件下质子化和脱质子化,从而控制孔口开合,达到pH控释效果.
[1]Vallet-Regi M,Rámila A,Real R P,et al.A New Property of MCM-41:Drug Delivery System[J].Chem Mater,2001,13:308-311.
[2]Horcajada P,Ramila A,Ferey G.Influence of Superficial Organic Modification of MCM-41Matrices on Drug Delivery Rate[J].Solid State Sci,2006,8:1243-1249.
[3]Tang Q L,Xu Y,Wu D,et al.A Study of Carboxylic-modified Mesoporous Silica in Controlled Delivery for Drug Famotidine[J].J Sol Sta Chem,2006,179(5):1513-1520.
[4]Munoz B,Rámila A,Vallet-RegíM,et al.MCM-41Organic Modification as Drug Delivery Rate Regulator[J].Chem Mater,2003,15(2):500-503.
[5]Manzano M,Ain V,Arean Co,et al.Studies on MCM-41Mesoporous Silica for Drug Delivery:Effect of Particle Morphology and Amine Functionalization[J].Chem Eng J,2008,137:30-37.
[6]张海群,张旭.pH 响应性可控释放材料[J].化工新型材料,2011,39(10):11-13.
[7]Yang Q,Wang S C,Fan P W,et al.pH-Responsive Carrier System Based on Carboxylic Acid Modified Mesoporous Silica and Polyelectrolyte for Drug Delivery[J].Chem Mater,2005,17(24):5999-6003.
[8]Gao Q,Xu Y,Deng F,et al.Synthesis,Characterization,and in Vitro pH-Controllable Drug Release from Mesoporous Silica Spheres with Switchable Gates[J].Langmuir,2010,26(22):17133-17138.
[9]Cauda V,Schlossbauer A,Kecht J,et al.Multiple Core-Shell Functionalized Colloidal Mesoporous Silica Nanoparticles[J].J Am Chem Soc,2009,131:11361-11370.
[10]Rosa C,María D M,Ramón M,et al.Toward the Development of Ionically Controlled Nanoscopic Molecular Gates[J].J Am Chem Soc,2004,126(28):8612-8613.
[11]罗忠,蔡开勇,张蓓璐,等.介孔硅纳米储存器在智能药物释放系统的应用[J].化学进展,2011,23(11):2326-2337.
[12]陈雷,张翻,宋丽娟,等.改性介孔分子筛对布洛芬的吸附与控制释放[J].化学工业与工程,2011,28(4):12-15.
[13]赵飞舟.布洛芬在中孔分子筛上的负载与缓释研究[D].大连:大连理工大学,2009.
[14]王旭.新型pH敏感型药物缓释系统[D].郑州:河南大学,2011.
