癌胚抗原在厄洛替尼治疗EGFR突变非小细胞肺癌中的作用
2013-08-24王惠临宁瑞玲周韶璋宋向群曾爱屏赵文华
王惠临,宁瑞玲,周韶璋,宋向群,曾爱屏,赵文华
(广西医科大学附属肿瘤医院化疗二科,南宁 530021)
肺癌作为发病率和病死率最高的恶性肿瘤[1],大部分为非小细胞肺癌(non-small cell lung cancer,NSCLC),其中有相当部分在确诊时已失去手术机会。系统化疗可在一定程度上延长患者生存期,但易产生耐药性,限制了治疗方案的选择。因此,分子靶向治疗,尤其是表皮生长因子受体(EGFR)酪氨酸激酶抑制剂在NSCLC治疗中得到了迅速的发展,其中厄洛替尼对EGFR突变的NSCLC患者有一线治疗的优势。有报道,约63.6%的进展期 NSCLC患者有癌胚抗原(CEA)升高[2]。本文对CEA在厄洛替尼单药治疗EGFR突变的NSCLC患者的疗效中的作用报道如下。
1 资料与方法
1.1 一般资料 选取2009年2月至2011年8月在本院化疗科收治的经病理组织学或细胞学检查证实的EGFR突变的晚期NSCLC 78例,其中男52例,女26例;年龄30~75岁,中位58岁;病理类型:腺癌56例,鳞癌18例,腺鳞癌4例;TNM分期:Ⅲb期12例,Ⅳ期66例。并依CEA的检测结果将患者分为CEA阳性组和CEA阴性组。纳入标准:(1)经病理或细胞学证实的无法手术切除且未经化疗的Ⅲb~Ⅳ期NSCLC患者;(2)不能耐受或拒绝接受化疗者;(3)全部患者KPS评分大于或等于60分,预计生存期超过3个月;(4)至少有1个可测量的病灶;(5)无心、肝、肾等严重脏器功能障碍;(6)患者自愿接受厄洛替尼治疗,并能够接受随访。
1.2 方法
1.2.1 EGFR的检测 对肿瘤组织行病理切片,用QIAGEN公司的DNeasy Blood&Tissue Kit(商品序列号:69504)提取DNA,紫外分光光度计测定DNA纯度及浓度。采用扩增耐突变系统(ARMS.PCR)法扩增EGFR基因18、19、20及21外显子。具体操作方法参照人类EGFR基因29种突变检测试剂盒(荧光PCR法)说明书进行,由厦门艾德生物医药科技有限公司提供,反应循环参数:95℃5min;95℃25s,64℃20s,72℃20s,循环15次;93℃25s,60℃35s,72℃20s,循环31次。
1.2.2 CEA的检测 治疗前采集患者肘部静脉血3mL,3 000 r/min离心10min,取上层血清,应用放射免疫检测试剂盒(罗氏公司),放免法检测CEA蛋白(CEA>8ng/mL为阳性)。
1.2.3 治疗与随访 厄洛替尼由罗氏公司生产,剂量每次150mg,口服,1次/天,直到肿瘤进展或因死亡而终止治疗为止,同时终止随访。
1.2.4 疗效评价 治疗前l周完成各项基线检查。近期疗效的评价按照实体瘤的疗效评价(RECIST)标准[3],分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。以CR+PR计算有效率;以CR+PR+SD计算疾病控制率。
1.2.5 不良反应评价 按照美国国家癌症研究所(NCI)常见毒性分级标准(第3版)评价不良反应[4]。
1.3 统计学处理 采用SPSS13.0软件进行统计学处理,计数资料采用率表示,两样本率的比较采用χ2检验,两组患者的无进展生存时间的比较采用Log-rank检验,检验水准α=0.05,以P<0.05为差异有统计学意义。
2 结 果
2.1 EGFR基因突变和CEA的检测情况 其中外显子18突变8例,占10.26%;外显子19突变29例,占37.18%;外显子20突变10例,占12.82%;外显子21突变31例,占39.74%。78例患者中,有48例(61.54%)患者CEA阳性,其中男33例,女15例;30例(38.46%)患者CEA阴性,其中男19例,女11例。两组患者性别构成差异无统计学意义(χ2=0.243 7,P=0.620 8)。
2.2 近期疗效 所有患者均可以得到评价疗效,见表1。CEA 阳性组的患者:CR 6例(12.5%),PR 35例(72.92%),SD 5例(10.41%),PD 2例(4.17%),有效率85.42%,疾病控制率95.83%;CEA阴性组的患者:CR 3例(10%),PR 16例(53.33%),SD 5 例 (16.67%),PD 6 例 (20%),有 效 率63.33%,疾病控制率80.00%。两组患者的有效率(χ2=4.495,P=0.033)和疾病控制率(χ2=5.028 2,P=0.024 8)比较差异有统计学意义。
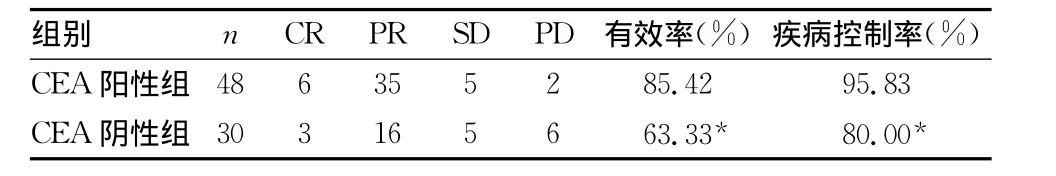
表1 两组患者近期疗效的比较
2.3 生存分析 所有患者均可得到随访。CEA阳性组的患者:CEA阳性组有1例于第19个月死亡,1例于第13个月死亡,1例于第16个月失访;CEA阴性组有2例分别于第7、13个月死亡,1例于第9个月失访。CEA阳性组的平均无进展生存时间为(14.97±0.65)个月,中位无进展生存时间为15个月[95%CI:(12.80,17.19)];CEA 阴性组的平均无进展生存时间则为(12.01±0.67)个月,中位无进展生存时间为12个月[95%CI:(10.61,13.39)]。两组的生存曲线比较差异有统计学意义(χ2=9.826,P=0.002),结合中位无进展生存时间和生存曲线(图1),在厄洛替尼单药治疗EGFR突变的晚期NSCLC患者中,血清CEA呈阳性的患者的无进展生存时间比CEA阴性患者的长。
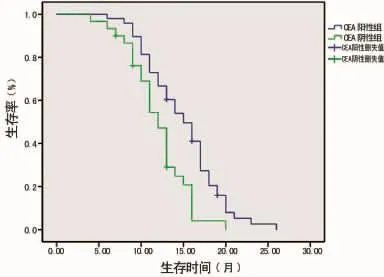
图1 两组患者无进展生存时间的比较
2.4 不良反应 78例患者中,有66例出现1~2度痤疮样皮疹,无需特殊处理便可自行消退。其他的尚有3例出现腹泻,无一例出现间质性肺炎。
3 讨 论
EGFR信号通路在NSCLC的发生和发展中起重要作用,激活后可促使肿瘤细胞增生、分化、转移、血管生成及凋亡抑制。大约80%的NSCLC存在EGFR的表达、过度表达和突变,因此,EGFR是治疗NSCLC的理想靶点[5]。EGFR酪氨酸激酶抑制剂是一类作用于细胞内EGFR酪氨酸激酶区的小分子药物,能抑制酪氨酸激酶磷酸化和下游信号转导,从而发挥抗肿瘤效应[6]。因此,EGFR突变阳性是EGFR酪氨酸激酶抑制剂一线治疗NSCLC的重要指标,其中厄洛替尼作为一线药物用于EGFR突变的NSCLC患者,其有效率和疾病控制率分别可达73.7%和89.9%[7]。
CEA在NSCLC患者中的水平显著高于肺部良性疾病者和健康者[8],在相当部分的肺癌患者中水平升高,且与肺癌的广泛程度相关,是评估其预后的独立因素[9]。本研究结果表明,经过厄洛替尼单药治疗后,两组的有效率分别可达63.33%和85.42%,疾病控制率则为80%和95.83%,两者差异均有统计学意义,说明在EGFR突变阳性的晚期NSCLC患者中,血清CEA升高的患者对厄洛替尼的治疗效果较好。而在远期疗效方面,血清CEA呈阳性的患者无进展生存时间也比CEA阴性患者的长。李醒亚等[10]也认为,吉非替尼或厄洛替尼治疗CEA水平高的患者的疗效更好。因此,如何有效地动态监测血清CEA水平来反映疗效及判断预后,将是今后研究的重点。
[1] Jemal A,Siegel R,Ward E,et al.Cancer statistics,2009[J].CA Cancer J Clin,2009,59(4):225-249.
[2] 王海燕,朱正学,肖燕,等.非小细胞肺癌血清中CAl25、CEA的浓度及意义[J].中国肺癌杂志,2008,2(11):97-100.
[3] Duffaud F,Therasse P.New guidelines to evaluate the response to treatment in solid tumors[J].Bull Cancer,2000,87(12):881-886.
[4] Trotti A,Colevas AD,Setser A,et al.CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J].Semin Badiat Oncol,2003,13(3):176-181.
[5] 周彩存.晚期非小细胞肺癌靶向治疗疗效预测标志物临床研究进展[J].肿瘤研究与临床,2010,22(9):581-584.
[6] 洪群英,白春学.晚期非小细胞肺癌表皮生长因子受体-酪酸激酶抑制剂靶向治疗进展[J].世界临床药物,2012,33(4):197-201.
[7] Maemondo M,Inoue A,Kobayashi K,et al.Gefitinib or chemotherapy for non-small cell lung cancer with mutated EGFR[J].N Engl J Med,2010,362(25):2380-2388.
[8] 罗疏薇,欧春萍,张莉萍,等.应用ROC曲线评价CEA、CYFRA21-1、SCC对非小细胞肺癌的诊断价值[J].重庆医学,2011,40(3):250-255.
[9] Tomita M,Matsuzaki Y,Edagawa M,et al.Prognostic significance of preoperative serum carcinoembryonic antigen level in lung adenacarcinoma but not squamous cell carcinoma[J].Ann Thorac Cardiovasc Surg,2004,10(2):76-80.
[10]李醒亚,成媛,刘杰,等.非小细胞肺癌患者血清CEA水平与EGFR-TKI疗效的关系[J].中国癌症杂志,2011,2l(3):193-196.
