肾血管低温灌注下后腹腔镜肾部分切除术处理2例复杂左侧肾肿瘤
2013-07-26马鑫郑涛史涛坪刘凤永宋鹏徐龙河赵艳军董隽祖强刘新张旭
马鑫 郑涛 史涛坪 刘凤永 宋鹏 徐龙河 赵艳军 董隽 祖强 刘新 张旭
1 中国人民解放军总医院泌尿外科100853 北京
2中国人民解放军总医院介入放射科
3中国人民解放军总医院麻醉科
随着泌尿外科手术技术的发展,保留肾单位手术越来越受到泌尿外科医生的重视。特别当对侧肾功不全,孤立肾或双肾肿瘤时,尤显重要。然而,肾缺血对肾功能的影响一直是一个难题。由于肾脏质脆且血流丰富的解剖生理特点,复杂肿瘤行部分切除术时,术中止血及对切除范围的辨认,会直接影响术后并发症及患者预 后[1,2]。2013年3~4月 我院采用肾血管低温灌注下后腹腔镜肾部分切除术处理复杂左侧肾肿瘤2例,效果良好,报告如下。
1 病例资料
例1 女,49岁。因“体检发现双肾占位4个月,后腹腔镜右肾部分切除术后”入院。患者2012年11月于当地医院体检发现双肾占位,当月就诊于我院,第一次入院后术前腹
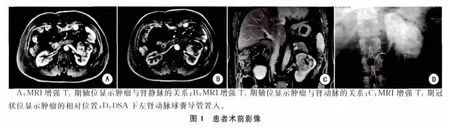
部CT 检查提示:双侧肾实质内可见右侧4.7 cm×4.0cm、左侧6.0cm×5.2 cm 类圆形低密度影,左侧较大。增强动脉期呈不均匀明显强化,静脉期强化幅度降低。病灶边界清楚。两肾盂肾盏及上段输尿管无扩张,左肾周筋膜稍增厚。肾静脉及下腔静脉未见充盈缺损。两肾上腺未见异常。肾脏MRI平扫和动态增强扫描提示:双肾上部见约40~67 mm 等和稍长T1、短和稍长T2异常信号肿块,似见假包膜,病变局部突向包膜外生长,反相位图像大病变局部信号轻度减低,DWI病变呈异常晕环状稍高和稍低信号;皮质期病变轻到中度不均匀强化,髓质期持续强化,延迟期强化程度减低;病变内部分区域无强化。双侧肾盂肾盏及输尿管未见异常狭窄或扩张,肾静脉及下腔静脉未见充盈缺损(图1A~C)。行后腹腔镜右肾部分切除术,术后病理诊断为:右肾上极嗜酸细胞瘤,肿瘤大小4.5cm×4.0cm×4.0 cm。肿瘤侵犯未侵透肾被膜,肾脏切缘未见肿瘤。2013年3月再次入院,初步诊断:左肾肿瘤,右肾肿瘤部分切除术后。
例2 女,49岁。于2013年3月在地医院行泌尿系超声检查提示:左肾上极占位。2013年4月18日入我院,肾脏CTA 检查提示:左肾上极可见3.4cm×4.5cm 大小肿物,肿物突出肾脏轮廓约2.7cm,肿物紧邻肾窦;左肾动脉以远可见副肾动脉,经肾门入左肾下极实质。初步诊断:左肾肿瘤。
1.2 手术方法
例1 完善术前检查后,于2013年3月在全麻下行左肾动脉球囊导管置入术+肾血管低温灌注下后腹腔镜左肾部分切除术。患者首先在介入科放射手术室取平卧位,常规腹股沟区消毒、铺巾,以1%利多卡因10ml局部麻醉后,采用改良Seldinger's技术穿刺右侧股动脉、导入F4动脉鞘,然后插入F4动脉导管行腹主动脉、选择性左肾动脉造影。血管造影(DSA)所见:①腹主动脉造影示主干及分支未见明显异常。②左肾动脉造影示主干走行自然,分支迂曲紊乱,供血区见巨大团状肿瘤染色,未见静脉早期显影,肾动脉主干于腹主动脉起始部上方1cm 处可见一直径2 mm 副肾动脉(图1D)。然后更换F6动脉鞘,插入F5.5(1.83 mm)Fogarty球囊导管(EMB,Edwards Lifesciences,12TLW805F35)至左肾动脉近端,距腹主动脉开口处约1.0~1.5cm。Fogarty球囊导管为双腔导管,在末端有一个乳胶球囊,一个腔用于球囊充气,另一个腔可用来输注液体,采血或作为导丝通道;此球囊充盈前直径F6.0,充盈后直径11mm,最大承受拉力2.0LBS。术后体外局部固定导管后送往腔镜一体化手术室。
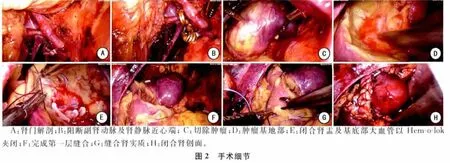
常规行后腹腔镜肾部分切除术[3],游离显露出左肾上部肿瘤,直径约6cm。于肾脂肪囊外肾后方腰大肌前方游离肾门处,游离出左肾动脉(图2A),发现左肾动脉上部约1cm 处有一直径2 mm 副肾动脉,发自腹主动脉。于肾动脉腹侧分离出肾静脉及生殖静脉,腰静脉汇入肾静脉处以两个Hem-o-lok夹闭并离断。
在阻断肾血流前10 分钟先静脉注入肌苷2.0g,左肾动脉球囊导管球囊中注入生理盐水0.9 ml,使其阻断肾动脉血流,用两个无损伤Bulldog 分别钳夹,阻断左肾副肾动脉和左肾静脉近心端,Hem-o-lok夹闭生殖静脉远心端,纵行切开生殖静脉近心端侧壁,作为灌注液流出道(图2B)。自球囊导管加压灌注入4℃离体肾保存用枸橼酸盐嘌呤溶液。
用剪刀沿左肾肿瘤边缘0.5 cm 切开肾实质,将肿瘤完整切除(图2C)。肿瘤基底部大血管以Hem-o-lok夹闭,2-0单荞线关闭肾盂及肾髓质层,1-0薇荞可吸收线连续缝合肾脏缺损全层,并用Hem-o-lok固定(图2D~H)。抽出动脉导管水囊以开放肾动脉,去除无损伤Bulldog钳开放副肾动 脉,用Hem-o-lok夹闭生殖静脉近心端,去除无损伤Bulldog钳开放肾静脉。给予速尿10mg快速静脉输入。观察创面无明显出血。
例2 以相同灌注方法实施类似手术,血管处理、灌注液和肾脏缝合方式则略有不同。该患者左肾动脉下方约0.5cm 处有一起源于腹主动脉的直径约2 mm的副肾动脉,供应左肾下极。肿瘤位于左肾上部,由肾动脉供血,故仅在左肾动脉球囊导管球囊中注入生理盐水,阻断肾动脉血流,副肾动脉则不阻断。患者肾动脉加压灌注4℃乳酸林格氏液。左侧肾静脉、腰静脉和生殖静脉不做处理。缝合肾脏时采用了单向倒刺可吸收线双层连续缝合左肾创面,并用Hem-o-lok固定。
2 结果
2例手术均获成功。例1术中出血约400 ml,未输血,使用灌注液2 000ml,肾动脉阻断62 min,手术历时约4h。例2术中出血约100 ml,未输血,使用灌注液1 400 ml,肾动脉阻断26 min,手术历时约3h。
术后常规抗感染止血及输液支持治疗,2例患者均无严重并发症发生,术后无肉眼血尿。例1术后绝对卧床5天,3天拔除引流管,4 天正常饮食,7 天出院。术后肌酐升高,最高达308.3 μmol/L,给予利尿等处理,于出院时恢复至195.2μmol/L。例2术后绝对卧床3天,4天正常饮食,5天拔除引流管,8天出院。患者术后肌酐最高61.8μmol/L,较术前无明显升高。病理结果均为:(左)肾透明细胞癌,未侵及肾被膜。
3 讨论
肾部分切适应证有三类:绝对适应证、相对适应证和可选择适应证。绝对适应证:包括肾癌发生于解剖性或功能性的孤立肾,根治性肾切除将会导致肾功能不全或尿毒症的患者,如先天性孤立肾、对侧肾功能不全或无功能者以及双侧肾癌[4,5]。由于肾血流丰富,为减少术中出血,保持术野清晰,避免肾组织肿胀变脆导致缝合困难,术中需暂时阻断肾血流。而肾脏对热缺血非常敏感,时间>25min将导致手术侧广泛不可逆肾功能损害[1,6,7]。为保护肾脏功能免受缺血-再灌注损伤,需采取低温及药物保护。一般认为20℃低温下可安全阻断肾动脉达3h[8]。低温保护是用来防止肾脏缺血性损伤最常用的一种技术。降低肾脏温度可以减少皮质细胞消耗能量的代谢活动,减少氧和ATP的消耗。低温的副作用则是使得细胞钠钾离子泵失活,最终导致水钠潴留,但温度在4℃以上时该过程是完全可逆的[9]。
目前报道的腹腔镜肾脏低温技术主要有三种:局部冰屑低温法,逆行输尿管插管灌注低温法和肾动脉灌注低温法。Marberger和Eisenberger[10]首 先 报道了肾动脉灌注冷却降温的速度为表面冷却的3倍。他们报道了63例因为巨大结石行低温肾切开取石术的患者资料。使用导管经皮穿刺到达肾动脉,用止血带或是动脉内带气囊的双腔导管阻断肾动脉。用4℃的平衡液或5%右旋糖苷灌注肾脏,同时测量肛温。对照组39例进行同种操作的肾脏用冰水混合物表面降温。动脉导管组的平均冷缺血时间为61.3min,冰水混合物组为59.8min。表面降温组肾脏术后肌酐清除率显著低于动脉灌注组。Janetschek等[11]报道了他们的腹腔镜下肾动脉灌注技术。肿瘤的平均大小为2.7cm(1.5~4cm)。通过阻断肾动脉同时配合以50ml/min速度灌注1000ml4℃的平衡液达到冷却效果。灌注后迅速进行手术。灌注开始后肾实质温度降到25℃的平均时间为10 min。平均手术时间为185min(135~220min)。放置血管导管平均花费16 min(10~20min)。平均总缺血时间40min(27~101min),灌注液平均用量1 580 ml(1 150~2 800 ml),体温平均降低0.64℃(0.5~1.1℃)。开始有2例患者因为肾动脉未被气囊完全阻断导致大量出血。有1例患者因为术后出血而二次腔镜手术。
我们对以上技术进行了改进,第1例术中以无损伤Bulldog钳夹闭肾静脉近心端开放生殖静脉作为灌注液输出道,避免了灌注液进入体循环而导致电解质紊乱及影响患者体温。第2例在第1例的基础上又有改进,仅阻断肾动脉,肾静脉、腰静脉和生殖静脉不作处理。以4℃乳酸林格氏液肾动脉灌注,灌注液直接通过静脉回流,减少了血管损伤和术中出血,缩短了手术时间。但可能会对患者的体温造成一定影响。虽然这一技术有潜在损伤腹主动脉和肾动脉的危险,主要是因为血管内膜的撕裂造成。术者在尝试第3例手术时,由于球囊导管移位,术中未能有效阻断肾动脉血流,故改行标准后腹腔镜肾部分切除术。肾血管低温灌注下后腹腔镜肾部分切除术,适用于有绝对适应证的复杂肾肿瘤。这一技术在保护肾功能的同时提供了清晰的手术视野,这2个病例初步证实了这一术式的安全性和可行性。
[1]Porpiglia F,Renard J,Billia M,et al.Is renal warm ischemia over 30 minutes during laparoscopic partial nephrectomy possible?One-year results of a prospective study.Eur Urol,2007,52(4):1170-1178.
[2]Janetschek G.Laparoscopic partial nephrectomy for RCC:how can we avoid ischemic damage of the renal parenchyma? Eur Urol,2007,52(5):1303-1305.
[3]Zhang X,Li HZ,Ma X,et al.Retroperitoneal laparoscopic nephron-sparing surgery for renal tumors:report of 32cases.Urology,2005,65(6):1080-1084.
[4]Touijer K,Jacqmin D,Kavoussi LR,et al.The expanding role of partial nephrectomy:a critical analysis of indications,results,and complications.Eur Urol,2010,57(2):214-222.
[5]Russo P.Open partial nephrectomy:an essential operation with an expanding role.Curr Opin Urol,2007,17(5):309-315.
[6]Baldwin DD,Maynes LJ,Berger KA,et al.Laparoscopic warm renal ischemia in the solitary porcine kidney model.Urology,2004,64(3):592-597.
[7]Orvieto MA,Tolhurst SR,Chu ang MS,et al.Defining maximal renal tolerance to warm ischemia in porcine laparoscopic and open surgery model.Urology,2005,66(5):1111-1115.
[8]Abukora F,Albqami N,Nambirajan T,et al.Long-term functional outcome of renal units after laparoscopic nephron-sparing surgery under cold ischemia.J Endourol,2006,20(10):790-793.
[9]Micali S,Silver RI,Kaufman HS,et al.Measurement of urinary N-acetyl-beta-D-glucosaminidase to assess renal ischemia during laparoscopic operations.Surg Endosc,1999,13(5):503-506.
[10]Marberger M,Eisenberger F.Regional hypothermia of the kidney:surface or transarterial perfusion cooling? A functional study.J Urol,1980,124(2):179-183.
[11]Janetschek G,Abdelmaksoud A,Bagheri F,et al.Laparoscopic partial nephrectomy in cold ischemia:renal artery perfusion.J Urol,2004,171(1):68-71.
