电池级超微细磷酸铁的制备
2013-04-21彭爱国贺周初余长艳庄新娟汪永斌
彭爱国 ,贺周初,余长艳,庄新娟,闻 杰,汪永斌
(湖南化工研究院,湖南 长沙 410014)
0 引 言
磷酸铁(FePO4)是一种米白色或灰白色粉末,最初的研究主要在农业、陶瓷玻璃、钢铁及表面钝化等领域,后来发现磷酸铁具有独特的催化特性、离子交换能力和电化学性能,还可作为新型电池正极材料,是制备锂离子电池正极材料磷酸亚铁锂的优良原料.由于磷酸铁具有丰富的骨架结构,同时在催化和锂电池电极材料等领域有着重要的应用,已逐渐引起了人们的关注[1].近年来有关其合成方法的探索引起了人们的极大兴趣.以往的合成路线往往需要苛刻的条件,对设备材质要求很高,而且生产成本也较高,寻求经济、温和、操作简便的制备方法具有重要意义.
磷酸铁的合成方法有很多种,最传统的是用三氯化铁或硝酸铁溶液与磷酸反应,在高温下使氯化氢或硝酸分解挥发,或用氨水中和过量酸得到磷酸铁[2-3].另一种方法是硫酸亚铁用磷酸酸化后与氯酸钠或过氧化氢反应,生成磷酸二氢铁,再用氢氧化钠或氨水调节pH值为2左右,生成磷酸铁[4-5].此外还有用磷酸盐与硫酸铁直接反应,在pH值小于2的条件下生成磷酸铁[6].本文以硫酸亚铁和磷酸铵为原料,采用先沉淀再转化的方法制备出了磷酸铁,该方法反应条件温和,对设备要求不高,生产成本低[7].
1 实验材料和方法
1.1 实验试剂和仪器
试剂:磷酸(H3PO4),工业品,质量分数85%(长沙明瑞化工有限公司);过氧化氢(H2O2),工业品,质量分数27%(长沙明瑞化工有限公司);七水硫酸亚铁,工业品,质量分数90%(长沙锐启化工产品有限公司);磷酸铵,工业品,质量分数98%(天津金汇太亚化学试剂有限公司).
仪器:JJ-1精密增力电动搅拌器(常州国华电器有限公司);SHB-Ⅲ型循环水式多用真空泵(郑州长城科工贸有限公司);DHG-9245A型电热恒温鼓风干燥箱(上海一恒科技有限公司);MASTERSIZER 3000粒度分析仪(Malven);XRD-6100 X-射线衍射仪(岛津);HK-9600型电感耦合等离子体发射光谱仪(北京华科天成科技有限公司).
1.2 反应原理和化学反应方程式
在酸性条件下,先将FeSO4用H2O2氧化成Fe2(SO4)3,然后用磷酸铵溶液沉淀硫酸铁生成磷酸铁,同时有少量硫酸铁水解生成氢氧化铁,最后用磷酸将水解产生的氢氧化铁转化成磷酸铁.
反应方程式如下:
2FeSO4+ H2SO4+ H2O2= Fe2(SO4)3+ 2H2O
Fe2(SO4)3+2(NH4)3PO4= 2FePO4+ 3(NH4)2SO4
Fe2(SO4)3+ 6H2O = 2Fe(OH)3+ 3H2SO4
Fe(OH)3+H3PO4=FePO4+ 3H2O
1.3 实验方法
称取280 g七水硫酸亚铁,加水溶解配制成350 mL溶液,加25 g浓硫酸酸化,然后用过氧化氢将亚铁氧化成三价铁盐溶液.在搅拌条件下往上述铁盐溶液中按化学计量比滴加磷酸铵溶液,生成黄色沉淀,过滤水洗得到黄色碱式磷酸铁.将上述黄色碱式磷酸铁用水调浆、搅拌,加入磷酸,使Fe(OH)3转化成FePO4.待物料颜色变白后,过滤、洗涤、烘干、粉碎得平均粒径小于3.0 μm的电池级超微细磷酸铁产品.反应过程中产生的硫酸铵溶液浓缩后可以生产农用硫酸铵,转化母液可以返回循环使用,生产过程中无“三废”产生.工艺流程如图1所示.
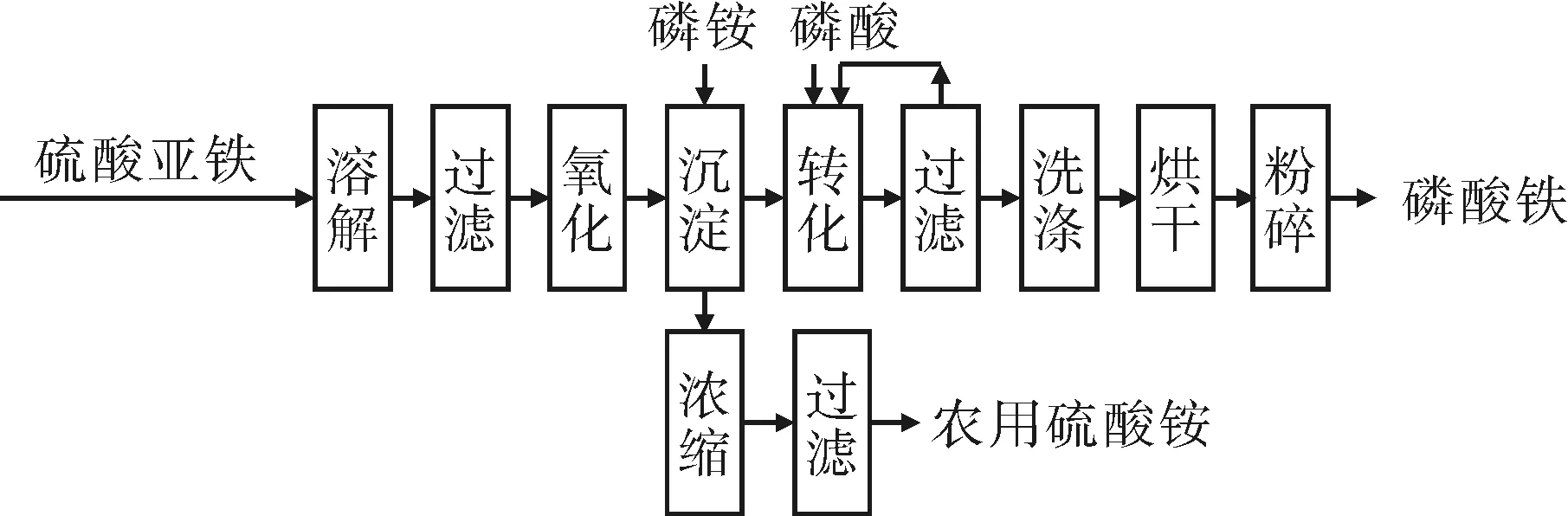
图1 磷酸铁生产工艺流程图Fig.1 Flow process chart for preparation of iron phosphates
2 结果与分析
2.1 氧化
为了不带入新的杂质,氧化剂选用H2O2.因为FeSO4的氧化过程需要消耗酸,所以先按n(H2SO4)∶n(FeSO4)=1∶2加入浓硫酸,然后加入H2O2氧化.H2O2在空气中特别是在高温条件下易分解失去氧化性,故氧化反应尽量控制较低的反应温度.氧化反应主要考察H2O2加料量和加料速度对氧化效果的影响.
2.1.1 H2O2加量的影响 在反应温度为40 ℃、氧化反应时间为2 h、加料时间为50 min条件下,考察H2O2加量对Fe2+氧化效果的影响,结果见图2.
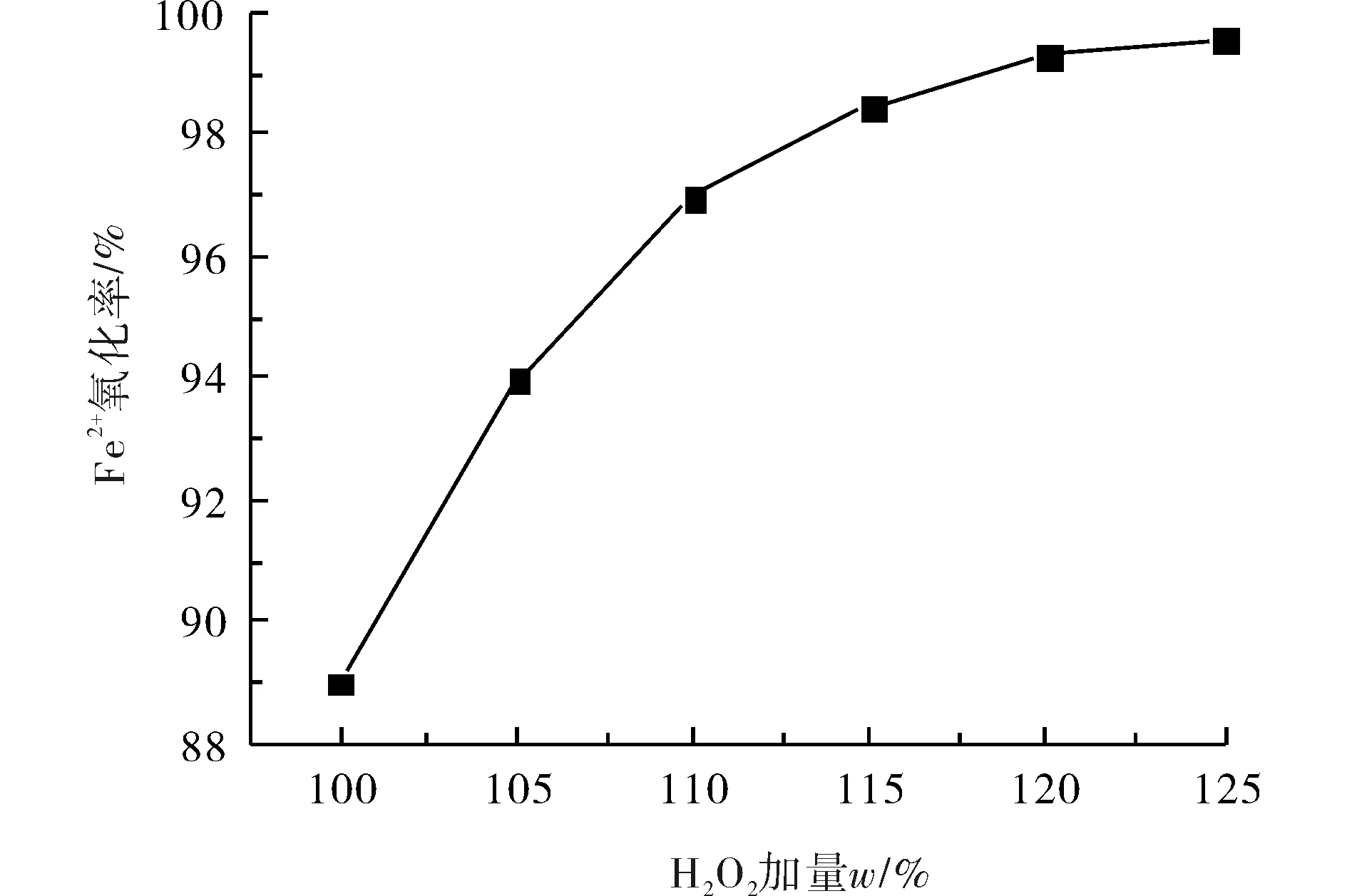
图2 H2O2加量对氧化反应的影响Fig.2 Effect of H2O2 feeding quantity on oxidation reaction
由图2可以看出:H2O2的加量对Fe2+的氧化率影响非常明显,H2O2易分解,反应过程中须保证一定的过量系数,随着H2O2过量系数的提高,Fe2+的氧化率也急剧升高,当H2O2加量达到理论量的120%时氧化率超过99.3%.因此H2O2加量按理论量的120%加入为宜.
2.1.2 H2O2加料时间的影响 在反应温度为40 ℃、氧化反应时间为2 h、H2O2加料量为理论量的120%条件下,考察H2O2加料时间对Fe2+氧化效果的影响,结果见图3.

图3 H2O2加料时间对氧化反应的影响Fig.3 Effect of H2O2 feeding time on oxidation reaction
氧化反应是一个放热反应,若H2O2加料太快则温度急剧升高,造成大量的H2O2分解.试验结果表明:随着加料时间的延长,Fe2+氧化得越来越完全,加料时间达到50 min时,Fe2+的氧化率接近100%,溶液中Fe2+含量很少,再继续延长时间已无必要,因此H2O2加料时间保持在50 min为佳.
2.2 沉淀
与在过量磷酸存在的条件下将硫酸铁与磷酸铵反应再中和生成磷酸铁相比,在接近中性的环境下先生成碱式磷酸铁,然后再用磷酸转化,可以节省大量磷酸,降低生产成本.采用先沉淀再转化的工艺,更容易得到超微细的磷酸铁产品.通过调节沉淀反应的条件可以控制产品粒径,其中磷酸铵加料时间和沉淀反应温度是影响粒径的两个重要因素.
2.2.2 磷酸铵加料时间的影响 在磷酸铵加料量为理论量的100%、沉淀反应温度为40 ℃条件下,考察磷酸铵加料时间对产品粒径的影响,结果见图4.

图4 磷酸铵加料时间对产品粒径的影响Fig.4 Effect of (NH4)3PO4 feeding time on particle size
磷酸铵加料时间是影响产品粒径的一个重要因素,加料速度快,反应体系中瞬时产生大量的一次成核的粒子,晶体成核的速率大于生长速率,粒子来不及生长,易得到粒径细小的晶体;加料速度慢,则开始产生的一次成核粒子少,后面新生成的微粒易于吸附在其表面,并逐渐长大,形成二次成核或多次成核的晶体.要得到粒径小于3.0 μm的磷酸铁产品,加料速度控制在40 min左右为宜.
2.2.3 沉淀反应温度的影响 在磷酸铵加量为理论量的100%、加料时间为40 min条件下,考察沉淀反应温度对产品粒径的影响,结果见图5.

图5 沉淀反应温度对产品粒径的影响Fig.5 Effect of precipitation reaction temperature on particle size
由图5可以看出,随着反应温度升高,产品的粒径逐渐增大,在沉淀反应温度不超过40 ℃的条件下可以得到粒径小于3.0 μm的超微细磷酸铁产品.
2.3 转化
转化反应是将沉淀反应得到的碱式磷酸铁结晶与磷酸溶液反应,使之转化成超微细磷酸铁产品.转化反应是否反应完全,直接影响到产品的外观及纯度,转化反应重点考察了反应温度和磷酸浓度两因素对产品纯度的影响.
2.3.1 转化反应温度的影响 在磷酸浓度为0.5 mol/L、转化反应时间为2 h的条件下,考察反应温度对产品纯度的影响,结果见表1.
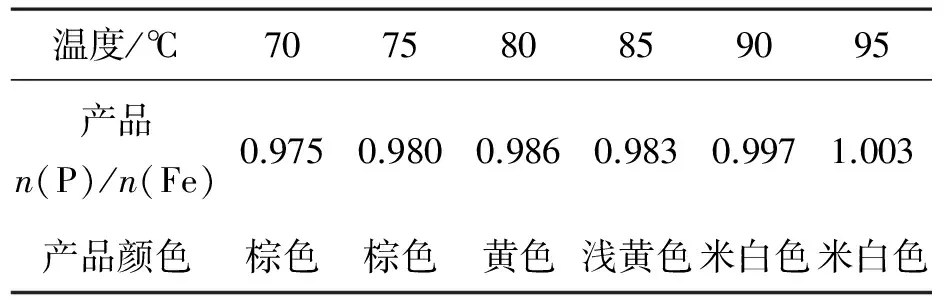
表1 转化反应温度对产品纯度的影响Table 1 Effect of conversion reaction temperature on purity
表1表明,当转化反应温度较低时,产品颜色呈棕黄色,表明氢氧化铁未完全转化成磷酸铁.随着转化反应温度的提高,产品的颜色越来越浅,磷铁比(物质的量的比,下同)也越来越接近1,这说明产品磷酸铁的纯度不断提高.当反应温度为90 ℃时,氢氧化铁已完全转化,磷酸铁产品的磷铁比达到0.997,颜色为米白色,因此转化反应温度以90 ℃为宜.
2.3.2 转化反应磷酸浓度的影响 在转化反应温度为90 ℃、转化反应时间为2 h的条件下,考察反应体系的磷酸浓度对产品纯度的影响,结果见表2.

表2 磷酸浓度对产品纯度的影响Table 2 Effect of H3PO4 concentration on purity
表2表明,在较低的酸度下碱式磷酸铁中的氢氧化铁未能得到有效转化,导致产品颜色较深,磷铁比也较低.随着磷酸浓度的提高,产品的颜色由棕黄色逐渐变为米白色,磷铁比也越来越接近1,表明产品磷酸铁的纯度在不断提高,当磷酸浓度为0.5 mol/L时,氢氧化铁已完全转化,磷酸铁产品的磷铁比达到0.998,颜色为米白色.当磷酸浓度提高到0.6 mol/L时,磷酸铁产品的磷铁比达到1.018,说明有酸式磷酸铁生成,因此磷酸浓度不宜过高,以0.5 mol/L左右为宜.
2.4 磷酸铁产品分析
产品元素分析用HK-9600型电感耦合等离子体发射光谱仪检测,粒度分析用MASTERSIZER 3000粒度分析仪检测,物相分析采用XRD-6100 X-射线衍射仪检测.表3为产品经电感耦合等离子体发射光谱仪分析的数据,元素分析结果表明产品中金属杂质的质量分数均小于0.005%,硫的质量分数小于0.022%,且磷铁比为1.01,说明产品磷酸铁纯度较高.图6为产品的粒度分布曲线图,d50为2.67 μm,d10为1.08 μm,d90为5.61 μm,测试结果表明粒度分布窄,产品粒径大小均匀.对未经高温处理和经高温处理后的产品进行X-射线衍射(X-ray diffraction,以下简称:XRD)检测,未经高温处理的产品无任何特征峰,表明液相直接合成的是一种无定形微细颗粒;而经过600 ℃高温煅烧后的产品,则出现了明显的特征峰,且与JCPDS卡上PDF#50-1635 FePO4标准图谱一致,表明经过高温处理后的产品结晶度高,晶型完美,图7为600 ℃处理后产品的XRD图.

表3 电池级磷酸铁产品质量Table 3 Product quality of battery-grade ultrafine iron phosphates
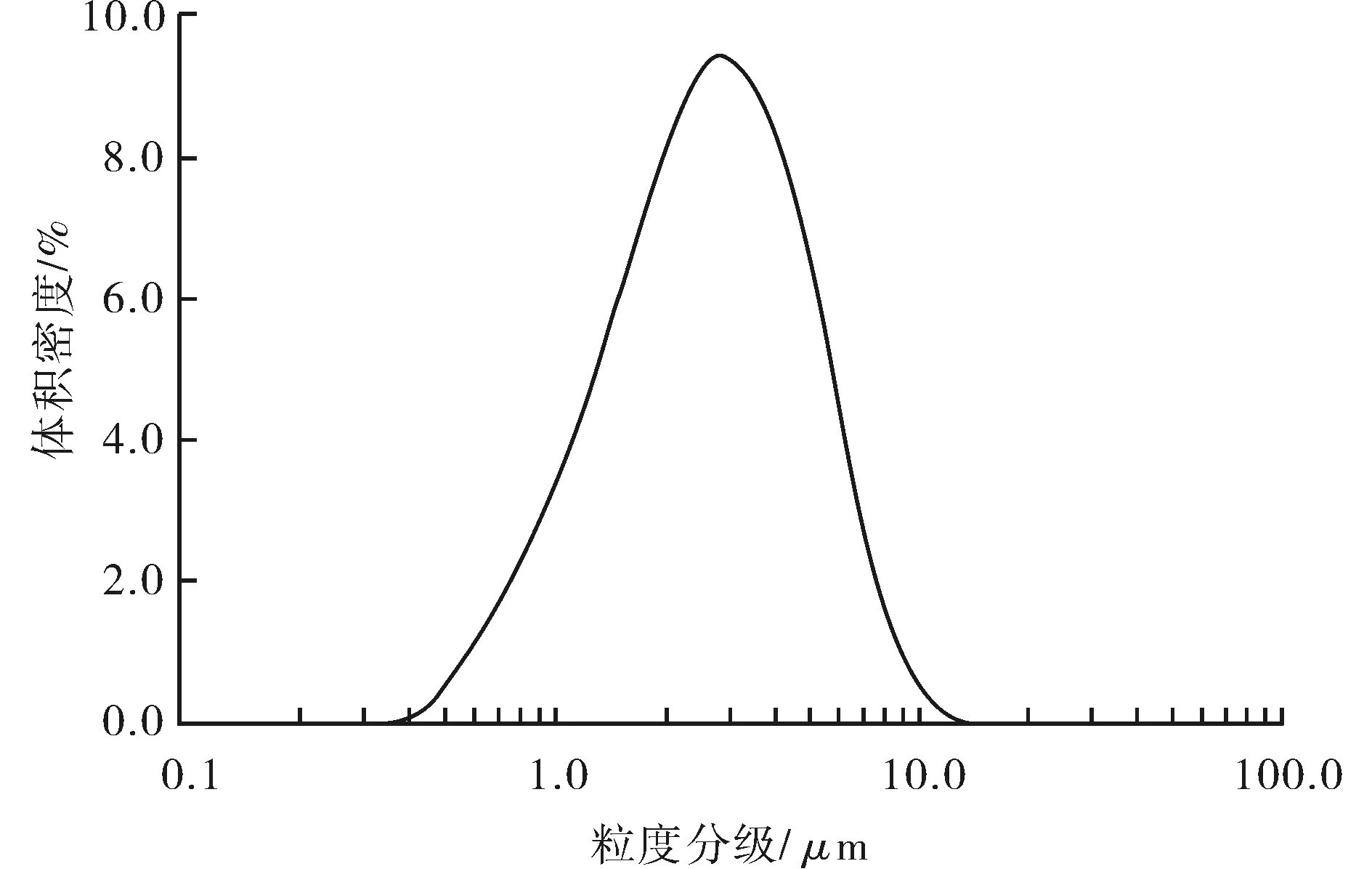
图6 粒度分布图Fig.6 Size distribution curve of product

图7 FePO4的XRD图Fig.7 XRD pattern of FePO4
副产品硫酸铵的质量分析如表4所示,硫酸铵产品质量达到硫酸铵国家标准GB535-1995合格品要求.

表4 副产硫酸铵产品质量Table 4 Byproduct quality of ammonium sulphate
3 结 语
探索了以硫酸亚铁和磷酸铵为原料,经氧化、沉淀和转化制备磷酸铁,同时副产硫酸铵的工艺,对反应条件进行了优化,取得了优化工艺条件.在H2O2加量为理论量的120%、加料时间为50 min、沉淀反应温度40 ℃、磷酸铵加料时间为 40 min、转化反应温度90 ℃、磷酸浓度为0.5 mol/L的条件下,制备出了平均粒径小于3.0 μm、杂质含量低的电池级超微细磷酸铁,副产硫酸铵达到GB535-1995合格品要求,生产过程中无“三废”排放.
致谢
本文产品检测得到了湖南化工研究院分析检测中心的支持与帮助,在此表示衷心感谢!
参考文献:
[1] 周伟家,何文,张旭东,等.磷酸铁的研究进展[J].化工科技市场,2008,31(9):7-10.
ZHOU Wei-jia,HE Wen,ZHANG Xu-dong,et al.Research and development of iron phosphate materials[J]. Chemical Technology Market, 2008,31(9):7-10.(in Chinese)
[2] 天津化工研究院.无机盐工业手册[M].北京:化学工业出版社,1981:625.
Tianjin Research Institute of chemical industry.Inorganic Salt Industry Handbook[M]. Beijing:Chemical Industry Press, 1981:625.(in Chinese)
[3] 张震,蒲薇华,任建国,等.控制结晶法制备球形磷酸铁的团聚尺寸模型[J].化学工程,2011,39(8):20-24.
ZHANG Zhen,PU Wei-hua,REN Jian-guo,et al. Agglomeration-size model of ferric phosphate spherical particle prepared by controlled crystalliza-tion[J].Chemical Engineering(China), 2011,39(8):20-24.(in Chinese)
[4] 马广成,丁士文,李青,等.正磷酸铁的合成及其性能的研究[J].河北大学学报:自然科学版,1993,13(4):54-57.
MA Guang-cheng, DING Shi-wen, LI qing, et al.Studies on synthesis and properties of iron(Ⅲ) phosphate[J]. Journal of Hebei University :Natural Science Edition, 1993,13(4):54-57.(in Chinese)
[5] 龚福忠,易均辉,周立亚,等.两种不同形貌FePO4的制备及其正极材料LiFePO4的电化学性能[J].广西大学学报:自然科学版,2009,34(6):731-735.
GONG Fu-zhong,YI Jun-hui,ZhOU Li-ya,et al.Preparation of two kinds of FePO4powders with different morphologies and electrochemical properties of LiFePO4[J].Journal of Guangxi University:Natural Science Edition,2009,34(6):731-735.(in Chinese)
[6] 左小虎,刘卫平,伍儒锋,等.一种磷酸铁的制备方法:中国,102040208[P].2011-05-04.
ZUO Xiao-hu,LIU Wei-ping,WU Ru-feng,et al.A process for producing iron phosphate: China,102040208[P].2011-05-04.(in Chinese)
[7] 彭爱国,贺周初,余长艳,等.高纯正磷酸铁的制备方法:中国,101327918[P].2008-12-24.
PENG Ai-guo,HE Zhou-chu,YU Chang-yan,et al.Method of preparing high pure iron phosphate: China,101327918[P].2008-12-24.(in Chinese)
