三聚氰胺与丙烯酰胺单体分子印迹相互作用的理论研究
2013-02-13刘俊渤孙佳妮唐珊珊胡耀辉靳瑞发
刘俊渤,石 杨,孙佳妮,唐珊珊,胡耀辉,靳瑞发
(1.吉林农业大学资源与环境学院,吉林 长春 130118;2.吉林农业大学食品科学与工程学院,吉林 长春 130118;3.赤峰学院化学化工学院,内蒙古 赤峰 024000)
三聚氰胺(MEL)俗称密胺或蛋白精,IUPAC命名为“1,3,5-三嗪-2,4,6-三氨基”,是一种三嗪类含氮杂环有机化合物,被用作化工原料。它是白色,几乎无味,对身体有害,不可用于食品加工或食品添加物。由于MEL含氮量较高,添加到牛奶等食品中可产生蛋白质含量高的虚假现象,从而导致了中国2008年9月发生的“三鹿奶粉事件”,造成数千名食用含有MEL问题奶粉的婴幼儿患上肾结石。因此对蛋白类食品中痕量组分MEL的分离与检测十分重要。
分子印迹技术(MIT)是源于高分子化学、材料化学、化学工程及纳米化学的交叉学科技术[1],该技术为人们提供具有期望结构和性质的分子组合体。当体系中存在模板分子(印迹分子、目标分子)时,功能单体与交联剂在适当溶剂中可以通过聚合使这些模板分子以互补形式固定下来,聚合后利用断“键”溶剂洗脱去除模板分子,从而可获得具有特异选择性的分子印迹聚合(MIP)[2]。由于MIP具极高的选择性、良好的稳定性,合成费用低,可以大批量制备等优点,近年来已在手性拆分[3]、色谱分离[4-5]、固相萃取[6-7]、天然抗体模拟[8]、模拟酶催化[9]与分子识别传感器[10]等方面得到广泛应用。但目前分子印迹技术领域欠缺从分子水平上探讨分子印迹过程的理论研究,因此,许多研究者开始尝试将分子模拟计算应用于分子印迹体系的理论研究,这不仅可以从分子水平上探讨分子印迹和识别机理,而且可以快速筛选功能单体、印迹比例及溶剂[11-17],提高研发效率。由于量子化学模拟计算准确度较高,所以其计算结果对于分子印迹体系的理论与实验研究具有指导意义。
目前,MEL分子印迹材料的制备通常是以甲基丙烯酸(MAA)[18-20]、AM[21-22]和衣康酸(IA)[22]为功能单体。以往MEL分子印迹聚合物合成时都采用MAA为功能单体,但张孝刚等[22]发现AM单体与MEL之间产生的氢键相互作用在甲醇溶剂中对印迹体系影响最大,且对于不同功能单体相互作用的印迹机理的研究报道仅局限于傅里叶变换红外光谱(FT-IR)、氢核磁共振波谱(1H NMR)和紫外光谱的简单分析[22-24],而关于在原子水平上建立分子模型用以模拟MEL与功能单体分子印迹相互作用的研究报道并未见到。因此,本实验尝试以MEL作为研究对象,AM为功能单体,研究MEL与AM的印迹比例不同时形成复合物的构型、成键情况、自然键轨道分析方法(NBO)电荷的变化以及反应的结合能等,表征了它们之间相互作用的强弱,探讨了MEL分子印迹的作用原理,这对于优化功能单体及功能单体与印迹分子的印迹比例,提高分子印迹聚合物的稳定性、选择性和吸附性,完善分子印迹理论都具有重要意义。
1 计算方法

图1 MEL化学结构Fig.1 Chemical structure of MEL
采用密度泛函理论(DFT)[25-27]的pbe1pbe方法和6-31G(d,p)优化MEL几何构型,见图1。pbe1pbe/6-31G(d,p)水平的计算结果如表1所示,表中引用了由李雪梅等[28]所报道的MEL晶体结构数据。观察表1数据,pbe1pbe方法的计算结果与晶体数据很接近,因此,用pbe1pbe方法优化结构比较适合。数据表明用pbe1pbe/6-31G(d,p)方法可以满足对MEL结构优化的要求。因此,在本研究中采用pbe1pbe/6-31G(d,p)方法优化模板分子、功能单体及其聚合物的几何构型。

表1 pbe1pbe/6-31G(d,p)方法计算的MEL分子几何构型与实验值对照Table 1 Structural parameters of MEL calculated at the pbe1pbe/6-31G(d,p) level and available experimental data
所有的计算均使用Gaussian 09软件Revision A.02版,分别对印迹分子和功能单体进行以下操作:1)对MEL、AM及其复合物进行几何构型优化,在同样水平下进行频率计算,得到没有虚频能量最低的几何构型,并采用NBO进行电荷分析。2)研究MEL与AM功能单体在其印迹比例不同时形成的复合物氢键键长、氢键数目及氢键作用的活性位点,探讨MEL与AM功能单体分子印迹的作用原理及其相互作用的强弱。3)计算MEL、AM功能单体以及其所形成复合物几何构型的能量,利用式(1)对得到的稳定几何构型进行结合能计算,表征MEL与AM功能单体相互作用的强弱。
在计算结合能时,基组迭加误差(BSSE)采用Counterpoise方法(CP)消除[29]。

式中:ΔEB为CP方法校正后的相互作用能,即结合能;EC为MEL与AM功能单体分子印迹聚合物体系的总能量;ET为MEL模板分子的能量;∑EF为AM功能单体的能量之和。
2 结果与分析
2.1 MEL与AM功能单体几何构型的优化
优化MEL和AM的分子几何构型并计算原子的NBO电荷。模板MEL分子中有1个三嗪环及3个胺基,三嗪环上的N原子可作为质子受体,而氨基上的H原子可作为质子给体;AM分子中有1个羰基和1个氨基,其中羰基中的O原子可作为质子受体,氨基上的H原子可作为质子给体。计算结果也表明MEL分子的质子受体为三嗪环上的N2、N5、N6,质子给体为胺基上的H8、H9、H11、H12、H14、H15;AM的质子受体为羰基中的O6,质子给体为氨基上的H9、H10。MEL与AM功能单体的质子受体与质子给体位点的电荷如图2所示。

图2 模板分子与功能单体的构型Fig.2 Conformation of the template molecule and the functional monomer
2.2 MEL与AM功能单体复合物几何构型的优化
根据MEL模板分子和AM功能单体分子几何构型优化的结果,构建MEL和AM功能单体之间形成的复合物几何构型,并通过计算模拟优化其复合物的几何构型。通过比较模板分子与功能单体在其印迹比例不同时形成复合物的几何构型、成键情况、NBO电荷的变化以及反应的结合能等,探讨MEL与AM功能单体分子印迹的作用原理及其相互作用的强弱。在选择功能单体进行计算机模拟时,分别选择模板分子与功能单体印迹比例为1:1、1:2、1:3、1:4、1:5、1:6和1:7等7种计算模型进行研究,当印迹比例为1:7时,由于分子间存在空间位阻,模板分子与功能单体分子间斥力增大,功能单体之间相互影响,得到的复合物稳定性减弱。
2.2.1 几何构型
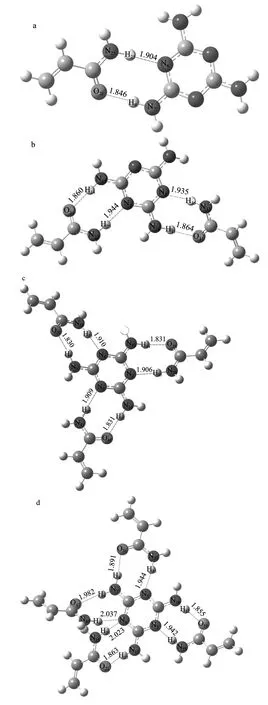

图3 模板分子与功能单体复合物的优化几何构型Fig.3 Optimized molecular structure of MEL/AM complexes

表2 模板分子与功能单体分子印迹相互作用体系的相关参数Table 2 Bonding parameters for the interaction between MEL and AM in MIPs
MEL模板分子与AM功能单体相互作用总共得到6个稳定几何构型,结果如图3所示,每个稳定构型中模板分子与功能单体通过分子间氢键作用,其氢键数目、键长与氢键作用活性位点列于表2中。MEL模板分子与AM功能单体印迹比例为1:1时,两者之间形成两个氢键,其相互作用的氢键作用活性位点是N6┅H25—N23与N7—H9┅O21两种形式,形成复合物后它们之间氢键的键长分别为1.904、1.846 ,这些值均在氢键范畴内[30-32]。由此可知,MEL与AM功能单体之间通过氢键相互作用。MEL模板分子与AM功能单体印迹比例为1:2、1:3、1:4、1:5时,两者之间分别形成为4、6、8、10个氢键,随着印迹比例增大,模板分子与功能单体之间形成氢键数目在增加,相互作用活性位点也在增多。MEL与AM印迹比例为1:6时,由图3f优化后的几何构型可以看出,MEL与AM功能单体之间形成12个氢键,其氢键的构成分别为N2┅H35—N33、N2┅H55—N53、N5┅H65—N63、N5┅H75—N73、N6┅H25—N23、N6┅H45—N43、N13—H15┅O21、N10—H12┅O31、N7—H9┅O41、N13—H14┅O51、N10—H11┅O61与N7—H8┅O71,氢键键长分别为1.991、1.991、1.982、2.011、1.982、2.014、1.916、1.878、1.875、1.879、1.909、1.878 。从文献[21-22]可以看出MEL与AM的最佳印迹比例为1:3,但计算表明当MEL与AM的比例大于1:3时,它们之间的结合能绝对值仍然在增大,单体与模板分子之间的氢键也在增多。分子印迹聚合物制备时,印迹比例越大,活性作用位点越多,其印迹聚合物也就越规则,而规则的聚合物有助于识别模板分子与辨别其同系物,从而使聚合物有更好的吸附性与选择性。

续表2
2.2.2 结合能
为了进一步分析MEL与AM功能单体的相互作用能,采用pbe1pbe/6-31G(d,p)方法计算了6个复合物的结合能。表3是根据式(1)模拟计算所得的MEL、AM和其复合物的能量E及经BSSE校正后的结合能ΔE。一般而言,当两个分子相互作用时,体系的能量会减少,即形成复合物的过程是一个能量降低的过程。结合能ΔE是形成复合物后,复合物的总能量减去形成复合物的模板分子能量与每一个单体能量之和。若复合物是稳定存在的,则ΔE为负值,且ΔE越低,模板分子与功能单体形成的复合物就越稳定,印迹效应也就越强。因此,用分子模拟计算模板分子、功能单体及其之间形成复合物的能量,比较其复合物结合能的大小,可以有效筛选出印迹效果更好的功能单体与模板分子印迹的比例,减少实际实验的时间与消耗。
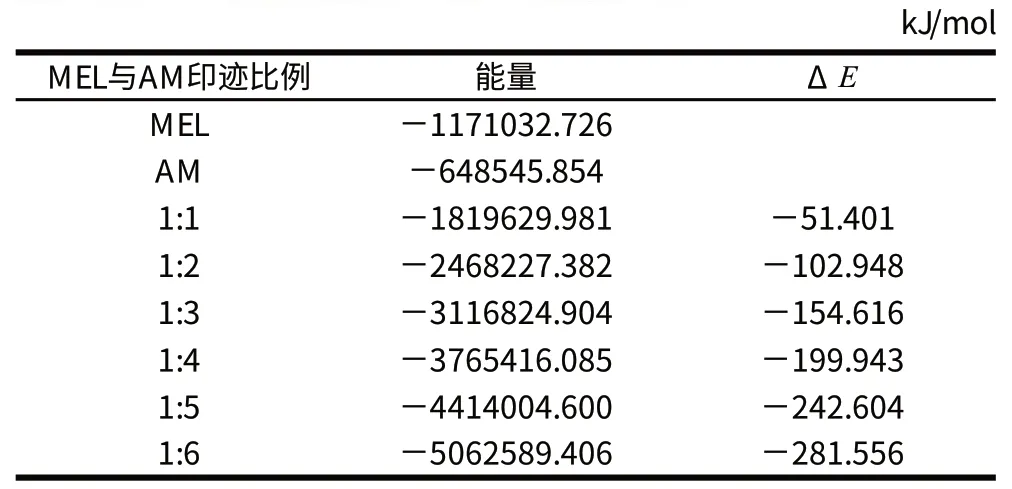
表3 复合物用pbe1pbe/6-31G(d,p)方法计算的结合能Table 3 Binding energies of MEL/AM complexes calculated at the pbe1pbe/6-31G(d,p) level
由表3可知,随着MEL与AM相互作用印迹比例的增加,其结合能ΔE绝对值越来越大。印迹分子与功能单体印迹比例1:2时比1:1时的结合能降低了51.547kJ/mol,降低了一倍左右。显然,在模板分子与功能单体比例为1:2时,MEL与AM形成的复合物稳定性显著增强。总体来看,当印迹比例1:6时,此时结合能最低为-281.556kJ/mol,其复合物最稳定。因此,较其印迹比例而言,MEL与AM功能单体比例为1:6时,形成的复合物稳定性最强。同时也说明分子印迹过程中印迹分子与功能单体印迹比例的选择非常重要,这不仅影响印迹分子的键合速度与释出,而且还制约着所制备的分子印迹聚合物稳定性、选择性与吸附特性大小。
2.2.3 电荷分布
氢键的形成引起电子重组,这与复合物中成键原子的电荷转移有关[33]。为解释相互作用的本质,用NBO研究复合物中原子电荷,评估整体的NBO电荷转移,从而判断氢键的形成及强弱。MEL模板分子与AM功能单体印迹比例为1:1时,从MEL与AM功能单体形成复合物的NBO电荷结果可以看出:MEL与AM功能单体相互作用前,MEL结构中N6的NBO电荷为-0.643,H9的NBO电荷为0.430;相互作用后,MEL结构中N6的NBO电荷为-0.686,H9的NBO电荷为0.453。结果表明,N6失去电荷0.043,H9得到电荷0.023,MEL质子受体与质子给体发生了一定的电荷转移,所以可以认为MEL印迹分子与AM功能单体之间发生了相互作用,形成了氢键。
MEL与AM功能单体印迹比例为1:2时,相互作用前,MEL结构中N2、N5的NBO电荷都为-0.643,H11、H14的NBO电荷都为0.430;相互作用后,MEL结构中N2、N5的NBO电荷分别为-0.683、-0.687,H11、H14的NBO电荷都为0.453。结果表明,N2、N5分别失去电荷0.040、0.044,H12、H14分别都得到电荷0.023。与印迹比例为1:1的复合物电荷转移相比,增加了一个N原子质子受体和一个H质子给体,且多形成了2个氢键。
MEL与AM功能单体印迹比例为1:3时,相互作用前,MEL结构中N2、N5、N6的NBO电荷都为-0.643,H9、H11、H14的NBO电荷都为0.430;发生相互作用后,MEL结构中N2、N5、N6的NBO电荷都变为-0.687,H9、H11、H14的NBO电荷都变为0.454。结果表明,N2、N5、N6都失去电荷0.044,H9、H11、H14都得到电荷0.024。与印迹比例为1:2的复合物电荷转移相比,MEL增多一个N质子受体位点及一个H质子给体位点,且多形成了2个氢键。
MEL与AM功能单体印迹比例为1:4时,相互作用前,MEL结构中N2、N5、N6的NBO电荷都为-0.643,H8、H9、H12、H15的NBO电荷都为0.430;发生相互作用后,MEL结构中N2、N5、N6的NBO电荷分别为-0.687、-0.684、-0.723,H8、H9、H12、H15的NBO电荷分别为0.452、0.442、0.450、0.454。结果表明,N2、N5、N6分别失去电荷0.044、0.041、0.080,H8、H9、H12、H15分别得到电荷0.022、0.012、0.020、0.024,与印迹比例为1:3的复合物电荷转移相比,MEL的N6质子受体电荷转移趋势明显增强,且多形成了2个氢键。
MEL与AM功能单体印迹比例为1:5时,相互作用前,MEL结构中N2、N5、N6的NBO电荷都为-0.643,H8、H9、H12、H14、H15的NBO电荷为0.430;发生相互作用后,MEL结构中N2、N5、N6的NBO电荷分别为-0.730、-0.686、-0.726,H8、H9、H12、H14、H15的NBO电荷分别为0.452、0.447、0.451、0.444、0.449。结果表明,N2、N5、N6分别失去电荷0.087、0.043、0.083,H8、H9、H12、H14、H15分别得到电荷0.022、0.017、0.021、0.014、0.019。与印迹比例为1:4的复合物电荷转移相比,MEL的N2质子受体转移电荷趋势明显增强,且多形成了2个氢键。
MEL与AM功能单体印迹比例为1:6时,作用前,MEL结构中N2、N5、N6的NBO电荷都为-0.643,H8、H9、H11、H12、H14、H15的NBO电荷都为0.430;发生相互作用后,MEL结构中N2、N5、N6的NBO电荷分别为-0.731、-0.730、-0.730,H8、H9、H11、H12、H14、H15的NBO电荷分别为0.449、0.450、0.446、0.448、0.449、0.446。结果表明,N2、N5、N6分别失去电荷0.088、0.087、0.087,H8、H9、H11、H12、H14、H15分别得到电荷0.019、0.020、0.016、0.018、0.019、0.016。与印迹比例为1:5的复合物电荷转移相比,MEL的N5质子受体转移电荷趋势明显增强,且多形成了2个氢键。因此,较其他印迹比例,MEL与AM功能单体比例为1:6时,形成的氢键相互作用力最强。从这些值可以判断,电荷转移量的大小顺序与结合能顺序是一致的。
3 结 论
以MEL为印迹分子,以AM为功能单体,采用量子化学计算通过比较印迹分子与功能单体在其不同印记比例时形成复合物的构型、成键情况、NBO电荷的变化及反应的结合能,探讨MEL与AM功能单体分子印迹的作用原理及其相互作用的强弱。通过计算机辅助计算分析研究表明,模板分子与功能单体印迹比例为1:6时,电荷转移趋势总体最大,其复合物的结合能最低,印迹复合物体系作稳定,其氢键作用的活性位点与形式分别是两个N2┅H—N、两个N5┅H—N、两个N6┅H—N、两个N7—H┅O、两个N10—H┅O与两个N13—H┅O。因此,对MEL模板分子,制备具有较高选择性和吸附能力的分子印迹聚合物其印迹分子与AM功能单体最佳印迹比例为1:6。通过模拟计算,有助于指导分子印迹聚合物合成时功能单体及功能单体与印迹分子最佳印迹比例的选择,减少了实际实验过程中的时间及消耗,更为完善分子印迹作用的原理提供系统的理论研究。
[1]陈金红, 方战强, 许振成.分子印迹及结合技术去除水中污染物的研究进展[J].水处理技术, 2010, 36(3): 1-4.
[2]梁金虎, 罗林, 唐英.分子印迹技术的原理及研究进展[J].重庆文理学院学报: 自然科学版, 2009, 28(5): 38-43.
[3]魏俊, 孙向英, 刘斌.手性拆分L-脯氨酸分子印迹聚合物的制备及其性能[J].应用化学, 2006, 23(12): 1336-1341.
[4]刘祥军, 刘吉众, 赵睿, 等.三甲氧基苄啶分子印迹整体柱的制备及色谱性能[J].高等学校化学学报, 2007, 28(10): 1878-1880.
[5]TAMAYO fG, MARTIN-ESTEBAN A.Selective high performance liquid chromatography imprinted-stationary phases for the screening of phenylurea herbicides in vegetable samples[J].Chromatogr A, 2005,1098(1/2): 116-122.
[6]贺利民, 刘开永, 武力, 等.分子印迹固相萃取气相色谱-质谱法测定鸡蛋中三聚氰胺[J].中国兽药杂志, 2011, 45(1): 2-5.
[7]杨海军.三聚氰胺分子印迹整体固相微萃取头的制备及在液相色谱分析中的应用研究[D].中山: 中山大学, 2009.
[8]PESAVENTO M, D′AGOSTINO G, BIESUZ R, et al.Molecularly imprinted polymer-based sensors for amperometric determination of nonelectroactive substances[J].Electroanalysis, 2009, 21(3/5):604-611.
[9]张挪威,丁明星, 刘国艳, 等.基于分子印迹膜的检测牛奶中琥珀酸氯霉素残留传感方法的研究[J].分析化学, 2008, 36(10): 1380-1384.
[10]赵硕, 崔莉凤, 申晴.一种快速检测液态奶中三聚氰胺的传感器制备[J].北京工商大学学报: 自然科学版, 2010, 28(6): 23-27.
[11]CHIANELLA I, LOTTERSO M, PILETSKY S A, et al.Rational design of a polymer specific for microcystin-lr using a computational approach[J].Anal Chem, 2002, 74(6): 1288-1293.
[12]SUN Jiani, LIU Junbo, TANG Shanshan, et al.Theoretical researches on the self-assembly system of ciprofloxacin Imprinted Polymers[J].Chin J Struct Chem, 2013, 32(8): 1204-1210.
[13]LIU Junbo, SUN Jiani, TANG Shanshan, et al.Theoretical researches on the recognizing characteristics of atrazine imprinted polymers with different functional monomers[J].Chin J Struct Chem, 2012, 31(12):1794-1802.
[14]WU Liqing, LI Yuanzong.Study on the recognition of templates and their analogues on molecularly imprinted polymer using computational and conformational analysis approaches[J].J Mol Recognit, 2004,17(6): 567-574.
[15]LI Xiufang, ZHONG Shian.Computer simulation and preparation of molecularly imprinted composite membranes with chlorogenic acid as template[J].Acta Chimica Sinica, 2011, 69(6): 693-700.
[16]HU Bo, ZHANG Jingping.Theoretical investigation on the white-light emission from a single-polymer system with simultaneous blue and orange emission[J].Polymer, 2009, 50: 6172-6185.
[17]YAO Junhai, LI Xin, WU Qin.Computational design and synthesis of molecular imprinted polymers with high selectivity for removal of aniline from contaminated water[J].Analytica Chimica Acta, 2008,610: 282-288.
[18]齐娜, 陈娜, 陈军, 等.三聚氰胺分子印迹聚合物的制备及固相萃取条件优化比较[J].河南科技学院学报, 2011, 39(6): 91-95.
[19]周文辉, 林黎明, 郭秀春, 等.三聚氰胺分子印迹聚合物的制备及奶制品中三聚氰胺的分离[J].分析测试学报, 2009, 28(6): 687-691.
[20]张红武, 温金莲, 唐睿, 等.三聚氰胺分子印迹整体柱识别性能的研究[J].化学通报, 2011(6): 545-550.
[21]程健琳, 吕昌银, 严成燕, 等.两类三聚氰胺分子印迹聚合物性能比较研究及应用[J].中国卫生检验杂志, 2011, 21(1): 44-47.
[22]张孝刚, 朱秋劲, 胡萍.三聚氰胺分子印迹预组装体系紫外光谱研究[J].食品科学, 2011, 32(21): 128-132.
[23]杨卫海, 严守雷, 卫晨, 等.沉淀聚合法制备三聚氰胺分子印迹聚合物微球[J].高分子学报, 2010(10): 1163-1169.
[24]LI Mu, ZHANG Liying, MENG Zihui, et al.Molecularlyimprintedmicrospheres for selective extraction and determination of melamine inmilk and feed using gas chromatography-mass spectrometry[J].Journal of Chromatography B, 2010, 878: 2333-2338.
[25]BECKE A D.Density-functional exchange-energy approximation with correct asymptotic behavior[J].Physical Review A: Atomic,Molecular, Optical Physics, 1988, 38(6): 3098-3100.
[26]LEE C, YANG Weitao, PARR R G.Development of the colle-salvetti correlation-energy formula into a functional of the electron density[J].Phys Rev B: Condens Matter Mater Phys, 1988, 37(2): 785-789.
[27]STEPHENS P J, DEVLIN fJ, CHABALOWSKI C F, et al.Abinitio calculation of vibrational absorption and circular dichroism spectra using density functional force fields[J].J Phys Chem, 1994, 98(45):11623-11627.
[28]李雪梅, 荆补琴, 李丽萍, 等.三聚氰胺晶体中的氢键作用[J].山西大同大学学报: 自然科学版, 2009, 25(2): 37-39.
[29]BOYS S F, BERNADI F.The calculation of small molecular interactions by the differences of separate total energies[J].Molecular Physics, 1970, 19: 553-566.
[30]周公度, 段连运.结构化学基础[M].北京: 北京大学出版社, 1995:178-192.
[31]JEFFREY G A.Hydrogen-bonding: an update[J].Crystallography Reviews, 2003, 9(2/3):135-176.
[32]STEINER T.C-H···O hydrogen bonding in crystals[J].Crystallography Reviews, 2003, 9(2/3): 177-228.
[33]STEINER T.The hydrogen bond in the solid state[J].Angew Chem Int Ed, 2002, 41(1): 48-76.
