1,2-二氧环乙烷类化学发光剂的合成研究
2012-11-14焦艳华郭卫强梁媛媛陈灿玉章鹏飞
焦艳华,郭卫强,何 睿,梁媛媛,陈灿玉,章鹏飞
(1. 杭州师范大学生物医药与健康研究中心,浙江 杭州 311121;2. 杭州师范大学材料与化学化工学院,浙江 杭州 310036)
1,2-二氧环乙烷类化学发光剂的合成研究
焦艳华1,郭卫强1,何 睿1,梁媛媛1,陈灿玉1,章鹏飞2
(1. 杭州师范大学生物医药与健康研究中心,浙江 杭州 311121;2. 杭州师范大学材料与化学化工学院,浙江 杭州 310036)
研究了1,2-二氧环乙烷类化学发光剂的合成方法,系统地探讨了反应温度、反应时间及反应物物质的量之比等因素对产物收率的影响,2-金刚烷酮与间羟基苯甲酸酯的McMurry分子间的交叉偶联反应,用TiCl4-Zn为还原剂,在最优实验条件下,主产物收率可达到81%.
化学发光剂;1,2-二氧环乙烷;合成
化学发光免疫分析(Chemiluminescence immunoassay, CLIA)是将化学发光与免疫反应相结合,用于检测微量抗原或抗体的一种新型标记免疫分析技术.免疫分析中目前应用较广的化学发光物质主要有鲁米诺及其衍生物[1-3]、吖啶酯和吖啶磺酰胺化合物[4-6]、1,2-二氧环乙烷类衍生物[7-10]等.其中金刚烷-1,2-二氧环乙烷衍生物是高量子效率、高稳定性的化学发光底物,最常使用的底物是3-(2′-螺旋金刚烷)-4-甲氧基-4-(3″-磷氧酰苯基)-1,2-二氧环乙烷(AMPPD),碱性磷酸酶(ALP)-AMPPD发光体系具有稳态发光特性,量子产率在0.90以上,用于碱性磷酸酶的测定,灵敏度可以高达10-21mol(<1 000AP)分子,是目前最灵敏的核酸检测方法之一[11].
AMPPD性质十分稳定,5 ℃下保存的固体AMPPD几乎不分解.但其合成条件较苛刻,目前国内还没有关于这类化学发光试剂的合成研究报道,因此,参考借鉴国外过期专利技术,研究改进1,2-二氧环乙烷类化学发光试剂的合成路线和方法,优化合成工艺,具有非常重要的意义.
1 实验部分
1.1 试 剂
实验中所用试剂除间羟基苯甲酸甲酯和2-金刚烷酮为市售化学纯外,其他均为市售分析纯,使用前按标准方法提纯干燥.
1.2 合成路线
如图1所示.

图1 AMPPD的合成路线Fig.1 The synthesis route of AMPPD
1.3 合成方法
AMPPD的合成分3步反应进行:第1步采用McMurry反应,以TiCl4/Zn为还原剂,在一定温度下,将一定配比的间羟基苯甲酸甲酯与2-金刚烷酮反应,即得到烯醇醚中间体(1).第2步,在冰水冷却下,向中间体(1)的四氢呋喃溶液中缓慢滴加PCl3,然后加NaOH溶液水解,即得到中间体(2).第3步,将适量中间体(2)溶于CH2Cl2中,以虎红或亚甲基蓝为光敏剂,通氧气,用高压钠灯光照36 h,柱层析提纯得到最终产物(3).
2 结果与讨论
合成1,2-二氧环乙烷类化学发光试剂,第1步烯醇醚的合成及第3步光敏氧化反应是关键,本文详细研究了这两步反应,探索出较优的合成条件.
2.1 McMurry酮酯偶联反应生成烯醇醚
国外文献报道2-金刚烷酮和3-取代苯甲酸酯的McMurry分子间的交叉偶联反应中结合使用TiCl3-LiAlH4试剂[12],但由于固体TiCl3非常易潮解,价格昂贵,市场上很难买到,所以需要寻找TiCl3的替代品.经过实验探索,我们使用TiCl4-Zn试剂,反应结果较好.2-金刚烷酮与3-取代苯甲酸酯发生McMurry偶联反应,除了主产物烯醇醚以外,还存在2-金刚烷酮自身偶联产物及酮等副产物,所以需要对反应条件进行优化,以提高主产物的收率.
2.1.1 反应温度的影响
由于四氯化钛与锌粉的还原反应会放出大量的热,所以该反应一般要求在低温下进行,本文分别在-60 ℃、-40 ℃、-20 ℃和0 ℃时,反应12 h,产物的收率见表1.从表中数据可以看出,反应在低温下收率较高,从节约能源角度出发,本文选择-40 ℃作为最佳的反应温度.
2.1.2 反应时间的影响
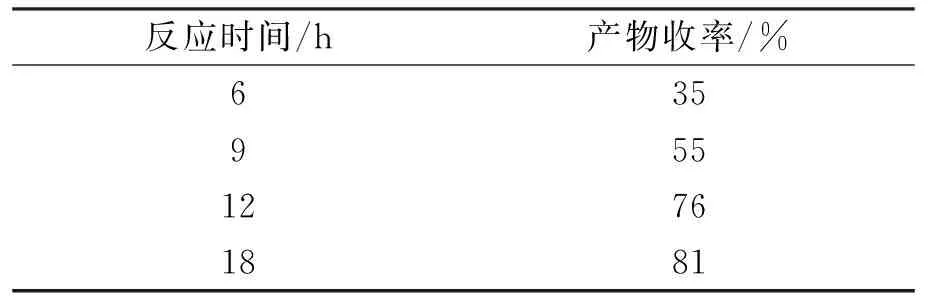
在最佳反应温度-40 ℃时,分别反应6、9、12、18 h,产物的收率见表2.由表2可以看出,随着反应时间的延长,产物的收率升高.当反应时间达到12 h时,产物的收率已很高,若再延长反应时间,产物的收率提高很少,所以选择反应时间为12 h左右.
表1反应温度对产物收率的影响
Tab.1Effectofreactiontemperatureonproductivity

反应温度/℃产物收率/%-6079-4076-2045031
注:反应时间12 h,n(2-金刚烷酮)∶n(间羟基苯甲酸甲酯)=1.5∶1
表2反应时间对产物收率的影响
Tab.2Effectofreactiontimeonproductivity
反应时间/h产物收率/%63595512761881
注:反应温度-40 ℃,n(2-金刚烷酮)∶n(间羟基苯甲酸甲酯)=1.5∶1
2.1.3 反应物投料配比的影响
2-金刚烷酮与间羟基苯甲酸甲酯发生McMurry偶联反应,除了主产物烯醇醚以外,还存在2-金刚烷酮自身偶联的副产物.本文在确定了反应温度和时间以后,改变反应物的物质的量之比,产物收率的测定结果见表3.
由表中结果可以看出,2-金刚烷酮与间羟基苯甲酸甲酯的物质的量之比为2∶1时,主产物的收率达到最高,即81%,所以选择物质的量之比为2∶1进行反应.
综上所述,2-金刚烷酮和间羟基苯甲酸甲酯的McMurry偶联反应的最优条件:TiCl4/Zn为还原剂,反应温度为-40 ℃,反应时间为12 h,酮与酯的物质的量之比为2∶1,在此条件下,主产物的收率达到81%.
2.2 光敏氧化反应
在光化学反应中,使用最广泛的光源是汞灯,而汞灯辐射的紫外线对人体皮肤有害,会引起皮肤癌,并伤害眼睛,存在一定的局限性.高压钠灯作为一种新型的绿色光源,具有高光效、长寿命、高节能等特点,其光谱能量分布主要集中于550~650 nm的可见光谱域内,其辐射对人体无伤害,因此本文选择高压钠灯为光源.由于光敏氧化反应存在着转化率较低、反应时间长等不足,而且存在副产物如环氧化合物等,所以需要对影响反应的因素如反应温度、光照时间、光敏剂的种类等进行系统研究和优化,以提高产物的收率.

表3 反应物物质的量之比对反应收率的影响Tab.3 Effect of reactants mole ratio on productivity
注:反应温度-40 ℃,反应时间12 h.

表4 反应温度对产物收率的影响Tab.4 Effect of reaction temperature on productivity
注:500 W 钠灯照射36 h.
2.2.1 反应温度对反应的影响
由于烯烃光敏氧化反应所得到的产物1,2-二氧环乙烷类化学发光剂是热不稳定的,高温时容易发生分解反应,所以烯烃光敏氧化反应要求在低温下进行,本文分别在-65 ℃、-45 ℃、-20 ℃和0 ℃时,反应36 h,通过高效液相色谱检测反应液中产物的含量,计算得到产物的收率见表4.从表中数据可以看出,温度越低,产物的收率越高,从节约能源角度出发,本文选择-45 ℃作为最佳的反应温度.

表5 光照时间对产物收率的影响Tab.5 Effect of reaction time on productivity
注:反应温度-45 ℃,500 W钠灯照射.
2.2.2 光照时间对反应的影响
烯烃的光敏氧化反应一般反应时间较长,本文在最佳反应温度-45 ℃时,分别反应12、24、36、48 h,取样,用高效液相色谱检测反应液中产物的含量,计算得到产物的收率见表5.从表中可以看出,反应36 h后产物的收率达到最高,再延长反应时间,收率呈下降趋势,这可能是因为产物不太稳定,在生成过程中会缓慢发生分解反应.

表6 光敏剂种类对产物收率的影响Tab.6 Effect of photosensitizer on productivity
注:反应温度-45 ℃,500 W 钠灯照射36 h.
2.2.3 光敏剂种类对反应的影响
本文以甲醇为溶剂,高压钠灯为光源,分别以亚甲基蓝、虎红为光敏剂,通氧气,光照36 h后,通过高效液相色谱检测反应液中产物的含量,计算收率,反应结果见表6.从表中数据可以看出,两种光敏剂得到的产物收率差别不大,因此这两种光敏剂对反应收率影响不大.
综上所述,该反应的最优反应条件:反应温度为-45 ℃,反应时间为36 h,虎红为光敏剂,甲醇为溶剂,在此条件下,主产物的收率达到73%.
3 结 论
1)2-金刚烷酮和间羟基苯甲酸甲酯的McMurry分子间的交叉偶联反应,用TiCl4-Zn为还原剂,在最优实验条件下,主产物收率可达到81%.
2)烯醇醚的光敏氧化反应,在-45 ℃下,以虎红为光敏剂,甲醇为溶剂,光照36 h,主产物的收率达到73%.
[1] Iwata R, Hayashi T, Nakao Y,etal. Direct determination of plasma endothelin-1 by chemiluminescence enzyme immunoassay[J]. Clin Chem,1996,42(8):1155-1158.
[2] Helen L, Larry J K. Influence of different luminols on the characteristics of the chemiluminescence reaction in human neutrophils[J]. J Biolumin Chemilumin,1995,10(6):353-359.
[3] Metelitxa D I, Eryomin A N. Enhanced chemiluminescence in the oxidation of luminol and an isoluminol cortisol conjugate by hydrogen peroxide in reversed micelles[J]. J Biolumin Chemilumin,1992,7(1):21-26.
[4] Hart R C, Taafe L R. The use of acridinium ester-labelled streptavidin in immunoassays[J]. J Immunological Methods,1987,101(1):91-96.
[5] Phillip G M. Chemiluminescent 10-methyl-acridinium-9-(N-sulphonylcarboxamide) salts. synthesis and kinetics of light emission[J]. J Biolumin Chemilumin,1991,6(2):107-114.
[6] Josefina M B, Neus G R. Evaluation of Ciba Corning ACS:180TMautomated immunoassay system[J]. Clin Chem,1994,40(3):407-410.
[7] Irena B, Brooks E, John C V. 1,2-Dioxetanes: novel chemiluminescencent enzyme substrates. Applications to immunoassays[J]. J Biolumin Chemilumin,1989,4(1):99-111.
[8] Schaap A P, Hashem A, Louis J. Chemiluminescencent substrates for alkaline phosphatase: application to ultrasensitive enzyme-linked immunoassays and DNA probes[J]. Clin Chem,1989,35(9):1863-1864.
[9] De Boever J, Mares A, Stans G,etal. Comparison of chemiluminescencent and chromogenic substrates of alkaline phosphatase in a direct immunoassays for plasma estradiol[J]. Analytica Chimica Acta,1995,303(1):143-148.
[10] Wood W G. Spiroadamantane dioxetane substrates stable label for luminescence-enhaced enzyme immunoassays[J]. J Clin Chem Clin Biochem,1990,28(7):481-482.
[11] Schaap A P, Akhavan H, Romanon L J. Chemiluminescent substrates for alkaline phosphatase:application to ultrasensitive enzyme-linked immunoassays and DNA probes[J]. Clin Chem,1989,35(9):1863-1864.
[12] Schaap A P, Detroit, Mich. Method and compositions providing enhanced chemiluminescence from 1,2-dioxetanes: US,5004565[P]. 1991-04-02.
Synthesisof1,2-DioxetaneChemiluminescenceReagent
JIAO Yan-hua1, GUO Wei-qiang1, HE Rui1, LIANG Yuan-yuan1, CHEN Can-yu1, ZHANG Peng-fei2
(1. Center for Biomedicine and Health, Hangzhou Normal University, Hangzhou 311121, China; 2. College of Materials and Chemical Engineering, Hangzhou Normal University, Hangzhou 310036, China)
The paper researched on the synthesis method of 1,2-dioxetane chemiluminescence reagent, discussed the effects of reaction temperature, reaction time and molar ratio of reactants on productivity. Under optimal experiment conditions, the productivity rate of methyl 3-hydroxybenzoate and 2-adamantanone via McMurry cross-coupling reaction exceeded 80% with TiCl4-Zn as the reductant.
chemiluminescence reagent; 1,2-dioxetane; synthesis
2012-03-12
国家自然科学基金项目(21005025); 浙江省公益技术应用研究资助项目(2010C33132).
焦艳华(1976—),女,副研究员,博士,主要从事化学发光免疫分析、功能性化合物的合成及应用研究.E-mail:yhjiao@hznu.edu.cn
11.3969/j.issn.1674-232X.2012.04.011
TQ421
A
1674-232X(2012)04-0342-04
