铬铁矿酸溶生产三价铬化合物
2012-10-17纪柱
纪 柱
(中海油天津化工研究设计院,天津 300131)
铬铁矿是制取各种铬化合物的唯一天然原料,其含铬成分称为铬尖晶石 (Mg,Fe)[Cr,Fe,Al]2O4,晶胞中Fe2+可被氧化,导致晶格畸变,稳定性下降,有利于铬尖晶石参与化学反应。从铬铁矿生产铬化合物的基本路线有下面3种。
第一种为碱性氧化路线,即铬铁矿同碱在空气或纯氧中反应,三价铬氧化为六价铬(铬酸钠),铬酸钠易制取重铬酸钠及其他价态的铬化合物。其中焙烧法由于具有良好的选择性,即矿石中仅铬以阴离子形式生成水溶性的铬酸钠,占铬铁矿质量1/2以上的杂质均以水不溶物残留在浸取渣中,致后续工艺变得简捷易行。此工艺路线已工业化200 a。目前碱性氧化路线所产铬化合物超过铬化合物总产量的95%。
第二种为高温还原路线,即铬铁矿在电炉内用焦炭还原制成碳素铬铁。全球工业开采的铬铁矿92%用于冶金,其中绝大部分消费在冶炼碳素铬铁。尽管目前碳素铬铁主要用于生产不锈钢,但由碳素铬铁硫酸溶解后制某些三价铬盐以及进而电解生产金属铬早已工业化;碳素铬铁经碱性氧化(无钙焙烧法、水热法)生产铬酸钠已完成工业试验。冶炼碳素铬铁无疑是铬铁矿的高效富集法,除铁外矿中杂质基本清除,故用碳素铬铁加工制铬化合物正引起学者的重视。
铬在铬尖晶石中处于三价态,占铬化合物消费量1/2以上的氧化铬、碱式硫酸铬,用作中间体的醋酸铬、氯化铬,以及正在医药、保健品和饲料添加剂、油气田开采等领域快速发展的氨基酸铬、有机酸铬均处于三价状态。故若由第一或第二种路线制取三价铬化合物,必须先对铬铁矿分别进行氧化制得铬酸钠或还原成碳素铬铁之后,再反过来将铬酸钠还原为三价铬或将碳素铬铁氧化为三价铬,这种价态的反复改变造成了资源、能源和人力的浪费。
第三种路线简称酸溶法,即铬铁矿直接同硫酸反应制得硫酸铬溶液,经分离杂质和复分解制成其他三价铬化合物,铬的价态不变。此法理论上最为合理,只需酸溶,无需氧化或还原等反应激烈工序。但因铬尖晶石极耐化学侵蚀,即使用过量沸腾浓硫酸长时间反应亦难以全溶;而且矿中杂质除硅不溶外,铁、铝、镁等亦同时酸溶,而溶液中三价的铬、铁、铝离子由于离子半径和电负性近似,许多化学性质相差无几,难以廉价高效分离,致使得到的硫酸铬无论在品质上还是在成本上均无法与第一种路线竞争,故迄今此工艺尚未工业化。但随着科学的发展和节能降耗的要求越来越高,酸溶法重新得到重视,并出现了一些新技术。
1 铬铁矿酸溶
铬尖晶石耐化学侵蚀,常用的强酸如硫酸、盐酸、硝酸在常压和沸点难以将其全溶,磷酸、磷酸加硫酸的混酸在沸点虽可使铬铁矿全溶,但磷酸根难以分离,且不免生成难溶的磷酸盐或焦磷酸盐,不利于制取纯净的铬化合物。
E.Vardar 等[1]曾引述 W.J.Biermann 等[2]研究了硫酸对铬铁矿的侵蚀作用,反应机理为质子H+攻击铬铁矿晶格,使金属成分依它们在晶格中占据的同样比例进入溶液;随着硫酸浓度的增加形成水及酸均不溶解的多核产物(包括硫酸铬沉淀)。A.M.Amer[3]研究了硫酸加压浸取铬铁矿,得到的最佳条件为:铬铁矿粒度小于64 μm,用质量分数为50%的硫酸于250℃浸取30 min。
如果在强酸中加入具有氧化作用的催化剂,则铬铁矿得以较快、较完全地溶解。其原因之一是铬尖晶石中的Fe2+首先被氧化为Fe3+,致晶格畸变而稳定性下降,易被酸侵蚀。文献所用催化剂均为常用氧化剂,其催化首先表现在氧化作用,但氧化的效果常大于作为单纯氧化剂的效果,故本文采用催化-氧化剂连用的写法。
高氯酸就是这种催化-氧化剂的一例。高氯酸既是最强无机酸,又是极强的氧化剂,故常作为铬矿石化验用的溶剂之一,例如铬矿石分析的国际标准ISO 6130—1985《铬矿石总铁含量的测定——还原滴定法》就是用硝酸、硫酸和高氯酸的混酸溶解铬铁矿后测定矿中总铁。但是高氯酸易挥发,高氯酸同铬生成剧毒的气体氯化铬酰CrO2Cl2导致铬挥发损失。另外高氯酸价格高昂,少量用作催化剂尚可,大量用作溶剂不适于工业生产。
E.Vardar等[1]使用表1组成的南非铬铁矿同硫酸、高氯酸于140~210℃进行反应,研究了硫酸铬生成动力学,查明反应的控制步骤为界面化学反应,使用质量分数为82%的硫酸于140~210℃的反应活化能为77 kJ/mol,得出铬溶浸的最佳条件:1)仅使用硫酸时,在硫酸质量分数为77%、固液质量比为1∶25、210℃浸取 6 h条件下,铬的浸出率为 66%;2)加高氯酸(HClO4质量分数为70%)时,在硫酸质量分数为82%、固液质量比为1∶25、高氯酸体积(mL)与铬铁矿质量(g)的比值取0.5、210℃浸取6 h条件下,铬可全溶。
A.Geveci等[4]也用硫酸、高氯酸对表 1 组成的土耳其铬精矿进行了溶解研究,得出以下结论:1)无高氯酸时,在硫酸体积分数为70%、于175℃浸取2 h条件下得到最大铬收率约58%;2)加高氯酸时,当高氯酸体积(mL)与铬铁矿质量(g)之比为0.5,在相同硫酸浓度和温度浸取2 h,得到最大铬收率约83%;3)无论有无高氯酸,铬收率均低于E.Vardar等[1]得到的收率;4)高氯酸能使部分三价铬氧化,既使是最大收率时,溶液中六价铬浓度依然很低;5)加高氯酸条件下,铬收率最大的固体渣经X射线衍射分析证明存在明显量的固体硫酸铬Cr2(SO4)3。

表1 南非铬铁矿和土耳其铬精矿组成%
同样使用硫酸和高氯酸溶解铬铁矿,A.Geveci等[4]的铬收率低于E.Vardar等[1],其原因 A.Geveci等[4]认为是所用土耳其铬精矿的组成与南非铬铁矿不同,土耳其矿MgO和SiO2含量高于南非矿。但根据后面第3节介绍可推定更主要的原因是南非矿的亚铁(FeO)含量是土耳其矿的3.2倍,在高氯酸作用下,亚铁氧化引起南非矿铬尖晶石晶格畸变更大,更不稳定,更易溶解。
John C.Stauter 等[5]研究了用海锰核(深海底发现的球核状锰矿)或天然锰矿为催化-氧化剂,对铬铁矿进行硫酸溶解试验。10 g铬矿与海锰核(MnO2质量分数为28.3%)混磨至粒径小于220 μm,海锰核与铬矿的质量比取(0.1~1)∶1。与不同量浓硫酸在烧杯中混匀,然后置于罐炉于350~400℃加热10 min至水分蒸发刚冒出硫酸烟雾时停止加热。冷至60℃并在此温度浸取搅拌3 h。海锰核与铬矿的质量比为1∶1时随硫酸量及温度不同铬浸出率为81.9%~100%。经核算,海锰核中二氧化锰同时发挥了催化剂及氧化剂作用,致被氧化的三价铬高达(二氧化锰仅为氧化剂)理论量的2倍。
前引文献中提到在高浓度硫酸中无水硫酸铬溶解性低,A.Geveci等[4]在溶解后的渣中证实存在固体 Cr2(SO4)3,这些不溶物必然不同程度地滞留在反应界面(待反应的铬尖晶石表面),不利于铬铁矿进一步溶解。与铬铁矿酸溶性类似的碳素铬铁,在硫酸中溶解时亦有硫酸铬沉淀,为防止沉积,Bruno München Wenzel等[6]在高碳铬铁生产鞣革剂硫酸铁和硫酸铬的研究中,使用了硫酸铵同硫酸铬形成易水溶的铬铵矾,当碳素铬铁用质量分数为75%的硫酸于170℃溶解2 h,若加入生成铬铵矾理论量100%的硫酸铵时,铬溶出率由不用硫酸铵时的87.5%增大到接近100%;铁溶出率亦有增加。预计在铬铁矿酸溶时,硫酸铵理应有同样的催化作用。
2 铬酸酐在铬铁矿酸溶时的催化-氧化作用
铬铁矿酸溶使用最多的催化剂是价格廉宜又不带入杂质的铬酸酐。实际上不用硫酸只用铬酸水溶液亦可溶解铬铁矿,如:1974年美国专利(US, 3787555),将铬铁矿在空气中预氧化,使90%的Fe2+氧化为Fe3+,然后同质量分数为50%的CrO3水溶液于沸点反应24 h,铬铁矿分解率为76%。
波格达洛夫[7]引述,早在1940年前苏联应用化学杂志就报道,将粒度为2.0 mm的铬精矿1 t,用质量分数为60%的硫酸3.78 m3和催化剂铬酸酐11.72 kg于140~150℃溶浸,滤液进行阳极氧化、蒸发析出晶体铬酸酐,离心过滤得到0.4825 t铬酸酐,铬收率为68.3%。
E.Vardar等[1]引述了 R.R.Lloyd 等[8]制电解铬的半工业试验,即铬铁矿用质量分数为40%的硫酸溶液于130~160℃的热压釜内溶浸,加2.5%~3.0%(质量分数)的铬酸(H2CrO4)作催化剂。
史培阳等[9]用质量分数为60%~95%的硫酸于110~170℃同铬铁矿反应,铬铁矿粒度为0.05~0.09 mm,硫酸质量为铬铁矿质量的的1~4倍,用重铬酸钠为催化剂,其量为铬铁矿质量的4%~20%,反应时间为1~8 h,经过滤、除铁、调碱度、干燥得到碱式硫酸铬,铬收率为79%~82%。
刘承军等[10]研究了硫酸加入量对铬铁矿硫酸浸出行为的影响,使用Cr2O3质量分数为40.0%、总Fe质量分数为7.7%的巴基斯坦铬铁矿,铬铁矿与硫酸的质量比取1.5~3.0,加入铬铁矿质量5%的铬酸酐作催化剂,于160℃反应60 min。其结论:随着硫酸用量的增加铬浸出率逐渐增大,铬铁矿与硫酸的质量比为3.0时铬浸出率为98.5%[11];但铁的浸出率随着硫酸用量的增加先增加后减小,在铬铁矿与硫酸的质量比 2.5时呈现极大值 70.1%[10]或71.9%[11]。
刘承军等[12]采用水热法溶解铬铁矿。例如:粒度为100 μm的铬铁矿(Cr2O3质量分数为40.0%、Fe2O3质量分数为11%),加入质量分数为68%的硫酸,其量为铬矿质量的1.0倍,加入铬矿质量3.2%的铬酸酐作催化剂,于155℃、0.7 MPa压力下反应60 min,搅拌速度为250 r/min。反应完成后用板框压滤机于1.6 MPa过滤,滤渣中铬的质量分数低于0.3%。
以上使用铬酸酐作催化剂的文献既未说明铬酸酐用量的依据,亦未说明铬酸酐加入量与铬收率之间的关系,且各文献用量极不一致。波格达洛夫[7]认为,前引铬精矿用硫酸和铬酸酐溶浸的铬收率过低(68.3%)的原因是铬酸酐用量太少,只占铬精矿质量的1.17%,或者对于铬精矿中FeO质量来说,仅为后者的8.64%,而按照下面所示的反应式:
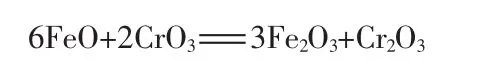
要将1 g FeO氧化为Fe2O3,需用0.464 g铬酸酐,因此,波格达洛夫提出铬酸酐的用量必需为铬矿中FeO质量的70%~100%,才能将铬铁矿充分溶解得到高收率。
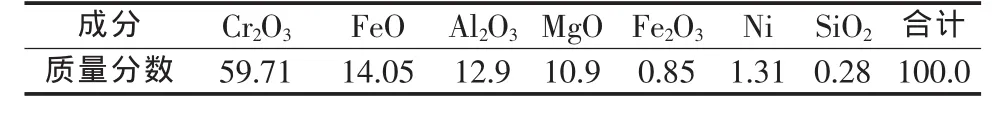
表2 重选得到的铬精矿 %
波格达洛夫[7]利用重选得到的铬精矿1000 g(组成见表 2)进行了一批试验,铬精矿粒度为2.0 mm,用3.7 L质量分数为60%的硫酸和不同量铬酸酐组成的溶液于140~150℃溶浸,然后离心分离、洗涤。当铬酸酐加入量相对于铬精矿中FeO质量分数分别为9.11%、66.2%、70.0%、99.64%、100.8%、106.8%时,铬收率分别为65.8%、75.0%、78.4%、86.48%、86.58%、86.67%。数据说明,催化剂铬酸酐用量如果与铬矿中FeO质量相同,铬浸出率超过86%。
3 从浸出液中分离铬
3.1 脱硅
将硫酸浸取后的悬浮液过滤、洗涤可以滤除不溶物,包括未溶解的铬铁矿、石英SiO2,以及酸溶过程中副产的不溶物,如某些硅酸盐类脉石酸溶后生成的水合硅酸及其盐,可以阻止硅进入浸出液。
3.2 除铁
滤除不溶物后的滤液主要成分为铬、铝、镁、铁的硫酸盐,若能除去铁,调整碱度后经蒸发浓缩、喷雾干燥可制得铬鞣革剂,这样得到的铬鞣革剂除含碱式硫酸铬外,尚含铝和镁,铝也有鞣革作用,镁对鞣革无害。史培阳等[9]在溶解铬铁矿后的滤液中加碳酸钠调游离碱至2.3%(质量分数),加氧化钙加热反应,过滤除去含铁渣,滤液加碳酸钠调碱度,干燥得到碱式硫酸铬,产品的组成未交待。史培阳等[13]在7 a后公开的另一专利改用萃取分离法,即向Cr、Fe质量分数分别为7%、4%的硫酸铬和硫酸铁混合液中加入混合液体积30%的萃取剂十八烷基二甲基叔胺进行萃取,分层后硫酸铬进入水相,硫酸铁进入有机相。水相直接结晶得到硫酸铬产品,含Cr2O3质量分数≥30%,含水不溶物、氯化物质量分数均≤0.01%,含Fe质量分数≤0.005%。有机相用氢氧化钠反萃后制成氧化铁红颜料,颜料含Fe2O3质量分数≥96%。
3.3 盐析法分离紫色硫酸铬
溶液中的硫酸铬因水合形式不同而有多种形态,10~30℃有利于生成紫色的六水合硫酸铬[Cr(H2O)6]2(SO4)3。 紫色盐在水中溶解度大,而在盐析剂与水的混合溶剂中溶解度小。硫酸铁恰好相反,故加入盐析剂并熟化后,硫酸铬可同硫酸铁盐析分离。例如,硫酸铬与硫酸铁的混合溶液含Cr质量浓度为40.6 g/L、Fe质量浓度为15.0 g/L,pH约为1,在15℃振动熟化24 h,硫酸铬几乎100%转化为紫色盐。加入盐析剂即99.5%乙醇 (约为溶液质量的50%),于20℃振动4 h,紫色盐便盐析出来。分离后铁及其他金属杂质的硫酸盐留在母液中,滤饼即紫色盐析物于150℃干燥24 h,产品含Cr质量分数为25.77%、Fe质量分数为 0.36%,以 Cr2(SO4)3计的纯度为97.13%,铬收率为96.41%。反复多次盐析及分离,硫酸铬纯度还可进一步提高[14]。
3.4 以六价铬形式分离
脱硅后的含 Cr、Fe、Al、Mg 等阳离子的滤液,若能将铬转变为阴离子,则其他阳离子的分离便易于完成。 John C.Stauter等[5]以二氧化锰作催化-氧化剂,用硫酸溶解铬铁矿后的浸出液中的铬为六价铬(可补加二氧化锰将浸出液中残存的三价铬离子继续氧化),溶液用萃取剂(体积组成为5%三辛叔胺溶液、5%起乳化作用的磷酸三丁酯、90%的煤油)萃取,六价铬进入有机相,分离后的有机相用水洗涤残留锰和铁。有机层用氢氧化铵水溶液将铬洗脱,得到铬酸铵。波格达洛夫[7]将铬精矿用硫酸、铬酸酐溶液溶浸,滤洗后溶液用装有隔膜和铅阳极的电解槽于30~50℃电解。电解完成液于140~150℃蒸发至硫酸质量浓度为1100 g/L,铬酸酐即结晶析出,离心分离,滤饼于140~150℃用硫酸(质量浓度为1140 g/L)洗涤。晶体铬酸酐于150℃干燥即为产品,其CrO3质量分数为99.73%,SO42-质量分数为0.15%,不溶物质量分数为0.10%,铁、铝、镁、镍等氧化物杂质质量分数为0.02%,符合俄罗斯标准。
3.5 参考碳素铬铁酸溶后的铬铁分离经验
碳素铬铁硫酸溶解时,生成硫酸铬与硫酸亚铁的溶液,一般采用莫尔盐法将硫酸铬与硫酸亚铁分离。例如,邬建辉等[15]在溶液pH为0.5、硫酸铵过量系数为3.0、Cr3+质量浓度为70 g/L左右、Fe2+质量浓度为5~20 g/L以及温度为70℃的条件下反应6 h,然后快速冷却结晶24 h,将析出的晶体硫酸亚铁铵[Fe(NH4)2(SO4)2·6H2O]过滤,除铁率达到 96.52%,铬损失只有1.85%。
北京有色金属研究总院提出用萃取法从碳素铬铁硫酸浸出液中回收铬。例如,含Cr3+质量浓度为60~80 g/L、Fe2+质量浓度为25 g/L的硫酸盐溶液,用伯胺 R,R′-CH-NH2作萃取剂 (R、R′代表 C8至 C12的烷基,平均相对分子质量为372),煤油作稀释剂并加5%(体积分数)的混合醇,萃取剂体积分数为25%~30%。于最佳pH(2~3)萃取,硫酸亚铁不被萃取,分离因子>200。进入有机相的 Cr3+用 2.5~3.0 mol/L的H2SO4反萃取,反萃率>98%,得到含Cr3+质量浓度为50 g/L、Fe质量浓度<0.05 g/L的硫酸铬溶液。
胡国华[16]利用草酸作亚铁的沉淀剂,可与三价铬高效分离。将高碳铬铁硫酸溶解后的溶出液先用氨水调pH至3,加入草酸,使铁以草酸亚铁沉淀同硫酸铬溶液分离;滤液再用氨水调pH至9,得到氢氧化铬沉淀,经过滤、洗涤、干燥后煅烧得到氧化铬,其含Fe质量分数为0.2%,铬收率为98%。
韩登仑等[17]用无钙焙烧渣制得的碳素铬铁硫酸溶出液生产草酸亚铁,实现铬铁分离。将含有硫酸铬和硫酸亚铁的溶出液加到饱和的热草酸溶液中,得到含草酸亚铁99.0%(质量分数)的产品。往含少量Fe3+和Fe2+的硫酸铬滤液中加适量金属铬细粉,将Fe3+还原为Fe2+,加入氢氧化钠溶液至pH为7,生成氢氧化铬沉淀,加絮凝剂后滤洗,得到的氢氧化铬含Cr2O3质量分数为53.7%,含铁(以Fe2O3计)质量分数<0.1%。
铬铁矿酸溶后,溶液中的铁为三价,要利用上述技术以亚铁形式同铬分离,只需在铬铁矿直接酸溶后仍含过量硫酸的溶液中加入适量粉状碳素铬铁或金属铬,反应析出的原子氢足以将溶液中的Fe3+还原为 Fe2+。
4 讨论
综上所述,提高铬收率及铬铁分离已取得新进展,若能进一步深入研究,可望不久的将来实现酸溶法工业化。所引文献中以下各项更为可取:1)选用品位(Cr2O3)高,亚铁含量多,铝、镁、硅少的铬精矿进行酸溶;2)使用硫酸、铬酸酐混合溶液作浸取剂,尝试用硫酸铵防止无水硫酸铬沉积在反应界面;3)向悬浮液中加入粉状高碳铬铁,借助高碳铬铁酸溶生成的原子氢将Fe3+还原为Fe2+,分离不溶物后的滤液以草酸为沉淀剂,使亚铁生成FeC2O4沉淀;4)滤除FeC2O4后的滤液同碱反应,生成铬和铝的氢氧化物沉淀,沉淀同氢氧化钠反应,将氢氧化铝以铝酸钠形式溶解分离后,经晶种分解制得氢氧化铝产品;5)滤洗后的氢氧化铬经煅烧制成氧化铬,或酸溶制成相应酸的三价铬盐。
[1]Vardar E,Eric R,Letowski F.Acid leaching of chromite[J].Miner.Eng.,1994,7(5/6):605-617.
[2]Biermann W J,Heinrichs M.The attack of chromite by sulphuric acid[J].Can.J.Chem.,1960,38(9):1449-1454.
[3]Amer A M.Processing of Ras-Shait chromite deposits[J].Hydrometallurgy,1992,28(1):29-43.
[4]Geveci A,Topkaya Y,Ayhan E.Sulfuric acid leaching of turkish chromite concentrate[J].Miner.Eng.,2002,15(11):885-888.
[5]Stauter John C,Um Richard T.Recovery of chromium values:US, 4029734[P].1977-06-14.
[6]Bruno München Wenzel,Nilson Romeu Marcilio,Marcelo Godinho,et al.Iron and chromium sulfates from ferrochromium alloy for tanning[J].Chem.Eng.J.(Amsterdam,Netherlands),2010,165(1):17-25.
[7]波格达洛夫.铬酸酐制法:RU, 2349551[P].2009-03-20.
[8]LloydRR,Rosembaum JB,Homme VB,etal.Pilo-plamt production of electrolytic chromium[J].Trans.Electrochemical Soc.,1948,94(3):122-138.
[9]史培阳,姜茂发,刘承军.一种碱式硫酸铬的制备方法:中国, 1526646A[P].2004-09-08.
[10]刘承军,史培阳.硫酸加入量对铬铁矿硫酸浸出行为的影响[J].工业加热,2011,40(3):59-60,76.
[11]Liu Chengjun,Qi Jie,Jiang Maofa.Experimental study on sulfuric acid leaching behavior of chromite with different temperature[J].Advanced Materials Research(Durnten-Zurich,Switzerland),2012,361-363 (Pt.1,Natural Resources and Sustainable Development):628-631.
[12]刘承军,史培阳,姜茂发.一种硫酸浸出处理铬铁矿的方法:中国, 101979679A[P].2011-02-23.
[13]史培阳,刘承军,姜茂发.由多组分溶液中分离铬离子和铁离子的方法:中国, 101974688A[P].2011-02-16.
[14]悦周,熊谷幹郎,高岛洋一.铬的分离回收方法:日本公开,平 8157219[P].1996-06-18.
[15]邬建辉,阳伦庄,湛菁,等.铬铁合金中铬、铁分离研究[J].湿法冶金,2011,30(1):51-56.
[16]胡国华.一种从碳素铬铁中生产三氧化二铬和草酸亚铁的方法:中国, 101041466A [P].2007-09-26.
[17]韩登仑,张忠元,何喜善,等.用无钙铬渣生产草酸亚铁副产金属铬和铬酸的方法:中国, 101445446B[P].2011-05-25.
