微米级壳聚糖微球的制备
2012-09-25陈宇,刘兆丽,吴庆辉
陈 宇, 刘 兆 丽, 吴 庆 辉
( 大连工业大学 轻工与化学工程学院, 辽宁 大连 116034 )
0 引 言
壳聚糖是自然界中唯一的碱性多糖,因其高安全性、良好的生物相容性以及黏合性、血液相容性、微生物可降解性等优良性能而在食品、医药等领域得到了广泛的应用[1-2]。将壳聚糖作为载体,一是由于它具有亲水性,可以延长药物微球在体内的循环时间,减少被巨噬细胞捕获,从而提高药物有效利用度;二是因其具有高的药物的包封率和载药量[3-4]。但是目前对于制备壳聚糖微球[5-6]的研究还较少,本实验研究的壳聚糖微球是以壳聚糖作为载体,将药物包敷在微球中,起到控释和缓释效应,并因其对特定器官和组织的靶向性而有效地作用于生物体内[7]。
本实验通过反相悬浮交联的方法,采用液体石蜡为分散介质,经甲醛和戊二醛交联制备微米级窄分布的壳聚糖微球。探讨了影响微球制备的主要因素,得出了较佳的制备条件,为壳聚糖微球的成型加工提供了一定的参考依据。
1 实 验
1.1 试 剂
壳聚糖(大连勃达生物科技有限公司,脱乙酰度>90%),戊二醛、甲醛、液体石蜡、煤油、乙酸乙酯、Span-80、冰乙酸、无水乙醇、氢氧化钠,均为AR级。
1.2 壳聚糖微球的形成机理
在含有表面活性剂中的有机溶剂中,在机械搅拌同时滴入壳聚糖溶液,经分散形成以壳聚糖为内相的W/O型乳液,然后通过甲醛或戊二醛进行内相的化学交联固化并分离制备微球。
1.3 制备方法
配制一定浓度的壳聚糖-乙酸溶液,静置2 d以上待用;于250 mL三口烧瓶中,分别加入油相液体石蜡、乳化剂Span-80,搅拌0.5 h后加入配制好的壳聚糖溶液,并调节一定的搅拌转速使其形成乳液。升温至60 ℃,加入一定量的甲醛溶液,将pH调至9后反应0.5 h,然后加入一定量的戊二醛,升温至80 ℃后再反应1 h。将溶液过滤并用煤油充分洗涤。用无水乙醇于索氏提取器中抽提24 h以去除残留的有机物。在烘箱中80 ℃ 烘至恒重,最后将干燥后的产物研磨成均匀的粉末,即可得壳聚糖微球。
1.4 性能测定
1.4.1 微球形貌观察及统计分析
取一定的干燥后的微球,真空镀金(壳聚糖是非导电体,需喷金)后用扫描电镜进行形貌观察。并选取任意区域的微球作为样本(至少30个),测定其直径,参照下述公式计算平均粒径d和分散度DP。
DP=δ/d
式中,di为单个微球的粒径,μm;d为平均粒径,μm;n为微球的个数;DP为分散度。
1.4.2 红外吸收光谱法分析
取1 mg左右的样品与100 mg干燥的溴化钾粉末研磨混合均匀后,将混合物放入特定的模子中压制成薄片,即可测定其红外吸收光谱。
1.4.3 吸附行为的表征
称取一定量干燥后的微球(m0),用吸油纸包好,然后将其完全浸入装有薄荷油的小烧杯中,每隔2 min测定微球的质量m,按下式计算微球的吸油率L。
L=(m-m0)/m0
2 结果讨论
2.1 壳聚糖和液体石蜡溶液两相体积比对微球制备的影响
其他实验条件不变,改变液体石蜡和壳聚糖溶液两相的体积比进行实验,结果见图1。由图1可知,随着液体石蜡和壳聚糖溶液体积比的增大,产物形状不规则;随着两相体积比的减小,所得微球的形状规则程度增加,微球尺寸也较均匀,但也不应过小。由图1(d)可知,当体积比小于1∶1.5时,微球的形状规则度下降且粒度偏细。可见两相体积比应控制在1∶1~1∶1.5。

图1 液体石蜡和壳聚糖溶液两相体积比对微球制备影响的SEM照片
Fig.1 SEM photograph of volume ratio of liquid paraffin and the chitosan solution on the preparation of chitosan microspheres
2.2 乳化剂用量对微球制备的影响
乳化剂的使用可以增强反应体系中形成的微乳滴在未固化交联之前的稳定性,使其保持较好的球体形态,且乳滴间不会发生相互黏着而导致乳液的破乳和聚并。乳化剂Span-80用量对微球形态的影响如表1所示。由表1可见,乳化剂Span-80使用量增大,可以提高微球形成的均匀性并减少微球间的黏着,乳化剂的最佳用量为9.0 mg/mL。
表1 Span-80质量浓度对微球制备的影响
Tab.1 The effect of Span-80 concentration on the preparation of the chitosan microspheres

ρ(Span-80)/(mg·mL-1)产物成球性2.3-4.5+6.8++ 9.0++注:-,成球性差,黏着严重,有不规则物;+,成球一般;++,成球均匀。
2.3 交联剂的种类及用量对微球制备的影响
为了得到具有一定刚性的壳聚糖微球,需要加入交联剂进行交联固化,选用甲醛和戊二醛作为交联剂,考察其用量对微球成形的影响,实验结果见表2。由表2可知,戊二醛的使用量对微球的形成有较大的影响,随着戊二醛用量增加,壳聚糖交联程度逐步增大。但戊二醛用量过多时,产物聚集严重,甚至相互粘连在一起难以分散开。甲醛的用量对产物特性影响较小。当戊二醛与壳聚糖溶液的体积比为1∶20时,不同甲醛用量均可得到形态较好的微球,因此选择戊二醛作为交联剂,其较佳戊二醛与壳聚糖溶液的体积比为1∶20。
表2 交联剂用量对壳聚糖成球特性的影响
Tab.2 The effect of crosslinker agent on microsphere formation of chitosan

V(甲醛)/V(壳聚糖溶液)V(戊二醛)/V(壳聚糖溶液)产物成球性01∶20++1∶100+1∶101∶8-1∶101∶10±1∶101∶20++1∶201∶20++注:++,成球均匀;+,成球一般;-,成球性差,黏着严重,有不规则物。
2.4 壳聚糖溶液质量分数对微球制备的影响
壳聚糖溶液的质量分数为1.5%、2.0%、2.5%、3.0%、3.5%、4.0%、4.5%、5.0%时,微球的平均粒径及分散性如图2所示。由图2可见,随着壳聚糖溶液浓度逐渐增大,微球的粒径逐渐变大,粒径分散度下降,即提高了成球性和均匀性。由于高浓度壳聚糖溶液黏度较大,致使微球互相聚集、不易分散。但高浓度下微球粒径的分散度减小,可获得粒度(平均粒径)均匀、单分散性(单位表面积中微球的分散性)好的微球。综合考虑,壳聚糖溶液质量分数为4.5%时较为理想。

图2 壳聚糖质量分数对壳聚糖微球的平均粒径、分散度的影响
Fig.2 The effect of chitosan concentration on the chitosan microspheres average particle size and its dispersity
2.5 搅拌速度对微球制备的影响
搅拌速度对微球形成的影响如图3所示,搅拌速度增加,制得的微球粒径逐渐变小。同时提高搅拌速度一定程度上能明显降低分散度,增加微球的均匀性且保持产物呈规整球形。搅拌速度很小时,难以使壳聚糖溶液分散均匀,得到的微球呈现皱缩形貌。当搅拌速度增加时,在形成乳液过程中,壳聚糖溶液被分散形成的液滴越来越小,所以使交联固化后得到的微球尺寸也变小。因此制备微米级窄分布壳聚糖微球的搅拌转速需大于800 r/min。

图3 搅拌速度对壳聚糖微球的平均粒径及分散度的影响
Fig.3 The effect of stirring speed on the chitosan microspheres average particle size and its dispersity
2.6 微球的红外光谱分析
交联壳聚糖微球和原壳聚糖的红外光谱如图4所示,经交联后在1 310 cm-1处的特征峰表明了产物仍有乙酰氨基的存在,同时原料壳聚糖1 587 cm-1处氨基的变形振动特征峰消失,表明壳聚糖的氨基参与了反应,从而证明其与戊二醛交联生成西佛碱反应的发生。
2.7 微球的形貌及吸附性能
选取最佳条件下制备的壳聚糖微球,测定其微观形貌(图5)及对薄荷油的吸附能力(图6)。由图6可见壳聚糖微球具有一定的吸附能力,在吸附初期吸附速度非常快,到4 min左右即接近饱和吸附,然后吸附曲线趋于平缓,符合吸附的一般规律。但其吸附能力并不是特别强,在后续研究中可以通过致孔剂的应用增加微球的孔隙率,从而进一步提高其吸附能力。

图4 原壳聚糖(a)及壳聚糖微球(b)的红外光谱图
Fig.4 IR spectra of the original chitosan (a) and chitosan microspheres (b)

图5 壳聚糖微球的SEM照片
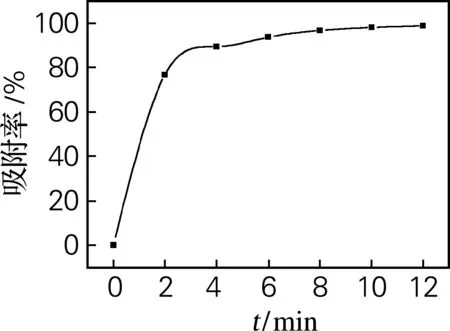
图6 壳聚糖微球对薄荷油的吸附曲线
Fig.6 Adsorption curve of the chitosan microspheres on the peppermint oil
3 结 论
采用反相悬浮交联法微米级窄分布的壳聚糖微球,其最佳制备条件为壳聚糖溶液质量分数为4.5%、油相液体石蜡和水相壳聚糖溶液的两相体积比1∶1.5、Span-80在油相中的质量浓度9.0 mg/mL,选用戊二醛作为交联剂,其体积与壳聚糖溶液的体积比1∶20,在高于800 r/min的搅拌转速下进行反应,所得产物是分布较窄的微米级壳聚糖微球。从微米级壳聚糖吸附性能的初步研究中看出,其吸附能力有一定的局限性,可以通过致孔剂的应用,增加壳聚糖微球的孔隙率,进一步提高壳聚糖微球的吸附能力。
[1] 杨东坡,史志铭,董香萍. 壳聚糖的应用现状及前景分析[J]. 内蒙古水利, 2007(3):167-168.
[2] 张步宁,崔英德,陈循军,等. 甲壳素/壳聚糖医用敷料研究进展[J]. 化工进展, 2008, 27(4):520-521.
[3] 蒋刚彪,张余,刘慧,等. 壳聚糖作为药物载体的应用[J]. 西部药学, 2007, 4(1):27-28.
[4] SINHA V R, SINGLA A K, WADHAWAN S, et al. Chitosan microspheres as a potential carrier for drugs[J]. International Journal of Pharmaceutics, 2004, 274(1/2):1-33.
[5] BANERJEE T, MITRA S, SINGH A K, et al. Preparation, characterization and biodistribution of ultrafine chitosan nanoparticles[J]. International Journal of Pharmaceutics, 2002, 243(1/2):93-105.
[6] 刘慧. 壳聚糖微球/纳米粒的制备及其性能研究[D]. 杭州:浙江大学, 2007.
[7] 车小琼,孙庆申,赵凯. 甲壳素和壳聚糖作为天然生物高分子材料的研究进展[J]. 高分子通报, 2008 (2):45-46.
