穿心莲有效部位Poloxamer188聚合物胶束的制备工艺
2012-04-06王钰涵
刘 蕾,王钰涵,韩 光,张 瑜
(河南大学 药物研究所,河南 开封 475004)
穿心莲有效部位Poloxamer188聚合物胶束的制备工艺
刘 蕾,王钰涵,韩 光*,张 瑜
(河南大学 药物研究所,河南 开封 475004)
目的制备Poloxamer188穿心莲有效部位的聚合物胶束。方法薄膜水化法制备穿心莲有效部位聚合物胶束,正交设计优化处方工艺。HPLC法测定其载药量和包封率,激光粒度仪测定粒径。结果载药胶束包封率为(85.7+2.1)%,载药量为(1.11+0.09)%,粒径为(198.32+3.35)nm。结论载药Poloxamer188胶束制备工艺简便易行,为中药制剂提供了新剂型。
穿心莲有效部位;Poloxamer188;聚合物胶束
穿心莲是我国治疗肺部感染疾病的传统中药,早在两千多年前,印度就有用穿心莲治疗肺部肿瘤的记载。现代研究表明[1-4],穿心莲提取物及以穿心莲内酯为代表的二萜内酯类成分具有广谱的抗肿瘤活性。穿心莲内酯类化合物主要通过细胞毒作用、诱导肿瘤细胞凋亡、阻滞细胞周期G0/G1期、抑制新生血管的形成及免疫调节等多种途径发挥抗肿瘤作用,从而被认为是一类重要的抗肿瘤候选药物[5-9]。穿心莲多采用乙醇法提取。近年来葛发欢、范云鸽等[10-11]报道了超临界CO2萃取和大孔吸附树脂富集穿心莲二萜内酯类成分的新方法,2种方法均使穿心莲内酯、脱水穿心莲内酯含量提高。
聚合物胶束是两亲性聚合物在水溶液中通过分子自组装原理形成的粒径均一、具有核壳结构的微粒,通过将难溶性抗肿瘤药物包载于胶束的疏水内核实现增加溶解度和肿瘤靶向性的目的,作为一种新型的药物传输系统日益引起人们关注[12-13]。
Poloxamer是目前最常用的聚合物胶束制剂材料之一,其结构为聚氧乙烯-聚氧丙烯-聚氧乙烯(PEO-PPO-PEO)三嵌段共聚物,可在水溶液中自发形成胶束。疏水嵌段PPO形成内核,PEO嵌段环绕在外形成外壳,不仅能增溶难溶性药物,还具有逆转肿瘤多药耐药性的作用[14]。
我们以Poloxamer188为载体材料,采用薄膜水化法制备穿心莲有效部位胶束。以有效部位中主要有效成分穿心莲内酯的包封率、载药量和粒径为评价指标,通过正交设计法优化得到最佳处方和制备工艺。
1 材料
1.1 药品和试剂
泊洛沙姆188(Pluronic F68,BASF);穿心莲有效部位(自制,HPLC法测定含量,其中含穿心莲内酯40.56%,脱水穿心莲内酯10.89%,14-去氧穿心莲内酯5.83%);对照品穿心莲内酯(中国药品生物制品检定所)。甲醇(CR,天津四友精细化学品有限公司);乙腈(CR,天津四友精细化学品有限公司)。
1.2 仪器
KQ-5200DA型双频数控超声波清洗器(昆山市超声仪器有限公司);旋转蒸发仪RE2000(上海亚荣生化仪器厂);SHZ-ⅢB循环水真空泵(上海仪表供应公司);日本岛津 LC-2010高效液相色谱仪(SEDEX蒸发光散射检测器,CLASS-VP色谱工作站);ZetasizerH-3000激光粒度测定仪 (英国马尔文公司)。
2 方法与结果
2.1 穿心莲有效部位聚合物胶束的制备
称取处方量的Poloxamer 188和穿心莲有效部位于250mL圆底烧瓶中,加入12mL甲醇,超声使之完全溶解成为透明均一的溶液。于一定温度和压力下旋蒸去溶剂,在瓶壁上形成较为均匀的干燥薄膜。加入适量缓冲溶液,轻轻振荡使膜溶入其中。以保鲜膜封口,室温放置4h以上。0.22μm微孔滤膜过滤,得透明均一的浅黄色胶束溶液。
2.2 单因素考察
其他条件固定的情况下,改变单一因素(投料比、旋转蒸发温度、水化温度、水化时水相用量、水化pH),以包封率为主要考察指标来考察其处方和工艺。
2.2.1 投药量的影响 固定载体量为120mg,水化溶液量为7.5mL,考察投药量为6、8、10、12、15mg时包封率的变化。结果显示:在不同投药量时,其包封 率 依 次 为 58.6%、66.7%、88.1%、94.4%、77.3%。表明:随着投药量的增加,包封率增加,当投药量为12mg时达到最大值,后又开始下降。
2.2.2 旋转蒸发温度的影响 固定载体量为120mg,投药量为12mg,考察旋蒸温度为40、50、60、70℃时包封率的变化。结果显示:在不同旋蒸温度下,其包封率依次为24.7%、40.7%、68.8%、69.3%。表明:随旋蒸温度升高,包封率增加,70℃时达到最高。
2.2.3 水化温度的影响 固定载体量120mg,投药量为12mg,在70℃下蒸去溶剂,水化体积为7.5mL,考察水化温度为4、35、50℃时包封率的变化。结果显示:在不同水化温度下,其包封率依次为75.7%、83.5%、69.4%。表明:随着水化温度升高,包封率增加,35℃时最高为83.5%,温度继续升高,包封率反而降低,总体来看影响不显著。
2.2.4 水化用量的影响 固定载体量120mg,投药量为12mg,在70℃下蒸去溶剂,考察水化体积各为6、7、8、9、10mL在室温下水化的包封率变化。结果显示:在不同水化用量下,其包封率依次为64.4%、88.7%、70.1%、36.7%、73.6%。表明:随着水化用量增加,包封率增加,继续增加用量,包封率降低后又有增加,变化呈波浪式,其中水化体积7mL,包封率最大。
2.2.5 水化pH的影响 固定载体量120mg,投药量为12mg,在70℃下蒸去溶剂,考察水相缓冲溶液在pH7.29、6.48、5.04条件下室温水化的包封率变化。结果显示:在不同水化用量下,其包封率依次为63.2%、51.3%、54.6%。表明:随着水化pH 值的增加,包封率变化不大。
结果表明:投药量、旋蒸温度、水相用量对药物的包封率有显著的影响,故而将这3个因素取适当水平进一步优化处方工艺。水化温度对包封率的影响波度较小,结合实验操作的实际情况,选择各个因素水平均置室温下水化。水相pH对包封率影响亦不大,结合药物性状和应用最终选择pH7.2的缓冲溶液。
2.3 正交设计
选择对胶束形成有显著影响的3个因素:投料比(A),旋转蒸发温度(B),水相用量(C),每个因素选择3个水平,采用L9(33)正交表进行试验。因素与水平见表1。以包封率为考察指标优化处方工艺,试验结果见表2。
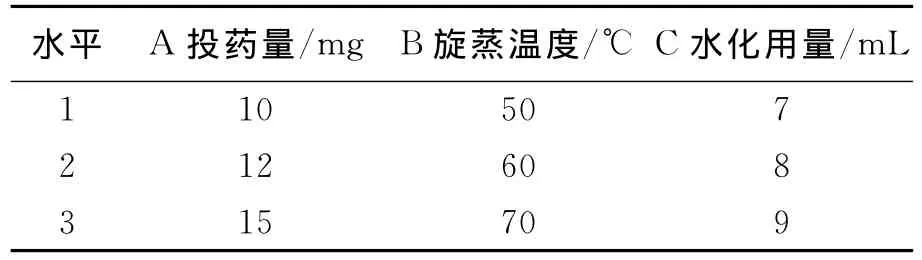
表1 因素水平表
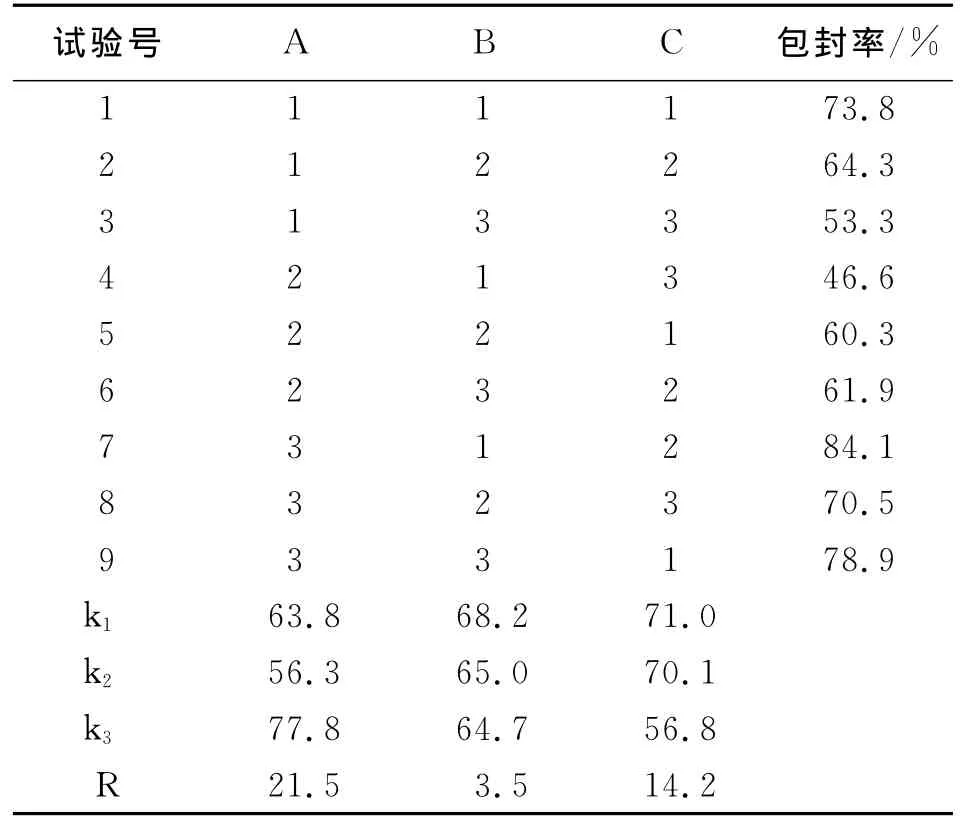
表2 正交试验结果
从分析结果可以看出,包封率的影响程度分别依次为A>C>B,即投药量对穿心莲有效部位胶束的包封率有十分显著的影响,水化用量的影响较小,旋蒸温度的影响不显著。穿心莲超分子的最佳因素水平组合为A3B1C1。综合考虑,投药15mg,于50℃下成膜,水相用量为7mL时,为聚合物胶束的最佳制备条件。
2.4 验证试验
按优化处方制备3批穿心莲有效部位聚合物胶束,测定包封率和载药量,结果见表3,包封率为(85.7+2.1)%,载药量为 (1.11+0.09)%。所得包封率和载药量均在理论预测范围内,表明优化处方重现性良好。
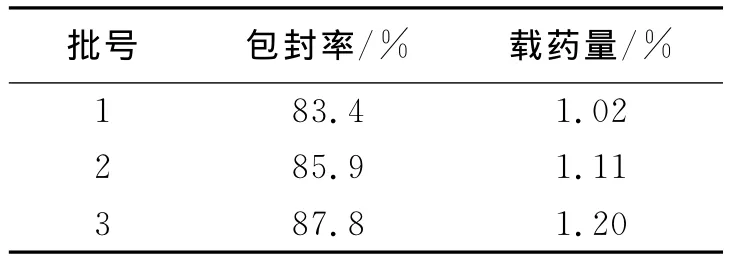
表3 优化条件的验证结果(n=3)
2.5 含量测定
2.5.1 对照品溶液的配制 精密称取对照品穿心莲内酯12mg,加甲醇适量,超声使溶解,冷却至室温后加甲醇定容至10mL。
2.5.2 色谱条件 色谱柱:Agliendt-ZORBAX Extent-C18(4.6mm×250mm,5μm);流动相:乙腈-水(30:70);流速:1.0mL/min;柱温:室温,理论塔板数以穿心莲内酯计不低于6000。
2.5.3 标准曲线的建立 取穿心莲内酯对照品溶液稀释10倍,分别进样2、4、8、10、15、20μL各2针,以进样量为横坐标,峰面积为纵坐标作标准曲线,求得回归方程为Y=659884 X-596486(r=0.9994)。结果表明:穿心莲内酯进样量在0.24~2.4μg范围内线性关系良好。
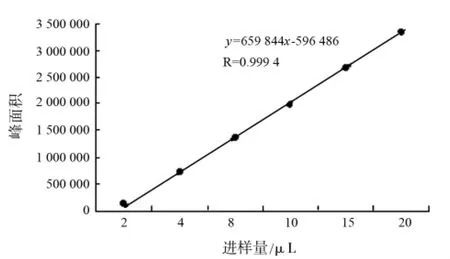
图1 穿心莲内酯的标准曲线
2.5.4 精密度试验 取穿心莲内酯对照品溶液10μL,连续进样5次,记录峰面积,计算日内精密度为0.9%;连续测定5d,计算日间精密度为1.0%。结果表明精密度良好。
2.5.6 加样回收率试验 按处方量的80%、100%、120%称取穿心莲有效部位适量,分别加处方比例的辅料,以甲醇溶解成为穿心莲内酯含量为0.48、0.60、0.72mg/mL的样品溶液,测定并计算得出穿心莲内酯的平均加样回收率为93.4%。该法的专属性、精密度及回收率均符合方法学要求。
2.6 包封率和载药量
采用微孔滤膜法测定。精密移取经0.22μm微孔滤膜过滤的载药胶束溶液50μL,置于10mL容量瓶中,用流动相将样品稀释刻度,混匀,在“2.5.2”项下色谱条件测定穿心莲内酯的含量,根据以下公式计算包封率和载药量:包封率(EE%)= Wi/Wt×100%,载药量(DL%)= Wi/(Wi+ Wc)×100%,其中Wt为投药量,Wi为胶束中被包封的药物量,Wc为poloxamer188的质量。
2.7 粒径测定
所得的胶束溶液无色透明。激光粒度仪测得其平均粒径为(198.32+3.35)nm。
3 讨论
以poloxamer188为载体材料,考察了注入法和薄膜水化法。结果表明,2种方法胶束包封率、载药量相似,但因注入法周期较长,不同人员操作时会带来一定的差异。故选择了制备工艺简单、周期短的薄膜水化法来制备载药聚合物胶束。
在胶束的制备过程中,单因素考察实验结果表明,影响穿心莲有效部位胶束包封率的主要因素有三个:投药量、旋转蒸发温度和水化体积。故可采用三因素三水平的正交设计表做处方优化。优化的制备条件重现性好,包封率为(85.7+2.1)%,载药量为(1.11+0.09)%,胶束溶液的浓度为(1.6+0.05)mg/mL,其中穿心莲内酯的有效浓度为(0.64+0.02)mg/mL。尽管有效部位主要包含穿心莲内酯、脱水穿心莲内酯和14-去氧穿心莲内酯3种有效成分,但因其中穿心莲内酯的含量高达40.56%,故而选取以穿心莲内酯的包封率为主要指标对载药胶束制备工艺进行评价。对其粒径考察的结果发现均在190nm左右。究其原因,认为是增大载药量,胶束会容易聚集,粒径随之增大[15],而且作为中药制剂,成分较为复杂,故粒径较大。
4 结论
选择载药量较高、制备工艺简单的薄膜水化法制备穿心莲有效部位的poloxamer188胶束,以包封率、载药量和粒径为主要考察指标,单因素考察投药量、水相用量等影响因素。在此基础上,正交设计优化胶束处方工艺,选用投药量、水相用量、蒸发温度为考察因素,最终确定的优化处方为:穿心莲有效部位15mg,poloxamer188120mg,水相用量7mL,于50℃下成膜。使穿心莲有效部位在水溶液中的浓度达到1.61mg/mL。重复实验证明,结果有较高的可靠性。而且本实验的制备工艺简便易行,为中药制剂提供了新剂型。
[1]Kim,TG,Hwi,KK and Hung,CS.Morphological and biochemical changes of andrographolide induced cell death in human prostatic adenocarcinoma PC-3cells[J].In Vivo,2005,19(3):551-557.
[2]Sheeja K and Kuttan,G.Modulation of natural killer cell activity,antibody-dependent cellular ytotoxicity,and antibodydependent complement-mediated cytotoxicity by andrographolide in normal and ehrlich ascites carcinoma-bearing mice[J].Integr Cancer Ther,2007,6(1):66-73.
[3]Sheeja K and Kuttan,G.Activation of cytotoxic T Lymphocyte responses and attenuation of tumor growth in vivo by Andrographis paniculata extract and andrographolide[J].Immunopharm.Immunot.,2007,29(1):81-93.
[4]Kumar RA,Sridevi K,Kumar NV.et al.,Anticancer and immunostimulatory compounds from andrographis paniculata[J].J.Ethnopharmacol.,2004,92(2):291-295.
[5]Rajagopal S.,Kumar R.A.,Deevi D.S.,Satyanarayana C,et al.,Andrographolide,apotential cancer therapeuticagent isolated from Andrographis paniculata[J].J Exp.Ther.Oncol.,2003,3(2):147-158.
[6]Geethangili M.,Rao Y.K.,Fang SH,et al.,Cytotoxic constituents from Andrographis paniculata induce cell cycle arrest in Jurkatcells[J].Phytother.Res.,2008,22(10):1336-1341.
[7]Zhou J,Lu GD,Ong CS,Ong CN,Shen HM.Andrographolide sensitizes cancer cells to TRAIL-induced apoptosis via p53-mediated death receptor 4up-regulation[J].Mol.Cancer.Ther.,2008,7(10):2170-2180.
[8]Yang L,Wu D,Luo K,Wu S,Wu P.Andrographolide enhances 5-fluorouracil-induced apoptosis via caspase-8-dependent mitochondrial pathway involving p53participation in hepatocellular carcinoma(SMM-C-7721)cells[J].Cancer Lett.,2009,27(6):180-188.
[9]Liang FP,Lin CH,Kuo CD,Chao HP,Fu SL.Suppression of v-Src transformation by andrographolide via degradation of the v-Src protein and attenuation of the Erk signaling pathway[J].J.Biol.Chem.,2008,28(3):5023-5033.
[10]葛发欢,林秀仙.超临界CO2流体萃取穿心莲有效成分的正交试验研究[J].中药材,2002,25(2):101-102.
[11]范云鸽,张秀莉.大孔吸附树脂提取穿心莲总内酯的研究 [J].高分子交换与吸附,2002,18(1):30-35.
[12]Yasuhiro M.Preclinical and clinical studies of anticancer drug-incorporated polymeric micelles[J].J.Drug Target,2007,15(7-8):507-517.
[13]邵铖祎,郦江平,涂家生.紫杉醇和多西紫杉醇双药胶束体外稳定性考察[J].中国药科大学学报,2010,41(5):428-434.
[14]Mu CF,Balakrishnan P,Cui F D,et al.The effects of mixed MPEG-PLA/Pluronic®copolymer micelles on the bioavailability and multidrug resistance of docetaxel[J].Biomaterials,2010,31(8):2371-2379.
[15]Gaucher G,Dufresne MH,Sant VP,et al.Block copolymer micelles:preparation,characterization and application in drug delivery[J].J Controlled Release,2005,109(1-3):169-188.
[责任编辑 段金卯]
Preparation and formulation of poloxamer188 loaded effective parts of andrographis paniculata nees polymeric micelles
LIU Lei,WANG Yu-han,HAN Guang*,ZHANG Yu(Institute of Pharmaceutics of Henan University,Kaifeng,Henan 475004,China)
ObjectiveTo prepare the capsule of poloxamer188polymeric micelles system loaded with effective parts of andrographis paniculata nees (AEP).MethodsAEP loaded Poloxamer188micelles were prepared by thin-film hydration method.The main factors affecting the drug-loading encapsulation ratio was studied by single factor analysis and optimization preparation condition was gained by orthogonal design.The drug-loading coefficient and encapsulation efficiency of AEP in micelles were determined by HPLC.The mean particle size was determined by ZetasizerH-3000 Laser Particle Size Analyzer.ResultsThe encapsulation efficiency and drug-loading coefficient were(85.7+2.1)%and(1.11+0.09)%,respectively.The diameter was(198.32+3.35)nm.ConclusionThe process is practical and simple for the preparation of AEP loaded Poloxamer188micelles.It is a new method for the preparation of Chinese Traditional Medicine.
Effective parts of Andrographis paniculata Nees(AEP);Poloxamer188;Polymeric micelles
R283
A
1672-7606(2012)02-0091-04
2012-02-23
河南大学科研基金项目(2009ZZZD006)。
刘蕾(1977-),女,河南南阳人,讲师,从事天然药物化学的教学和研究工作。
*通讯作者:韩光(1966-),女,北京人,教授,从事天然药物化学的教学和研究工作。
