表面活性素分子结构对其胶束化行为的影响
2011-11-30邹爱华叶汝强牟伯中
李 翌 邹爱华 叶汝强 牟伯中
(华东理工大学应用化学研究所,上海200237)
表面活性素分子结构对其胶束化行为的影响
李 翌 邹爱华 叶汝强 牟伯中*
(华东理工大学应用化学研究所,上海200237)
采用表面张力、界面张力、荧光、动态光散射(DLS)和冷冻刻蚀电镜(FF-TEM)等方法,研究了由Bacillus subtilis HSO121所产生的一组表面活性素的胶束化行为.通过对表面活性素溶液表面张力、表面活性素对水/正己烷界面张力的影响、表面活性素胶束微极性以及胶束粒径和形态的研究,发现随着表面活性素脂肪链长度的增加,其表界面活性增强,溶液中趋向于形成更大的聚集体.
表面活性素;胶束;荧光;动态光散射;冷冻刻蚀电镜
1 引 言
表面活性素(surfactin)是脂肽家族中一类具有代表性的生物表面活性剂.脂肽是由微生物在细胞表面或者由胞外分泌产生的一类由脂肪酸和肽组成的具有两亲结构的化合物,是优良的生物表面活性剂.枯草芽孢杆菌(Bacillus subtilis)产生的脂肽主要有表面活性素(surfactin)、1地衣素(lichenysin)、2伊枯草素(iturins)3和丰原素(fengycin)4等.表面活性素在1968年由Arima等1鉴定命名,其化学结构由Kakinuma等5确定为含有7个α-氨基酸和β-羟基脂肪酸构成的环状脂肽类化合物.表面活性素可以在1×10-5mol·L-1浓度时,将水的表面张力由72 mN· m-1降低到27 mN·m-1,是表面活性最强的一类脂肽.6,7另外表面活性素还表现出特殊的生物活性,如抗病毒、抗肿瘤、抗真菌、抗HIV和溶血等.8-13表面活性素的这些表面和生物活性与它在水溶液中的物理化学性质有着密切的关系,因此研究表面活性素溶液的性质以及胶束化过程对于进一步探索表面活性素的生物物理活性以及拓展其在化学工业和生物医药领域的应用有着重要的意义.
表面活性素的自身结构,脂肪链和氨基酸部分的不同,对表面活性素的物理化学性质和生物活性都会产生一定的影响.Gallet等14用分子模拟的方法研究了脂肪链长度为13、14、15的表面活性素同系物在亲水/亲油界面上的不同构型.Razafindralambo等15用动态表面张力法研究了脂肪链长为13、14、15的表面活性素,发现随着链长的增加,动态界面张力降低得更快.Song等16用LB膜技术研究了烃链长度对表面活性素界面形态的影响.Deleu等17计算模拟了表面活性素和生物膜的作用,Eeman等18研究了烃链长度为13、14、15的环状表面活性素以及烃链长为15的直链表面活性素,都发现链长的增加大大加强了表面活性素的表面活性,同时也影响着表面活性素和磷脂膜的相互作用.因此系统研究表面活性素分子结构对其溶液性质的影响,对表面活性素的化学和生物应用都有一定的指导意义.
目前,对表面活性素溶液性质的研究已有一些报道,但是基于分离纯化技术的限制,大多数研究都是针对表面活性素同系物及其类似物的混合体系.这样得到的结果难以准确地表征表面活性素胶束化过程以及表面活性素溶液体系的各个参数,而且各个研究结果之间差异较大,结果不稳定.本文由一株枯草芽孢杆菌HSO121出发,发酵培养及分离纯化得到了5种主要表面活性素,通过表面张力、界面张力、荧光法、动态光散射(DLS)和冷冻刻蚀电镜(FF-TEM)对不同结构的表面活性素溶液胶束化行为比较,得到表面活性素结构差异对其溶液性质和胶束化行为的影响规律.
2 实验部分
2.1 表面活性素的制备以及分离纯化
实验所用的表面活性素样品由本实验室分离鉴定的枯草芽孢杆菌Bacillus subtilis HSO121培养产生.19,20表面活性素粗提物用常压反相柱(YMC ODS C18柱,Φ 3.0 cm×10 cm,50 μm)纯化,去除色素.然后再由高效液相色谱(JASCO LC-2000,日本, HIQ sil C18W柱,Φ 21.2 mm×250 mm,5 μm),采用甲醇、水体系进一步分离,得到各个表面活性素的组分,如图1所示.
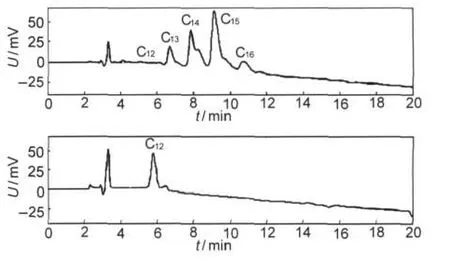
图1 表面活性素的分析型高效液相色谱图Fig.1 Analytical high performance liquid chromatography(HPLC)of surfactinC12,C13,C14,C15,and C16:the surfactins with fatty acid chains having 12,13,14,15,and 16 carbon atoms
得到的脂肽先由氨基酸自动分析仪获得脂肽的氨基酸组成,然后用电喷雾四极杆-飞行时间串联质谱(ESI Q-TOF MS/MS)和气相色谱/质谱连用(GC/MS)对脂肽结构进行解析.21
实验所用的表面活性素样品结构如图2所示,脂肪酸链碳数分别为12、13、14、15、16.
2.2 试 剂
KCl,分析纯,上海凌峰试剂有限公司;正己烷,分析纯,上海菲达工程有限公司;使用0.05 mol·L-1, pH为8.5的Tris(Gene-Tech,纯度>99.95%)缓冲溶液;水为二次重蒸水.
2.3 实验方法
2.3.1 表面张力的测定
配置一系列浓度的表面活性素水溶液,0.05 mol·L-1Tris缓冲液,pH 8.5,25°C,用DCA315表/界面张力仪及动态接触角分析系统DCA315(Thermo Cahn,美国)测定其表面张力.
2.3.2 界面张力测定
固定表面活性素浓度为4×10-5mol·L-1,用旋滴界面张力仪TX-550A型(Bowing,美国)测定了各个不同结构的表面活性素对于水和正己烷的油水界面张力的影响.由TX-550A旋滴界面张力仪测得表面活性素水溶液中正己烷液滴的长度L(cm)和宽度D(cm),计算得到界面张力.当L/D≥4时,可根据式(1)计算液液界面张力:22
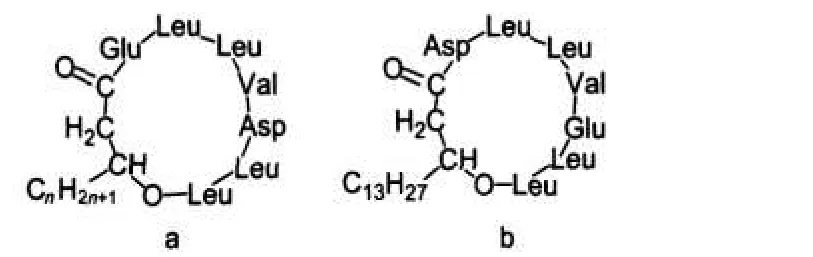
图2 表面活性素结构图Fig.2 Structures of surfactins (a)n=9(surfactin-C12),n=10(surfactin-C13),n=11(surfactin-C14)and n=12(surfactin-C15);(b)surfactin-C16;Asp:aspartate, Glu:glutamic acid,Leu:leucine,Val:valine
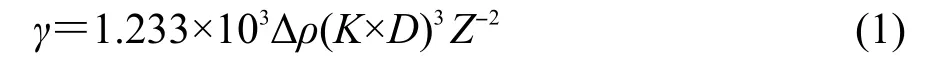
式中γ为界面张力(mN·m-1),Δρ为两相密度差(g· cm-3),Z为仪器上显示的旋转周期(ms·2π-1),K为常数0.3817.当L/D<4时,可根据式(2)计算:
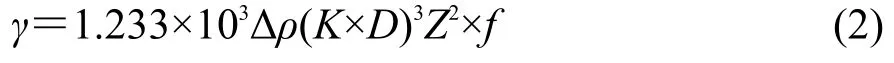
式中f为校正参数,由不同的L/D值对应得到.
2.3.3 荧光法
表面活性素溶液的胶束微环境性质由荧光分光光度计F-4500(Hitachi,日本)测定,采用芘(Sigma-Aldrich,99%(w))作为荧光探针.在激发光波长为335 nm时,芘的荧光发射光谱在350-500 nm有5个特征峰,其中第一峰的荧光强度I1在极性溶剂中呈现出较大的增加,第三峰的荧光强度I3在非极性溶剂中较强,其强度随条件变化不大,因此I1与I3之比值强烈依赖于环境极性.23测定芘在不同结构表面活性素溶液(4×10-5mol·L-1)的荧光光谱,研究表面活性素结构对其胶束微环境性质的影响.
2.3.4 动态光散射
通过激光粒度仪Nano-ZS(Malvern,英国)测定了不同结构表面活性素溶液中胶束粒径的分布,样品槽温度恒定在25°C,表面活性素浓度为4×10-5mol·L-1.
2.3.5 冷冻刻蚀电镜
将样品滴入样品杯内并迅速投入液氮(约77 K)中冷冻固定.在液氮环境下,样品杯转移到样品座上,然后送入冷冻蚀刻仪BALZERS BAF-400D (Bal-tec,列支敦士登)的真空腔中(真空腔中的样品台及冷刀预冷到约100 K).取出样品杆,抽真空.等到系统压力小于1×10-9Pa时,将样品断裂.以45°角向样品断裂面喷镀厚约2 nm的铂,然后以垂直方向喷镀1-20 nm的碳层.取出样品,重蒸水漂洗,用铜网将复型捞起,晾干后,用透射电子显微镜JEM-1400 (JEOL,日本)观察.24,25
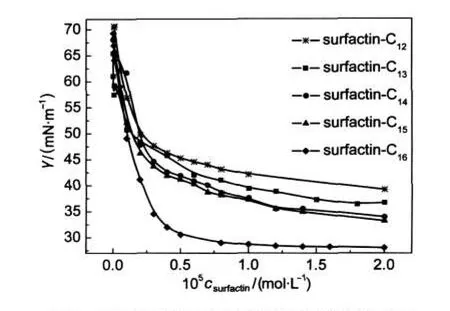
图3 不同链长表面活性素溶液的表面张力图Fig.3 Surface tension of surfactins with different fatty acid chain lengths
3 结果与讨论
3.1 表面活性素分子结构对其表面、界面活性的影响
用吊环法分别测得一系列浓度的表面活性素, surfactin-C12、C13、C14、C15、C16在0.05 mol·L-1的Tris缓冲溶液中的表面张力,实验温度为25°C,表面张力和表面活性素浓度变化关系如图3所示.由图可见,表面张力先随着表面活性素浓度的增加急剧降低,在达到临界胶束浓度,形成胶束以后表面张力降低幅度变慢,趋于一个定值.从图3可以得到各个表面活性素的cmc值(表1),随着碳链的增加各个表面活性素溶液的cmc值变化在一个较接近的范围内,脂肪链长的表面活性素有较小的cmc值.各个表面活性素体系最终达到的最低表面张力(γcmc)也随结构的不同而不同,脂肪链长的表面活性素能够使溶液达到更低的γcmc,表面活性剂水溶液的表面张力越低,其润湿、起泡、乳化、分散等性能越好.因此,γcmc是表面活性剂的一个主要性质.图3显示,表面活性素surfactin-C16较其他表面活性素有更低的γcmc.表面活性素surfactin-C16在亲水基团和疏水脂肪酸链上都和其他表面活性素有着不同.对于相同性质的疏水基,结构不同时,表面活性剂的性质会有显著差异,有支链的结构会显著降低γcmc.表面活性素surfactin-C16脂肪链比其他表面活性素多一个碳原子,因此更复杂的支链使其γcmc更低.另一方面,它的氨基酸结构上Asp和Glu的位置和其他表面活性素不同.表面活性素分子在溶液中呈马鞍型结构,Asp和Glu在亲水的一面,其余四个氨基酸和烃链在另一面.26,27两个亲水氨基酸位置的改变,会使疏水烃链受到的邻近氨基酸的位阻作用变小,对胶束的形成产生一定的影响.而关于氨基酸部分对表面活性素性质的影响,我们还需要改进研究手段做进一步的探索.
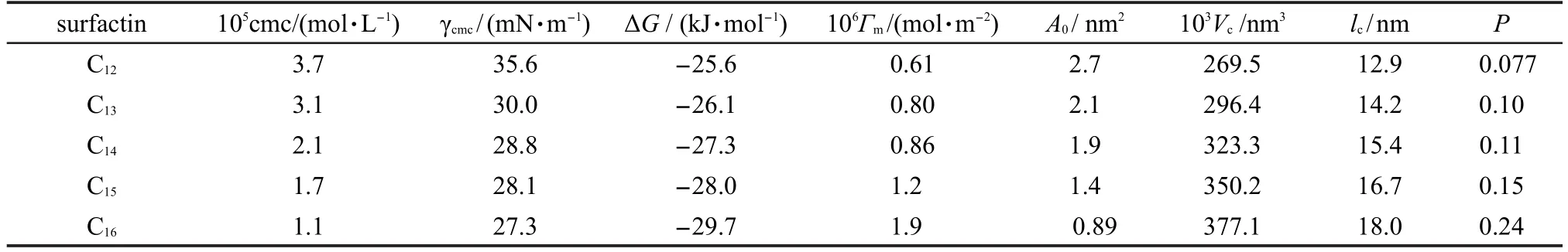
表1 不同链长表面活性素在气液界面的吸附参数Table 1 Adsorption parameters of surfactins with different chain lengths at the air-aqueous-solution interface
根据Gibbs等温吸附式,由表面活性素溶液浓度和表面张力的关系,可以计算得到表面活性素的表面吸附量(Γ)和单位分子在表面所占面积(A).28
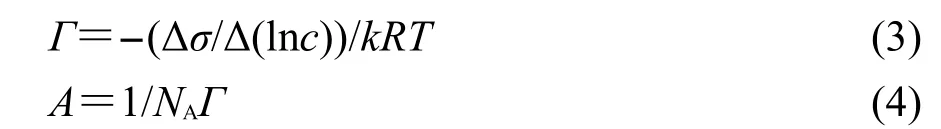
式中σ为溶液表面张力,c为溶液浓度,R为摩尔气体常数,T为热力学温度,NA为阿伏伽德罗常数,k为和表面活性剂结构类型有关的常数,表面活性素在完全电离的条件下,是二价的离子型表面活性剂, ksurfactin=3.29对一系列表面活性素计算结果如表1所示,由表1中的数据可以看出,表面活性素在溶液表面的吸附量随着脂肪链长度的增加,单分子表面活性素表面面积从2.7 nm2降到0.89 nm2,表面活性素胶束化的标准自由能降低.由于碳原子的增加,使得疏水链更易于在气液界面伸展,界面上的氨基酸环也随之变化位置,单位分子所占面积减少.Gallet14和Song16,30等都用LB膜方法研究了脂肽的界面性质,由π-A曲线上可以得到表面活性素的分子面积在1.5 nm2左右,π为表面压,这和我们计算得到分子面积的结果相一致.Maget-Dana31和Ptak26等也通过表面张力得到表面活性素surfactin-C14的分子面积,为1.32 nm2,略低于我们测得的surfactin-C14的结果1.9 nm2.这有可能是溶液电解质、pH值、温度等实验条件不同带来的.Shen等27通过气液界面中子散射得到的结果为1.47 nm2,并且认为surfactin的脂肪酸链和疏水的氨基酸部分产生强烈的相互作用,能够向后折叠在肽环的亮氨酸里.
在此基础上还进行了几何排列参数的计算,计算中我们将β羟基脂肪酸链算作疏水部分,氨基酸肽环作为亲水部分.为计算几何排列参数(P)所需的A0、lc和Vc的值可以分别由实验测定和理论计算得到,32计算结果见表1.由初步计算的P值来看,都小于1/3,这一结果说明单纯从表面活性素分子几何结构来看,表面活性素趋向于形成球状胶束.随着脂肪链长度的增加,P增大,趋向于形成其他不对称胶束结构.我们得到的几何排列参数值和Shen等27报道的结果较为相近,他们得到的表面活性素sufactin-C14的P值为0.21.另外,他们也根据对表面活性素脂肪酸链和疏水氨基酸相互作用情况的推测,估算了另一个几何堆积常数,将亮氨酸和脂肪酸链整体作为疏水部分,得到堆积常数为0.65.这一几何排列参数的结果大于1/2,表明脂肪酸链和疏水基的相互作用,使得分子构型改变,表面活性素也有可能趋向于形成一个层状聚集结构.
加入不同链长的表面活性素以后,水/正己烷的界面张力变化结果如表2所示,表面活性素可以将缓冲溶液存在的条件下将水/正己烷的界面张力由25 mN·m-1降低到1 mN·m-1左右.并且随着表面活性素脂肪链长度的增加,表面活性素使得水/正己烷的界面张力降低得更多,这是由于表面活性素脂肪链的增加使得疏水的烃链部分更容易进入到正己烷相,与之相互作用,降低了水相和正己烷相的界面张力.
由一系列表面活性素溶液表面和界面活性实验可以看出,随着表面活性素脂肪链长度的增加,使得表面活性素的表面、界面活性加强,更有助于胶束的形成.
3.2 表面活性素分子结构对其溶液微极性的影响
荧光法可以用来研究溶液微环境性质,芘探针的荧光光谱有5个特征峰,其中第一和第三峰的值可以分别表示出探针分子所处微环境中极性和非极性的强弱,第一和第三峰的比值I1/I3可以作为胶束微极性的指标.23,33本实验用荧光法测定不同浓度表面活性素溶液中芘探针荧光光谱,得到第一和第三峰值的比例,研究表面活性素溶液微环境极性随表面活性素结构的变化,结果如表3所示.
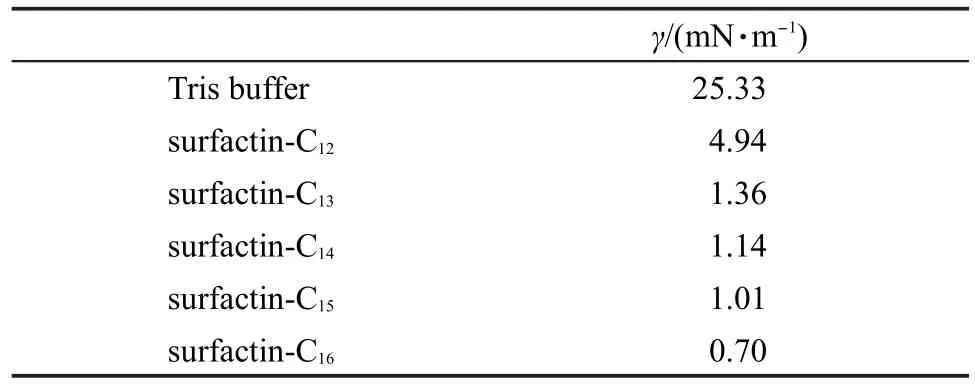
表2 不同链长表面活性素溶液和正己烷的界面张力Table 2 Interfacial tension of surfactin solution with different chain lengths and hexane
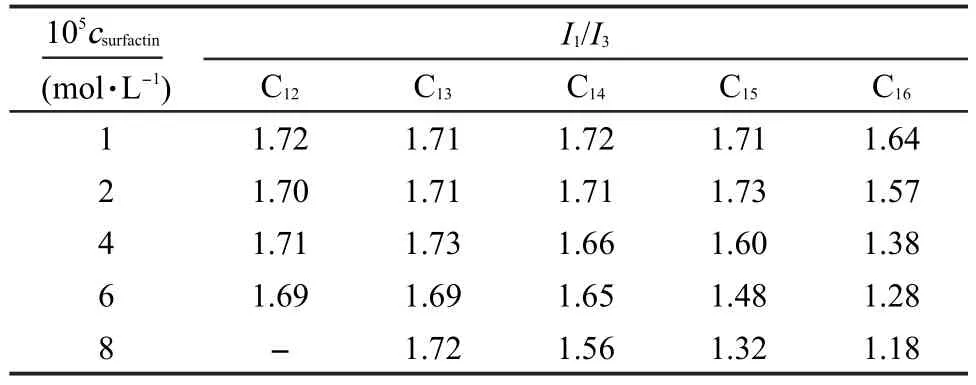
表3 表面活性素浓度对胶束微极性(I1/I3)的影响Table 3 Effect of surfactin concentrations on the micelle micropolarity(I1/I3)
随着表面活性素浓度的增加,溶液的微极性降低,且脂肪链长度对微极性有明显影响.从表3中可见,在形成胶束以后,脂肪链较短的表面活性素微极性变化不大,脂肪链长度越大,微极性越低.胶束微极性的降低表明探针分子所处微环境的极性降低,更多探针分子被增溶在胶束中.随着脂肪链长度的增加,表面活性素的疏水性增加,因此形成的胶束微环境极性即胶束微极性降低.胶束微极性的降低表明溶液胶束中水分子减少,疏水的非极性物质增加,说明脂肪链长度较长的表面活性素随着浓度的增加能够形成更大的胶束聚集体,使得胶束中疏水部分更加密集,而链长较短的表面活性素胶束结构较稳定,随浓度变化较小.
3.3 不同链长表面活性素胶束形态的变化
为了了解不同链长的表面活性素胶束粒径分布和形态的变化,我们通过动态光散射和冷冻刻蚀方法对同一浓度的表面活性素胶束溶液进行了研究.用Nano-ZS激光粒度仪测定了各个表面活性素在溶液中聚集体粒径大小分布.不同表面活性素溶液中聚集体粒径的体积相关分布如图4所示.
由图可以看出,表面活性素在溶液中聚集体的粒径分布有2个范围,较小的胶束小于100 nm,较大的聚集体在300 nm左右.最早由Ishigami等6对于表面活性素胶束性质研究表明,表面活性素通过β折叠结构形成胶束.β折叠结构是蛋白质中常见的二级结构,是由伸展的多肽链组成的.折叠片的构象是通过一个肽键的羰基氧和位于同一个肽链或相邻肽链的另一个酰胺氢之间形成的氢键维持的.氢键几乎都是垂直伸展的肽链,这些肽链可以是平行排列(走向都是由N到C方向);或者是反平行排列(肽链反向排列).由于有这样的结构存在,使得胶束间的氢键作用加强,胶束之间有相互作用,能够形成大的胶束聚集体.所以表面活性素的水溶液中除了形成一般的胶束结构之外,胶束之间也容易产生相互作用,形成较大的胶束聚集体.
这一结果也和我们之前对surfactin-C16溶液体系的研究34以及Han等35对表面活性素胶束溶液的研究结果相一致.由于表面活性素具有β折叠结构,除了形成一般的胶束结构之外,胶束之间也容易产生相互作用,形成较大的聚集体.但是从胶束粒径大小角度出发,Ishigami等6采用光散射方法测得表面活性素的胶束形状,是直径为5.8 nm,长115.5 nm的棒状胶束.Han等35的动态光散射结果也显示两个分布分别是在4-6 nm和100 nm附近有两个吸收峰.我们的结果要比他们的粒径更大,这可能是体系的差别引起的结果,还有待进一步考证.
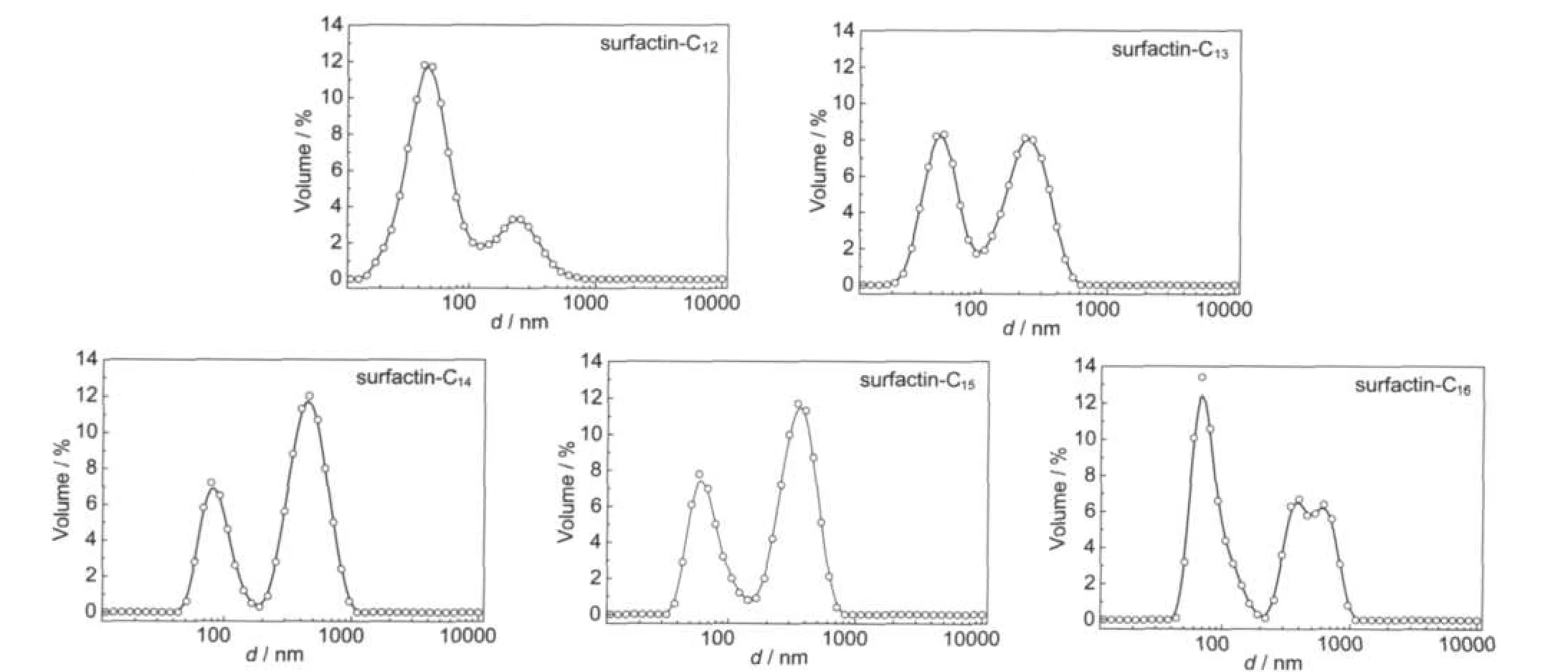
图4 不同表面活性素溶液中聚集体粒径(d)的体积相关分布图Fig.4 Volume particle size(d)distribution of aggregations in different surfactin solutionsThe concentration of surfactin is 4×10-5mol·L-1,T=25°C.

图5 不同链长表面活性素溶液的冷冻刻蚀透射电镜照片Fig.5 Freeze-fracture transmission electron microscopy(FF-TEM)images of surfactin solutions with different chain lengths(a)surfactin-C13,(b)surfactin-C16,csurfaction=4×10-5mol·L-1
由图4可知,从相对体积比例来看,链长较短的surfactin-C12大部分是形成直径为40 nm左右的胶束,少部分形成直径大于200 nm的胶束聚集体.随着表面活性素烷基链的增长,形成的聚集体的直径明显增加,也有更多的大粒径聚集体形成.
为了进一步观察表面活性素胶束溶液的形态,我们还进行了冷冻刻蚀实验.图5是表面活性素surfactin-C13和-C16溶液的冷冻刻蚀电镜照片,表面活性素溶液浓度为4×10-5mol·L-1.
由图可以观察到,表面活性素surfactin-C13胶束多数为直径在25 nm左右的、球形的、较为均匀的粒子,还有一些较大的100 nm左右的聚集体,这与动态光散射的结果(图4)一致,小粒径的胶束占多数;表面活性素surfactin-C16主要是有较小的半径约50 nm的不规则胶束,以及粒径较大的几百纳米复杂聚体两种聚集体,并且可以观察到一些层状聚集结构.动态光散射也显示几百纳米的胶束聚集体增多,动态光散射和冷冻刻蚀的结果也和荧光实验的结果相一致,可以看出,随着表面活性素脂肪链的增加,胶束之间β折叠作用加强,使得表面活性素更容易发生胶束之间的聚集,形成大的聚集体.
4 结论
通过表面张力、界面张力、荧光、动态光散射和冷冻刻蚀透射电镜研究了由Bacillus subtilis HSO121所产生的一系列表面活性素的胶束化行为.研究发现:随着表面活性素脂肪链的增加,表面活性素的临界胶束浓度以及胶束形成以后的表面张力都降低,使水/正己烷的界面张力降低幅度加大,这表明表面活性素表面、界面性质增强.通过表面活性素胶束溶液聚集体的粒径分布以及形态的研究,得到表面活性素结构对其胶束性质的影响规律.由于表面活性素分子间的β折叠结构,链长较短的表面活性素趋向于形成半径较小的胶束,胶束结构比较稳定,随着表面活性素浓度增加变化不大;对于链长较长的表面活性素,由于分子间β折叠结构作用的增强,还能够形成半径较大的复杂聚集体,并且随着浓度的增加,聚集体增大.
致谢:感谢中国科学院生物物理研究所生物电镜中心提供的测试服务,感谢孙树锋老师在电镜测试中心帮助我们制作了电镜观察样品.
(1)Arlma,K.;Kakinuma,A.;Tamum,G.Biochem.Biophys.Res. Commun.1968,31,488.
(2)Yakimov,M.M.;Abraham,W.R.;Meyer,H.;Giuliano,L.; Golyshin,P.N.Biochim.Biophys.Acta 1999,1438,273.
(3)Peypoux,F.;Guinand,M.;Michel,G.;Delcambe,L.;Das,B. C.;Lederer,E.Biochemistry 1978,17,3992.
(4) Vanittanakom,N.;Loeffler,W.;Koch,U.;Jung,G.J.Antibiot. 1986,30,888.
(5) Kakinuma,A.;Hori,M.;Isono,M.Agr.Biol.Chem.1969,33, 971.
(6) Ishigami,Y.;Osman,M.;Nakahara,H.;Sano,Y.;Ishiguro,R.; Matsumoto,M.Colloids Surf.B 1995,4,341.
(7) Peypoux,F.;Bonmatin,J.M.;Wallach,J.Appl.Microbiol. Biotechnol.1999,51,553.
(8) Beven,L.;Wroblewski,H.Res.Microbiol.1997,148,163.
(9) Vollenbroich,D.;Pauli,G.;Özel,M.;Vater,J.Appl.Environ. Microbiol.1997,63,44.
(10) Weislow,O.S.;Kiser,R.;Fine,D.L.;Bader,J.;Shoemaker,R. H.;Boyd,M.R.J.Natl.Cancer Inst.1989,81,577.
(11)Kameda,Y.;Matsui,K.;Kato,H.;Yamada,T.;Sagai,H.Chem. Pharm.Bull.1972,20,1551.
(12) Kameda,Y.;Ouhira,S.;Matsui,K.;Kanatomo,S.;Hase,T.; Atsusaka,T.Chem.Pharm.Bull.1974,20,938.
(13) Bernheimer,A.;Avigad,L.J.Gen.Microbiol.1970,61,361.
(14) Gallet,X.;Deleu,M.;Razafindralambo,H.;Jacques,P.; Thonart,P.;Paquot,M.;Brasseur,R.Langmuir 1999,15,2409.
(15) Razafindralambo,H.;Thonart,P.;Paquot,M.J.Surfactants Deterg.2004,7,41.
(16) Song,C.S.;Ye,R.Q.;Mu,B.Z.Colloids Surf.A 2008,330,49.
(17) Deleu,M.;Bouffioux,O.;Razafindralambo,H.;Paquot,M.; Hbid,C.;Thonart,P.;Jacques,P.;Brasseur,R.Langmuir 2003, 19,3377.
(18)Eeman,M.;Berquand,A.;Dufrêne,Y.F.;Paquot,M.;Dufour, S.;Deleu,M.Langmuir 2006,22,11337.
(19) Liu,X.Y.;Yang,S.Z.;Mu,B.Z.J.Peptide Sci.2008,14,864.
(20) Namir,H.;Liu,X.Y.;Yang,S.Z.;Mu,B.Z.Protein Peptide Lett.2008,15,265.
(21)Liu,X.Y.;Namir,H.;Yang,S.Z.;Mu,B.Z.Protein Peptide Lett.2007,14,766.
(22) Princen,H.M.;Zia,I.Y.Z.J.Colloid Interface Sci.1967,23, 99.
(23) Osman,M.;Høiland,H.;Holmsen,H.Colloids Surf.B 1998,11, 167,
(24) Bolzinger-Thevenin,M.A.;Grossiord,J.L.;Poelman,M.C. Langmuir 1999,15,2307.
(25) Xu,J.;Li,G.Z.;Zhang,Z.Q.;Zhou,G.W.;Ji,K.J.Colloids Surf.A 2001,191,269.
(26)Bonmatin,J.M.;Genest,M.;Labbe,H.;Ptak,M.Biopolymer 1994,34,975.
(27) Shen,H.H.;Thomas,R.K.;Chien-Yen,C.;Darton,R.C.; Baker,S.C.;Penfold,J.Langmuir 2009,25,4211.
(28)Heins,A.;Garamus,V.M.;Steffen,B.;Stöckmann,H.; Schwarz,K.Food Biophysics 2006,1,189.
(29) Zana,R.Adv.Colloid Interface Sci.2002,97,205.
(30) Song,C.S.;Ye,R.Q.;Mu,B.Z.Colloids Surf.A 2007,302,82.
(31) Maget-Dana,R.;Ptak,M.J.Colloid Interface Sci.1992,153, 285.
(32) Zhao,G.X.;Zhu,B.Y.Principles of Surfactant Action;China Light Industry Press:Beijing,2003;pp 231-233.[赵国玺,朱 瑶.表面活性剂作用原理.北京:中国轻工业出版社, 2003:231-233.]
(33)Thomas,J.K.Chem.Rev.1998,80,283.
(34)Li,Y.;Zou,A.H.;Ye,R.Q.;Mu,B.Z.J.Phys.Chem.B 2009, 113,15272.
(35)Han,Y.C.;Huang,X.;Cao,M.W.;Wang,Y.L.J.Phys.Chem. B 2008,112,15195.
November 15,2010;Revised:January 17,2011;Published on Web:March 17,2011.
Effects of Molecular Structure on Surfactin Micellization Activity
LI Yi ZOU Ai-Hua YE Ru-Qiang MU Bo-Zhong*
(Institute of Applied Chemistry,East China University of Science and Technology,Shanghai 200237)
We produced a group of surfactin isoforms using Bacillus subtilis HSO121.The micellization activity properties such as surface and interfacial tensions,micropolarity,micelle size distribution and morphology of this group of surfactin micellar solutions were investigated by surface and interfacial tension, fluorescence,dynamic light-scattering(DLS),and freeze-fracture transmission electron microscopy (FF-TEM)measurements.With an increase in the chain length,we found that the surface and interfacial activities of the surfactins increased and the surfactins tended to form larger micelle aggregates.
Surfactin;Micelle;Fluorescence;Dynamic light-scattering;Freeze-fracture transmission electron microscopy
O648
∗Corresponding author.Email:bzmu@ecust.edu.cn;Tel:+86-21-64252063;Fax:+86-21-64252458.
The project was supported by the Research Fund for the New Teacher of the Doctoral Program of Higher Education of China(200802511024)and Shanghai Municipal Science and Technology Commission,China(071607014).
博士点新教师基金项目(200802511024)和上海市国际合作项目(071607014)资助
