硝酸银硅胶柱分离纯化蛇鲻鱼油中的EPA和DHA
2011-11-20刘美玲刘书成郝记明
张 良 刘美玲 董 强 刘书成 郝记明 张 静
(广东海洋大学食品科技学院1,湛江 524025)
(广东省高等学校水产品深加工重点实验室2,湛江 524025)
(西安市产品质量监督检验院3,西安 474100)
硝酸银硅胶柱分离纯化蛇鲻鱼油中的EPA和DHA
张 良1,2刘美玲1,2董 强3刘书成1,2郝记明1,2张 静1,2
(广东海洋大学食品科技学院1,湛江 524025)
(广东省高等学校水产品深加工重点实验室2,湛江 524025)
(西安市产品质量监督检验院3,西安 474100)
采用NaOH-乙醇皂化再硫酸酸化的方法制备蛇鲻鱼油混合脂肪酸,然后用硝酸银硅胶柱色谱分离纯化EPA和DHA。结果表明:15 g硅胶与1 g硝酸银充分混合后装柱,置于5℃的恒温层析柜中,待色谱柱平衡后,上样0.75 g混合脂肪酸,然后依次用100 mL石油醚,2%,4%,8%,10%无水乙醚-石油醚溶液各100 mL进行洗脱,洗脱液流速为0.5~1.0 mL/min,收集200 mL以后的洗脱液,进行旋转蒸发,EPA和DHA的质量分数分别从4.43%和13.94%提高至21.47%及70.13%,总质量分数可达90%以上。
硝酸银-硅胶 DHA EPA 分离
EPA(二十碳五烯酸)和DHA(二十二碳六烯酸)等n-3 PUFA(n-3多不饱和脂肪酸)具有很多的生理功能,是制造预防心血管疾病和益智保健食品的良好基料[1]。硝酸银硅胶柱层析法是20世纪60年代由De Vries等[2-3]首先用来分离脂肪酸及其脂类,目前已广泛应用于脂肪酸、甾体化合物、萜类化合物的分离纯化[4]。该方法是基于吸附在硅胶上的银离子与不饱和脂肪酸分子中的—CC—之间发生电子迁移形成络合物,从而改变了各饱和度不同的脂肪酸在吸附剂(硝酸银-硅胶)上的分配系数,使之得以分离[2-5]。
蛇鲻是南海重要经济鱼类,天然的蛇鲻鱼油中EPA和DHA总质量分数17.90%,低于30%,不能满足于生产保健鱼油的要求。本研究以蛇鲻精制鱼油为原料,采用硝酸银硅胶柱层析技术分离纯化EPA和DHA,考察硝酸银用量、上样量以及洗脱体系对分离纯化效果的影响,并初步探讨硝酸银-硅胶对脂肪的吸附特性的影响。
1 材料与方法
1.1 材料
蛇鲻(saurida elongate)精制鱼油,从蛇鲻鱼糜漂洗物下脚料(北海天鲜海洋食品有限公司提供)中提取,经脱胶、脱酸、脱色和脱臭等精制而成。鱼油中的主要脂肪酸含量见表1所示。
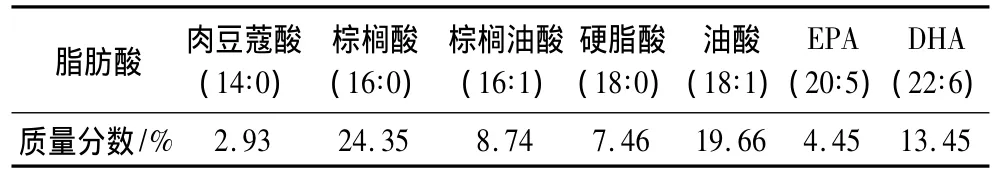
表1 精制蛇鲻鱼油的主要脂肪酸含量
硝酸银,薄层层析硅胶,无水乙醚,石油醚Ⅱ,正己烷,无水乙醇,95%乙醇,浓硫酸,甲醇,氢氧化钾,氯化钠等试剂均为分析纯。脂肪酸甲酯标准品:含有C4~C24等多种脂肪酸甲酯,Sigma公司(商品号18919-1AMP)。
气相色谱仪GC-14B:日本岛津公司;电脑恒温层析柜CXG-1:上海青浦沪西仪器厂;全温振荡培养箱:哈尔滨东联电子技术开发有限公司;旋转蒸发仪:托普仪器有限公司。
1.2 试验方法
1.2.1 混合脂肪酸的制备
称取100 g鱼油放入 500 mL烧瓶中,加入200 mL 0.1 mol/L的氢氧化钠乙醇溶液,安装好回流管,置于60℃恒温水浴锅中,并不断搅拌,反应2 h后,冷却后加入适量石油醚除去非皂化物,然后用6 mol/L硫酸酸化至pH=1~2,然后加入石油醚萃取,收集石油醚层,然后用旋转蒸发仪下脱出溶剂即得混合脂肪酸。
1.2.2 EPA 和 DHA 的分离纯化[6-7]
硅胶柱规格(35 cm×1.6 cm),分离效果以洗脱液中DHA和EPA相对百分含量为指标。
硅胶的活化:称取100 g硅胶,在120℃的真空干燥箱内活化2 h后,取出冷却后,放于干燥器中备用。银化硅胶的制备:按比例称取硝酸银和硅胶放入研钵内,混合研磨充分混匀。装柱:取上述活化银化硅胶,加入80 mL石油醚(沸程:60~90℃),搅拌后匀浆静置1 h,使其充分溶胀,在层析柱底部预先放入高约1 cm的石英砂,加入20 mL石油醚,将溶胀的银化硅胶缓慢倾入,柱外用黑纸包裹,装完后垫上一层滤纸,加适量无水硫酸钠,打开旋塞,用石油醚洗柱平衡2 h后使用。上样:待层析柱内石油醚液面略高于硅胶面2 cm时,开始上样。取一定质量的脂肪酸用5 mL石油醚溶解,缓慢倒入柱内,注意不要使硅胶面浮动。洗脱:洗脱体系为含有无水乙醚的石油醚,洗脱液流速0.5~1 mL/min,每40 mL收集一次。脂肪酸回收:将收集到的各流分分别加入适量饱和氯化钠水溶液和石油醚振摇1 min,静置分层,除去下层残渣及氯化银与废液,再加入15%氯化钠水溶液洗涤2遍,最后用水冲洗1~2次,取上层有机相,在40℃条件下旋转蒸发除去溶剂,即得分离的脂肪酸组分,用于分析DHA和EPA含量。
1.2.3 脂肪酸的分析
甲酯化:氢氧化钾甲醇法。气相分析条件:色谱柱,FFAP石英毛细管柱,30 m ×0.25 mm(内径)×0.25 μm(膜厚);检测器为FID;进样口温度250℃,检测器温度250℃;色谱柱升温程序200℃保留15 min,以5℃/min升至240℃,直到分析完成;载气为氮气,压力500 kPa,空气压力50 kPa,氢气压力50 kPa,尾吹气压力200 kPa;分流方式进样,分流比为40∶1,进样量为1 μL。脂肪酸甲酯的定性采用标准品对照法。脂肪酸甲酯定量采用面积归一法。
1.2.4 游离脂肪酸吸附特性的研究[6]
准确称取银化硅胶(硅胶∶硝酸银 =15∶1)0.1 g,加入50 mL 50 mg/mL的脂肪酸-石油醚溶液,于30℃下恒温振荡,每隔0.5 h测定一次上清液中的总脂肪酸浓度(mg/mL),测定混合脂肪酸的吸附量随时间的变化趋势,得到混合脂肪酸的吸附动力学曲线,同时计算相应间隔时间内FFA的平均吸附速率。总脂肪酸浓度的测定参考GB/T 5530—2006。
2 结果与分析
2.1 硝酸银用量对EPA和DHA分离纯化效果的影响
洗脱效果见图1。
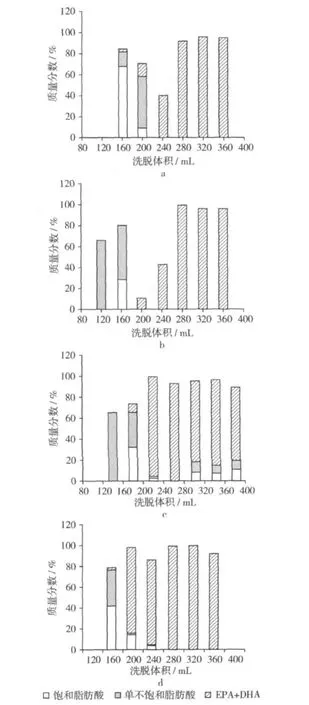
图1 硝酸银用量对EPA和DHA分离纯化效果的影响
硝酸银与硅胶用量的比值越大,则多不饱和脂肪酸与固定相结合的机会越多,其吸附将更完全。但一些单不饱和脂肪酸也可被吸附,在洗脱过程中,造成单不饱和脂肪酸和多不饱和脂肪酸难于分离或是需要更多的流动相才能将EPA和DHA洗脱下来。本试验采用15 g活化过的硅胶按照硅胶与硝酸银20∶1(图1a)、15∶1(图 1b)、10∶1(图 1c)和 8∶1(图1d)的比例混匀,进行试验。
从图1可看出,当硝酸银用量为1.00 g(硅胶∶硝酸银=15∶1)时,DHA和EPA分离效果最好,DHA和EPA与饱和脂肪酸和单不饱和脂肪酸的重合较少,流分中DHA和EPA的最高质量分数为99.29%;而当硝酸银用量分别为 0.75、1.50 和1.875 g时,虽然也可以获得高纯度的 DHA和EPA,但是与饱和脂肪酸和单不饱和脂肪酸并不能很好的分离(图中有重叠),或者是洗脱时间滞后,造成分离效果的不理想。因此,综合考虑选择以硅胶∶硝酸银的比例为15∶1较合适,即硅胶用量15 g和硝酸银用量1 g。
2.2 上样量对EPA和DHA分离纯化效果的影响
上样量直接影响层析柱的分离性能,当样品过载程度过大,会严重降低分离效率,甚至使色谱柱失去分离能力;而上样量不足,样液浓度低,扩散作用大,也可造成分离效率低。本试验称取15 g活化过的硅胶与1 g硝酸银,分别称取1.0 g(图2a)、0.75 g(图2b)、0.6 g(图2c)和0.5 g(图2d)混合脂肪酸上样,EPA和DHA分离纯化效果见图2。
从图2可以看出,当上样量为1.0 g时,色谱柱过载,分离效果差;当上样量为0.6 g时,EPA和DHA与饱和脂肪酸和单不饱和脂肪酸的分离有重叠,而且分离出的EPA和DHA总质量分数在75%左右;当上样量为0.5 g,脂肪酸浓度太低,EPA和DHA与固定相结合紧密,需要大量洗脱液才能将其洗脱下来;而当上样量为0.75g时,图2b中的曲线几乎没有重叠,EPA和DHA的质量分数可达99%左右,说明其分离效果较好。因此综合考虑选择在硅胶用量15 g和硝酸银用量1 g的情况下上样量为0.75 g。

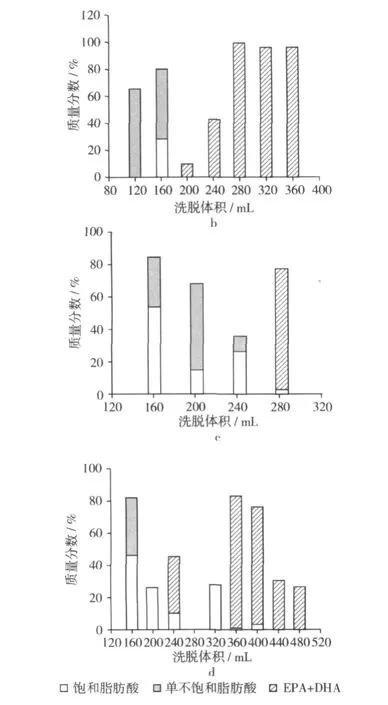
图2 脂肪酸上样量对EPA和DHA分离纯化效果的影响
2.3 洗脱体系对EPA和DHA分离纯化效果的影响
石油醚的极性较小,对于饱和脂肪酸有较好的洗脱力,加入无水乙醚调节极性后,较适合DHA和EPA等不饱和脂肪酸的彻底洗脱。石油醚具有洗脱饱和脂肪酸时速度快,洗脱效果彻底等优势,而洗脱体系中无水乙醚含量的多少对EPA和DHA的洗脱效果有明显影响。本试验采用硅胶用量15 g,硝酸银用量1 g,上样量0.75 g时,考察洗脱体系a(图3a,500 mL 4%无水乙醚的石油醚溶液)、b(图3b,500 mL 8%无水乙醚的石油醚溶液)、c(图3c,500 mL 10%无水乙醚的石油醚溶液)、d(图3d,依次用100 mL石油醚,2%,4%,8%,10%无水乙醚-石油醚溶液各100 mL)等对EPA和DHA分离纯化效果的影响。

图3 洗脱体系对EPA和DHA分离纯化效果的影响
从图3可以看出,当洗脱体系为a、b、c时,EPA和DHA与饱和脂肪酸和单不饱和脂肪酸的分离都不理想;而当洗脱体系为d时,EPA和DHA的分离效果较好,其质量分数可达99%左右。因此综合考虑选择洗脱体系为d,即依次用100 mL石油醚,2%,4%,8%,10%无水乙醚-石油醚溶液各100 mL进行洗脱。
2.4 EPA和DHA的含量分析
采用15 g硅胶与1 g硝酸银充分混合后装柱,上样0.75 g混合脂肪酸,然后依次用100 mL石油醚,2%,4%,8%,10%无水乙醚-石油醚溶液各100 mL进行洗脱。对分离前后的脂肪酸组成进行气相色谱分析,结果见图4和图5。

将图4和图5进行比较分析可以看出,蛇鲻鱼油经硅胶-硝酸银色谱柱分离后,EPA和DHA与饱和脂肪酸和单不饱和脂肪酸得到了有效的分离,分离产物中EPA和DHA的总质量分数可达90%以上。因此,试验结果表明采用上述分离纯化工艺可以获得高含量的EPA和DHA产物。
2.3 洗脱体系对EPA和DHA分离纯化效果的影响
2.5 FFA的吸附动力学曲线
准确称取银化硅胶0.1 g加入50 mL 50 mg/mL的游离脂肪酸-石油醚溶液于30℃下恒温避光振荡,每隔0.5 h测定一次上清液中的总脂肪酸浓度(mg/mL)。测定混合脂肪酸的酸度随时间的变化趋势,得到混合脂肪酸的酸度变化曲线,结果见6,同时计算相应间隔时间内混合脂肪酸的平均吸附量,结果见7。

从游离脂肪酸的吸附动力学曲线(图6)可以看出,随吸附时间的延长吸附量增加,约2 h后达到平衡;从银化硅胶对FFA的平均吸附速率曲线(图7)可以看出,吸附速率在前2 h迅速降低,以后逐渐缓和至平衡后几乎不再下降,基本符合单分子层吸附理论[6]。
3 结论
蛇鲻鱼油经过硅胶-硝酸银柱色谱分离纯化后,EPA和 DHA的质量分数分别从 4.43%和13.94%提高至21.47%和70.13%,总质量分数可达90%以上。因此,硝酸银-硅胶柱层析法是一种较理想的分离纯化EPA和DHA的方法,银化硅胶对脂肪酸的吸附符合单分子层吸附理论。
[1]刘书成,章超桦,谢燕,等.脂肪酶水解低值鱼油富集EPA和DHA甘油酯的研究[J].中国粮油学报,2009,24(3):79-83
[2]De Vries B.Quantitative separations of higher fatty acid methyl esters by adsorption chromatography on silica impregnated with silver nitrate[J].Journal of the American Oil Chemists'Society,1963,40(5):184 -186
[3]De Vries B.Separation of triglycerides by column chromatography on silica impregnated with silver nitrate[J].Journal of the American Oil Chemists'Society,1964,41(6):403 -406
[4]Williams C M,Mander L N.Chromatography with silver nitrate[J].Tetrahedron,2001,57(3):425 -447
[5]邱榕,范维澄.银离子络合物萃取DHA乙酯的络合机理研究.光谱学与光谱分析,2001,21(3):328-330
[6]张汆,阚建全,陈宗道.硝酸银-硅胶纯化α-亚麻酸的研究[J].离子交换与吸附,2005,21(01):47 -54
[7]夏向东,吕飞杰,台建祥,等.硅胶和硝酸银硅胶柱层析分离生育酚与生育三烯酚[J].中国粮油学报,2004,19(03):85-88.
Separation and Purification of EPA and DHA from Saurida elongate Oil by Silver Nitrate-Silica Gel Column
Zhang Liang1,2Liu Meiling1,2Dong Qiang3Liu Shucheng1,2Hao Jiming1,2Zhang Jing1,2
(College of Food Science and Technology,Guangdong Ocean University1,Zhanjiang 524088)
(Key Laboratory of Advanced Processing of Aquatic Products of Guangdong Higher Education Institution,Guangdong Ocean University2,Zhanjiang 524088)
(Product Quality Supervision and Inspection Institute of Xi'an3,Xi'an 474100)
Free fatty acids from saurida elongate oil were prepared by saponification of NaOH-alcohol and acidification of H2SO4.EPA and DHA were then separated and purified by using silver nitrate - silica gel column.The results showed that 15 g silica gel and 1 g silver nitrate were mixed thoroughly and put into the constant temperature chromatography cabinet at 5 ℃.After the balance of the chromatographic column,0.75 g free fatty acid was added and eluted respectively by 100 mL petroleum ether,100 mL petroleum ether of 2%diethyl ether,100 mL petroleum ether of 4%diethyl ether,100 mL petroleum ether of 8%diethyl ether,100 mL petroleum ether of 10%diethyl ether.The eluting speed was controlled at 0.5~1.0 mL/min;the elution was collected after 200 mL and evaporated by rotary evaporator.The contents of EPA and DHA were improved from 4.43 and 13.94%to 21.47%and 70.13%respectively.The total content of EPA and DHA was above 90%.
silver nitrate -silica gel,DHA,EPA,separation
TS254.9
A
1003-0174(2011)12-0063-06
2005粤港关键领域重点突破招标项目(2005A203 01002),2007年广东省自然科学基金(7301127),广东海洋大学引进人才基金(0612044)
2011-03-09
张良,男,1987年出生,硕士,水产品加工与贮藏工程
刘书成,男,1977年出生,副教授,硕士生导师,食品科学与工程
