邻二氮菲-Fe3+法测定保健食品中水溶性成分的抗氧化能力
2011-10-27刘雯佳刘彦霞
刘 薇,刘雯佳,刘彦霞,赵 建,文 镜*
(北京联合大学应用文理学院,生物活性物质与功能食品北京市重点实验室,北京 100191)
邻二氮菲-Fe3+法测定保健食品中水溶性成分的抗氧化能力
刘 薇,刘雯佳,刘彦霞,赵 建,文 镜*
(北京联合大学应用文理学院,生物活性物质与功能食品北京市重点实验室,北京 100191)
目的:建立用邻二氮菲-Fe3+测定保健食品中水溶性成分抗氧化能力的方法。方法:用水相提取保健食品中的水溶性抗氧化成分,使其还原反应体系中的Fe3+,生成的亚铁离子与邻二氮菲反应成稳定的橙红色络合物,用分光光度计在536nm波长处测定吸光度。以水溶性VE为对照,由此计算样品水溶性成分中抗氧化(还原性)物质的多少。通过对方法线性关系、最低检测限、精密度、准确度等指标进行测定,验证方法的可行性。结果:检测Trolox在质量浓度0.66~10.53μmol/L范围内呈现良好的线性关系(R2=0.9999);最低检测下限为0.54μmol /L;平行性精密度为2.7%;重复性精密度为3.3%;5次重复加标回收率为(99.9±4.6)%。结论:邻二氮菲-Fe3+法可用于保健食品中水溶性成分抗氧化能力的检测。
保健食品;抗氧化能力;邻二氮菲-Fe3+法
随着人们对自由基研究的日渐深入,发现损害人体健康的自由基几乎都与活性较强的含氧物质有关,因而把与这些物质相结合的自由基定义为活性氧自由基。活性氧自由基对人体的损害本质是一种氧化过程[1-3]。要降低自由基的损害,就需要抗氧化。抗氧化剂能够提供电子给自由基,并且在此过程中不会产生具有毒性或能引起自由基链式反应的活性产物,从而消除氧自由基,终止链式反应[4-7]。体外测定抗氧化物质清除自由基的方法主要包括化学发光法、分光光度法、电子自旋共振法、电化学检测法,气相色谱法和荧光法等[8-14]。这些方法中有些仪器试剂昂贵,操作复杂,使其应用受到限制。分光光度法仪器价格便宜,操作简单,是一般实验室的常规分析仪器。邻二氮菲比色法最初是用于检测样品中Fe2+含量,其原理是邻二氮菲可与Fe2+生成稳定的橙红色络合物,而这种物质在可见光区有显著的吸收,利用这一性质可对样品中的Fe2+进行测定[15-16]。标准的Fenton试剂是由H2O2与Fe2+组成的混合体系,Fe2+可以催化分解H2O2产生羟自由基(·OH),由此出现了对样品清除自由基的能力进行检测的邻二氮菲- Fe2+氧化法[17-18]。本实验室曾用分光光度计及邻二氮菲- Fe2+法检测保健食品的抗氧化能力[19]。该方法虽然具有操作简单,快速等优点,但由于方法中通过Fenton反应产生的自由基容易受到多方面因素的干扰,使方法的重复性受到影响。本实验采用分光光度计及邻二氮菲-Fe3+测定保健食品中水溶性成分抗氧化能力,使保健食品中的水溶性抗氧化成分直接与反应体系中的Fe3+作用,试图避开额外产生自由基的影响,提高方法的精密度。
1 材料与方法
1.1 材料与试剂
山竹粉 义乌章舸生物工程有限公司;葡萄籽胶囊艾申特生物科技有限公司;保健食品(品名:健康启程)北京北卫药业有限责任公司;茶色素 江西绿色制药有限公司;雅培牌胰肽素软胶囊 北京北卫药业有限责任公司。
1,10-邻二氮菲(分析纯) 广东汕头市西陇化工厂;水溶性维生素E 美国Sigma公司;磷酸(分析纯);磷酸二氢钠;磷酸氢二钾;硫酸高铁铵(分析纯);磷酸缓冲液PBS (75mmol/L、 pH7.4)、硫酸高铁铵(10mmol/L)、邻二氮菲(1.5mmol/L)、Trolox标准储备液(0.2g/L Trolox)。
1.2 仪器与设备
HH-4型数显恒温水浴锅 江苏省金坛市荣华仪器制造有限公司;PP-15专业型pH计 梅特勒-托利多仪器(上海)有限公司;P211D分析天平 北京赛多利斯有限公司;METTLER AE100电子天平 梅特勒-托利多仪器(上海)有限公司;涡旋混匀器 德国IKA公司;TDL-5CENTRIFUGE离心机 上海安亭科学仪器厂;KQ-100B台式超声波清洗器 昆山市超声仪器有限公司;UV-2450 紫外-可见分光光度计 日本Shimadzu 公司。
1.3 方法
1.3.1 邻二氮菲-Fe3+分光光度法原理
将待测保健食品样品粉碎,用磷酸缓冲液提取样品中水溶性抗氧化成分。反应体系中的三价铁离子(Fe3+)被提取液中的抗氧化成分(还原性物质)还原为Fe2+,亚铁离子再与反应体系中的邻二氮菲生成稳定的橙红色络合物,其吸光度与Fe2+浓度的关系符合朗伯-比耳定律,可用分光光度计检测,由此测定出样品中抗氧化(还原性)物质的多少。以水溶性VE为标准,用每单位抗氧化样品还原能力相当于水溶性VE的当量作为该样品的抗氧化能力。
1.3.2 样品提取
准确称取样品(例如葡萄籽胶囊0.025g)用20mL缓冲液溶解后,超声提取20min, 5000r/min离心10min,将上清移入50mL容量瓶内,沉淀用20mL缓冲液溶解后再提取一次,合并两次提取液,用缓冲液定容至50mL摇匀,即为待测样品。
1.3.3 样品及Trolox的测定
在干净试管中加入1mL磷酸缓冲液PBS,再加入0.1mL样品或标准Trolox(分别为样品管或标准Trolox管),再加入2mL邻二氮菲和0.5mL硫酸高铁铵,水浴30min后取出试管再加入0.2mL磷酸,室温静置10min;以不加入任何样品或标准Trolox,其他条件与上述相同的试管为对照管;以只加0.1mL样品其余体积用磷酸缓冲液PBS补齐,该试管为样品空白管。在536nm波长处以蒸馏水调零比色测定其吸光度,记录数值。
反应中Fe3+会被抗氧化剂还原为Fe2+,但未反应完剩余的Fe3+也会与邻二氮菲生成黄色络合物,因此当Fe2+和Fe3+共存情况下,Fe3+的干扰是客观存在且不可忽视的。因此选用磷酸(H3PO4)当掩蔽剂,Fe3+可与H3PO4形成稳定的无色Fe(HPO4)+配离子,从而有效地排除了显色时Fe3+对Fe2+离子的干扰。H3PO4不具有氧化性,测定时不参与对Fe2+离子的氧化作用。
1.3.4 抗氧化能力计算

式中:抗氧化能力值以Trolox当量(μmol Trolox当量/g)表示,即1g样品相当于Trolox微摩尔数;A样品、ATrolox、A对照分别为样品管、标准管和对照管的吸光度;MTrolox为标准管所含Trolox的微摩尔数;M样品为样品管所含样品的质量。
1.3.5 标准曲线的绘制
取0.2g/L Trolox标准储备液1mL加1mL磷酸缓冲液稀释为0.1g/L应用液,再将应用液用磷酸缓冲液稀释为0.05、0.025、0.0125、0.00625g/L的Trolox标准品溶液。按1.3.3节方法测定。
1.3.6 最低检测下限
连续测定对照管吸光度10次,根据最低检测限的计算公式计算结果。
DL=3SD/K
式中:DL为最低检测限;SD为标准偏差;K为斜率。
1.3.7 平行性精密度实验
准确称取山竹粉0.025g 5份,平行操作,用1.3.3节方法提取并测定。
1.3.8 重复性精密度实验
每天准确称取山竹粉0.025g 3份,用1.3.3节方法提取并测定。连续测定5 d。
1.3.9 加标回收率实验
准确称取0.025g山竹粉2份,其中一份定量加入0.0025g标准Trolox,样品处理及测定方法同上。重复测定5次。

2 结果与分析
2.1 Trolox标准曲线的绘制

图1 Trolox标准曲线Fig.1 Troloxst and ardcurve
由图1可知,Trolox 在质量浓度0.00625~0.1g/L范围内有较好的线性关系和较低的检测下限。
2.2 最低检测下限测定
平行测定10次对照管值,计算可得方法检测Trolox的最低检测下限为0.27μmol/L。由于在实际样品测定时干扰因素较多,因此将这一数值再放大2倍作为本方法的最低检测下限,即0.54μmol/L。
2.3 平行性精密度实验
用山竹粉样品进行平行性精密度实验,5个平行测定结果为(396±11.0)μmol/g ,变异系数为2.7%,表明方法的平行性精密度良好。
2.4 重复性精密度实验结果
用山竹粉进行重复性精密度实验,其5次重复性测定结果为(402±13.2)μmol/g ,变异系数为3.3%,表明方法的重复性精密度良好。
2.5 加标回收率实验结果
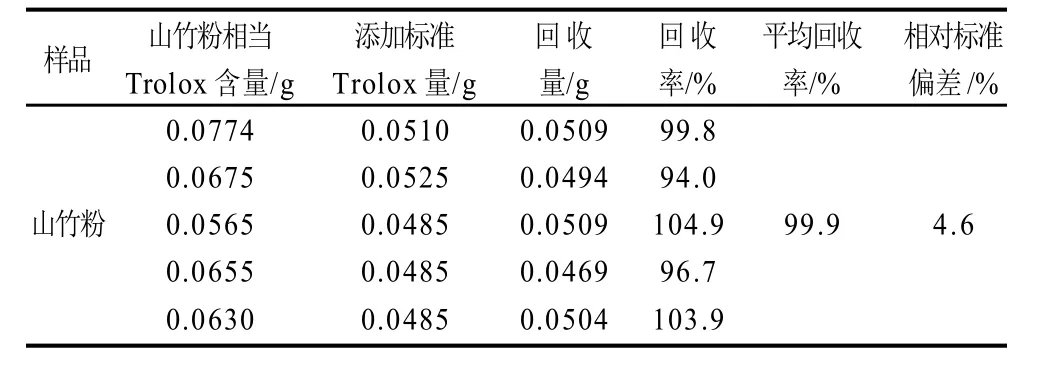
表1 加标回收率实验结果Table1 Spiker ecoveries for Trolox in mangosteen powder
用山竹粉样品进行加标回收率实验(表1),5次重复结果为(99.9±4.6)%,表明方法具有较好的准确度。用邻二氮菲-Fe2+法测定同一样品(山竹粉),将邻二氮菲-Fe3+法与邻二氮菲-Fe2+法[19]测定结果进比较(表2)。结果表明,邻二氮菲-Fe3+法测得最低检测下限有了明显的下降,这可能与邻二氮菲-Fe2+法反应体系中有H2O2的有关。当H2O2加量过多,过量的H2O2与样品中还原性物质反应,还原性物质对Fe2+保护的灵敏性下降,使得检测下限偏高。另外,邻二氮菲-Fe3+法重复性精密度明显好于邻二氮菲-Fe2+法,其他指标都与邻二氮菲-Fe2+法相差不大。说明与邻二氮菲-Fe2+法比较,邻二氮菲-Fe3+法测定保健食品抗氧化能力有更好的稳定性。

表2 邻二氮菲-F e2+法与邻二氮菲-F e3+法方法学对比Table2 Methodological comparisonbetween phenan throline-Fe2+ and phen an throline-Fe3+ methods
2.6 5种样品抗氧化能力的测定结果

表3 样品抗氧化能力测定结果(n=5)Table 3 Antioxidant capacity of various commercial functional foods determined by phenanthroline-Fe3+ method (n=5)
用该方法顺利测定了山竹粉等5种样品中水溶性部分的抗氧化能力,结果见表3。重复测定结果的变异系数为2.2%~2.8%,表明用此方法实测样品,结果具有良好的重复性。
3 讨 论
3.1 方法的适用性
由于方法的显色反应是在水相中进行,因此对于样品的提取、分离等前处理过程采用磷酸缓冲液,标准参照物也选择了水溶性VE。保健食品中的抗氧化活性成分可以分为脂溶性和水溶性两部分。本方法只能检测到保健食品中水溶性成分的抗氧化能力,样品中脂溶性成份的抗氧化能力不能被测定出来。 因此此方法适用于检测不含脂溶性成份或脂溶性成份含量低的保健食品。对于脂溶性成份含量高的保健食品,本方法只能检测其水溶性成份的抗氧化能力,脂溶性成份的抗氧化能力需采用其他方法检测。
3.2 方法的局限性
保健食品中的抗氧化成份绝大部分为能够给出电子将自由基转变为阴离子的还原剂。常见金属离子氧化性排列顺序如下:K+<Ca2+<Na+<Mg2+<Al3+<Mn2+<Zn2+<Cr3+<Fe2+<Ni2+<Sn2+<Pb2+<(H+)<Cu2+<Hg2+<Fe3+<Ag+<Pt2+<Au2+从这个排列顺序可知Fe3+具有很强的氧化性,因此能够与保健食品中的绝大部分还原剂反应,故采用邻二氮菲Fe3+法可将这些具有还原性的抗氧化成份检测出来。但是个别样品可能会含有一些高氧化还原电位的抗氧化物质,它们不能将Fe3+还原,尽管它们能够与自由基发生反应但用本方法却不能将它们检测出来,这是本方法的局限性。
4 结 论
邻二氮菲-Fe3+法具有良好的准确度(RSD 2.7%)和精密度(RSD 3.3%);最低检测下限为0.54μmol/L;在0.66~10.53μmoL/L Trolox浓度范围内具有较好的线性关系(R2=0.9999)。邻二氮菲-Fe3+法避开自由基的生成和消耗,简化了实验的步骤,与邻二氮菲-Fe2+法相比具有更好的稳定性,实验证明邻二氮菲-Fe3+法适用于保健食品水溶性成份抗氧化能力的检测。
[1] ABDI S, ALI A. Role of ROS modified human DNA in the pathogenesis and etiology of cancer[J]. Cancer Letters, 1999, 142(1): 1-9.
[2] OLSEN H, SELJEFLOT I, KHLER H, et al. Increased leukocyte levels of reactive oxygen species (ROS) in populations at risk for atherosclerotic disease[J]. Atherosclerosis, 2000, 151(1): 57-59.
[3] ANGELOPOULOU R, LAVRANOS G, MANOLAKOU P. ROS in the aging male: Model diseases with ROS-related pathophysiology[J]. Reproductive Toxicology, 2009, 2(28): 167-171.
[4] 李云. 综述自由基对人体健康的影响及目前的预防措施[J]. 内蒙古石油化工, 2011(1): 87-89.
[5] 方允中. 自由基生物学的理论与应用[M]. 北京: 科学出版社, 2002: 649-703.
[6] RYAN P, HYNES M J. The kinetics and mechanisms of the complex formation and antioxidant behaviour of the polyphenols EGCg and ECG with iron(Ⅲ)[J]. Journal of Inorganic Biochemistry, 2007, 101(4): 585-593
[7] CASALINO E, CALZARETTI G, SBLANO C, et al. Molecular inhibitory mechanisms of antioxidant enzymes in rat liver and kidney by cadmium[J]. Toxicology, 2002, 179(1/2): 37-50.
[8] 文镜, 刘璇, 赵建. 荧光法及化学发光法在保健食品抗氧化体外实验中的应用[J]. 中国酿造, 2009(11): 130-133.
[9] 杨芬, 张瑞萍, 贺玖明, 等. 羟自由基的产生、捕集及检测方法[J].药学学报, 2007, 42(7): 692-697.
[10] 陈培榕, 李景虹, 邓勃. 现代仪器分析试验与技术[M ]. 北京: 清华大学出版社, 2006,17(11): 65-67.
[11] 丛建波, 孙存普, 莫简. 自旋捕集短寿命自由基的低温保存[J]. 生物化学与生物物理进展, 1993, 20(4): 326-327.
[12] 续洁琨, 姚新生, 栗原博. 抗氧化能力指数(ORAC)测定原理及应用[J]. 中国药理学通报, 2006, 22(8): 1015-21.
[13] 程宏英, 曹玉华. 毛细管电泳-电化学检测法测定硫酸铜-维生素C反应体系中的羟基自由基和菊花的抗氧化活性[J]. 2007, 25(5): 681-685.
[14] ONOR, ODA T. Measurement of hydroxyl radicals in pulsed corona discharge[J]. Journal of Elect rostatics, 2002, 55: 333-342.
[15] SAYWELL L B, CUNNINGHAM B B. Determination of iron: colorimetric o-phenanthroline method[J]. Analytical Chemistry, 1937, 9(2): 67-69.
[16] TAMURA H, GOTO K, YOTSUYANAGI T, et al. Spectrophotometric determination of iron(Ⅱ) with 1,10-phenanthroline in the presence of large amounts of iron(Ⅲ)[J]. Talanta, 1974, 21(4): 314-318.
[17] 陈胜兵, 何少华, 娄今生, 等. Fenton试剂的氧化作用机理及其应用[J]. 环境科学与技术, 2004, 3(27):105-107.
[18] 金鸣, 蔡亚欣, 李金荣, 等. 邻二氮菲-Fe2+氧化法检测H2O2/Fe2+产生的羟自由基[J]. 生物化学与生物物理进展, 1996, 23(6): 553-555.
[19] 文镜, 刘薇, 王宏君, 等. 邻二氮菲-Fe2+法测定保健食品的抗氧化能力[J]. 食品科学, 2010, 31(18): 333-337.
Determination of Antioxidant Capacity of Water-soluble Compounds in Functional Food by Phenanthroline-Ferric Ion Method
LIU Wei,LIU Wen-jia,LIU Yan-xia,ZHAO Jian,WEN Jing*
(Beijing Key Laboratory of Bioactive Substances and Functional Foods, College of Arts and Science, Beijing Union University, Beijing 100191, China)
Objective: To establish a colorimetric method to determine the antioxidant capacity of water-soluble compounds in functional food based on the reaction between 1,10-2 phenanthroline and Fe3+to form yellow complexes. Methods: The hydrophilic antioxidants in functional foods were extracted with pH 7.4 PBS buffer solution (75 mmol/L) and allowed to reduce Fe3+to Fe2+. Fe2+was exposed to 1,10-2 phenanthroline to form a stable Fe2+-phenanthroline complex. The absorbance of the complex was determined on a spectrophotometer at 536 nm and used to calculate the antioxidant capacity of water-soluble compounds in functional food using Trolox, a water soluble vitamin E analog, as the reference standard. The accuracy, linearity, repeatability, recovery rate and limit of detection (LOD) of this method were studied, and its feasibility was also verified. Results: This method showed a good linearity over the Trolox concentration of 0.66-10.53 μmol/L (R2= 0.9999). The LOD was 0.54 μmol/L. The replicability and repeatability was 2.7% and 3.3% relative standard deviation (RSD), respectively. The mean spike recovery was (99.9±4.6)% (n = 5). Conclusion: This method is applicable to determine the antioxidant capacity of water-soluble compounds in functional food.
functional food;antioxidant capacity;phenanthroline-Fe3+method
TS207.3
A
1002-6630(2011)16-0261-04
2011-05-16
北京市教委科技发展计划项目(KM201011417006)
刘薇(1986—),女,助理工程师,主要从事保健食品功能评价研究。E-mail:liuwei4465@sina.com
*通信作者:文镜(1952—),男,教授,主要从事保健食品功能学评价机理和方法学研究。E-mail:wenjing@ygi.edu.cn
