载铁活性炭对水中草甘膦吸附性能研究
2011-10-20徐炎华南京工业大学环境学院江苏南京210009
谢 明,徐炎华(南京工业大学环境学院,江苏 南京 210009)
载铁活性炭对水中草甘膦吸附性能研究
谢 明,徐炎华*(南京工业大学环境学院,江苏 南京 210009)
通过浸渍-焙烧法制备载铁活性炭,并用SEM电镜分析了载铁活性炭表面形态,研究了载铁活性炭(Fe-AC)对草甘膦溶液的吸附等温线和吸附动力学,并分析了各种影响因素对载铁活性炭吸附性能的影响.实验表明,Freundlich方程可以对Fe-AC草甘膦吸附等温线进行很好拟合,最大吸附量约为5.8mmol/g;其吸附动力学过程用Lagergren方程拟合,吸附速率常数在0.088min-1左右,且随着温度的升高逐渐减小.根据Kannan & Sundaram颗粒内扩散模型拟合,颗粒内扩散速率常数kp大于10mg·min-1/2/g,并随着起始温度的升高而减小.由于草甘膦的存在形态和Fe-AC材料表面性质的变化,AC-Fe对草甘膦的吸附能力随水溶液的pH升高而降低.NaCl的存在产生拮抗效应使得Fe-AC对草甘膦的吸附容量大大下降,随着NaCl浓度增加至4g/L后,盐析效应开始占主导地位,使得Fe-AC的吸附容量略有增加;由于草甘膦分子的空间位阻效应和亚磷酸根与载铁活性炭表面形成较强的络合物,使得随亚磷酸根浓度的升高Fe-AC对草甘膦的吸附量持续下降.
吸附;草甘膦;载铁活性炭
草甘膦(分子式 C3H8NO5P)是一种除草有机磷农药,杀草谱广,杀草力强[1].草甘膦分子中含有羧基、氨基、甲基膦酸基,其化学性质兼有这些基团的某些特性,在适当的条件下,可以进行酯化、羟烷基化、胺化、亚硝化、磺酰化、膦羧甲基化和脱水等典型化学反应.我国草甘膦产量达到25万t/a,且主要生产企业多分布在江苏、浙江等人口密度大、环境容量小且位于长江、太湖等地区.草甘膦生产废水排放量大、有机污染物浓度高、无机盐含量高、治理难度大.因此,成为该行业迫切需要解决的共性问题.
常用的处理草甘膦生产废水的方法主要包括光催化氧化法[2-3]、氯氧化[4-5]、电极电解法[6]、物化-生化组合法[7-11]等.考虑到废水中含有较高浓度的草甘膦,吸附法是一种潜在的处理废水、回收草甘膦的有效方法.目前对草甘膦的吸附研究主要集中于不同吸附剂[12-13]对低浓度草甘膦的吸附过程,以及针对土壤环境中痕量[14-17]的草甘膦在黏土、铝铁的(氢)氧化物上的吸附.
活性炭是一种比表面积大,耐酸、耐碱,具有良好热稳定性的吸附剂.但是活性炭对草甘膦的亲和力相对较弱,选择性低,吸附容量小.通过金属盐的负载[18],形成活性炭表面的金属氧化层,以增强对草甘膦的吸附选择性,提高对草甘膦的吸附容量.本实验以活性炭为载体,在活性炭表面通过浸渍-焙烧的方法负载氧化铁,研究了载铁活性炭对水溶液中草甘膦的吸附过程,重点研究了溶液pH值以及氯化钠、亚磷酸根对载铁活性炭吸附性能的影响.
1 实验部分
1.1 仪器与试剂
THZ2C恒温振荡器(太仓市光明实验分析仪器厂);UV-2450型紫外-可见分光光度计(日本岛津公司);PHS-3C型pH计(上海精密科学仪器有限公司);椰壳活性炭(溧阳竹溪活性炭有限公司).
草甘膦(≥98%,南通江山农化有限公司)、盐酸(HCl),氢氧化钠(NaOH),氯化钠(NaCl),亚磷酸(H3PO3),硝酸铁(Fe(NO3)3·9H2O)均为分析纯.实验用水为超纯水.草甘膦浓度采用测定.
1.2 载铁活性炭的制备
将颗粒活性炭置于0.01mol/L HNO3溶液中清洗浸洗12~15h,抽滤后用去离子水洗涤;再用去离子水煮沸2~3h后漂洗至pH值为中性,在110℃下烘干备用.
将经预处理后的活性炭 2g用 10%的Fe(NO3)3·9H2O浸渍液100mL过量浸渍24h.过滤后,将活性炭在室温下自然晾干,在 80℃下干燥4~5h后,放于箱式电阻炉中在氮气保护气氛中以300℃恒温焙烧 2h,在氮气保护的气氛中冷却至室温,制得载铁活性炭(记为Fe-AC).
1.3 吸附实验
1.3.1 吸附等温线实验 分别准确称取 Fe-AC吸附剂0.2g于250mL具塞锥形瓶中,然后依次向一系列锥形瓶中分别加入 100mL浓度为 500,1000,1500,2000,3000,4000,5000mg/L的草甘膦溶液 (pH值不做调整),分别在288,289K下恒温振荡 24h,使吸附达到充分平衡.测试平衡后溶液中草甘膦的浓度Ce(mg/L),并根据式(1)计算Fe-AC的平衡吸附量:

式中:C0和Ce分别为吸附前后溶液中草甘膦的浓度,mg/L;V为溶液的体积,L;m为吸附剂的质量,g;M 为草甘膦分子量;Qe为平衡吸附量,mmol/g.
1.3.2 静态吸附动力学学实验 准确称取Fe-AC 0.500g于1000mL的锥形瓶中,加入浓度为900mg/L的草甘膦模拟溶液800mL.控制环境温度分别为 288,298K,在恒温振荡器中振荡,间隔取样时间分别为 5,10,15,20,40,60min,直至达到吸附平衡.测定溶液中溶质含量Ct,计算即时吸附量Qt(mmol/g).

式中:C0和 Ct分别为原溶液和 t时刻溶液的浓度,mg/L;V为溶液的体积,L;m为Fe-AC重量,g;M为草甘膦的分子量.
2 结果与讨论
2.1 载铁活性炭上的表征
由图 1可见,实验中使用的活性炭以椰壳为原料,载铁粒径在0.5~1μm左右,整体分布较为均匀,对活性炭的表面形态没有大的影响.由表1所示,与原活性炭相比,通过惰性气氛下载铁焙烧改性的活性炭比表面积有所提高,其原因可能是在高温下,硝酸铁分解产生的气体冲击形成了更多的孔道.然而,在此过程中产生的孔道因气流的不均匀性导致了一定程度的塌陷,因此活性炭平均孔径减小.元素分析结果表明,本实验中采用的载铁方法在活性炭上引入了8%(质量百分比)的铁.所担载的铁在活性炭上的存在形态可能是铁单质与氧化物的混合物,因为制备过程中在惰性气体保护高温条件下活性炭具有较强的还原性,有可能将氧化铁还原为单质铁,刘成等[19]也有类似的报道.

图1 载铁前后活性炭SEM照片Fig.1 Scanning electron magnification photos of origin and supported ferric active carbon

表1 活性炭载铁前后比表面积和平均孔径变化Table 1 The changes on specific surface area and average pore diameter of active carbon before and after ferric surpoorted
通过高温焙烧在活性炭表面上进行铁的担载,载铁活性炭的比表面积因分解气体的冲击而增大,与此同时,通过铁和氧化铁对草甘膦的较强络合能力,使得载铁活性炭的吸附性能力有明显的提高.
2.2 吸附等温线
AC-Fe和未载铁的活性炭(AC)对草甘膦的吸附等温线如图2所示.由表2可见,AC-Fe对草甘膦的吸附等温线可以被 Freundlich方程很好地拟合,最大吸附量约为 5.8mmol/g.与活性炭相比,负载铁之后AC-Fe对草甘膦的吸附量大大提高.通过载铁后,活性炭的吸附点位增加,吸附量有明显的提高.同时,Fe-AC吸附等温方程中 Kf值均大于AC,表明Fe-AC对草甘膦的吸附能力明显优于AC.对于同一种Fe-AC来讲,温度升高时 Kf值减小,表明降低温度有利于吸附.此外方程中的n值均大于1,表明草甘膦在Fe-AC上的吸附过程为优惠吸附.

表2 草甘膦的Freundlich吸附等温方程Table 2 Freundlich adsorption isotherm equation of glyphosate

图2 Fe-AC和AC的草甘膦吸附等温线Fig.2 The glyphosate adsorption isothermal equations of Fe-AC and AC
2.3 静态吸附动力学
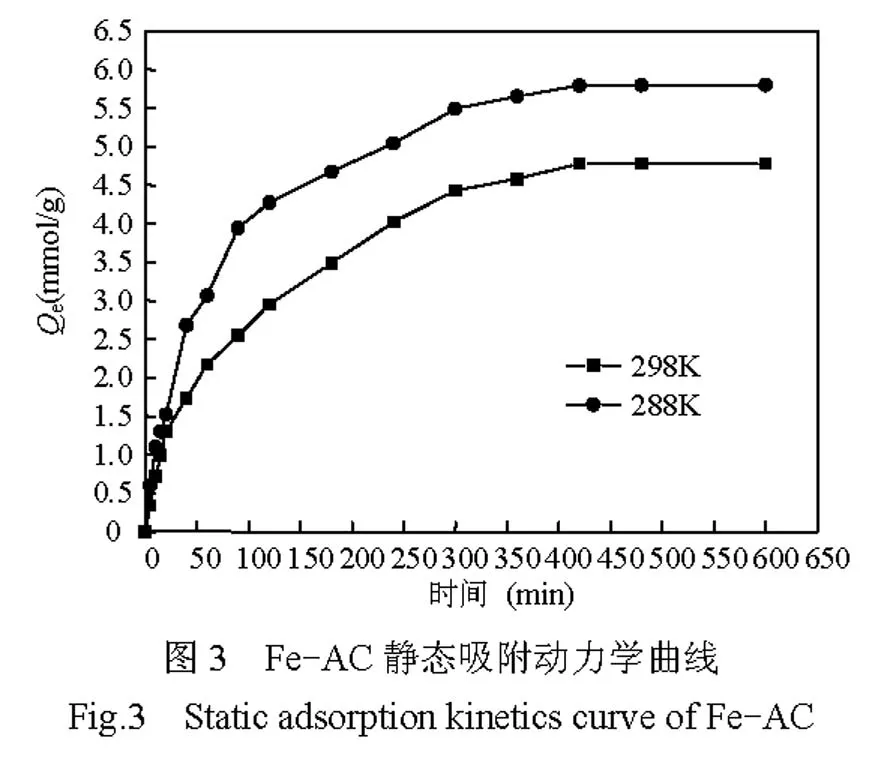
Fe-AC静态吸附动力学实验中Qt随t的变化曲线见图 3.曲线为指数形式,表明为一级吸附动力学特征.
取前 300min为初始快速吸附阶段,采用Lagergren一级速率方程[20-21]计算吸附速率.

式中:F=Qt/Qe代表t时刻的吸附分数;Kad为吸附速率常数,min-1;Qe和Qt分别为吸附达到平衡和t时刻单位质量吸附剂吸附草甘膦的量,mmol/g.
吸附速率常数Kad及相关参数见表3.
表3 Lagergren方程中吸附速率常数及相关系数Table 3 Adsorption rate constant and related coefficientsof lagergren equation

表3 Lagergren方程中吸附速率常数及相关系数Table 3 Adsorption rate constant and related coefficientsof lagergren equation
注:初始浓度5000mg/L
参数 298K 288K Kad(min-1) 0.078 0.088截距 -0.037 -0.0714 R20.984 0.981
Lagergren方程拟合的相关系数大于0.98,可见该方程的应用是可信的.吸附速率常数在0.088min-1左右,且随着温度的升高逐渐减小.
根据Kannan & Sundaram[22]颗粒内扩散模型:

式中:kp为颗粒内扩散速率常数,mg⋅min-1/2/g.
经拟合得到的颗粒内扩散速率常数及其他参数见表4所示.

表4 颗粒内扩散速率常数及相关系数Table 4 Inner diffusion constant and related coefficients
根据Kannan & Sundaram颗粒内扩散模型拟合的方程的相关系数>0.98,因此该模型的应用是可靠的.颗粒内扩散速率常数 kp的值大于10mg·min-1/2/g,并随着起始温度的升高而减小.根据McKay理论[23],表4中直线的截距代表了界面层的厚度,其数值越大则界面越厚,从本实验中可以看出初始温度越高,界面层越厚.在不同的初始温度下,拟合方程直线均不经过原点,表明了颗粒内扩散过程对草甘膦在Fe-AC上的吸附虽有较大影响,但不是该过程的唯一影响因素[23],可能还存在其他影响扩散速率的因素,如液膜传质扩散与颗粒内扩散共同作用等.
2.4 pH值对草甘膦吸附性能的影响

由于草甘膦在不同pH值条件下的电离形态不同,因此吸附剂Fe-AC对草甘膦的吸附也存在着较为明显的影响.溶液 pH值通过影响草甘膦的电离形态和吸附材料的荷电性质,从而影响草甘膦和吸附材料的亲和性,最终影响平衡吸附量.图4表明,随着pH值的增加,载铁活性炭对草甘膦的吸附效果逐渐下降.当pH值2左右时,草甘膦平衡吸附量最大;当pH值10左右时,草甘膦的吸附量只有pH值2时的10%左右.从草甘膦电离形态来看,根据草甘膦的三级电离常数[24],草甘膦在pH值2左右时呈分子态,与载铁活性炭的亲合力大,最易被吸附.当随着pH值增加,草甘膦在溶液中以带负电的离子状态存在时,吸附在Fe-AC表面上的草甘膦分子间由于带有相同的电荷而产生静电排斥力,降低了其平衡吸附量.从吸附材料表面的电荷性质[25]来看,载铁活性炭的荷电在不同pH值下也发生变化:随溶液pH值升高时,氧化铁表面的正电荷密度降低,减弱了其与草甘膦之间的亲和力.以上两方面的共同作用影响了草甘膦与载铁活性炭的亲和力,使吸附效果随pH值的升高而逐渐下降.
2.5 NaCl对草甘膦吸附性能的影响
在草甘膦的甘氨酸—亚磷酸甲酯工艺中,其生产废水的NaCl浓度在0.5~2g/L.由图5可以看出,溶液中 NaCl的存在对活性炭吸附草甘膦的效果影响较大,NaCl的存在使得各种活性炭对草甘膦的吸附容量大大下降.这主要是由于 C1-与草甘膦分子对载铁活性炭表面的活性吸附点位具有很强的竞争作用,降低了载铁活性炭对草甘膦的吸附量.对于载铁活性炭吸附草甘膦来说,溶液中NaCl对吸附产生的是拮抗效应.从图5还可以看出,NaCl浓度从0增加到4g/L时,活性炭对草甘膦的吸附容量呈下降趋势,主要原因是溶液中C1-越多,拮抗效应的影响程度就越大.当NaCl浓度>4g/L后,这种竞争拮抗效应不再增加,盐析效应开始占主导地位,主要原因可能是此时活性炭表面的活性吸附点位已全部被占用,此时再提高 Cl-的浓度只可能增加盐析效应的影响程度,降低溶质的溶解度,从而使得溶质析出后在活性炭上被吸附,因此活性炭的吸附容量略有增加.

2.6 亚磷酸根对草甘膦吸附性能的影响
亚磷酸根广泛存在于甘氨酸-亚磷酸二甲酯法草甘膦生产废水中,典型的草甘膦生产废水中的亚磷酸根的浓度在1.1g/L左右.由于亚磷酸根对铁具有很强的亲和力,其存在可以严重地影响着载铁活性炭对草甘膦的吸附性能.图6表明,溶液中亚磷酸根的存在对草甘膦在Fe-AC上的吸附具有明显抑制作用.

图6 亚磷酸根对草甘膦吸附性能影响Fig.6 Effect of phosphite on the glyphosate adsorption
随着水溶液中亚磷酸根浓度的升高,Fe-AC对草甘膦的吸附量持续下降.当亚磷酸根浓度达到2g/L时,草甘膦的吸附量降至原来的15%左右.从亚磷酸根和草甘膦分子结构的角度可以知道,亚磷酸根和草甘膦分子均有相似的 P—OH键,因此两者对载铁活性炭表面存在着竞争吸附.然而,草甘膦的分子直径明显大于亚磷酸根,其空间位阻效应导致载铁活性炭表面的吸附点位更容易被亚磷酸根占据.另一方面,亚磷酸以HPO32-的形式与载铁活性炭中的氧化铁形成较强的络合物[26],进一步占据活性炭吸附点位,从而降低草甘膦的平衡吸附量.
3 结论
3.1 Freundlich方程拟合Fe-AC对草甘膦的吸附等温线,最大吸附量约为5.8mmol/g.
3.2 Lagergren方程拟合Fe-AC对草甘膦的吸附动力学过程,吸附速率常数在 0.088min-1左右,且随着温度的升高逐渐减小.
3.3 Kannan & Sundaram颗粒内扩散模型拟合,颗粒内扩散速率常数kp大于10mg·min-1/2/g,并随着起始温度的升高而减小.
3.4 AC-Fe对草甘膦的吸附能力随水溶液的pH升高而降低,这主要是因为草甘膦的存在形态和Fe-AC材料表面性质的变化所引起的.
3.5 NaCl的存在产生拮抗效应使得Fe-AC对草甘膦的吸附容量大大下降,随着 NaCl浓度增加至 4g/L后盐析效应开始占主导地位,使得Fe-AC的吸附容量略有增加.
3.6 由于草甘膦分子的空间位阻效应和亚磷酸根与载铁活性炭中的氧化铁形成较强的络合物,使得随亚磷酸根浓度的升高,Fe-AC对草甘膦的吸附量持续下降.
[1] 卢 信,赵炳梓,张佳宝,等.除草剂草甘膦的性质及环境行为综述 [J]. 土壤通报, 2005,36(5):785-790.
[2] Chen Yong, Wu Feng, Lin Yixin, et al. Photodegradation of glyphosate in the ferrioxalate system [J]. Journal of Hazardous Materials, 2007,148:360-365.
[3] Chen Shifu, Liu Yunzhang. Study on the photocatalytic degradation of glyphosate by TiO2photocatalyst [J]. Chemosphere,2007,67:1010-1017.
[4] Akbar Mehrsheikh, Marian Bleeke, Stephan Brosillon, et al.Investigation of the mechanism of chlorination of glyphosate and glycine in water [J]. Water Research, 2006,40:3003-3014.
[5] Brosillon S, Wolbert D, Lemasle M, et al. Chlorination kinetics of glyphosate and its by-products: Modeling approach [J]. Water Research, 2006,40:2113-2124.
[6] Aquino Neto S, Andrade A R. Electrooxidation of glyphosate herbicide at different DSA compositions: pH, concentration and supporting electrolyte effect [J]. Electrochimica Acta, 2009,54:2039-2045.
[7] 曹晓莹,沈耀良.ABR反应器处理草甘膦废水的研究 [J]. 工业水处理, 2004,24(7):28-30.
[8] 沈耀良,曹晓莹.草甘膦生产废水及其厌氧处理技术 [J]. 工业用水和废水, 2005,36(1):28-31.
[9] 程 鸣,何文英,彭光明,等.农药草甘膦生产废水处理的研究[J]. 工业用水和废水, 2003,34(1):30-32.
[10] 郭艳华,胡望平,杨宏沙.草甘膦生产废水除磷的工程实例 [J].能源环境保护, 2007,21(4):47-49.
[11] 胡大锵,司知侠.草甘膦农药废水处理工程改造设计及运行 [J].工业给排水, 2008,34(10):58-61.
[12] 沈丽静,乐清华.杨毓华,等.活性炭处理草甘膦废水的静态吸附研究 [J]. 化学工程师, 2006,133(10):46-49.
[13] 彭 波,王黎之,李艳荣.活性氧化铝吸附法处理草甘膦生产废水的研究 [J]. 化学工业与工程技术, 2007,28(2):44-48.
[14] Sheals J, Sjoberg S, Persson P,et al. Adsorption of glyphosate on goethite:molecular characterization of surface complexes [J].Environment Science and Technology, 2002,36(14):3090-3095.
[15] Gimsing A L, Borggaard O K. Phosphate and glyphosate adsorption by hematite and ferrihydrite and comparisonwith other variable-chargeminerals [J]. Clays Minerals, 2007,55(1):110-116.
[16] Gimsing A L, Szilas C, Borggaard O K. Sorption of glyphosate and phosphate by variable-charge tropical soils from Tanzania [J].Geoderma, 2007,138:127-132.
[17] 卢 信,赵炳梓,张佳宝,等.磷酸盐对农药草甘膦在不同土壤中迁移的影响 [J]. 中国环境科学, 2005,25(5):607-610.
[18] Shi Qianqian, Zhang Jian, Zhang Chenglu, et al. Adsorption of Basic Violet 14in aqueous solutions using KMnO4-modified activated carbon [J].Journal of Colloid and Interface Science,2010,343:188-193.
[19] 刘 成,高乃云,黄廷林.活性炭的表面化学改性研究进展 [J].净水技术, 2005,24(4):50-52.
[20] Dutta M, Baruah R, Dutta N N, et al. Adsorption of 6-aminopenicillanic acid on activated carbon [J]. Separation and Purification Technology, 1997,12:99-102.
[21] McKay G. The adsorption of dyestuff from aqueous solution using activated carbon: analytical solution for batch adsorption based on external mass transfer and pore diffusion [J]. Chemical Engineering Journal, 1983,27:187-190.
[22] Kannan N, Sundaram M M.Kinetics and mechanism of removal of methylene blue by adsorption on various carbons--a comparative study [J]. Dyes and Pigments, 2001,51:25-29.
[23] McKay G, Otterburn M S, Jamal A Aga, et al. Fullter’s earth and fired clay as adsorbents for dyestuffs [J]. Water Air Soil Pollution,1985,24:307-310.
[24] Romina C Pessagno, Rosa M Torres Sanchez, Marıa dos Santos Afonso. Glyphosate behavior at soil and mineral-water interfaces[J]. Environmental Pollution, 2008,153:53-59.
[25] Nowack B, Stone A T. Adsorption of phosphonates onto the goethite-water interface [J]. Journal of Colloid and Interface Science, 1999,214(1):20-30.
[26] Persson P, NilssonN, Sjoberg S. Structure and bonding of orthophosphate ions at the iron oxide-aqueous interface [J]. J.Colloid. Interface Sci., 1996,177(1):263-275.
Glyphosate adsorption by ferric supported active carbon.
XIE Ming, XU Yan-hua*(College of Environment, Nanjing University of Technology, Nanjing 210009, China). China Environmental Science, 2011,31(2):239~244
Ferric supported active carbon was prepared by impregnation-calcination method and the characteristics of its surface were investigated by scanning electron magnification (SEM), and both adsorption isotherm and adsorption kinetics of Fe-AC were studied. The effects of different factors on the adsorption process were also studied. Freundlich equation fitted well to supported ferric active carbon adsorption isotherm, the maximum adsorption capacity was 5.8mmol/g; and the adsorption kinetics was fitted well by Lagergren equation, so adsorption rate constant can be calculated out 0.088min-1that can decrease with the temperature increase. According to Kannan & Sundaram internal diffusion model, the internal diffusion constant was higher than 10mg·min-1/2/g, which decreased with the temperature increase. Due to the ionization form of glyphosate and the change of Fe-AC surface characteristics, the adsorption capacity of glyphosate decreased when the pH of solution increased. Antagonistic effect caused the adsorption capacity decrease of Fe-AC due to the existence of NaCl, and when the concentration of NaCl reached 4g/L, salting-out effect became dominant, which increased the adsorption capacity slightly. Because of the steric hindrance of glyphosate and the complex formation between phosphate and supported ferric active carbon surface, the Fe-AC adsorption capacity decreased continuously while the concentration of phosphate increase.
adsorption;glyphosate; ferric supported active carbon
X703.1
A
1000-6923(2011)02-0239-06
2010-06-09
国家“863”项目(2007AA06A402);国家科技支撑重大项目课题(2006BAC0A15);国家水体污染控制与治理科技重大专项(2008ZX07101-003)
* 责任作者, 教授, xiemingconan@gmail.com
谢 明(1985-),男,江苏南京人,南京工业大学环境学院硕士研究生,主要从事废水处理和资源化回收研究.发表论文3篇.
