CdTe/CdS量子点在Nafion/羟基磷灰石膜上的电化学发光及其应用于肌红蛋白的高灵敏检测*
2011-10-19王国涛贾丽萍陶绪泉贾文丽王怀生
王国涛,贾丽萍,赵 倩,陶绪泉,贾文丽,崔 慧,王怀生*
(1.聊城大学化学化工学院,山东聊城 252059;2.聊城大学材料科学与工程学院,山东 聊城 252059)
由于其自身优良的光化学性质和光谱性质,量子点逐渐引起人们的广泛关注[1-2]。量子点的ECL包括阴极发光和阳极发光,有关量子点的阴极ECL研 究 及 应 用 比 较 广 泛,比 如 H2O2[3],O2[4]和S2O82-[5]等通常被用作共反应物来增强量子点的阴极ECL。为了进一步扩大量子点在生命分析中的应用,量子点阳极ECL的应用也引起了人们的注意,2-(二丁基氨基)乙醇(DBAE)和SO32-等通常被用作增强量子点阳极ECL的共反应物[6-9]。三丙胺在Ru(bpy)32+体系中应用的比较广泛[10-12],但据我们所掌握的资料,三丙胺在量子点发光方面的报道并不多见[13-15]。
早期量子点的ECL大多是研究量子点分散在液相中扩散到电极表面的电化学发光行为,传统电极如铂盘电极、ITO电极、玻碳电极等被用作工作电极[16-18]。因为液相中的电化学发光强度较弱,后来人们将量子点固定在电极表面研究其电化学发光,并且在这方面取得了一定的研究成果,比如鞠熀先课题组将CdSe量子点沉积到浸蜡石墨电极制备成量子点修饰电极并研究了在液相中的传感应用[19];朱俊杰课题组将CdS和石墨混合制备了碳糊电极,并且对其在水相和非水相中的ECL进行了研究[20]。
肌红蛋白[21]由153个氨基酸残基组成的多肽链和一个血红素(铁卟啉)所构成,它主要是通过可逆性地与氧结合和释放,为肌肉组织储存和转运氧。由于Mb是一个较小分子的球蛋白,心肌或骨骼肌损伤时释放出的Mb可以从肌肉组织漏到循环血中去,最后经肾脏代谢和清除从尿中排出,形成高肌红蛋白血症和肌红蛋白尿。在诊断急性冠状动脉综合症、心血管疾患以及急性心肌缺血致死等疾病时,较其他生化标志物呈阳性结果早。因此,建立快速、灵敏的的检测肌红蛋白含量的分析方法具有重要的临床意义。
羟基磷灰石是人类骨骼的主要成分,在化学领域,羟基磷灰石主要用于填充色谱柱、分离DNA及蛋白质等生物分子,但是,它在电化学方面的应用还很少[22-23]。研究表明,在 HAp颗粒与蛋白质之间存在多种相互作用,如蛋白质表面的—COO-与HAp表面的Ca2+之间、蛋白质的—NH2与HAp表面之间存在较强的静电作用、官能团的疏水作用以及蛋白质分子间各种功能团的协同作用。因此蛋白质可以稳定地固定在 HAp颗粒表面,并且保持其生物活性。
我们利用HAp膜的多孔性和Nafion的良好成膜性[24],将 CdTe/CdS QDs修饰在HAp和Nafion的复合膜内,制备了Nafion-QDs-HAp修饰玻碳电极。以TPrA为共反应物,研究了该量子点在该复合膜修饰电极上的电化学发光行为。结果表明,修饰在复合膜内的量子点的电化学发光强度和稳定性都要远远好于分散在溶液中的量子点在裸电极上的电化学发光行为。基于Mb对量子点阳极ECL的猝灭作用,建立了测定Mb的新方法。
1 实验部分
1.1 仪器
AG135电子天平(上海梅特勒公司);78HW-1型恒温磁力搅拌器(江苏省金坛市荣华仪器制造有限公司);PHS-3C型精密酸度计(上海雷磁仪器厂);SK3300LH超声波清洗器(上海科导超声仪器有限);CHI 760C电化学工作站(中国上海)。电解池采用三电极系统,其中工作电极为玻碳电极(直径为3 mm)或者Nafion-QDs-HAp/GCE修饰电极,对电极为铂丝电极,参比电极为Ag/AgCl电极。
1.2 试剂
肌红蛋白(Sigma,美国),NaBH4、Te 粉(国药集团),3-巯基丙酸(Alfa公司),3-丙基氨(Alfa 公司),硫化钠(Na2S·9H2O)、氯化镉(CdCl2·2.5H2O),其它试剂均为分析纯。实验用水为二次去离子水,高纯氮除氧。0.1 mol/L PBS缓冲溶液由 0.1 mol/L的KH2PO4和NaOH制成。
1.3 实验方法
1.3.1 水溶性CdTe/CdS量子点的合成
按照文献[25]报道的合成方法,将加热回流的时间优化为5 h,制备了水溶性的核壳型的CdTe/CdS量子点。然后用丙酮将得到的核壳型量子点以6 000 rpm进行离心分离10 min以除去多余的Cd2+和3-巯基丙酸。将离心得到的沉淀用丙酮洗涤3次,再将沉淀重新分散在水中,根据量子点的紫外吸收光谱,参考单核量子点的浓度计算方法[26],得到浓度约为1.2×10-6mol/L的量子点。取其中少量通过透射电子显微镜分析(TEM)进行表征,结果显示量子点分散性良好,尺寸分布均匀,平均粒径约5.6 nm。量子点不用时放在4℃的冰箱中备用。
1.3.2 HAp 纳米溶胶的制备
参照文献[27]我们制备了羟基磷灰石纳米溶胶(HAp):在不断搅拌的情况下,以5 mL/min的速度向饱和的Ca(OH)2溶液中滴加0.01 mol/L H3PO4溶液,直到pH达到8.2。然后,将所得悬浊液静置12 h,过滤,再分别用二次蒸馏水和乙醇洗涤两次。所得到的沉淀用二次水超声分散,即形成大约8 mg/mL的HAp纳米溶胶。然后放入4℃冰箱中保存备用。
1.3.3 量子点修饰电极的制备
将直径3 mm的GCE先用0.05 μm的Al2O3悬浊液研磨、抛光,再分别用二次蒸馏水和乙醇超声5 min,用氮气吹干。将制备得到的量子点溶液同羟基磷灰石混匀(1:1),超声均匀;取8 μL上述混合液滴涂到处理好的玻碳电极表面,静置于4℃低温下干燥8 h;再取3 μL 5%Nafion滴到该修饰电极上,低温晾干,从而制得 Nafion-QDs-HAp GCE修饰电极。
2 结果与讨论
2.1 加热回流时间对制备的量子点荧光性质的影响
图1为不同回流时间(1 h~6 h)合成的量子点的荧光图谱,由图可见,随着回流时间的延长,得到的量子点的荧光发射峰位逐渐红移(从曲线1到6),加热回流5 h得到的量子点荧光强度最高。故我们选择回流5 h得到的CdTe/CdS QDs作为我们实验所用量子点。

图1 不同回流时间制备的CdTe/CdS量子点的荧光光谱
2.2 CdTe/CdS量子点结构表征
图2为制得的CdTe/CdS量子点的透射电镜图像。从图中可以看出,该CdTe/CdS量子点为球形颗粒,大小分布基本均匀,对其粒径分布进行高斯拟合可以得出CdTe/CdS量子点的平均粒径约为5.6 nm。证明了合成的 CdTe/CdS量子点为纳米级晶体。

图2 CdTe/CdS QDs的TEM图
2.3 量子点在不同条件下ECL行为比较
我们将4 μL CdTe/CdS量子点加入到4.0 mL PBS溶液中,以0.020 mol/L TPrA作为共反应物,用裸玻碳电极做工作电极进行循环伏安扫描,得到量子点在电极上的ECL曲线如图3(a)所示。图3(b)是在同样条件下,将4 μL量子点修饰到玻碳电极上后再用Nafion膜覆盖得到的ECL曲线。图3(c)是将4 μL量子点和4 μL羟基磷灰石的混合液修饰到玻碳电极上再用Nafion膜覆盖后测定的ECL曲线。可以清楚的看到,量子点用Nafion固定在电极表面后的发光强度要比量子点扩散到裸电极表面的发光强度要高约十倍,而通过Nafion/HAp膜固定的量子点的电化学发光强度要比单独使用Nafion固定的量子点的电化学发光强度高出近一倍。
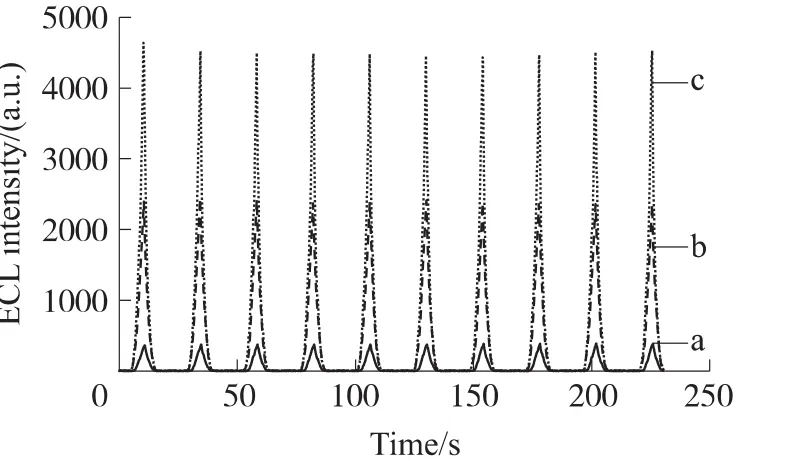
图3 0.05 μmol/L QDs在裸电极上的 ECL强度(a),Nafion-QDs GCE(b)和 Nafion-QDs-HAp GCE(c)在0.1 mol/L pH 6.5的PBS中的ECL强度,三丙胺浓度为0.020 mol/L
由不同电极的电化学发光-电位曲线(图4)可以看出,将量子点固定到电极表面后,其发光起始电位明显负移,而用Nafion和HAp固定的量子点的起始发光电位最负(图4(c)),大约在在0.56 V左右,这更加有利于生命物质的检测。
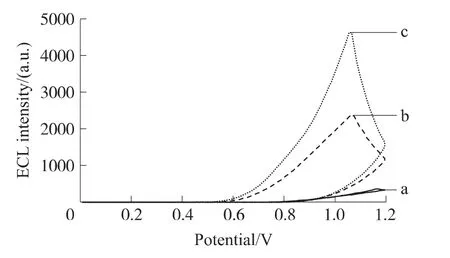
图 4 0.05 μmol/L QDs在裸电极(a),Nafion-QDs GCE(b)和 Nafion-QDs-HAp GCE(c)于 0.1 mol/L pH 6.5的PBS中的ECL-电位曲线
2.4 扫速和溶液pH值对量子点ECL行为的影响
缓冲溶液的pH值对量子点的ECL行为也有很大影响。我们分别研究了电极表面的CdTe/CdS QDs在0.1 mol/L不同pH的 PBS缓冲溶液中的ECL行为,结果如图5(a)所示,可见,当pH达到6.5时,体系的ECL强度(I0)最大。所以实验中我们选择0.1 mol/L pH 6.5的PBS缓冲溶液。

图5 溶液pH值(a)和扫描速度(b)对Nafion/HAp膜中量子点电化学发光强度的影响
在0.1 mol/L PBS 溶液中,以 0.020 mol/L TPrA为共反应物,以Nafion-QDs-HAp GCE作为工作电极研究了扫描速度对CdTe/CdS QDs的ECL行为的影响,结果如图5(b)所示。从图中可以看出,当扫描速度从20 mV/s逐渐增大到260 mV/s时,发光强度先随扫速的增加而增加,然后逐渐降低,在200 mV/s时ECL强度最大(图5(b))。所以实验中我们选择扫速为200 mV/s。
2.5 Nafion-QDs-HAp GCE的ECL发光的稳定性和重现性
对于表面电化学发光来说,量子点固定的是否牢固是影响测定的重要因素。我们利用电极表面的量子点电化学发光强度的稳定性来衡量量子点固定的牢固程度。图6是以Nafion-QDs-HAp GCE为工作电极,在0.020 mol/L TPrA的存在下,CdTe/CdS量子点在0.1 mol/L PBS中的重复发光实验结果。可以看出,固定在Nafion/HAp膜内的量子点表现出良好的ECL的稳定性和重现性,可以满足电化学发光分析的要求。

图6 Nafion/HAp膜内CdTe/CdS量子点连续电化学发光的曲线.实验条件同图3
2.6 分析应用
向体系中加入肌红蛋白,膜内量子点的发光会被猝灭。在最佳实验条件下,将肌红蛋白连续地加入到体系中,量子点的发光强度会持续降低。结果表明,肌红蛋白浓度在0.59 nmol/L~10.59 nmol/L范围内,分析信号lg(I-I0)/I与肌红蛋白的浓度的对数lg[CMb]有良好的线性关系(如图7所示),线性回归方程符合静态猝灭的Lineweaver-Burk双倒数函数关系,lg(I0-I)/I=lgKA+nlg[Q],检出限为0.12 nmol/L,线性相关系数为0.9972,线性方程为 lg(I0-I)/I=0.019+2.525 lg[CMb]。

图7 Mb对Nafion/HAp膜内CdTe/CdS量子点电化学发光的猝灭曲线.插图为相应的线性关系曲线.其他条件同图3
2.7 常见物质的干扰
实验中我们考察了一些可能共存的物质的干扰情况。肌红蛋白浓度为2.4×10-9mol/L时,10倍的血红蛋白;20倍的多巴胺、L-甘氨酸、L-组甘酸、DL-丝氨酸、L-精氨酸、L-胱氨酸;50倍的维生素B1、维生素B6、维生素K3对肌红蛋白的电化学发光检测基本不产生影响,除Cu2+、Hg2+、Ni2+外,大部分金属离子不干扰测定。
3 机理探讨
3.1 量子点电化学发光机理
根据上述实验结果,我们提出了 CdTe/CdS QDs/TPrA体系的ECL可能的机理。本实验中在0~1.2 V之间进行扫描只有氧化型离子生成,所以不会是湮灭机理。因为湮灭机理是氧化型离子和还原型粒子相互碰撞发生湮灭,进而生成激发态的粒子[28]。所以我们提出了可能的氧化还原模式:当体系施加上0~1.2 V电压后,在循环伏安扫描过程中QDs被氧化失去一个电子生成带正电荷的量子点QDs+,同样,TPrA也会被氧化生成带正电荷的[TPrA·]+,然而[TPrA·]+不稳定,它会从 α-碳上失去一个质子生成具有强氧化能力的 TPrA·[29]。TPrA·将带正电荷的量子点 QDs+激发到激发态QDs*。激发态的QDs*在回到基态的过程中就会发出可见光。整个过程由以下方程表示:
QDs-e→QDs+
TPrA-e→[TPrA·]+→TPrA·+H+
QDs++TPrA·→QDs*+products*
QDs*→QDs+hν
3.2 肌红蛋白猝灭量子点的机理
从图 8(A)可以看出,当 2.4×10-9mol/L Mb 加入CdTe/CdS体系后,CdTe/CdS紫外吸收峰并没有发生偏移,可以得知它们之间属于静电结合,这与其它相关的报道结果一致[30-31]。CdTe/CdS 和 Mb 形成了具有一定结构的超分子化合物,而这种超分子化合物在循环伏安扫描过程中不能被氧化。随着肌红蛋白浓度的不断加大,与其结合的量子点越来越多,使量子点的非辐射中心增大,能被氧化的量子点越来越少,所以体系的电化学强度随着肌红蛋白浓度的增大而降低,从而电化学发光被猝灭。
从图8(B)中可以看出,同浓度的Mb要比Hb的猝灭作用要大,我们推测可能的原因:虽然血红蛋白与肌红蛋白结构相似,但血红蛋白是由四个亚基组成的寡聚蛋白,大致为四面体的四级结构,空间结构过大,使它不易与量子点结合;而肌红蛋白是单链蛋白,并且具有极性的氨基酸残基几乎全部分布在分子表面,这样它可以更容易与量子点结合,能够有效地猝灭量子点的电化学发光,所以在本实验中,通过CdTe/CdS量子点在Nafion/羟基磷灰石膜上的电化学发光来检测肌红蛋白的过程中,血红蛋白对其测定没有产生干扰。

图 8A 2.4×10-9mol/L CdTe/CdS QDs的紫外光谱(a),a+2.4×10-9mol/L Mb 的紫外光谱(b);图 8B 2.4×10-9mol/L CdTe/CdS QDs 的荧光光谱(a),a+2.4×10-9 mol/L Hb的荧光光谱(b),a+2.4×10-9mol/L Mb 的荧光光谱(c)
4 结论
我们将CdTe/CdS QDs修饰到Nafion和羟基磷灰石复合膜内,研究了量子点在膜内的电化学发光行为,同时还考察了缓冲溶液的pH值、扫速等因素对CdTe/CdS QDs的电化学发光的影响。在最佳实验条件下,CdTe/CdS QDs的阳极电化学发光强度高且稳定,基于Mb对该电化学发光的猝灭作用,建立了一种检测Mb的新方法。该方法灵敏度较高、选择性较好,而且操作简便。同时我们提出了CdTe/CdS QDs的电化学发光的可能机理以及Mb猝灭CdTe/CdS QDs的电化学发光的可能机理。
[1]Burda C,Chen X B,Narayanan R,et al.Chemistry and Properties of Nanocrystals of Different Shapes[J].Chem Rev,2005,105(4):1025-1102.
[2]魏荣山,邓宁,王民生,等.以Si3N4作增透膜的Si基Ge量子点探测器的研究[J].传感技术学报,2006,19(5):1771-1774.
[3]Han H Y,Sheng Z H,Liang J G.Electrogenerated Chemiluminescence from Thiol-Capped CdTe Quantum Dots and Its Sensing Applicationin Aqueous Solution[J].Anal Chim Acta,2007,596:73-78.
[4]Jiang Q H,Hakansson M,Suomi J,et al.Cathodic Electrochemiluminescence of Lucigenin at Disposable Oxide-Coated Aluminum E-lectrodes[J].J Electroanal Chem,2006,591(1):85-92.
[5]Jie G F,Liu B,Zhu J J,et al.CdS Nanocrystal-Based Electrochemiluminescence Biosensor for the Detection of Low-Density Lipoprotein by Increasing Sensitivity with Gold Nanoparticle Amplification[J].Anal Chem,2007,79(15):5574-5581.
[6]Liu X,Jiang H,Lei J P,et al.Anodic Electrochemiluminescence of CdTe Quantum Dots and Its Energy Transfer for Detection of Catechol Derivatives[J].Anal Chem,2007,79(21):8055-8060.
[7]Zhang L H,Shang L,Dong S J.Sensitive and Selective Determination of Cu2+by Electrochemiluminescence of CdTe Quantum Dots[J].Electrochem Commun,2008,10(10):1452-1454.
[8]Liu X,Guo L,Cheng L X,et al.Determination of Nitrite Based on Its Quenching Effect on Anodic Electrochemiluminescence of CdSe Quantum Dots[J].Talanta,2009,78(3):691-694.
[9]Liu X,Ju H X.Coreactant Enhanced Anodic Electrochemiluminescence of CdTe Quantum Dots at Low Potential for Sensitive Biosensing Amplified by Enzymatic Cycle[J].Anal Chem,2008,80(14):5377-5382.
[10]Miao W J,Choi J P,Bard A J.The Tris(2,2'-Bipyridine)Ruthenium(Ⅱ),(Ru(bpy)32+)/Tri-n-Propylamine(TPrA)System Revisited—A New Route Involving TPrA*+Cation Radicals[J].J Am Chem Soc,2002,124(48):14478-14485.
[11]Miao W J,Bard A J.Determination of Immobilized DNA and C-Reactive Protein on Au(Ⅲ)Electrodes Using Tris(2,2'-Bipyridyl)Ruthenium(Ⅱ)Labels[J].Anal Chem,2003,75(21):5825-5834.
[12]Choi H N,Cho S H,Lee W Y,et al.Electrogenerated Chemi-luminescence from Tris(2,2'-Bipyridyl)Ruthenium(Ⅱ)Immobilized in Titania—Perfluorosulfonated Ionomer Composite Films[J].Anal Chem,2003,75(16):4250-4256.
[13]Miao W J,Choi J P,Bard A J.The Tris(2,2'-Bipyridine)Ruthenium(Ⅱ),(Ru(bpy)32+)/Tri-n-Propylamine(TPrA)System Revisited—A New Route Involving TPrA+Cation Radicals[J].J Am Chem Soc,2002,124(48):14478-14485.
[14]Sardesai N,Pan S,Rusling J.Electrochemiluminescent Immunosensor for Detection of Protein Cancer Biomarkers Using Carbon Nanotube Forests and[Ru-(bpy)3]2+-Doped Silica Nanoparticles[J].Chem Commun,2009,7(23):1968-4970.
[15]Pang Y Q,Cui H,Zheng H S.Flow Injection Analysis of Tetracyclines Using Inhibited Ru(bpy)32+/Trinpropylamine Electrochem-iluminescence System[J].Luminescence,2005,20(1):8-15.
[16]Han H Y,You Z H,Liang J G,et al.Electrogenerated Chemiluminescence of CdSe Quantum Dots Dispersed in Aqueous Solution[J].Front Biosci,2007,12:2352-2357.
[17]Liu X,Ju H X.Coreactant Enhanced Anodic Electrochemiluminescence of CdTe Quantum Dots at Low Potential for Sensitive Biosensing Amplified by Enzymatic Cycle[J].Anal Chem,2008,80(14):5377-5382.
[18]Liu X,Guo L,Cheng L X,et al.Determination of Nitrite Based on Its Quenching Effect on Anodic Electrochemiluminescence of CdSe Quantum Dots[J].Talanta,2009,78(3):691-694.
[19]Zou G Z,Ju H X.Electrogenerated Chemiluminescence from a CdSe Nanocrystal Film and Its Sensing Application in Aqueous Solution[J].Anal Chem,2004,76(23):6871-6876.
[20]Ren T,Xu J Z,Tu Y F,et al.Electrogenerated Chemiluminescence of CdS Spherical Assemblies[J].Electrochem Commun,2005,7(1):5-9.
[21]Zhang L,Tian D B,Zhu J J.Direct Electrochemistry and Electrochemical Catalysis of Myoglobin-TiO2Coated Multiwalled Carbon Nanotubes Modified Electrode[J].Bioelectrochemistry,2008,74(1):157-163.
[22]潘壮英,马荣娜,王怀生,等.羟基磷灰石/离子液体混合膜修饰电极的制备及其应用于水中痕量镉离子的高选择性测定[J].化学学报,2009,67(23):2716-2721.
[23]秦玉华,张袁健,徐修冬.细胞色素c在羟基磷灰石修饰玻碳电极上的直接电化学细胞色素c在羟基磷灰石修饰玻碳电极上的直接电化学[J].化学学报,2004,62(9):860-863.
[24]许红岩,王丽莉,王怀生,等.没食子酸在Nafion/单壁碳纳米管/聚(3-甲基噻吩)复合膜修饰电极上的电化学行为及测定[J].传感技术学报,2008,21(7):1113-1118.
[25]Liu B,Ren T,Zhang J R,et al.Spectro Electrochemistry of Hollow Spherical CdSe Quantum DotAssembliesin Water[J].Electrochem Commun,2007,9(4):551-557.
[26]Jiang H,Ju H X.Enzyme-Quantum Dots Architecture for Highly Sensitive Electrochemiluminescence Biosensing of Oxidase Substrates[J].Chem Commun,2007,4:404-406.
[27]马荣娜,王斌,刘燕,等.葡萄糖氧化酶在羟基磷灰石/Nafion复合膜修饰电极上的直接电化学及其对葡萄糖的生物传感[J].中国科学 B 辑,2009,39(11):1544-1550.
[28]Mei Y L,Wang H S.Electochemiluminescence of CdTe/CdS Quantum Dots with Triproprylamine as Coreactant in Aqueous Solution at a Lower Potential and Its Application for Highly Sensitive and Selective Detection of Cu2+[J].Electroanalysis,2010,22(2):155-160.
[29]Elasco J G V.Electroluminescence[J].Electroanalysis,1991,26(3):1-271.
[30]Lin Z,Cui S,Zhang H,et al.Studies on Quantum Dots Synthesized in Aqueous Solution for Biological Labeling Via Electrostatic Interaction[J].Anal Biochem,2003,319(2):239-43.
[31]Hua D H,Wu H M,Liang J G,et al.Study on the Interaction Between CdSe Quantum Dots and Hemoglobin[J].Spectrochim Acta,A Mol Biomol Spectrosc,2008,69(3):830-834.
