含吡啶环的十聚钨酸季铵盐催化合成环己酮
2011-10-12高玉环吕振波张彦佳桂建舟
高玉环, 吕振波, 刘 丹, 张彦佳, 杨 爽, 桂建舟
(辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001)
含吡啶环的十聚钨酸季铵盐催化合成环己酮
高玉环, 吕振波*, 刘 丹, 张彦佳, 杨 爽, 桂建舟
(辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001)
以十聚钨酸季铵盐([BunPy]4W10O32)为催化剂、质量分数30%的H2O2为氧化剂,研究了环己醇催化氧化生成环己酮的反应,考察了反应时间、反应温度、H2O2和催化剂的物质的量等因素对此反应的影响。得出了此反应的最佳条件:反应温度为80℃,催化剂物质的量为0.06mmol,H2O2物质的量为125mmol,环己醇物质的量为50mmol,回流反应8h。在最佳反应条件下,环己醇的转化率为86.5%,环己酮的选择性可达到98.3%。反应后催化剂不溶于反应体系,简单过滤即可回收,重复使用3次后其活性基本不变。
十聚钨酸季铵盐; 催化氧化; 环己醇; 环己酮
环己酮作为一种重要的有机化工原料,广泛应用于纤维、合成橡胶、工业涂料、医药、农药和有机溶剂等工业[1]。同时,环己酮也是一种重要的有机化工原料,是制备己内酰胺、己二酸、尼龙66的主要中间体[2]。环己酮的传统工业生产方法有两种:(1)将苯加氢生成环己烷,再将环己烷催化氧化制得环己酮;(2)将苯酚加氢生成环己醇,环己醇经催化脱氢得到环己酮。此类反应多采用定量Cr(Ⅵ)、Mn(Ⅴ)类的无机氧化剂[3-6]。而这些氧化剂会产生对环境有害的有毒废物,在环保要求日益提高的今天,迫切需要研制出对环境友好的醇类催化氧化方法。
近几年来,寻找一种以H2O2为清洁氧化剂、高效且环境友好的催化氧化方法成为合成环己酮的研究热点。在催化剂的选择上,国内外学者大多以相转移催化剂为主。相转移的方法有许多优点,如收率高、反应条件温和、产物易处理等。唐文明等[7]在离子液体[Bmim]PF6中,以三氯化钌作催化剂,用叔丁基过氧化氢氧化环己醇,得到的主产物为环己酮,转化率在90%以上,但此反应过程中采用有毒的CH2Cl2作为溶剂,污染环境。因此非常有必要进一步研究开发无污染,对环境友好的环己酮生产技术。
本课题组合成了多种含杂环的十聚钨酸季铵盐[8]。在此基础上,本文以含吡啶环的十聚钨酸季铵盐为催化剂,H2O2为氧源,在无任何有机溶剂和卤素的条件下,研究了环己醇的催化氧化,取得了良好的催化效果。该反应体系具有催化剂反应活性高、反应条件温和、反应物用量少、操作简单、产物易分离等优点。由于未使用任何有毒的有机溶剂,无污染,真正实现了对环境的友好。其反应式如式(1)所示。
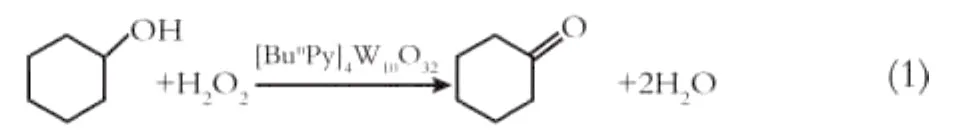
其中催化剂阳离子[BunPy]+的结构式为:
1 实验部分
1.1 仪器与试剂
1.1.1 仪器 美国Perkin-Elmer SPECTRUM GXIII型红外谱仪(KBr压片);聚四氟乙烯反应釜(大连伟达分析仪器配件厂);SP-2100气相色谱仪(北京北分瑞利分析仪器公司);循环水式真空泵(巩义市予华仪器有限责任公司);80-2离心分离器(上海手术器械厂)。
1.1.2 试剂 Na2WO4·2H2O(分析纯,沈阳国药化学试剂有限公司);环己醇(分析纯,沈阳国药化学试剂有限公司);质量分数为30%的H2O2(分析纯,沈阳国药化学试剂有限公司);离子液体。其它试剂均为分析纯,没有特别说明均未进一步提纯。
1.2 催化剂的制备与表征
(1)离子液体(IL)的合成
参照文献[9]成功合成了离子液体1-丁基吡啶硫酸氢盐([CH3(CH2)3Py][HSO4])。
(2)催化剂的制备与表征
将3.832g Na2WO4·2H2O和一定量的离子液体放入100mL圆底烧瓶中,并在磁力搅拌器上加热,缓慢升温至60℃,保持回流6h,反应后有亮黄色晶体十聚钨酸季铵盐[BunPy]4W10O32生成[10-11],水洗,抽滤,干燥,备用。同时采用IR技术对反应前后的催化剂进行了表征。
1.3 催化氧化反应
将0.06mmol的十聚钨酸季铵盐(约0.2g)和50mmol的环己醇(约5.2mL)放入25mL的圆底烧瓶中,并在装有冷凝回流装置的磁力加热搅拌器上缓慢升温至80℃,逐滴滴加125mmol的H2O2,滴加时间约为10min,完毕,继续加热,并保持冷凝回流8h,反应结束后,溶液分上下两层,冷却后,离心分离。
1.4 定量分析
用环己酮的标样做对比在SP-2100气相色谱仪上进行定性分析,并在其基础上进行定量分析,所使用的气相色谱柱类型为ATSE-54(30m×0.25 mm×0.5μm),分析条件:柱温采用程序升温方式由60℃升至200℃,升温速率5℃/min,检测器与进样器温度均为250℃。由该气相色谱仪仪器自带的色谱软件系统根据不同组分的峰面积直接给出定量数据,质量分数小于0.5%的产物未计算在内。
2 结果与讨论
2.1 反应时间对环己醇氧化反应的影响
在[BunPy]4W10O320.0 6mmol,H2O21 2 5 mmol,环己醇50mmol,温度80℃的条件下,考察了反应时间对环己醇氧化反应的影响,结果见图1。

Fig.1 Influence of different time on cyclohexanol oxidation图1 反应时间对环己醇氧化反应的影响
从图1可以看出,随着反应时间的增加,转化率逐渐升高。选择性较稳定,变化幅度不大,反应8h时,转化率为86.0%,选择性可达到96.7%,当反应时间超过10h时,延长反应时间,选择性趋于稳定,但转化率有所下降。综合考虑选择反应8h为最佳的反应时间。
2.2 反应温度对环己醇氧化反应的影响
在催化剂[BunPy]4W10O320.06mmol,H2O2125mmol,环己醇50mmol,冷凝回流8h的条件下,考察反应温度对环己醇氧化反应的影响,结果见图2。
从图2中可以看出,反应温度从70℃升到80℃,环己醇的转化率不断的上升,主要是由于温度的升高增加了各个反应物的活性,使其不断地向产物转化;但随着反应温度继续升高,生成的环己酮会进一步氧化,生成羧酸,导致环己酮选择性下降。同时过氧化氢的无效分解也使得转化率随之降低。故80℃是该反应的最佳反应温度。
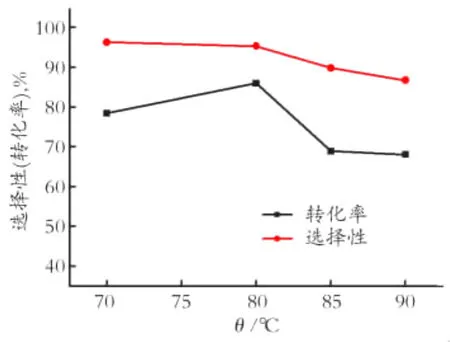
Fig.2 Influence of different tempretures on cyclohexanol oxidation图2 温度对环己醇氧化反应的影响
2.3 H2O2的物质的量对环己醇氧化的影响
从化学平衡的角度考虑,增大反应物的物质的量比有利于提高收率。由于环己醇的价格高,本实验固定环己醇50mmol,在催化剂[BunPy]4W10O320.06mmol,温度80℃,冷凝回流8h的条件下,考察H2O2的物质的量对环己醇氧化反应的影响,结果见图3。

Fig.3 Influence of the amount of H2O2on cyclohexanol oxidation图3 H2O2物质的量对环己醇氧化的影响
从图3可以看出,随着H2O2物质的量的不断增加环己醇的转化率先增大后趋于稳定,环己酮的选择性逐渐降低;当H2O2物质的量达到125mmol时,其转化率和选择性较高,综合考虑,H2O2的最佳物质的量为125mmol。
2.4 催化剂物质的量对环己醇氧化反应的影响
分别取H2O2125mmol,环己醇50mmol,温度80℃,冷凝回流8h的条件下,考察催化剂物质的量对环己醇的催化氧化反应的影响,其结果见图4。
从图4中可以看出,随着催化剂物质的量的增加,环己醇的转化率不断增加。当催化剂的物质的量为0.06mmol时,再增加催化剂的物质的量,环己醇的转化率反而下降。此时,环己醇的转化率为86.5%,环己酮的选择性为98.3%,因此催化剂的最佳物质的量为0.06mmol。

Fig.4 Influence of the amount of catalyst on the cyclohexanol oxidation图4 催化剂物质的量对环己醇氧化反应的影响
2.5 产物的分离和催化剂的重复使用
2.5.1 催化剂分离与重复使用 反应结束后,将溶液冷却。离心分离,溶液分两层,上层为有机相,下层为水相。取上层有机相,待测。
由于该催化剂不溶于水,经离心分离,即可从反应体系中沉淀出,用去离子水清洗3次,抽滤,干燥,再次应用于环己醇的催化氧化反应,催化剂可重复使用3次,其重复使用次数与转化率和选择性的关系如表1所示。

表1 催化剂回收重复实验Table 1 Recycle of catalysts%
2.5.2 反应前后催化剂的IR表征 催化剂反应前后的IR谱图如图5所示。
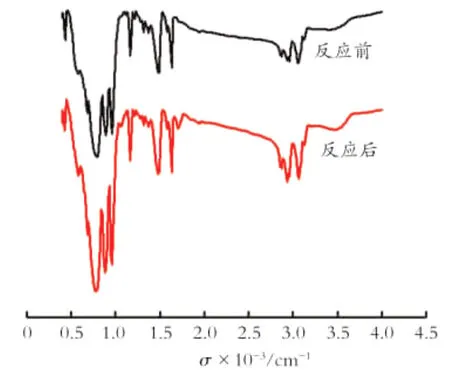
Fig.5 IR spectra of the[BunPy]4W10O32before and after catalytic reaction图5 [BunPy]4W10O32反应前后的IR谱图
由图5可见,催化剂反应前后在960,891,795和682cm-1处均出现特征峰,这四个特征峰是由阴离子[W10O32]4-中的W-Oa,W-Ob-W和WOc-W振动产生的,但反应后回收催化剂的峰稍发生了位移,此外,催化剂反应前后在3 057,2 962,2 871cm-1和1 630~1 464cm-1也均有特征峰出现,这些特征峰是由阳离子[BunPy]+产生。这些说明反应前后催化剂的结构基本上无明显改变。
[1]江雪源,宋华.氧化法合成环己酮技术研究进展[J].工业催化,2005,13(11):41-46.
[2]赵睿,吕高孟,季东,等.Au/ZSM-5催化选择氧化环己烷制环己酮和环己醇的研究[J].分子催化,2005,19(2):115-120.
[3]曾昭琼.有机化学实验[M].北京:高等教育出版社,1987:123-124.
[4]Muzart J.Chromium-catalyzed oxidations in organic synthesis[J].Chem.rev.,1992,92(3):113-140.
[5]Regen S L,Koteel C.Activation through impregnation-permanganate-coated solid supports[J].Chem.soc.,1977,99(5):3837-3838.
[6]Rebelo S L H,Simbes M M Q,Neves M G P M,et a1.Oxidation of bicyclic arenes with hydrogen peroxide catalysed by Mn(Ⅲ)porphyrins[J].J.mol.catal.A:Chem.,2005,232(1):135-142.
[7]唐文明,李朝军.三氯化钌催化下环己烷和环己醇在离子液体中的氧化反应研究[J].化学学报,2004,62(7):742-744.
[8]鲁凤,桂建舟,杨玉莲,等.十聚钨酸季铵盐的合成[J].合成化学,2009,17(6):714-715.
[9]Gui J,Cong X,Liu D,et al.Novel brφnsted acidic ionic liquid as efficient and reusable catalyst system for esterification[J].Catal.commun.,2004,5:473-477.
[10]王恩波,胡长文.多酸化学导论[M].北京:化学工业出版社,1998:170-214.
[11]刘光启,马连湘,刘杰.化学化工物性数据手册[M].北京:化学工业出版社,2002:3-5.
(Ed.:YYL,Z)
The Synthesis of Cyclohexanone Catalyzed by Quaternary Ammonium Decatungstate Containing Pyridine
GAO Yu-huan,LÜZhen-bo*,LIU Dan,ZHANG Yan-jia,YANG Shuang,GUI Jian-zhou
(College of Chemistry and Materials Science,Liaoning Shihua University,Fushun Liaoning113001,P.R.China)
Catalytic oxidation of cyclohexanol to cyclohexanone catalyzed by quaternary ammonium decatungstate,with 30%H2O2as the oxidant,had been investigated.The effect of reaction time,reaction temperature,the oxidant amount and catalyst amount on catalytic performance were studied.The results show that the optimum reaction conditions are as follows:50mmol cyclohexanol,0.06mmol catalyst,125mmol H2O2,80℃reacting for 8h;At the optimum reaction conditions,the conversion of cyclohexanol is 86.5%and the selectivity of cyclohexanone could reach 98.3%.After reaction,the catalyst is immiscible in the reaction system and could be recycled after simple filtering,and no obvious changes on the catalytic activity could be found after recycling three times.
Quaternary ammonium decatungstate;Catalytic oxidation;Cyclohexanol;Cyclohexanone
O621.3
A
10.3696/j.issn.1006-396X.2011.01.008
2010-10-27
高玉环(1983-),女,山东菏泽市,在读硕士。
国家自然科学基金项目(20706027);教育部重点项目(209031);辽宁省教育厅优秀人才计划(LR201024);辽宁省自然科学基金(20102131)。
*通讯联系人。
1006-396X(2011)01-0034-03
Received27October2010;revised4December2010;accepted29December2010
*Corresponding author.Tel.:+86-13841300912;e-mail:lzhb6684708@163.com
