碳包裹软磁金属纳米粒子的绿色合成及热稳定性研究
2011-09-29姬广斌常晓峰
王 鑫 姬广斌 张 斌 常晓峰
(南京航空航天大学材料科学与技术学院,南京 210016)
碳包裹软磁金属纳米粒子的绿色合成及热稳定性研究
王 鑫 姬广斌*张 斌 常晓峰
(南京航空航天大学材料科学与技术学院,南京 210016)
本文报道了一种制备碳包裹软磁金属纳米粒子的绿色合成方法:将金属醋酸盐溶液与可溶性淀粉均匀混合,蒸发、烘干后在 N2保护下热处理,得到金属纳米复合粒子(C@Ni,C@Co,C@Fe,C@CoNi,C@CoFe,C@FeNi)。TEM 结果表明金属粒子均匀分散在碳介质中,粒径为3~5 nm。样品在室温下具有良好的抗氧化性、热稳定性和软磁性能。
可溶性淀粉;磁性金属;热稳定性;软磁性能
0 引 言
铁、钴、镍的金属/合金纳米粒子具有比块体金属优异的磁学性能,在催化、磁性器件及吸波等领域有着广泛的应用[1-2]。然而金属纳米粒子高的比表面积和比表面能使其具有极高的活性,容易发生氧化和团聚,限制其进一步使用。因此,防止磁性金属纳米粒子的团聚和氧化成为一个热门的研究课题。通过在金属纳米粒子表面包裹绝缘性好的材料(如:SiO2、Al2O3、C) 制成核/壳复合结构材料是一种研究较多且被认为行之有效的方法之一[3-4]。景茂祥等[5]利用非均相沉淀包裹工艺,首先制备了前驱体碱式碳酸镍(NCH)包裹α-Al2O3,然后将前驱体在500℃下氢气还原2 h,成功制备了表面较光滑、致密的金属氧化铝包裹镍球形微粉。Guerrero-Martínez等[6]采用微乳液法,成功制得了SiO2与金属纳米粒子的核-壳结构。碳在常温下非常稳定,能够耐强酸、强碱,和有机物及氧化物相比,更适合作为保护金属纳米粒子的外壳。Lu等[7]以P123和钴纳米粒子为原料制成复合物,氮气保护下1000℃热处理,得到Co/C核壳结构纳米粒子,在强酸和强碱条件下具有极高的稳定性。Hamaoui等[8]加热分解钴离子与树枝状低聚苯的配合物,得到具有碳外壳的钴纳米棒和钴纳米球。Tang等[9]通过溶胶凝胶结合高温氢气还原的方法得到了Fe/SiO2核壳纳米结构材料。XPS测试只发现 Si2p(130.4 eV)和 O1s(532.8 eV)的特征峰,表明制备的样品并不是SiO2和Fe的简单物理混合物而是形成了复合材料,对样品磨损3 min后未发现Fe的存在;磨损至7 min才发现Fe的特征峰。表明合成的是以Fe为核SiO2为壳的核-壳复合材料。Won等[10]采用CVD及氢气热还原的方法合成了7 nm左右的FeCo/C核壳纳米结构,饱和磁化强度 Ms=200 emu·g-1,矫顽力较小,软磁性能良好;但TEM结果表明粒径不是很均匀。Wang等[11]在有机溶剂中,先利用羰基钴裂解合成Co纳米粒子,然后在利用羰基铁裂解得到10 nm左右的Fe/Co核壳结构材料。Jing等[12]采用反微乳液法制备出CdTe/SiO2核壳结构纳米粒子,结果显示,粒子基本成单分散状态,粒径80 nm左右,但有些粒子为纯SiO2粒子,没有形成包覆层。孙彦红等[13]利用溶胶法制备了以Au为核。以Ag为壳的双金属核壳结构纳米颗粒,粒径为20 nm左右。刘桂霞等[14]以稀土元素的硝酸盐和葡糖糖为原料,采用一步水热法和后续高温处理的方法,得到了多层核壳结构Cd2O3∶Eu3+空心微球,测试结果表明,微球直径为3 μm左右,壁厚为100 nm。
近年来,化学化工业的飞速发展,造成了严重的环境污染,威胁着人类的生存和发展。因此,发展绿色化学成为当今化学化工业发展的方向。生物大分子除了具有高聚物分子的优点外,还具有可再生,无毒性,溶于水等优点,吻合绿色化学的主题。人们已经用鸡蛋壳膜[15]、树木纤维[16]、昆虫翅膀[17]等合成纳米材料。多糖(如糊精,纤维素,淀粉等)由于其较大的分子量,特殊的结构及环境友好的性质,在材料合成领域受到越来越多的关注。我们课题组CHEN等[18]以可溶性淀粉和醋酸盐为原料,制备了20 nm左右的Co/C、Ni/C纳米粒子,其分散不均匀,有部分团聚,也没有对样品的热稳定性和磁学性能进行描述。Raveendran等[19]以β-D-葡萄糖为还原剂,可溶性淀粉为模板剂,在水溶液中合成了银纳米粒子。Engelbrekt等[20]以葡糖糖为还原剂,以可溶性淀粉为稳定剂合成了粒径为1.7 nm的淀粉保护的Pt纳米粒子并研究了其催化性能。Filippo等[21]以麦芽糖和蔗糖为还原剂合成了6.0 nm的Ag纳米粒子。
本文利用Fe、Co、Ni的二价盐和可溶性淀粉为原料,采用溶胶-凝胶及后续的高温热处理方法,原位合成C包裹的金属Fe、Co、Ni及其合金的核壳纳米结构,借助X射线衍射(XRD),透射电子显微镜(TEM),选区电子衍射(SAED),氮气等温吸-脱附曲线,热重-差热(TG-DTA)及振动样品磁强计(VSM)等一系列测试手段对所制备出的核壳纳米结构进行晶体结构、孔结构、抗氧化能力及磁性质进行研究。
1 实验部分
1.1 所用药品
可溶性淀粉 (A.R.、南京宁氏化学试剂有限公司);Co(Ac)2·4H2O(A.R.、国药集团化学试剂有限公司);Ni(Ac)2·4H2O(A.R.、成都市科龙化工试剂厂);维生素 C(A.R.、上海试四赫维化工有限公司);FeSO4·7H2O(A.R.、国药集团化学试剂有限公司)。
1.2 实验方法
称取10 g可溶性淀粉,溶于150 mL蒸馏水,80℃搅拌至淀粉全部溶解,冷却至室温,得溶液(1);取0.01 mol·L-1的金属盐(单一金属盐或两两按物质的量之比为 1∶1的比例混合),1 g VitC,溶于 50 mL蒸馏水中,搅拌均匀,得溶液(2);将溶液2倒入溶液1中,搅拌均匀得溶液(3);将溶液(3)置于恒温式磁力加热搅拌器中,加热蒸干得到粘稠的胶状物,并将此胶状物80℃烘干后用行星式球磨机研磨2 h,然后在密封的高温管式炉中,氮气保护条件下600℃热处理3 h。在有铁盐的反应中加入1 g VitC,防止二价铁离子被空气中的氧气氧化成三价铁,影响高温还原。
1.3 表征及性能测试
采用Bruker D8 ADVANCE X射线衍射仪(Cu靶Kα射线,λ=0.154178 nm)对粉体样品进行广角扫描,扫描功率40 kV×40 mA,扫描范围2θ=30°~80°;利用JEOL JEM 2100型透射电子显微镜对所制备的样品进行形貌、SAED及EDS分析,制样时将分散在乙醇中的样品滴到铜网中,从而得到铜网支持的待测固体样品;采用Micromeritics ASAP 2010仪器测试样品氮气等温吸脱附曲线;采用SDT 2960热分析仪分析样品的抗氧化性能及其耐热温度;采用Lake shore 7410振动样品磁强计对所制备样品的磁学性能进行分析。
2 结果与讨论
2.1 XRD分析
图1(a)为以Ni盐和淀粉为原料得到样品的XRD图,在 2θ角分别为 44.3°、51.6°和 76.1°的位置,出现了3个尖锐的峰,与PDF卡片上(PDF No.65-0380)Ni的(111)-44.347°、(200)-51.673°、(220)-76.095°晶面衍射峰对应,说明得到的样品中存在Ni单质相。图1(b)为以Fe盐和淀粉为原料得到样品的XRD图,在2θ角分别为44.9°的位置,出现了1个峰,与PDF卡片上(PDF No.65-4899)Fe的(110)-44.662°晶面衍射峰对应,说明得到的样品中存在Fe单质相;峰强较低,可能是由于结晶度不够,或者Fe元素的质量百分比较小。另外在图1(b)上,2θ角为34.5°处还能看到1个较弱的峰,与PDF卡片上(PDF No.28-0491)Fe3O4(-102)-34.466°晶面衍射峰相一致,说明样品中还存在小部分的铁的氧化物。这说明有小部分的金属盐没有还原成单质,以氧化物的形式存在。这可能是由于在合成过程中,部分的亚铁离子被空气氧化为铁离子,在高温还原时没有完全还原,以氧化物的状态保存下来。图1(c)为以Co盐和淀粉为原料得到样品的XRD图,在2θ角分别为44.24°、51.53°和75.88°的位置,出现了3个尖锐的峰,与PDF卡片上 (PDF No.15-0806)Co的 (111)-44.216°、(200)-51.522°、(220)-75.853°晶面衍射峰对应,说明得到的样品中存在Co的单质相。
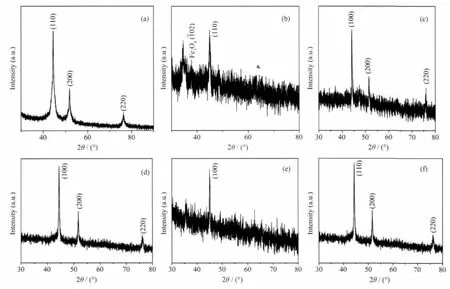
图1 不同原料所得碳包覆金属纳米粒子样品的XRD图,(a)Ni盐;(b)Fe盐;(c)Co盐;(d)Co盐-Ni盐;(e)Co盐-Fe盐;(f)Fe盐-Ni盐Fig.1 XRD patterns of the metal nanoparticles coated by carbon prepared by adopting different starting materials of nickel salt(a);ferric salt(b);cobalt salt(c);cobalt-nickel salts(d);cobalt-ferric salts(e);ferric-nickel salts(f)
实验表明,Co与Ni不能形成合金新相,至今为止不存在具有固定相的CoNi合金。图1(d)为以Co盐、Ni盐和淀粉为原料得到样品的XRD图,在2θ角分别为 44.36°、51.74°和 76.05°的位置, 出现了 3个尖锐的峰,与PDF卡片上(PDF No.65-0380)Ni的(111)-44.374°、(200)-51.673°、(220)-75.095°晶面衍射峰对应,但略有差别,这是因为Co原子替换了Ni金属晶胞中的Ni原子,因为与Ni原子大小不同,使晶胞参数发生微小变化,影响了衍射峰的位置。由此说明得到的样品为镍基NiCo固溶体合金。图1(e)为以Co盐、Fe盐和淀粉为原料得到样品的XRD图,在2θ角为44.97出现的峰与PDF卡片上(PDF No.65-4131)FeCo的 (110)-44.967°晶面衍射峰对应,说明得到的样品中存在FeCo的合金相。图1(f)为Fe盐、Ni盐原料得到的样品的XRD图。实践表明,FeNi与NiCo固溶体合金一样,Fe与Ni也不能形成合金新相,目前不存在具有固定相的FeNi合金。图2.3 中,在 2θ角分别为 44.37°、51.70°和 76.10°的位置,出现了3个尖锐的峰,与PDF卡片上(PDF No.65-0380)Ni的(111)-44.374°、(200)-51.673°、(220)-75.095°晶面衍射峰对应,但略有细小差别,这是因为Fe原子进入Ni金属晶胞,对Ni金属晶胞参数产生影响,导致衍射峰位置的变化。以上分析可以说明得到的样品为镍基NiFe固溶体合金。
XRD分析结果表明,本实验中,我们利用可溶性淀粉和金属盐,经过简单的步骤,成功的使金属离子被还原变成零价态的金属单质或合金:Ni、Fe、Co、NiCo、FeCo、NiFe。 在合成过程中,并没有添加其他还原剂,只有可能是可溶性淀粉在碳化时产生的还原性气氛使金属离子还原,因此说可溶性淀粉起到了还原的作用[16]。在热处理过程中,淀粉碳化为碳,而金属离子被还原成零价态的金属或合金。
金属Fe、Co、Ni及其合金的XRD衍射峰位置十分接近,单独利用XRD测试结果分析,不能够将它们区分。为了使XRD测试结果更具有说服力,对合成的 Fe、Co、NiCo、FeCo、NiFe 样品做了 EDS 能谱分析,如图2。从能谱数据中,与XRD分析结果一致,证明XRD结果是正确的。

图2 合成样品的EDS分析图Fig.2 EDS images of as-prepared samplee
2.2 TEM测试分析
图3(a)为合成的Ni样品的TEM图和SAED图,测试时,金属颗粒和碳对电子效应不同,因而金属颗粒和碳呈现不同影像,图中黑点为Ni金属粒子,白色条纹状态为碳,从图3(a)中可以看出碳组成骨架,而Ni金属粒子均匀的分散在其中,周围被碳紧紧包围,形成核壳结构的C@Ni,金属颗粒大约2~3 nm,分散均匀;选区电子衍射图显示金属粒子为多晶结构。图3(b)~(f)分析方法类似。从图3(b)中可得:成功制备出了C@Fe的核/壳结构纳米颗粒,粒径均匀,为5 nm左右,金属颗粒为多晶结构。另外TEM图上有一条黑白颜色不同的区域,这可能是金属粒子和碳原子比例不同造成的:较黑的区域金属粒子较多,较白的区域金属粒子含量较少。从图3(c)中可得:成功制备出了C@Co的核/壳结构纳米颗粒,粒径均匀,为2~3 nm,金属颗粒为多晶结构。从图3(d)中可得:成功制备出了C@NiCo的核/壳结构纳米颗粒,粒径均匀,为5 nm左右,金属颗粒为多晶结构。从图3(e)中得到:成功制备出了C@FeCo的核/壳结构纳米颗粒,粒径不大均匀,在2~8 nm之间,金属颗粒为多晶结构。从图3(f)中可知:成功制备出了C@NiFe的核/壳结构纳米颗粒,粒径均匀,为3 nm左右,金属颗粒为多晶结构。在成像区内,有部分团聚,形成较大颗粒。
2.3 BET氮气吸脱附曲线
对合成的样品进行氮气等温吸脱附分析,以C@Ni为例,得到其比其表面积为475 m2·g-1;图4(a)为C@Ni样品的氮气等温吸脱附曲线,表明样品中有无序的孔结构,图4(b)为其吸附支对应的BJH孔径分布,表明其为微孔结构。这是由于在C@Ni粒子形成过程中,高温碳化还原时,释放大量的气体如(CH4、CO、H2)使样品中形成大量的孔道结构,与文献报道[7]类似。

图3 溶胶凝胶法制备样品的TEM照片(插图为选区电子衍射)Fig.3 Representative TEM/SAED images of as-prepared sample

图4 (a)C@Ni样品的氮气等温吸脱附曲线;(b)与吸附支对应的BJH孔径分布曲线Fig.4 N2adsorption-desorption isothermal curves and BJH pore-distribution(calculated from the adsorption branch of the isotherm curves)of as-prepared C@Ni sample
2.4 抗氧化能力分析
以C@Ni为例,将最终得到的样品空气中放置2个月,其磁性信号无减弱,对其进行XRD测试分析。发现只有Ni的衍射峰,说明样品基本没有被氧化,表明其在常温条件下具有很好的抗氧化能力,如图5所示。
为测试其耐高温性能,将样品在空气氛条件下作热重-差热分析,温度范围:0~600℃,升温速率10℃·min-1。图6为合成的C@Ni样品的TG-DTA曲线,从图6中看到,在109℃有1个吸热峰,对应样品有质量的降低,这是样品失去吸附水分的结果;从300℃开始,样品放热增加,并伴随缓慢失重,在400℃以后,失重速度加剧,说明样品发生化学反应,样品不再稳定。由此说明制备的样品耐高温性能较好,能够在300℃条件下保持稳定。
合成的 C@Fe、C@Co、C@NiCo、C@FeCo、C@NiFe样品的TG曲线见图7。参照上述分析方法,可知:合成的各样品的热稳定性良好,其中合成的C@Fe、C@Co和C@NiFe样品在约340℃时质量开始缓慢下降,说明这些样品能耐340℃;合成的C@NiCo和C@FeCo样品在约260℃温度下质量开始下降,说明合成的C@NiCo和C@FeCo样品能耐260℃。

图5 所制备的C@Ni样品放置2个月后的XRD图Fig.5 XRD patterns of as-prepared C@Ni sample placed for 2 months

图6 所制备C@Ni样品的TG-DTA曲线Fig.6 TG-DTA curves of as-prepared C@Ni sample
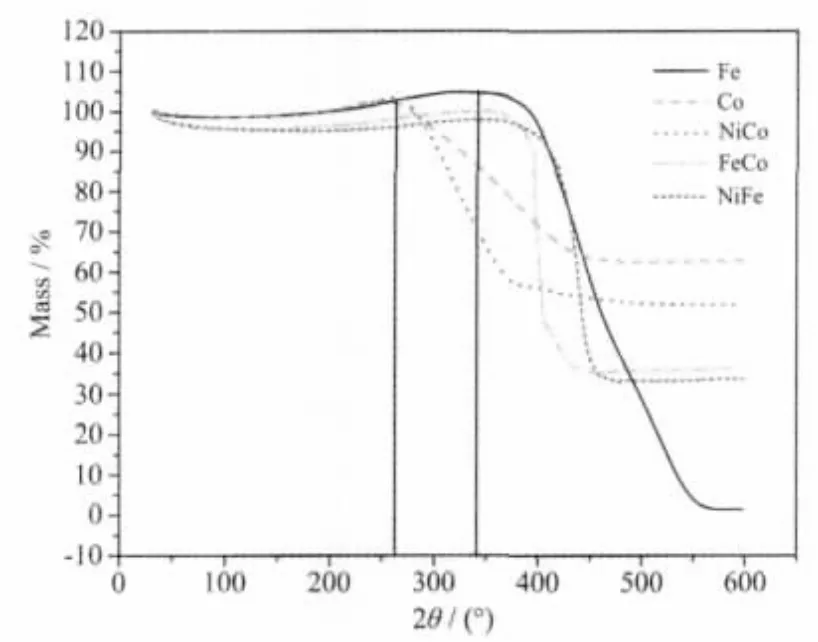
图7 所制备的 C@Fe、C@Co、C@NiCo、C@FeCo、C@NiFe样品的TG曲线Fig.7 TG curves of as-prepared C@Fe,C@Co,C@NiCo,C@FeCo,C@NiFe samples
2.5 VSM分析
由于合成的样品含有相当量的碳,而且很难确定碳和金属元素的质量百分比,讨论饱和磁化强度的意义不大,在这里,从Hs和Hc的大小上来讨论样品磁化和退磁的难易,来衡量样品软磁性能的好坏。图8为各合成的核壳结构磁性纳米颗粒的室温M-H图,从图中得到各样品的Hs和Hc参数,见表1。

图8 室温下合成的核壳结构C@Ni、C@Fe、C@Co、C@CoNi、C@FeCo、C@NiFe 纳米颗粒的室温磁滞回线图Fig.8 M-H loops of as-prepared C@Ni,C@Fe,C@Co,C@CoNi,C@FeCo,C@NiFe nanoparticles with core-shell structure at room temperature

表1 各合成样品的Hs和HcTable 1 Hsand Hcof as-prepared samples
如表1所示:合成的样品除C@Fe外,Hs都比较小,在3 000 Oe甚至1 000 Oe以内,很容易达到饱和;另一方面,合成的样品的矫顽力很低,在100 Oe甚至30 Oe以内,而与一般软磁材料(矫顽力为90 Oe[22])相比,说明合成的样品更易退磁,具有一定的优势。由此说明制备的样品为易磁化易退磁的软磁颗粒,这优异的性质使其在要求快速磁化和快速退磁的领域具有巨大的应用前景。
3 结 论
以可溶性淀粉和金属盐为原料,采用溶胶凝胶和高温还原的方法成功制备了炭包覆的核/壳结构纳 米 金 属 软 磁 颗 粒(C@Ni、C@Fe、C@Co、C@NiCo、C@FeCo、C@NiFe)。颗粒直径在10 nm以内,粒径均为;合成的样品在空气具有很好的稳定性,并且能耐260℃和340℃的高温;此复合纳米粒子Hs较小,容易磁化,矫顽力低至100 Oe以内甚至达到27 Oe;在软磁领域尤其是要求快速磁化和退磁的领域具有很好的应用前景。该方法在合成磁性纳米材料时具有很大的优点:绿色环保,无毒害物质产生;分子级混合,实现最大程度的包裹;无中间过程,防止了二次包裹过程中带来的氧化和聚合;耗能少,操作简单可行,原料来源广,能大量生产,有利于实现工业化。但是在合成过程中淀粉会有部分的分散不均匀,造成碳颗粒的团聚,因此还需要进一步研究。
[1]Tartaj P,Morales M P.J.Appl.Phys.,2003,36:182-197
[2]Sun S,Zeng H,Robinson D B,et al.J.Am.Chem.Soc.,2004,126:273-279
[3]Bao Y P,Beerman M,Pahomov A B,et al.J.Phys.Chem.B,2005,109:7220-7222
[4]Wu M Z,Zhang Y D,Hui S,et al.J.Appl.Phys.,2002,92(1):491-495
[5]JING Mao-Xiang(景茂祥),SHEN Xiang-Qiang(沈湘黔),LI Dong-Hong(李东红),et al.J.Jiangsu Univ.(Jiangsu Daxue Xuebao),2005,26:501-505
[6]Guerrero-Martínez A,Pérez-Juste J,Liz-Marzán L M.Adv.Mater.,2010,22:1182-1195
[7]Lu A H,Li W C,Matoussevitch N,et al.Chem.Commun.,2005,1:98-100
[8]Hamaoui B E,Zhi L J,Wu J S,et al.Adv.Mater.,2005,17:2957-2960
[9]Tang N J,Jiang H Y,Zhong W.J.Alloys Compd.,2006,419:145-148
[10]Won S S,Lee J H,Sun X X,et al.Nature Mater.,2006,5:971-976
[11]Wang C,Sheng P,Lise M,et al.J Nano Res.,2009,2:380-385
[12]Jing L H,Yang C H,Qiao R R,et al.Chem.Mater.,2010,22:420-427
[13]SUN Yan-Hong(孙彦红),ZHANG Min(张敏),YANG Jian-Jun(杨建军).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(11):1965-1970
[14]LIU Gui-Xia(刘桂霞),LIU Shu-Jun(刘姝君),DONG Xiang-Ting(董香廷),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(1):36-39
[15]Hall S R,Bolger H,Mann S.Chem.Commun.,2003,22:2784-2785
[16]Wang L Q,Shin Y,Samuels W D,et al.Phys.Chem.B,2003,107(50):13793-13796
[17]Silver J,Withnall R,Ireland T G,et al.J.Mod.Opt.,2005,52(7):999-1007
[18]CHEN Jin-Hua(陈金花),ZHENG Ming-Bo(郑明波),CHEN Yong-Ping(陈勇平),et al.J.Chem.Ind.Eng.(Huagong Xuebao),2010,61(1):259-264
[19]Raveendran P,Fu J,Wallen S L,et al.J.Am.Chem.Soc.,2003,125(46):13940-13941
[20]Engelbrekt C,Sorensen K H,Lubcke T,et al.Chem.Phys.Chem.,2010,11(13):2844-2853
[21]Filippo E,Serra A,Buccolieri A,et al.J.Non-Cryst.Solids,2010,356(6/7/8):344-350
[22]FAN Shu-Hong(范淑红),GUO Xin-Chun(郭新春),LIU Yao-Jun(刘跃军),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(2):330-333
“Green” Synthesis and Thermal Stability of Carbon-Coated Metallic Nanoparticles with Soft Magnetism
WANG Xin JI Guang-Bin*ZHANG Bin CHANG Xiao-Feng
(School of Materials Science and Technology,Nanjing University of Aeronautics and Astronautics,Nanjing 210016,China)
We present a route for the “green” synthesis of carbon-coated metallic nanoparticles with soft magnetism by using soluble starch,mentallic acetate as the raw materials.The final products can be obtained via evaporating the mixture of aqueous solutions then annealing under the nitrogen flow.X-ray diffraction(XRD)analysis showed the carbon-protected metallic nanoparticles(C@Ni,C@Co,C@Fe,C@CoNi,C@CoFe,C@FeNi)were successfully synthetized.Transmission electron microscopy (TEM)image indicated that the particles were well dispersed with the average particle diameter of 3~5 nm.The as-synthesized samples had good srability at room temperature in empty atmosphere,excellent stability and soft magnetic property too.
soluble starch;magnetic metallic nanoparticles;thermostability;soft magnetic properties
O614.81
:A
:1001-4861(2011)04-0711-07
2010-11-15。收修改稿日期:2010-12-31。
国家自然科学基金资助项目(No.50701024)。
*通讯联系人。 E-mail:gbji@nuaa.edu.cn
